糠醛转化生成糠醇的反应机理研究
2020-04-07付雨飞欧阳明燚赵一慧石荣欣
付雨飞,欧阳明燚,赵一慧,唐 晴,石荣欣,石 云
(临沂大学 化学化工学院,山东 临沂 276000)
糠醛,生物油中常见的多种含氧化合物之一,含有羰基和由两个C=C双键及一个环醚键组成的呋喃环,具有高活性,可以通过加氢、加氢脱氧、脱羰等转化为众多有用的化学产品:例如糠醇、2-甲基呋喃、呋喃等。所以在实验上得到了研究人员的广泛关注。
在实验上,对于糠醛的研究,不仅局限于单金属催化剂,双金属催化剂的研究也日渐增多。常用的单金属催化剂有Cu、Ni、Pd、Ru、Pt等。近年来,人们发现当在一种金属中掺入另一种金属构成双金属催化剂后,其催化作用会有较大改变,所以实验工作者对于非贵金属NiCu催化剂催化糠醛的研究较多。Lukes等人[1]早在1951年就研究了200℃时,NiCu催化剂上糠醛生成呋喃的反应;Merat的研究小组发现[2],在1∶1的NiCu催化剂,糠醛加氢的主产物为四氢糠醇。
虽然实验上对于糠醛的研究较多,但是理论上的研究相对较少,尤其在双金属催化剂上的研究更少。本文采用色散校正的PBE-D3方法来研究双金属CuNiCu(111)面上糠醛加氢生成糠醇的反应机理,通过计算得到的相关数据,可以推断反应的最佳路径。该研究可以为生物质衍生的含氧化合物的选择性加氢脱氧反应的催化剂设计提供理论指导。
1 计算方法和模型
所有计算采用VASP 5.3.5软件包[3],利用密度泛函理论(Density Functional Theory)方法下的PBE交换相关泛函,同时考虑色散校正来优化结构和计算能量。过渡态的搜索采用CI-NEB方法[4]。
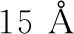
表面物种吸附在周期性模型的最上方,并且允许所有吸附物种弛豫。物种吸附能、反应能垒以及反应热的计算公式见文献[5]。
2 结果与讨论
2.1 稳定中间体的吸附
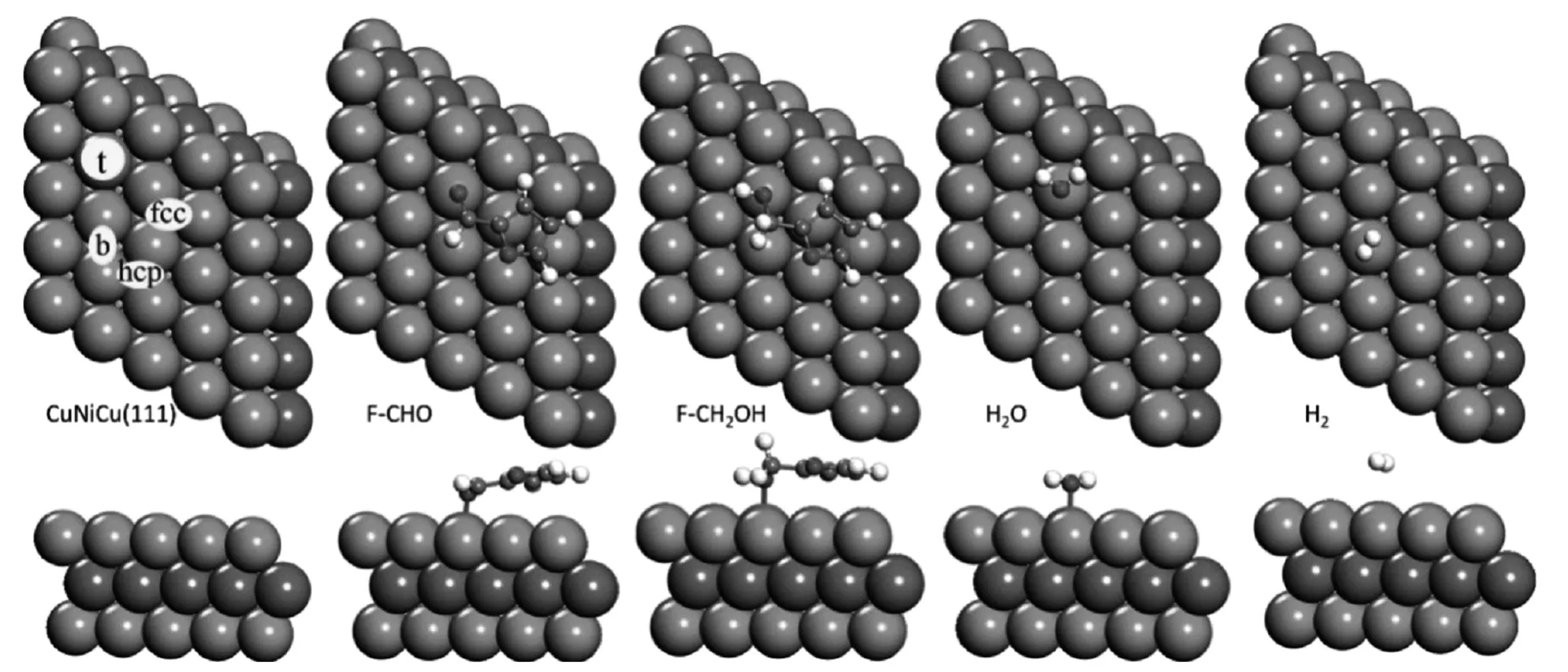
图1 CuNiCu(111)表面的俯视图、侧视图和吸附位点以及中间体的吸附结构
Fig.1 Top and side views of the CuNiCu(111) surface structure and adsorption sites as well as the adsorption configurations of surface intermediates
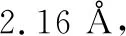
2.2 糠醛加氢生成糠醇的反应机理
糠醛加氢生成糠醇有两种反应路径,一种是支链碳首先加氢生成F-CH2O中间体(R1: F-CHO+H = F-CH2O),然后该中间体进一步加氢生成糠醇(R2: F-CH2O+H = F-CH2OH);另一种是支链氧首先加氢生成F-CHOH中间体(R3: F-CHO+H = F-CHOH),然后进一步加氢生成糠醇(R4: F-CHOH+H = F-CH2OH)。计算得到所有中间体和过渡态的结构如图2所示。

图2 R1-R4反应路径所有优化结构的俯视图
Fig.2 Top views of the optimized geometries for the reaction routes of R1-R4
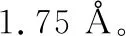

2.3 讨论
根据以上计算结果得知,糠醛支链碳加氢生成烷氧基中间体(F-CH2O)要比支链氧加氢生成羟烷基中间体(F-CHOH)的反应能垒低9.7 kJ/mol,同时F-CH2O中间体的生成为放热反应,而F-CHOH的生成为吸热反应,所以不管是从动力学上还是从热力学上来讲,F-CH2O的生成都是更有利的,因此在CuNiCu(111)面上,糠醛生成糠醇的最低能量路径为:F-CHO→F-CH2O→F-CH2OH。
3 结论
本文采用考虑色散作用的密度泛函理论下的PBE-D3方法计算了NiCu双金属催化剂上糠醛加氢生成糠醇的反应机理,计算了两种可能路径的反应能垒和反应热。根据计算得到的热力学和动力学数据得知,糠醛生成糠醇的最低能量路径为:F-CHO→F-CH2O→F-CH2OH。该理论研究可以拓宽人们对从生物质材料获得的含氧化合物的加氢脱氧反应的基本理解,有着重要的理论指导意义。
