生物黏合水凝胶研究进展
2020-04-02林柏仲王宏伟朱浩鹏盖广清王立艳丁建勋
林柏仲, 赵 丽, 王宏伟, 朱浩鹏, 盖广清, 王立艳, 丁建勋
(1. 吉林建筑大学材料科学与工程学院,建筑节能技术工程实验室,长春 130118;2. 中国科学院长春应用化学研究所,生态环境高分子材料重点实验室,长春 130022)
近年来,内脏器官、皮肤、结缔组织、肌肉等创伤处的出血控制和伤口愈合成为研究的热点[1-3]。缝合是出血控制和伤口闭合的首选途径,但手术缝合带来的周围组织损伤以及较高的手术技能需求限制了其应用。生物黏合剂用于软组织修复可缩短手术时间并减少对软组织的损伤,有望取代传统缝合线、铆钉、器械缝合伤口的处理方式[4]。因此,生物黏合剂克服缝合缺陷并促进伤口愈合成为研究热点。
生物黏合剂是具有高度黏合力和一定生物相容性的凝胶或贴剂,可替代传统手术线缝合的伤口闭合器械并具有促进伤口愈合的功效[3,5,6]。水凝胶是天然或合成高分子的水合三维(3D)网络,因其与生物组织的相似性被广泛应用于生物医用领域。其中,温敏性水凝胶、化学交联水凝胶、酶催化水凝胶等由于其独特且可调节的性能使其在生物医用材料领域得到广泛应用。本课题组制备了一系列原位可注射水凝胶,并在抗肿瘤治疗[7-9]、生物黏附[10,11]、药物递送[12]、创面愈合[13]以及软骨组织工程[14-18]等领域具有较好的应用前景。目前,水凝胶的功能性,如黏合性、韧性、自愈性等也成为研究热点[19,20]。传统水凝胶在固体表面滑动摩擦系数较低,黏合性能差。此外,系统中存在的大量水与水凝胶中官能团产生的氢键相互作用进一步削弱了水凝胶的黏合强度,限制了水凝胶基黏合剂的开发应用[21]。
随着研究人员的不断努力,生物黏合水凝胶取得了较好的进展,但由于各种基底表面对水凝胶的黏合要求不同,导致难以构建用于各种用途的通用黏合剂。生物黏合水凝胶的改性研究除了应满足安全性高、成本低、可用性强、生物相容性好等要求外,还应以理想生物黏合水凝胶的特性为标准来提高水凝胶基黏合剂的综合性能。理想的生物黏合水凝胶应具有以下特性:(1)较强的组织黏合性、止血性能和组织愈合特性;(2)在整个愈合过程中保持所需要的力学性能;(3)流动特性,能准确地应用于所需区域;(4)在生理条件下快速固化,尽量减少出血和缩短手术时间;(5)在规定的时间内降解和吸收;(6)安全、无毒、良好的生物相容性且易于制备;(7)价格低廉且在临床中操作方便。
虽然能够满足以上理想特性的生物黏合水凝胶尚未出现,但生物黏合水凝胶仍取得了快速发展。生物黏合水凝胶的黏合力来源于原位水凝胶形成过程中高分子中活性基团与生物组织中活性基团的相互反应,或与被黏物表面间的物理或化学相互作用。目前对于生物黏合剂的综述多聚焦于单方面研究[22-26],并没有全面归纳生物黏合水凝胶的制备方法和黏合机理,缺乏对生物黏合水凝胶整体研发趋势分析。依据不同的制备方法和黏合机理,如图1所示,生物黏合水凝胶可以分为化学交联水凝胶、物理交联水凝胶、化学和物理协同交联水凝胶,以及生物和生化结合水凝胶。本文对生物黏合水凝胶的制备方法进行了阐述,并详细讨论了每种水凝胶的黏合机理,对生物黏合水凝胶的医学应用也进行了介绍。
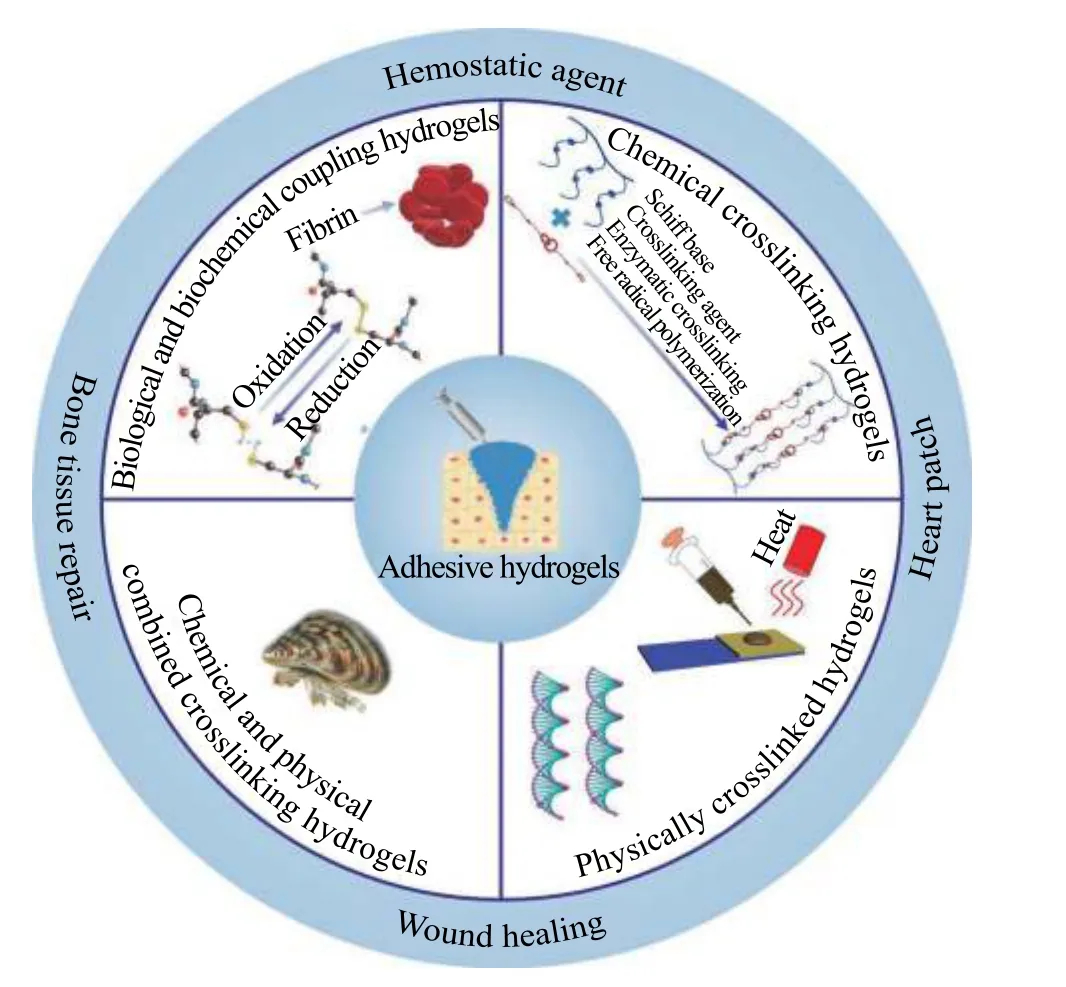
图 1 生物黏合水凝胶的制备及应用Fig. 1 Preparation and applications of bioadhesive hydrogels
1 生物黏合水凝胶的制备及黏合机理
1.1 化学交联水凝胶
生物黏合水凝胶因其优异的黏合性能已作为黏合剂应用于临床,目前大多数生物黏合水凝胶的黏合机制是水凝胶和生物组织表面上不同官能团之间的化学结合[27]。化学交联水凝胶可通过醛基和氨基反应形成席夫碱和多个交联点而得到,并且水凝胶中多余的醛基可以进一步与生物组织中的氨基共价结合,从而显示出对活组织的高黏合强度[28-33]。本课题组[13]通过羧甲基壳聚糖的氨基和氧化右旋糖酐的醛基原位发生席夫碱反应,制备了原位可注射黏性水凝胶。对大鼠进行烧伤创面后原位注入该水凝胶,可促进细胞黏附,使上皮细胞迁移到伤口区域促进皮肤再生。Ye 等[32]将侧基带有儿茶酚的ε-聚赖氨酸与氧化葡聚糖通过席夫碱原位形成黏性水凝胶。体系中的氨基和醛基反应生成的席夫碱提供了水凝胶的内聚力,部分儿茶酚随时间氧化产生的多巴醌和组织表面氨基之间的席夫碱也提供了界面黏合力。使用猪皮进行黏合性能测试的结果表明,儿茶酚基团和席夫碱共价交联的综合作用使该黏合水凝胶具有更高的黏合强度。Yan 等[34]将多巴胺(DOPA)修饰到醛改性的藻酸盐(ALG)骨架形成双功能化ALG,通过酰肼改性聚(L-谷氨酸)和双功能化ALG 的席夫碱反应制备了可注射生物黏合水凝胶(PGA/ALG-CHO)(图2)。剪切黏附实验表明随着儿茶酚接枝率的提高,该水凝胶的黏合强度可达到(21.8 ± 3.1) kPa。采用原位形成的PGA/ALG-CHO 儿茶酚水凝胶,可将两段猪骨或猪肾紧密黏接,表明该水凝胶可以锚定在各种组织表面的多肽和蛋白质上。此外,大鼠肝出血模型中应用该水凝胶后,由于通过席夫碱得到的PGA/ALG-CHO 水凝胶凝胶化快速,儿茶酚基团与组织之间的氢键和π-π 堆积等多种相互作用形成水凝胶的网络屏障,使大鼠肝失血得到快速控制。Yu等[33]也通过狄尔斯-阿尔德和酰腙键反应制备了双交联网络生物黏合水凝胶,该水凝胶也具有很好的组织黏合性能。
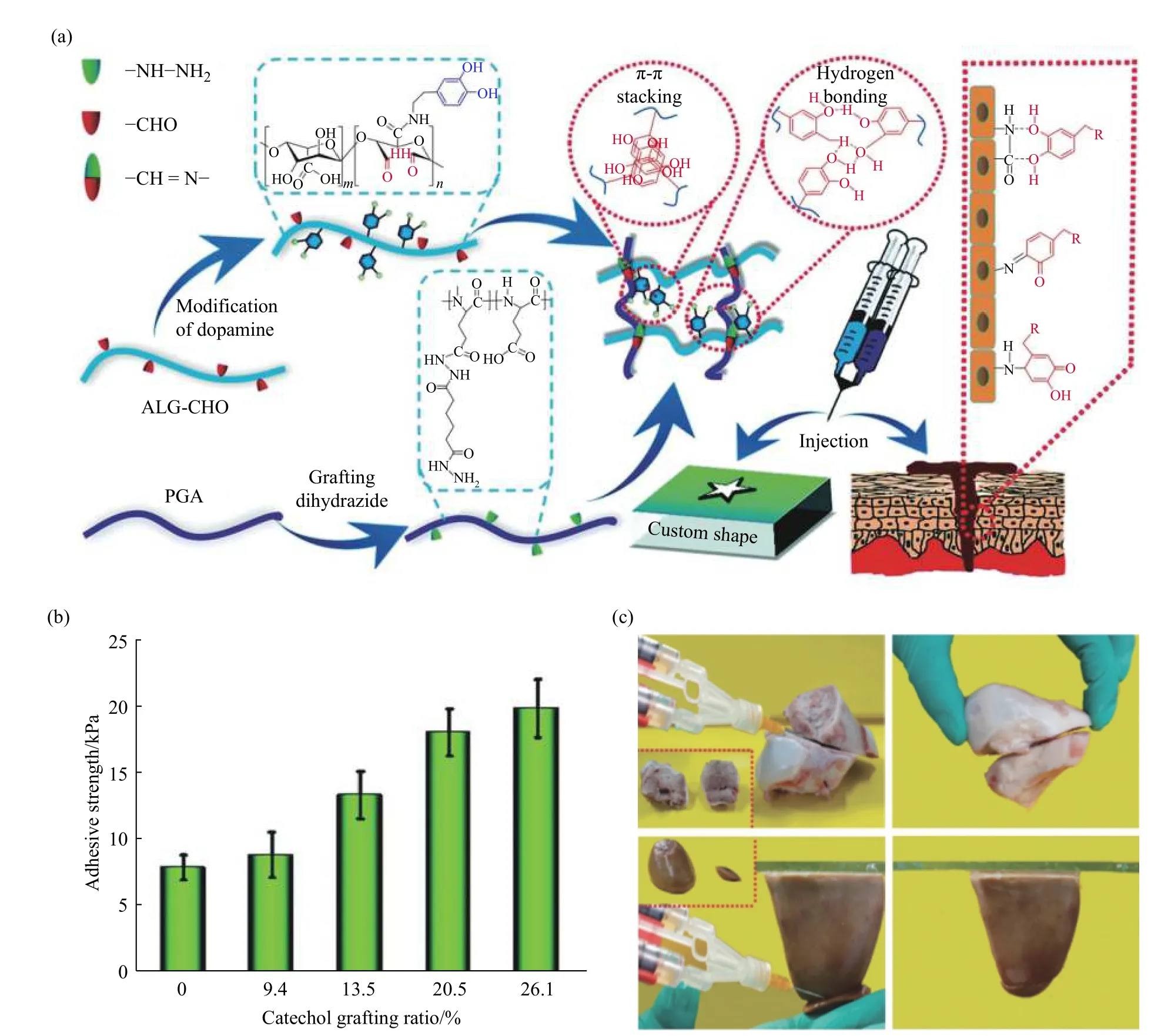
图 2 可注射生物黏合水凝胶PGA/ALG-CHO 的制备及性能分析[34]:(a)可注射生物黏合水凝胶PGA/ALG-CHO 的合成机理示意图;(b)用不同儿茶酚接枝率制备PGA/ALG-CHO 水凝胶的黏合强度;(c)通过使用原位形成的PGA/ALG-CHOcatechol 水凝胶可以紧密胶合两片猪骨或猪肾Fig. 2 Preparation and property analysis of injectable adhesive hydrogels PGA/ALG-CHO[34]:(a)Schematic illustration for preparation of PGA/ALG-CHO adhesive injectable hydrogels;(b)Adhesive strength of PGA/ALG-CHO hydrogels with different catechol grafting ratios;(c)Two pieces of porcine bones or porcine kidneys could be tightly glued by using the in situ formed PGA/ALG-CHO-catechol hydrogels
除了基于席夫碱的原位生物黏合水凝胶外,酶介导的原位交联水凝胶研究也取得了较大进展。酶介导的生物黏合水凝胶具有力学性能可调、快速凝胶化和低毒特性,温和的交联条件也使其作为黏合剂在组织工程中受到广泛关注。本课题组[35]设计了双端酪胺修饰的聚乙二醇(PEG),并在辣根过氧化酶(HRP)和过氧化氢(H2O2)存在下形成酶交联水凝胶,阐明了线性聚合物凝胶化的酶催化反应机理。该凝胶化通过HRP 催化的H2O2的氧化反应消耗酚类化合物,如酪胺中的活性氢生成聚多酚来实现。Lee 等[36]从酶催化苯酚类化合物的聚合出发,通过将羟基苯基丙酸和酪胺与明胶骨架结合,制备了一系列具有不同酚含量的明胶衍生物,并考察了明胶衍生物的成凝胶行为和水凝胶性能。通过改变HRP 和H2O2的浓度可调控水凝胶的成凝胶时间。明胶衍生物在HRP 和H2O2的存在下发生酶催化反应,使明胶衍生物中的苯酚基团相互反应形成寡聚体,足够多的寡聚体作为交联点即可形成水凝胶。HRP 浓度的增加降低了明胶-羟基苯基丙酸和明胶-羟基苯基丙酸-酪胺的凝胶化时间,证实酚基明胶水凝胶的交联速率可通过H2O2和HRP 浓度进行调控。对玻璃表面与水凝胶间的黏合性能测试表明,该酶催化交联水凝胶的黏合强度可以由H2O2浓度来调控。该水凝胶具有较好的黏合强度,其黏合强度是纤维蛋白黏合剂的2~3 倍,可用于常规组织黏合剂的替代物。Hou 等[37]在HRP 和H2O2存在下,实现了ALG-DOPA 水凝胶的原位凝胶化。水凝胶的黏合力随着HRP 和H2O2浓度的增加而增加。较高的HRP 和H2O2浓度使水凝胶的交联密度增加,而交联密度高的凝胶网络可以提供更强的黏合相互作用。但进一步增加H2O2浓度时,过多的交联可能降低高分子的润湿性从而使水凝胶的黏附性能降低。此外,酚基功能化的水溶性高分子也可通过酶促交联反应形成原位水凝胶。Wang 等[38]在HRP 和H2O2存在下制备了ε-聚赖氨酸黏合水凝胶。酶催化交联水凝胶用于黏合剂,因其酶促反应条件温和、原位凝胶化可控,以及黏合强度、力学性质和降解时间可调等特性,在外科手术止血和组织黏接等医疗领域中具有较大应用潜力。
近年来,自由基聚合水凝胶由于固化速率快和可控聚合等优势引起广泛关注,其在可见光或紫外光(UV)照射下可实现体内或体外光聚合得到光敏生物黏合水凝胶,且可通过改变单体浓度、光引发剂浓度、光强度和照射时间等调控凝胶性能[39,40]。葡聚糖(DEX)中存在着大量羟基侧基,可通过化学修饰形成水凝胶,被广泛应用于组织黏合剂和组织工程领域[41-43]。Wang 等[39]采用光聚合生物材料甲基丙烯酸2-羟乙酯(HEMA)和氨基甲酸酯葡聚糖(DEX-U),通过紫外辐射交联得到生物黏合水凝胶(DEX-H)。当高分子溶液暴露在低功率UV 下时,由于聚合前HEMA 易于渗透进入明胶表面的凹槽形成机械互锁,同时多官能团的DEX-U 提供了内聚力,导致DEX-H 的黏合性能优于市售纤维蛋白黏合剂。甲基丙烯酸甲酯修饰的明胶(GelMA)可通过光引发自由基聚合以共价交联形成水凝胶,由于其良好的生物学特性和可调的物理特性已被广泛用于各种生物医学领域。Annabi 等[44]为了避免紫外光照射造成潜在的DNA 和组织损伤,采用细胞外基质(ECM)衍生物GelMA 和甲基丙烯酰取代重组人原弹性蛋白(MeTro)通过可见光交联制备了MeTro/GelMA 生物黏合水凝胶。这种可见光活化光引发剂制备的生物黏合水凝胶避免了采用UV 光带来的生物安全问题。此外,相对于UV 光介导的生物黏合水凝胶,可见光介导MeTro/GelMA 生物黏合水凝胶的力学性能更优。MeTro/GelMA 水凝胶的黏合性能可依据实际使用生理环境进行微调且与高分子浓度有关,其黏合强度随着水凝胶中GelMA 比例的增加而增大,可达(57.26 ± 5.68) kPa,远高于市售组织黏合剂的黏合强度。如此高的黏合强度可归因于水凝胶与组织的机械互锁、交联过程中产生的自由基间的共价键合以及水凝胶基质中游离羟基的氢键相互作用。
多数生物黏合水凝胶由大分子和一种或多种小分子组成,大分子作为主要骨架结构提供力学性能,而小分子通常作为交联剂与大分子反应提供黏合水凝胶的内聚强度。适当选择交联剂可以增加水凝胶的黏度并使其与天然组织紧密连接。Nie 等[45]将马来酰亚胺基团引入到ε-聚赖氨酸上得到氨基化多肽交联剂(EPLM),硫醇修饰的壳聚糖(CSS)通过EPLM 快速原位交联形成水凝胶。该水凝胶内部的三维网络结构来源于大分子上的羟基和硫醇基团与EPLM 上氨基间的共价键合。同时,离子相互作用以及氢键相互作用也增强了水凝胶内部的键合力。此外,该生物黏合水凝胶的黏合强度是商业纤维蛋白胶的4 倍,这是由于EPLM 上的阳离子基团增强了明胶和水凝胶间的黏合作用。Strehin 等[46]采用六臂聚乙二醇胺(PEG-(NH2)6)作为交联剂将N-羟基琥珀酰亚胺(NHS)接枝的硫酸软骨素(CS-NHS)大分子单体进行交联制备了硫酸软骨素-聚乙二醇(CS-PEG)黏合水凝胶。通过调节前驱体PEG-(NH2)6溶液的pH 可控制水凝胶的交联密度。CS-PEG 对软骨的黏合强度是纤维蛋白胶的10 倍,可作为生物黏合剂用于伤口愈合和再生医学领域。
基于席夫碱、酶促反应、自由基聚合和小分子或大分子交联剂交联的原位水凝胶用于生物黏合,具有性能可控,以及可用于病患部位原位治疗的特性,这些特性使其在伤口处理和组织黏结等医学领域具有潜在的应用价值。
1.2 物理交联水凝胶
目前,可注射物理交联水凝胶作为生物黏合剂已显示出诸多优点:(1)因其不使用小分子交联剂毒性较低;(2)凝胶化时间通常比化学交联水凝胶短,可以准确作用于目标部位,防止水凝胶流向其他组织;(3)热响应性高分子也被应用于生物黏合水凝胶中,因其在低温下以溶胶形式存在,在体温下可转变为凝胶,使热响应温敏水凝胶具有较好的生物医学应用潜力。本课题组[10]制备了聚乙二醇-block-聚(γ-炔丙基-L-谷氨酸)(PEG-PPLG)温敏性水凝胶,PEG-PPLG 共聚物中炔基侧基能够使叠氮化物修饰的生物活性分子(例如生物素和半乳糖)进一步官能化。乳糖对ECM 中的纤维蛋白具有吸附作用,将半乳糖基团掺入水凝胶中可提高其对细胞的黏附性能。Chen 等[47]将氧化石墨烯(GO)纳米片和四重氢键脲基嘧啶酮(UPy)引入热敏聚合物聚(N-异丙基丙烯酰胺)(PNIPAM)基质中得到热响应超分子水凝胶(GO-HSH)。GO-HSH 水凝胶对载玻片、塑料盘、钛、铬板以及柔软的生物组织等材料均表现出良好的黏附性。使用猪皮作为模型底物的剪切测量表明,GO-HSH 水凝胶具有较好的生物黏合力。GO-HSH 水凝胶的最大黏合力在37 ℃时为1.30 N,几乎是25 ℃时的2 倍,表明GO-HSH 水凝胶具有用于生物黏合材料的潜力。GO-HSH 水凝胶增强的黏合强度来源于UPy 单元的二聚化,其可形成四重氢键交联网络并有效提高GO-HSH 水凝胶的力学强度。
除了温度敏感生物黏合剂,近红外光(NIR)响应生物黏合剂也引起了广泛关注。温度和NIR 响应生物黏合剂因其黏合强度、照射时间可控和定位精准在生物医学领域具有潜在应用价值。Di 等[48]开发了一种多功能PNIPAM/DOPA/黏土纳米复合水凝胶,该水凝胶具有可调节的拉伸性能、导电性能、光热双响应拉伸性能和黏合性能。聚多巴胺纳米粒子(PDA NP)具有优异的黏合性能和光热性能,将其作为高效光热剂引入到热敏PNIPAM 网络中制备的水凝胶具有可控的NIR 响应变形和宏观热响应行为。当黏土含量一定时,该水凝胶的黏合强度随着体系中PDA NP 含量的增加而增大,可以黏附在玻璃、橡胶、纸和塑料基质上且黏合性具有热可控重复性。该水凝胶与塑料和纸张表面的高黏合强度来源于PDA NP 表面上大量儿茶酚基团与基质表面之间的氢键和疏水作用。此外,协同π-π 叠加、阳离子-π 和氢键相互作用增强了水凝胶和橡胶及玻璃间的黏合强度。与传统PNIPAM 水凝胶相比,这种温敏可逆黏合水凝胶可作为黏合剂广泛应用于各领域。
此外,采用核碱基也可制备物理交联生物黏合水凝胶。核碱基是一类含氮碱基,是脱氧核糖核酸(DNA)和核糖核酸(RNA)的基本单元,在遗传和进化中发挥着重要作用。DNA 和RNA 存储和编码信息的能力来自体液环境中的碱基互补配对,包括腺嘌呤-尿嘧啶(A-U)和鸟嘌呤-胞嘧啶(G-C)[49-51]。这种碱基互补配对的独特分子结构,使碱基水凝胶具有一定的黏合强度。通常水凝胶的黏合强度与水凝胶和固体表面间的氢键、疏水相互作用、金属络合、π-π 堆积和阳离子-π 相互作用等有关。在水凝胶和固体基质之间的界面处可能同时存在几种协同相互作用,而基于腺嘌呤和胸腺嘧啶修饰水凝胶的黏合力仅取决于水凝胶与固体表面间的物理相互作用。
Liu 等[21,50,52]研究了来自DNA 和RNA 的独立碱基(腺嘌呤、胸腺嘧啶、鸟嘌呤、胞嘧啶和尿嘧啶)增强的生物黏性水凝胶,将每种碱基独立引入到聚丙烯酰胺(PAM)中以赋予水凝胶强黏合性能。如图3 所示,水凝胶与各种固体材料之间黏合的相互作用包括氢键、疏水相互作用、金属络合、π-π 堆积和阳离子-π 相互作用。独立碱基―NH2和-N=基团可与固体材料的N、O、F、―OH 和―NH2等形成氢键。此外,―N=和―C=O 基团也可以与材料的金属成分产生金属络合。由于不饱和的杂环结构的存在,使水凝胶与固体材料之间的界面可能产生π-π 堆积和阳离子-π 相互作用。碱基黏性水凝胶对有机、无机材料和生物组织均表现出优异的黏合性能。因此,碱基黏性水凝胶将在组织工程和基因治疗中获得广泛应用。

图 3 碱基水凝胶的黏合机理与性能[52]:(a)可能的黏附机制包括氢键、金属络合、疏水作用和其他相互作用(阳离子-π 或π-π 堆积);(b)不同的被黏物和水凝胶之间的黏合力,包括塑料、聚四氟乙烯、聚乙烯、橡胶、硅橡胶、陶瓷、玻璃、硅玻璃、红玉髓、木材、不锈钢、金、银、铜和铝(从左到右,从顶部到底部);(c)(上层)黏合水凝胶与小鼠内皮组织之间的黏合性和(下层)水凝胶从手臂皮肤剥离的过程中没有残留现象Fig. 3 Adhesion mechanism and performance of nucleobase hydrogel[52]: (a) Possible adhesion mechanisms, including hydrogen bonding,metal complexation, hydrophobic association, and other interactions(cation-π or π-π stacking); (b) Adhesion between hydrogels and different adherends, including plastic, polytetrafluoroethylene, polythene, rubber, silica rubber, ceramic, glass, silica glass, carnelian,wood, stainless steel, gold, silver, copper, and aluminum (from left to right and then from top to bottom) ; (c) Adhesion between adhesive hydrogels and endothelial tissue of mice (Top) and no residual of hydrogel in the process of peeling from skin of arm (Bottom)
1.3 化学和物理协同交联水凝胶
海洋生物贻贝通过足丝腺体分泌的黏附蛋白使其能够黏附在有机、金属和无机非金属表面。贻贝中至少有6 种足丝黏附蛋白,这些黏附蛋白含有的DOPA 是酪氨酸在酪氨酸羟化酶作用下羟化产生的一种氧化物,具有儿茶酚羟基,属儿茶酚胺。研究表明DOPA 主要通过共价或者非共价作用与各类有机或无机表面相互作用(图4)[22]。DOPA 的侧基能够与亲水表面形成强氢键,与金属离子、金属氧化物(Fe3+、Mn3+)和半金属硅形成强络合物[53-55]。DOPA 和金属氧化物之间强且可逆的相互作用与多巴儿茶酚和氧化物表面金属原子之间形成的双齿金属-氧配位键有关。此外,儿茶酚还能与金属氧化物表面形成强可逆界面键[56,57]。邻苯二酚的苯环能够与其他芳环通过π-π 相互作用来改善含儿茶酚聚合物的内聚力,使其能够附着于富含芳香族化合物的表面[58-61]。阳离子-π 相互作用则增强了富含芳香族和阳离子官能团材料的内聚性[62,63]。
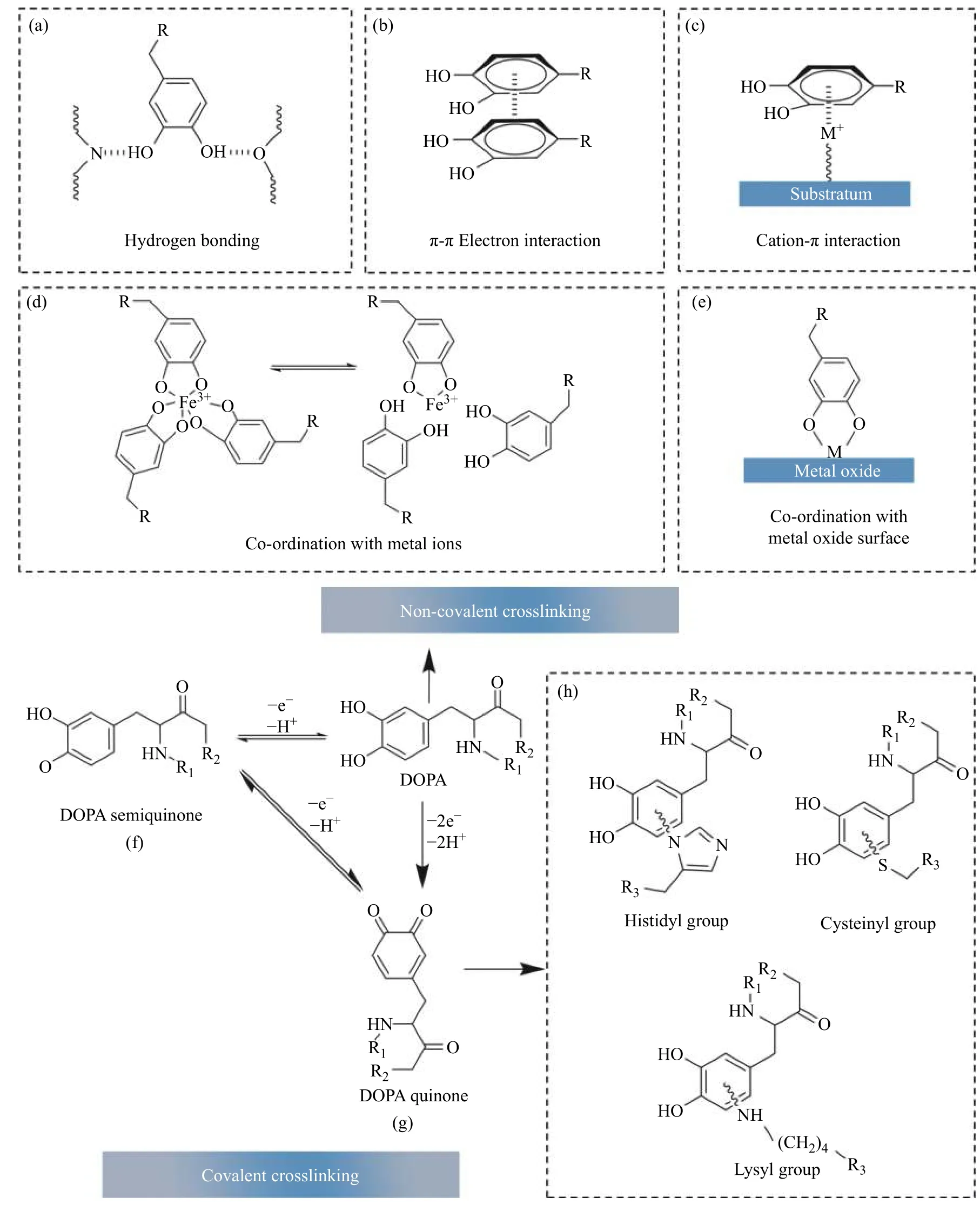
图 4 儿茶酚多巴侧基与其他基团间的相互作用[22]:(a)与羟基形成氢键;(b)与另一个苯环发生π-π 相互作用;(c)与带正电离子的阳离子-π 相互作用;(d)与金属离子的螯合以形成自我修复的交联;(e)与金属氧化物表面的配位键;(f、g)DOPA 氧化形成具有高反应性的半醌和醌;(h)醌与组织表面的亲核试剂(即―NH2、―SH)的界面共价交联反应Fig. 4 Possible interactions between side chain DOPA of catechol and other groups[22]: (a) Hydrogen bonds with ―OH groups; (b) π-π Interaction with another benzene ring; (c) Cation-π interaction with positively charged ions; (d) Self-healing crosslinking formed by catechol chelating metal ions; (e) Co-ordination bonds with metal oxide surfaces; (f, g) DOPA oxidizing to its highly reactive semiquinone and quinone forms; (h) Interfacial covalent crosslinking reaction between quinone and nucleophiles (i.e., ―NH2, ―SH) on tissue surface
贻贝黏附蛋白分子通过DOPA 残留物氧化为多巴醌而相互交联,儿茶酚氧化后形成的半醌和醌参与分子间的共价交联导致DOPA 黏合剂的固化。其次,DOPA 与无机或有机表面的黏合作用可以是共价键或非共价键作用,使DOPA 原位氧化成高反应性多巴醌与组织表面上的官能团(即―NH2、―SH 或咪唑)共价交联[64-67]。此外,在不同pH 条件下进行的单分子研究表明,DOPA 和伯胺表面之间通过迈克尔加成或席夫碱反应形成了共价键,并且采用DOPA 和其他邻苯二酚衍生物与吸附基材之间的相互作用实现材料的黏附性能,可用于仿生生物黏合水凝胶的制备。因此,Cencer 等[65]制备了DOPA 封端的四臂聚乙二醇(PEG-D)生物黏合水凝胶。该水凝胶的生物黏合性来源于PEG-D 与组织基质上的亲核物质(如―NH2、―SH)间的化学键。此外,PEG-D 和软组织之间界面键的形成也与pH 有关。所以,pH 在含邻苯二酚的黏合性水凝胶氧化分子间交联中发挥着重要作用。在温和的酸性条件下,由于瞬时氧化中间体的稳定性增加,PEG-D 的固化较慢,在pH=8 时PEG-D 则快速固化。但相互竞争的交联反应和分子间交联所需的邻苯二酚的减少可能会降低这些水凝胶的DOPA 聚合程度和黏附强度。在pH=7.4 条件下配制的胶黏剂在快速固化、提高力学性能和界面结合力方面表现出良好的平衡,在组织修复和靶向给药的生物黏合剂方面具有潜在应用前景。
几种基于PEG 的仿贻贝黏附蛋白高分子已显示出对组织的强附着力[68-72]。这些黏合剂的宏观黏合性测试表明其搭接剪切、破裂强度和剥离黏合力均优于纤维蛋白胶。目前通过化学方法将DOPA 和其他邻苯二酚衍生物连接到各种高分子上是制备DOPA 基黏合剂的主要方法,如以PEG[71-77]、透明质酸(HA)[78,79]、ALG[80,81]、PAM[82]和壳聚糖[26,83-86]等来提高材料的黏合性能已成为研究热点。基于DOPA 与其他基团发生的共价和非共价作用,为理想生物黏合水凝胶的设计和合成提供了一定的基础。Chen 等[87]采用化学交联和物理交联合成了生物黏合水凝胶,该水凝胶通过DOPA 接枝的氧化海藻酸钠的醛基与PAM 的氨基之间的席夫碱反应形成动态共价交联,在DOPA 接枝的氧化海藻酸钠的儿茶酚基团之间形成可逆的氢键。因此,该化学和物理交联协同的生物黏合水凝胶在保持弹性的同时,还能承受较大变形。此外,由于氧化海藻酸钠链上存在大量儿茶酚基团和DOPA 接枝氧化海藻酸钠链上的醛基,使水凝胶具有独特的细胞亲和力和组织黏附性,更有利于其在伤口敷料中的进一步应用。
1.4 生物和生化结合水凝胶
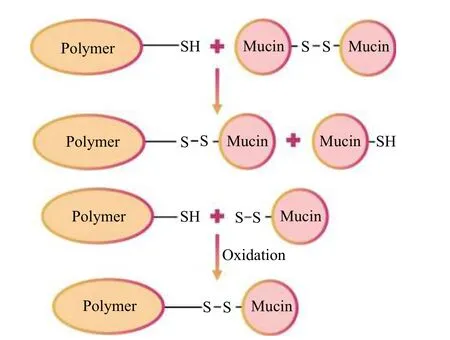
图 5 硫醇和黏蛋白形成二硫键的机理[89]Fig. 5 Forming mechanism of disulfide bond between thiomer and mucin[89]
二硫键是可逆的共价键,能够在相对弱的氧化剂存在下由2 个硫醇基团形成,并能够在温和条件下还原成硫醇,且硫醇基团还能与组织上的氨基进行结合[88]。通过硫醇-二硫化物交换反应或简单的氧化反应,含有硫醇的高分子和富含半胱氨酸的黏液糖蛋白亚结构域之间可以形成二硫键(图5)[89]。二硫键存在于生物物质中,对稳定蛋白质的折叠结构非常重要。本课题组[11]制备了精氨酸-甘氨酸-天冬氨酸序列(RGD)肽修饰的可注射酶交联PGA 基水凝胶。细胞黏附RGD 配体通过二硫键与水凝胶网络缀合,并提升了细胞对水凝胶的黏附性能。同时,以含-SH 的谷胱甘肽分子处理调控水凝胶中RGD 的表达,可使水凝胶具有可调节的生物活性。此外,硫醇功能化高分子和丙烯酸酯或甲基丙烯酸酯聚合物能在生理条件下原位形成水凝胶且没有副产物。其中硫醇化壳聚糖通过与富含半胱氨酸的黏液糖蛋白结构区域形成二硫键而显示出较强的黏合性。Zeng 等[90]由聚乙二醇二甲基丙烯酸酯和CSS 制备了硫醇-丙烯酸酯生物黏合水凝胶。该水凝胶的黏合强度高于纤维蛋白胶的相应值。CSS 上的―SH具有生物反应活性,可以与―COOH、―OH、―SH或其他基团反应,而这些活性基团多存在于生物组织的主要成分蛋白质、糖类和脂肪中。CSS 上的―SH与生物组织中的活性基团间的反应提高了该水凝胶的黏合强度,且黏合强度显著高于普通市售的纤维蛋白的相应值。该课题组还制备了―SH 接枝儿茶酚-共轭壳聚糖水凝胶[85]。质量分数4%的儿茶酚-共轭壳聚糖水溶液可以在1 min 或更短的时间内原位快速形成水凝胶。水凝胶中的硫醇基团不仅提供了抗氧化机制保护了还原形式的儿茶酚,而且丰富的硫醇基团与生物组织活性基团形成的二硫键或产生的迈克尔加成反应提高了水凝胶的黏合强度。由硫醇化高分子组成的水凝胶有望作为软组织黏合剂。
在生物黏合水凝胶系统中,纤维蛋白水凝胶因其促细胞黏附、增殖、干细胞分化及促血管生成性能而引起广泛关注[91-93]。纤维蛋白水凝胶是由纤维蛋白原形成的可降解生物高分子,其凝胶化过程主要模仿凝血级联的最后一步并产生纤维蛋白凝块。纤维蛋白水凝胶中的纤维蛋白原和凝血酶是血液凝固过程涉及的主要成分,纤维蛋白原通过凝血酶的介导转化为纤维蛋白,纤维蛋白通过凝血因子交联固化成纤维蛋白水凝胶网络结构[94,95]。纤维蛋白可通过共价键、氢键或其他机械互锁与生物组织结合提高纤维蛋白水凝胶的黏合强度。纤维蛋白水凝胶用于生物体后,可以被纤溶酶和基质金属蛋白酶等蛋白酶降解,降解产物可被巨噬细胞吞噬并最终被身体吸收。此外,增加凝血酶的浓度会加速水凝胶的凝胶化并产生更细的纤维结构和更密集交联的网络结构,而降低凝血酶浓度则导致水凝胶具有更高的孔隙率。即使纤维蛋白水凝胶具有较好的生物降解性和生物黏合性,其在组织工程中的应用仍然存在着力学性能差和潜在的疾病传播风险等障碍[96,97]。目前可以通过化学改性纤维蛋白水凝胶的结构来改善水凝胶的力学性能和水凝胶的收缩问题。京尼平作为一种低毒性源自栀子果实的天然交联剂,当其与纤维蛋白交联后所得到的纤维蛋白水凝胶力学性能良好[98,99]。优异的生物相容性、可控的降解速率、黏合性和原位固化能力的结合使纤维蛋白水凝胶在组织工程应用中具有较大潜力。
基于醛基和生物组织中氨基的席夫碱反应,酶催化苯酚类化合物相互反应形成寡聚体进一步形成的原位水凝胶,和通过自由基聚合制备的生物黏合水凝胶,以及采用小分子天然生物交联剂或大分子交联剂得到的化学交联水凝胶用于生物黏合均具有性能可控的特性。物理交联的温度敏感水凝胶和碱基水凝胶也具有较好的生物黏合力,这些水凝胶在生物医学领域中均具有潜在的应用价值。基于DOPA 和其他邻苯二酚衍生物可制备具有化学和物理协同交联作用的黏合水凝胶,有望为设计多功能生物黏合水凝胶开辟新思路。将生物与生化相结合,通过硫醇与生物组织中的活性基团的反应或通过纤维蛋白与生物组织的结合可提高水凝胶的黏合力并促进其应用。生物黏合水凝胶均应具有生物相容性、可生物降解性、快速交联、易于应用、黏合力较强、黏合力可调且持久的特性,能够促进组织再生和伤口愈合也是理想黏合剂的特点之一。
2 生物黏合水凝胶的生物医学应用
2.1 伤口愈合
慢性伤口或创面极易受多种致病菌的感染,如大肠杆菌、铜绿假单胞菌、金黄色葡萄球菌、表皮葡萄球菌、丝状真菌和酵母等。其中耐甲氧西林金黄色葡萄球菌及绿脓杆菌感染可导致严重的组织损伤,甚至脓毒血症等并发症。为了避免伤口感染,伤口敷料应具有良好的抗菌活性。在生物黏合水凝胶中加入抗菌剂或直接使用具有抗菌活性的材料可有效治疗伤口感染。生物黏合水凝胶负载的抗菌剂包括金属纳米粒子、石墨烯、抗菌肽以及有机抗菌剂如环丙沙星、万古霉素和氯霉素等。抗菌纳米粒子(TiO2、ZnO、SiO2和AuNPs 等)已被引入生物黏合水凝胶体系中,它们可吸收皮肤组织ECM 中的许多蛋白质链(如胶原蛋白)并可用作网络结构之间的连接体[100,101]。Mao 等[102]将Ag/Ag@AgCl/ZnO 杂化纳米结构嵌入水凝胶中,ZnO 释放的Zn2+可促进成纤维细胞对真皮和创面周围皮下组织的增殖和分化。此外Ag 通过提高与抗菌活性有关的光催化活性也能增强ZnO 的抗菌活性。因此,在体内实验中Ag+和Zn2+产生的协同抗菌作用加速了伤口愈合。天然高分子壳聚糖不仅具备止血和抑菌作用,还能以多种形式用于组织再生。Hoque 等[103]利用聚醛和聚阳离子相互反应并与ECM 交联相互作用,将壳聚糖衍生物N-2-羟丙基三甲基氯化铵壳聚糖作为抗菌成分,与聚葡聚糖醛共混原位制备了具有抗菌活性的生物黏合水凝胶。在评估大鼠伤口愈合实验中,该生物黏合水凝胶的创面愈合率高达(78 ± 9)%,表现出良好的伤口愈合性能,有望应用于临床伤口治疗。另一种常用的天然多糖HA 具有良好的生物相容性以及促进细胞增殖的能力[104,105],在部分降解后可诱导血管生成。合成聚乙烯基膦酸(PVPA)由于能够在水凝胶中形成3D 网络并与血清蛋白相互作用,可以增强细胞黏附和增殖。
2.2 心肌组织工程
心肌梗塞(MI)是目前世界上最常见的死亡原因之一,导电水凝胶有利于电学信号传导可促进MI 后受损心脏功能的重建[106]。导电水凝胶因其高含水量和与天然软组织的分子相似性而成为MI 治疗的软导体之一。导电水凝胶通常采用导电聚合物,如聚苯胺和聚吡咯,使其具有固有的电子传导性能。此外,将具有导电功能的碳纳米管[107-110]、炭黑[111,112]和金属纳米粒子[113,114]等与传统水凝胶相结合制备导电生物材料,能够提高材料的导电性并促进细胞成熟和组织再生。为了实现与皮肤、心脏和其他组织的黏附,导电水凝胶还应具有黏合性能。Liang 等[113]通过Fe3+触发的含有DOPA 的超支化聚吡咯的原位凝胶化反应制备了可涂覆和快速黏合的导电水凝胶贴片。Fe3+作为固化剂可以引发超支化聚吡咯中端基吡咯的聚合,使吡咯基团均匀分布在所形成的水凝胶中,避免吡咯单体的毒性和泄漏,可直接用于机体。此外,Fe3+作为固化剂还可以在中性pH 条件下与超支化聚合物中的DOPA 基团结合,增强水凝胶的湿黏附。这种水凝胶贴片无需缝合或外部光刺激,能够快速贴合到心脏表面。这种同时结合自发性黏附和导电性的功能性贴片鲜见报道。该导电黏合水凝胶贴片能够在凝胶状态下流动,可以在潮湿状态下方便地涂覆和黏合到非平坦的组织表面,有效促进心脏功能恢复并增强电生理信号的传导和梗塞心肌的血运重建。目前,除了将生物黏合水凝胶应用于MI 外,对于穿透性心脏损伤的密封和止血也需要湿组织壁和黏合剂之间的强黏附、维持血压的高力学强度和组织再生的良好生物相容性。因此,Hong 等[115]采用GelMA 和邻硝基苄基类光扳机分子(NB)修饰的HA(HA-NB)设计了一种模拟ECM 成分的光反应型黏合剂,该水凝胶的有效湿黏附性质来自光生成的醛基与组织表面上的氨基键合,其力学强度来自其两个内部共价交联网络。在UV 照射后,甲基丙烯酸酯胶迅速产生水凝胶的第一交联网络元素。同时,生物黏合水凝胶界面HA-NB 上的一些光生醛基与组织蛋白的氨基发生了席夫碱反应。水凝胶HA-NB 上的光生醛基与聚甲基丙烯酸酯的氨基反应形成了第二交联网络。随着反应的进行,剩余的醛基与组织表面的氨基和聚甲基丙烯酸酯反应以结合组织并增加内部交联。两种化学交联基质的产生使水凝胶的组织黏附和内部强度显著增强。该生物黏合水凝胶在紫外线照射后可以快速黏附和密封出血动脉和心脏壁,这项研究为设计多功能性生物黏合水凝胶开辟了一条新途径。
2.3 止血剂
人体自身的凝血过程分为初级止血和凝血级联,使血液转化为稳定的不溶性纤维蛋白,从而达到止血的目的。采用纱布压迫、缝扎和电凝止血的传统止血方法,存在感染率高、血源性疾病传播和组织反应性等风险[116,117]。此外,这些传统止血方法仅适用于轻微损伤,不能用于治疗大量出血,特别是心血管、肝脏、肾脏、骨科和脊柱手术的出血控制[118]。传统止血剂纤维蛋白胶的力学强度弱[119],而氰基丙烯酸酯的细胞毒性大,均不适合体内临床止血[120]。因此,开发生物相容性好、可生物降解和固化快的生物黏合水凝胶用于止血剂成为研究热点。Wang 等[121]使用聚赖氨酸接枝的PEG 和酪胺通过酶促交联反应制备了原位水凝胶。聚赖氨酸会刺激血小板聚集和促使纤维蛋白原凝胶化,具有优异的止血性能,而PEG 具有良好的生物相容性,两者的协同作用使该水凝胶能黏合周围组织并诱导血液凝固,可以用作局部止血剂。壳聚糖因其优异的组织黏附性、止血活性和抗感染活性而被用作伤口敷料,用PEG 修饰壳聚糖可以增强壳聚糖的水溶性。Lih 等[122]用酪胺改性的PEG 接枝壳聚糖,通过HRP 和H2O2原位快速形成生物黏合水凝胶。当该水凝胶应用于大鼠肝脏缺损或大鼠皮肤切口模型时,通过酶交联方法固化的水凝胶在5 s 内显示出优异的止血特性和伤口愈合效果。因此,该原位可固化壳聚糖水凝胶具有伤口止血和愈合的应用潜力。此外,Nie 等[45]采用硫醇改性壳聚糖和ε-聚赖氨酸通过迈克尔加成反应开发了原位壳聚糖/ε-聚赖氨酸黏性水凝胶,该水凝胶可用作黏合密封剂和止血剂,在治疗大鼠肝脏出血时显著阻止出血,其优异的止血性能使其具有用于新型组织密封剂和止血剂的潜力。
2.4 骨组织修复
由于缺乏血液供应和神经支配,关节软骨的自我修复能力有限,而采用组织工程技术,利用生物材料组织工程技术进行软骨修复是行之有效的手段。生物材料可以以两种形式用于关节软骨治疗:一种是作为永久性植入物来替换受损软骨;另一种是作为细胞载体材料以促进组织再生。生物材料作为骨修复基质可以促进细胞增殖和分化以及组织形成。硫酸软骨素(CS)是一种用于骨修复的基础材料,它来源于动物软骨和体内其他组织,可以改善伤口愈合,有助于恢复关节炎的关节功能[123,124]。将CS 引入到水凝胶中可以促进细胞增殖,增加软骨ECM 沉积,从而显著促进软骨形成。Lu 等[125]采用点击化学和动态酰腙键交联制备了生物黏合水凝胶,由于氧化硫酸软骨素中过量的醛基与动物组织中的氨基之间形成了席夫碱,使该水凝胶具有优异的黏合性能。此外,将具有促进骨修复性能的骨形态发生蛋白生长因子引入到该水凝胶后,在体内颅骨修复实验中发现颅骨缺损区域检测到新生骨组织。因此,该生物黏合水凝胶有应用于临床骨修复的潜力。Han等[126]通过将聚多巴胺-硫酸软骨素(PDA-CS)复合物引入弹性PAM 网络,开发了一种新型的组织黏合水凝胶(PDA-CS-PAM)。由于PDA 上有大量的反应性儿茶酚基团,PDA 和CS 自组装形成软骨特异性复合物(PDACS)。这种儿茶酚基丰富的PDA-CS 复合物赋予水凝胶良好的细胞亲和力和组织黏附性,可以促进细胞黏附和组织整合。与裸细胞相比,水凝胶中的PDA-CS 复合物能更有效地发挥其对黏附细胞的作用,从而促进软骨分化。由于PDA-CS 复合物和共价交联的PAM 网络引起的非共价相互作用的协同效应,水凝胶表现出优良的弹性和韧性,可以满足软骨修复的力学要求。该PDA-CS-PAM 水凝胶为软骨细胞生长和软骨再生创造了一个无生长因子和仿生的微环境,提供了无生长因子软骨修复生物材料设计的新思路。
3 结论与展望
生物黏合水凝胶可用于伤口愈合、心肌组织工程、止血剂和骨组织修复等生物医用领域并取得了很好的研究进展。但对其制备方法和黏合机理的深入研究鲜见报道。生物黏合水凝胶的黏合力与水凝胶的制备方法及其带有的活性基团相关。在原位水凝胶形成过程中,水凝胶中的活性基团可以与生物组织中的活性基团进行物理或化学相互作用。依据制备方法的不同,生物黏合水凝胶可以分为化学交联水凝胶、物理交联水凝胶、化学和物理协同交联水凝胶,以及生物和生化结合水凝胶,不同类型的水凝胶具有不同的黏合机理。
化学交联水凝胶可以采用席夫碱反应、酶促反应、自由基聚合和小分子天然生物交联剂或大分子交联剂进行交联固化成三维网状结构。在交联固化过程中,水凝胶与生物组织发生化学反应并产生黏附。物理交联的温敏水凝胶和碱基黏性水凝胶通过氢键和疏水相互作用等发挥强黏合力作用。生物和生化结合水凝胶是将生物与生化相结合得到的具有黏合力的水凝胶。在生物组织主要成分蛋白质、糖类和脂肪中存在着―COOH、―OH、―SH 或其他可反应基团,通过硫醇基团与这些活性基团形成二硫键或产生迈克尔加成反应可以提高水凝胶的黏合强度。此外,通过纤维蛋白与生物组织间共价键、氢键或其他机械互锁等方式的结合可以提高纤维蛋白水凝胶的黏合强度。基于DOPA 可能与其他基团发生的共价和非共价作用,为制备化学和物理协同交联水凝胶提供了研究思路。贻贝足丝蛋白的黏结性来自于其有效基团DOPA。DOPA 与金属离子的络合作用、活性氢基的化学键合,以及氧化后邻位二醌与活性基团间的反应提供了DOPA 基水凝胶的黏附性能。此外,富含芳香族和阳离子官能团的水凝胶也可通过π-π 相互作用增强其与基底材料的黏结力。
生物黏合水凝胶可以通过增强水凝胶的内聚力以及水凝胶和天然组织之间的黏合力来促进受损组织的修复和重建。对于生物黏合剂而言,研制适用于更广泛的组织类型和组织环境(湿组织和干组织)的水凝胶是研究重点方向之一。此外,将生物黏合水凝胶和药物输送技术相结合提高病理手术愈合率或组织恢复性能也是一个重要的研究方向。开发多功能生物黏合水凝胶用于3D 生物打印,可以适应组织工程再生或靶向药物递送的特定要求,也是生物黏合水凝胶研发的新方向。
