多巴胺修饰的竹炭纳米粒子的合成及其光热控制药物释放的研究
2020-04-01刘箫洪沙沙张羱双少敏王煜
刘箫,洪沙沙,张羱,双少敏,王煜
(山西大学 化学化工学院,山西 太原 030006)
0 引言
癌症是严重威胁人类健康的一种疾病,传统的癌症治疗方法主要有化疗、放疗和手术。这些治疗方法都有不同程度的缺陷[1]。例如,化疗药物的副作用在于杀灭癌细胞的同时也会不可避免地造成正常细胞和组织的损害[2-4]。光热治疗具有无创性、安全性和有效性,在癌症治疗中引起关注[5-6]。
光热治疗是利用光热试剂在近红外光照射下将吸收的光能转化成热能引起局部高温,利用癌细胞比正常细胞对热的敏感性,从而杀死癌细胞[7-8],并且刺激药物释放。由于其非侵入性、对正常细胞无损害以及近红外光的时空控制药物释放方式特性,研究者将光热治疗与化疗结合,从而提高化疗药物治疗肿瘤的效果。
近年来,具有近红外光吸收的纳米材料作为药物载体在癌症治疗中引起人们的研究兴趣。近红外纳米材料包括不同的贵金属(例如Au、Ag、Pt)[9-12]、过渡金属硫化物或氧化物[13-14]等,但是贵金属材料价格昂贵,过渡金属或氧化物材料制备工艺复杂。而竹炭纳米材料是一个新型的碳纳米材料,不仅无毒、价廉,而且易于制备。最初Teraoka等确定了竹炭粉的红外特性,证明其具有近红外光吸收。基于竹炭粉具有近红外吸收的研究现状,Zhao等[15]用竹炭粉为原料合成了竹炭纳米粒子(BCNPs),在其表面修饰吐温80来增加生物相容性,且以其作为药物载体将抗癌药物运输到肿瘤部位,具有集化疗与光热协同治疗于一体的特性。在此基础上,通过修饰D-α生育酚聚乙二醇1000琥珀酸(TPGS)抑制p-gp外排蛋白改善了抗癌药物的生物利用率,提升了纳米药物的疗效,并为耐药性肿瘤细胞的治疗提供了新思路[16]。
多巴胺是一类蛋白类生物材料,具有良好的亲水性和生物相容性。多巴胺几乎可以在任何材料表面形成黏合层聚多巴胺(PDA)[17]。据文献报道,PDA多修饰在二氧化硅药物载体上,一方面可以提升载体的生物相容性;另一方面,由于PDA在酸性环境中不稳定,也可用于pH触发的药物释放。基于上述特性,我们尝试将PDA与BCNPs结合构筑多功能智能的药物载体。因此,本研究中利用多巴胺在碱性条件下的自聚反应合成PDA[18],并对竹炭纳米材料表面进行改性,形成多巴胺竹炭纳米材料药物载体系统。将其用于抗癌药物阿霉素(DOX)的负载与近红外光(NIR)触发的药物释放。
1 实验部分
1.1 主要试剂和仪器
试剂:商业竹炭粉(浙江旺林生物科技有限公司);盐酸阿霉素(麦克林,≥98%(质量分数));盐酸多巴胺(上海阿拉丁,分析纯);0.05 mol/L Tris-HCl 缓冲溶液和0.01 mol/L PBS缓冲溶液由实验室配置;实验用水为二次蒸馏水。
仪器:球磨机(DECO-PBM V-0.41 长沙市德科仪器设备有限公司);光纤耦合功率可调二极管激光器(MDL-Ⅲ-808nm-2.5W,长春新工业光电科技有限公司),超声波细胞粉碎机(Scientz-Ⅱ D,宁波新芝生物科技股份有限公司);透射电子显微镜(JEM-1011,日本电子公司);红外光谱仪(TenSor Ⅱ,德国Brukeroptics 公司);马尔文粒度仪(英国 Nano ZS90);气浴恒温振荡器(ZD-85A);真空干燥箱(上海一恒科技仪器有限公司);冷冻干燥(宁波新芝生物科技股份有限公司);磁力电热套搅拌器(SZCL-3A型,杭州瑞佳仪器有限公司);酸度计(FE20,上海梅特勒托利多仪器有限公司)。
1.2 实验方法
1.2.1 竹炭纳米粒子的合成
称取商业竹炭粉250.7 mg,球磨机870 r/mim研磨10 h。将研磨后的竹炭粉与去离子水混合,静置8~10 h后取出上清液。上清液超声30 min后,进一步在320 W的功率下进行超声处理。冰水浴中孵育6 h后得到竹炭纳米粒子(BCNPs)。
1.2.2 竹炭纳米粒子——阿霉素的合成
称取制得的竹炭纳米粒子50.0 mg,加入到含有浓度为0.1 mg/mL的10 mL阿霉素溶液的烧杯中,在室温下避光搅拌24 h,通过离心的方法去除未负载的阿霉素,用去离子水洗涤3次,得到阿霉素负载的竹炭纳米粒子(BCNPs-DOX)。
1.2.3 竹炭纳米粒子修饰多巴胺的合成
称取50.0 mg 多巴胺溶于含有50 mL Tris-HCl缓冲溶液(0.5 mol/L,pH=8.6)的烧杯中,缓慢加入制得的药物负载的竹炭纳米粒子(BCNPs-DOX)50.0 mg,在避光条件下搅拌6 h,然后用二次水离心洗涤3次,得到聚多巴胺修饰的纳米材料(BCNPs@PDA/DOX)。
1.3 仪器表征及测试方法
1.3.1 透射电子显微镜(TEM)测试
将制备的BCNPs分散在二次水中配成纳米悬浮液,滴加在覆盖碳膜的铜网上,干燥后,采用JEM-1011型透射电子显微镜对所制备的纳米粒子的表观形貌进行观察并拍照。
1.3.2 红外吸收光谱(FTIR)测试
将制备的BCNPs和BCNPs-PDA样品冷冻干燥,分别与溴化钾混合研成粉末,压片,用 TenSor Ⅱ FTIR 红外光谱仪对样品分别进行扫描。扫描范围为 4 000~500 cm-1。
1.3.3 Zeta电位测试
测试前分别将BCNPs、BCNPs-DOX以及BCNPs@PDA-DOX分散在二次水中配成纳米悬浮液,采用Nano ZS90型马尔文粒度分析仪分别表征所制备样品的Zeta电位。
1.3.4 竹炭纳米粒子光热转换测定
将竹炭纳米粒子溶于二次水中,分别配置成浓度为1 mg/mL、2 mg/mL和4 mg/mL,用808 nm激光分别对不同浓度的竹炭纳米粒子溶液进行照射10 min,以二次水为对照,利用热电偶温敏计测量溶液温度的变化,并绘制出温度的变化曲线。
1.3.5 体外药物释放测定
准确称取5.0 mg的BCNPs@PDA/DOX 4份分别装在4个棕色小瓶中,其中两份各加入pH 5.4的PBS(0.01 mol/L)缓冲溶液10 mL,另两份各加入pH 7.4的PBS (0.01 mol/L)缓冲溶液10 mL,将4个小瓶放在气浴恒温振荡器(37℃)中。在预定的时间间隔从释放液中取出 2 mL 释放液, 同时加入 2 mL新鲜缓冲液;其中一份pH 5.4和一份pH 7.4的小瓶置于808 nm的近红外光下照射5 min,然后再从中分别取出2 mL的上清液。检测取出的释放液荧光强度,使用标准曲线法计算溶液中释放的DOX含量。
2 结果与讨论
2.1 BCNPs@PDA/DOX的制备
BCNPs@PDA/DOX合成路线如图1所示。采用物理球磨和尖端超声法制备竹炭纳米粒子,将竹炭纳米粒子加入抗癌药物阿霉素溶液中,黑暗下避光搅拌,通过π-π堆积作用将DOX分子被吸附到BCNPs。将负载阿霉素的BCNPs分散于多巴胺Tris-HCl缓冲液中,在氧气作用下多巴胺氧化自聚到BCNPs表面,合成了BCNPs@PDA/DOX。
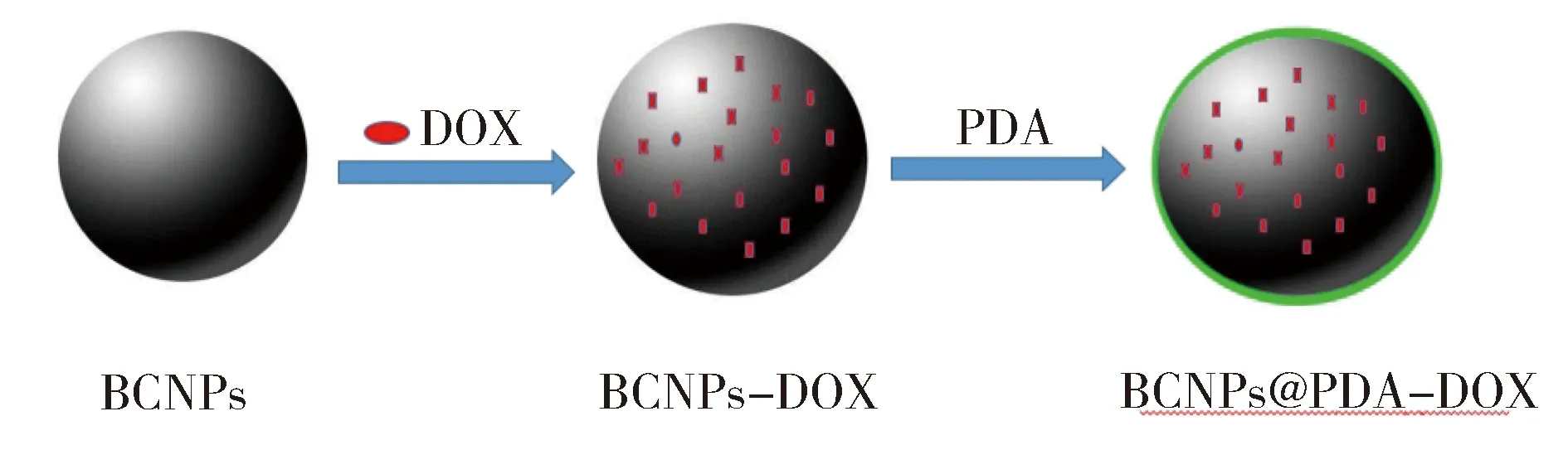
图1 多巴胺修饰的竹炭纳米材料的合成路线Fig.1 Synthesis routes of BCNPs@PDA/DOX
2.2 形貌分析
通过透射电镜观察所制备的竹炭纳米材料的尺寸。从透射电镜图2所示,可以看到竹炭纳米粒子尺寸在(42±10) nm左右,粒子形貌均一、形态良好,分散均匀,不粘连。
2.3 BCNPs的光热转换
使用808 nm近红外光对BCNPs的光热转化情况进行考察,如图3所示。随着BCNPs的浓度的增加,BCNPs水溶液的温度明显升高;当BCNPs的浓度为4 mg/mL时,近红外光照射10 min内升高的温度可达49.7℃。二次水在照射10 min后,温度显示出较温和的变化,温度仅升高13℃。这些结果表明BCNPs具有良好的光热性能。
2.4 电位分析
图4是BCNPs、BCNPs-DOX以及BCNPs@PDA/DOX的电位分析。如图所示,BCNPs的Zeta电位为-33.2 mV;载上抗癌药物阿霉素之后,BCNPs-DOX的Zeta电位变为-18.2 mV,电位变大的原因是这主要是由于阿霉素带有氨基的缘故;在表面上修饰多巴胺之后,BCNPs@PDA/DOX的Zeta电位变为-6.9 mV,电位变大的原因是由于多巴胺吸附于BCNPs-DOX表面,氨基增多的缘故。
2.5 红外图谱光谱(FTIR)分析
FTIR光谱用于表征BCNPs的表面化学基团组成,如图5所示。3 441 cm-1和1 596 cm-1两个峰是BCNPs的羟基伸缩振动峰。用聚多巴胺进行表面修饰后出现了新的吸收峰,将3 420 cm-1和3 135 cm-1的吸收峰分别归于多巴胺的羟基峰和氨基峰,1 620 cm-1处的峰是多巴胺的芳环C-C的共振振动峰。

图2 BCNPs(A)、BCNPs-DOX(B)和 BCNPs-DOX-PDA(C)的透射电镜图Fig.2 TEM pictures of BCNPs (A)、BCNPs-DOX (B) and BCNPs-DOX-PDA (C)

(1) water (2) 1 mg/mL (3) 2 mg/mL (4) 4 mg/mL图3 不同浓度的BCNPs溶液在808 nm的激光(2 W/cm2)照射下的温度变化曲线Fig.3 Photothermal conversion of different concentrations of BCNPs
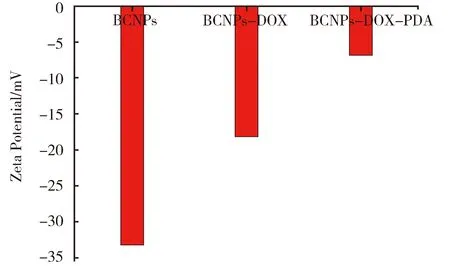
图4 样品的电位图谱Fig.4 Zeta Potential analysis of sample

图5 样品的红外图谱Fig.5 Fourier transform infrared spectra of sample
2.6 紫外可见近红外光谱分析
图6是BCNPs、BCNPs-DOX和BCNPs-DOX-PDA的紫外可见近红外光谱,从图中可以看出竹炭纳米材料在可见光到近红外区域范围内有广泛的吸收,负载上抗癌药物阿霉素以后,在480 nm附近出现阿霉素的紫外吸收峰,说明阿霉素成功负载在竹炭纳米材料上,而且在可见近红外范围内也有广泛的吸收,并没有影响竹炭纳米材料的吸收;修饰多巴胺以后,480 nm仍然存在阿霉素的吸收峰,而且在可见近红外范围内也有广泛的吸收。

图6 BCNPs、BCNPs-DOX和BCNPs-DOX-PDA的紫外可见近红外吸收光谱Fig.6 UV-vis-NIR absorption spectrum of BCNPs,BCNPs-DOX and BCNPs-DOX-PDA.
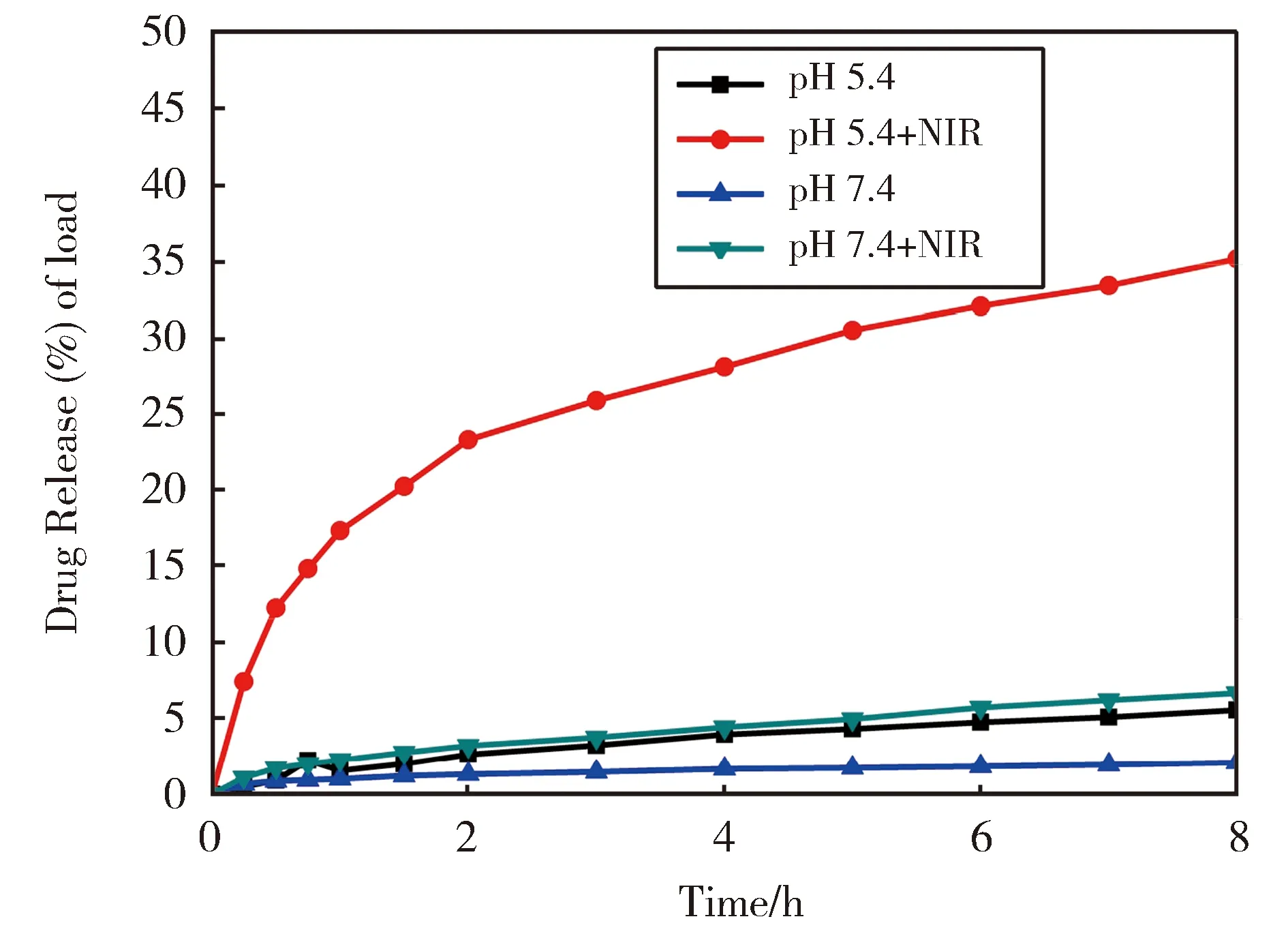
图7 BCNPs@PDA/DOX在不同pH和光照条件下的释药行为Fig.7 Release behavior of BCNPs@PDA/DOX under different pH and light conditions
2.7 药物体外释药行为分析
在37 ℃条件下,在5.4和7.4的两种不同的pH条件下研究BCNPs@PDA-DOX的DOX的释放曲线,结果如图7所示。两种pH条件下都显示出持续的药物释放模式。DOX在中性条件下(pH 7.4)中非常缓慢的释放,在无近红外光照射条件下8 h后仅释放了2.1%,在有近红外光的照射条件下,药物释放了6.7%。在弱酸性(pH 5.4)条件下,药物的释放速度比在中性条件下的释放速度快。在pH 5.4的弱酸以及没有近红外光照射的条件下,在8 h内药物的释放量仅为5.59%,在有近红外光照射条件下,药物的释放量达到了35.19%,明显高于没有照射情况下的药物释放量,表明其可通过外部NIR光刺激刺激药物释放。NIR照射下DOX的快速释放可归因于BCNP的光热效应,因为局部温度升高可增加DOX与纳米载体的解离,因此更多的DOX分子与BCNP分离。
3 结论
通过物理方法获得竹炭纳米材料(BCNPs),负载抗癌药物阿霉素,进一步采用聚多巴胺对BCNPs-DOX进行表面改性,制备成功负载抗癌药物DOX的竹炭聚多巴胺纳米复合物,此制备方法简单、易行。设计的纳米复合物具有近红外吸收的特性,能够吸收808 nm的近红外激发光,并转化为热量,可显著提升环境温度;此外,所合成的智能纳米载体亦可用于近红外触发的药物释放,为构建基于多巴胺修饰的竹炭纳米粒子用于光热触发的药物释放和光热治疗提供了新的策略。
