TNF-α拮抗剂治疗复发性疱疹样脓疱病一例
2020-03-31王娟娟苏玉华丁瑜洁
王娟娟 苏玉华 丁瑜洁 冷 红 季 江 施 辛
苏州大学附属第二医院皮肤科,苏州,215004
“疱疹样脓疱病”(impetigo herpetiformis, IH)是一种好发于孕妇的少见严重皮肤病,具体机制尚不完全清楚。病情严重时可伴有高热、谵妄、昏迷、呼吸困难。孕妇常发生流产、死胎等,血液和疱液细菌培养一般为阴性,血钙常较正常人低。治疗上可予糖皮质激素、抗生素、免疫抑制剂、维A酸类和钙剂等。症状难以控制的患者可考虑加用环孢素或生物制剂等。我们采用以TNF-α拮抗剂为主的综合疗法治疗1例复发性疱疹样脓疱病,效果显著,现报道如下。
临床资料患者,女,31岁。因“孕期反复脓疱再发加重1个月”于2018年9月18日入院。8年前患者怀孕6~7个月时,无明显诱因下出现躯干皱褶部皮肤红斑、脓疱,外用曲安奈德药膏控制,产后皮损自行消失。此次怀孕2~3个月时在既往发病部位再发红斑、脓疱,有灼热感,无瘙痒,后皮疹增多渐累及头皮、四肢皮肤。外院诊断为“疱疹样脓疱病”,予甲泼尼龙40 mg静脉输入,联合环孢素50 mg日两次口服等控制病情,出院后停药即复发,考虑药物对胎儿副作用,于孕7个月时行引产术,逐渐激素减量至停用,更换为雷公藤多苷口服,皮损控制。本次入院前1个月患者自行停药,躯干、四肢爆发大片红斑、脓疱,部分融合形成大片脓湖,无明显瘙痒感,于我院门诊行皮肤活检并收住入院。既往史、家族史、个人史、过敏史无特殊。
体检:T 38.4℃,头皮、面、耳部皮肤无皮疹,躯干部尤其腰部皮肤见大面积红斑,中央部厚痂,红斑边缘见圈状排列的片状脓湖及密集分布脓疱,颈部腹股沟部等皱褶部位及四肢皮肤见类似皮疹,未见明显Ausptiz征,右手指甲明显甲小凹现象,关节无活动受限或畸形(图1a~1c)。辅助检查:血常规示白细胞计数7.0×109/L、中性粒细胞比率 75.5%(50%~70%)、 C-反应蛋白70.4 mg/L(0~5 mg/L);生化、电解质、肝肾功能、血钙正常;甲状旁腺激素31.80 pg/mL(<70 pg/mL);降钙素<2.0 ng/L(<100 ng/L);胸腹盆CT平扫:①两侧腋窝区多发淋巴结、部分增大;②右肺上叶结节样影,两肺下叶少许索条状影。行皮损取材活检,组织病理:表皮轻度角化不全,棘层肥厚,棘层中上部细胞间水肿,可见大量中性粒细胞浸润,形成kogoj海绵状微脓疱,真皮浅层毛细血管扩张,周围有部分淋巴细胞、嗜酸及中性粒细胞浸润(图2)。
患者入院后完善相关检查,排除感染、结核、肿瘤等禁忌,采用以TNF-α拮抗剂治疗为主的综合治疗,予50 mg TNF-α拮抗剂(强克,上海赛金生物医药有限公司生产)皮下注射,3天1次,及阿奇霉素、复方甘草酸苷抗炎治疗。前两次注射TNF-α拮抗剂之间,患者有发热,最高体温38.5℃,双上臂内侧、颈部仍有新发小脓疱,腰腹部皮损趋于好转,脓疱干涸,结痂逐渐脱落。第三次注射TNF-α拮抗剂之后,患者全身无新发脓疱,无发热,皮损处大部分结痂。评估患者病情好转,予出院。三日后复诊,继续予强克皮下注射,患者皮疹处痂皮已全部脱落,仅遗留少许暗红斑及色素沉着(图1d~1f、图3)。患者治疗期间日最高体温、C反应蛋白、白细胞计数和皮损面积随治疗时间延长而逐渐下降(图4)。

图1 1a~1c:颈部、腰腹部、上臂内侧可见大片红斑基础上密集脓疱,片状脓湖,上覆黄色厚脓痂。1d~1f:治疗1周后,原有皮损大部分结痂脱落,遗留少许暗红斑及色素沉着。皮损面积从13%体表面积(BSA)降至8%BSA

图2 表皮轻度角化不全,棘层肥厚,棘层中上部细胞水肿,可见大量中性粒细胞浸润,形成kogoj海绵状微脓疱,真皮浅层毛细血管扩张,周围有部分淋巴细胞、嗜酸及中性粒细胞浸润(2a、2b:HE,×40;×200)图3 患者同一部位治疗前后皮肤镜图像 3a:治疗前,3b:治疗1周后
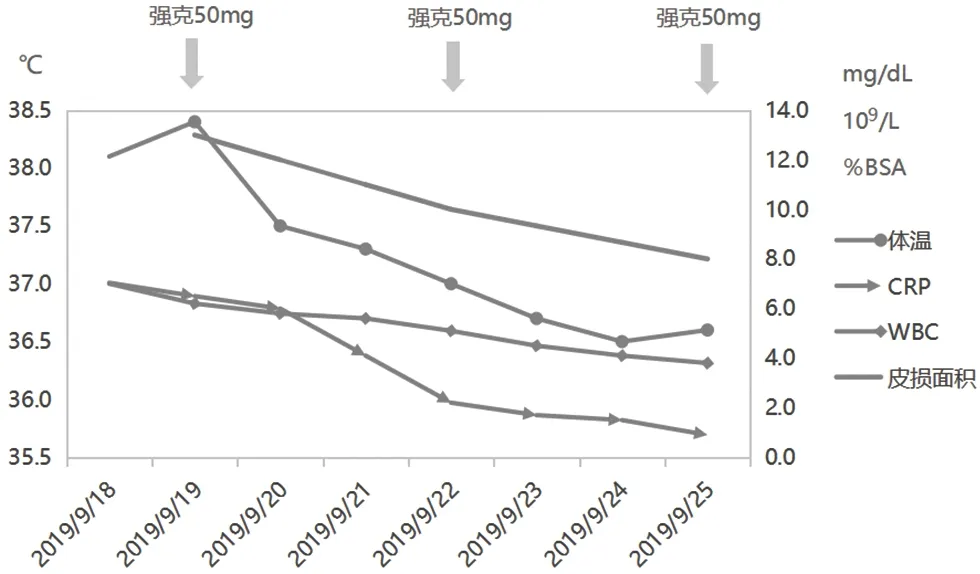
图4 患者治疗期间日最高体温、C反应蛋白、白细胞计数和皮损面积随治疗时间延长而逐渐下降
讨论“疱疹样脓疱病”(IH)是一种少见的妊娠期脓疱性皮肤病,基本皮损是在红斑基础上出现群集无菌性脓疱,常伴有严重全身症状。妊娠晚期可导致胎儿宫内窘迫,病情严重,偶可致母亲或胎儿死亡[1]。妊娠终止可缓解病情,再次妊娠即复发,且病情更重、预后更差。IH在临床和组织学上与脓疱型银屑病相似。关于妊娠脓疱型银屑病是一种单独的疾病,还是发生在妊娠期的广泛型脓疱型银屑病(generalized pustular psoriasis,GPP)的脓疱期,还存在争议,目前尚无实验或遗传数据证明IH和GPP是同一种疾病。
IH的病因及发病机制尚不完全明确,有化脓性感染及妊娠产生的毒素中毒学说,皆缺乏佐证。研究表明IH的病因及加重因素包括感染、基因突变、遗传、药物等[2]。低钙血症、低蛋白血症和血清低维生素D水平与IH的发病有关,但这些因素的病理生理学机制仍有待确定[3]。近年来以遗传背景的研究为热点,IH遗传背景复杂,目前发现遗传易感基因有白介素36受体拮抗剂基因(interleukin-36 receptor antagonist gene,IL-36RN) ,发病可能是由于 IL-36RN 基因突变导致炎性细胞因子分泌失调引起[4]。有学者发现不伴寻常型银屑病(psoriasis vulgaris,PV)的GPP患者IL-36RN基因纯合突变的发生率显著高于伴PV的GPP患者,表明不伴PV的GPP是一种独特的GPP亚型,该亚型绝大多数是由IL-36RN基因纯合突变引起IL-36受体拮抗剂缺陷而导致[5]。IH的诊断主要是基于临床的评估,该病需与妊娠疱疹、角层下脓疱病、AGEP、接触性皮炎等疾病相鉴别。
目前尚无标准治疗IH的指南,糖皮质激素通常被选择作为IH的一线治疗,病情控制后可予减量,但停药后易复发。在难治性病例中,环孢素、抗生素、甲氨蝶呤、光疗和维A酸已被用作二线治疗[6]。其中,抗生素是有效治疗IH/GPP的药物之一,但临床上不推荐作为一线用药,在初期排除败血症之后可考虑联合糖皮质激素和/或环孢素A使用[7]。关于IH生物制剂治疗的有效性报道较少,TNF-α拮抗剂为治疗难治性IH/GPP的新型药物,能快速缓解病情,且不良反应少。美国 FDA 将其列为妊娠 B 类药物。TNF-α拮抗剂包括英夫利昔单抗、依那西普、阿达木单抗等,其中英夫利昔单抗使用最为广泛,其次为依那西普[8]。Yamashita等[9]采取吸附分离血液粒细胞和单核细胞法(GMA,granulocyte and monocyte adsorption apheresis)治疗1例IH患者,取得良好效果,但分娩后迅速复发,予阿达木单抗治疗6个月后患者未再复发,且该患者基因组DNA样本测序的所有IL-36RN编码区域的结果中未发现突变。该研究表明阿达木单抗可能是一种有望预防IH患者产后复发的药物。Andrulonis等[10]曾报道1例采用乌司奴单抗治疗顽固性严重IH患者取得良好疗效。储小燕等[11]采用重组人 II 型肿瘤坏死因子受体-抗体融合蛋白(益赛普)治疗1例IH孕妇取得良好疗效。
本例患者既往两次怀孕期间躯干皮肤出现红斑、脓疱、脓湖,外院曾使用中等剂量糖皮质激素2周后病情仍进展迅速,加用环孢素才得以控制病情,此次行引产术后,病情缓解又复发,入院评估患者病情目前虽非重症,但仍快速进展,权衡利弊,采用以TNF-α拮抗剂(强克)为主的综合治疗方法取得明显效果,患者体温下降,皮损迅速控制,脓疱、脓湖大片结痂、脱落,仅遗留少许色素沉着。此外,生物制剂治疗能够调节免疫和炎症反应,本例患者体温降低、C反应蛋白和白细胞计数下降以及皮损面积减少可能与其治疗效应相关。
