原人参二醇纳米混悬液体外含量测定及冻干保护剂的研究
2020-03-27陈晨孙倩
陈晨,孙倩
原人参二醇纳米混悬液体外含量测定及冻干保护剂的研究
陈晨,孙倩
(辽宁医药职业学院, 辽宁 沈阳 110101)
20(S)-原人参二醇作为研究对象,用反溶剂沉淀法制备20(S)-原人参二醇纳米混悬液。通过优化液相的条件,本章建立了原人参二醇HPLC的体外分析方法,确定了乙腈∶水(/)=90∶10(/)作为流动相,波长 210 nm 的液相条件。对标准曲线,精密度和准确度的考察结果显示:原人参二醇在23.08~1 154 μg/mL范围内线性良好,日内、日间精密度RSD值小于3%,准确度在96%~103%之间,加样回收率为100.84%,该方法满足体外检测原人参二醇定量的要求。考察冻干保护剂,最后确定为1.5%的羟丙基-β-环糊精。
原人参二醇; 含量测定; 冻干保护剂
人参是五加科植物人参属人参的干燥根茎,在我国应用历史悠久,最早记录于我国传统医学专著《神农百草经》[1, 2]。人参中有多种有效的化学成分,如皂苷、氨基酸挥发油及多糖等,其中人参皂苷类是人参的主要活性成分[3]。人参皂苷主要分以下三类[4, 5]:(1)、原人参二醇型,有Rb1, Rb2, Rb3, Rc,等;(2)、原人参三醇型,有R1, R2, R3, Rg等;(3)、齐墩果酸型,有Ro, Rh3, Ri等。研究表明,在胃肠道中,人参皂苷代谢成苷元或次苷元更好的表达药理活性。
近年来,难溶性药物原人参二醇(PPD)由于其抗肿瘤活性[6-8]和抗疲劳[9],抗抑郁[10]等脑内活性近年来成为研究的热点,但其溶解性差,生物利用度低限制其脑内活性的研究。据统计,约70%的有较强药理活性的候选药物由于水溶性差导致研发被迫中止[11]。现今已有很多方法解决难溶药的溶解度问题,如添加增溶剂,形成包合物或络合物等,但是这些技术局限于某些结构的化合物,如环糊精包合物需要分子大小与其中间的环状结构契合。而把药物制成纳米晶混悬液是一种适合难溶药制剂开发的新技术,纳米晶具有载药量为100 %,没有纳米粒聚合物载体材料[12],可提高药物的溶解度,进而提高药物的生物利用度等优点。因此,可以通过制剂化手段改善PPD的生物利用度来提高其血药浓度,针对PPD的理化性质,纳米晶体混悬液给药系统可望解决以上问题。
作者利用高效液相色谱法测定纳米混悬液体外含量。实验结果表明 ,该方法重复性良好,方便快捷。为日后20(S)-原人参二醇纳米混悬液制剂的含量测定、质量控制提供了依据。
1 仪器与试料
高效液相色谱仪(Agilent 1200 Series)由四元泵、在线脱气机、自动进样器、柱温箱、二极管数组检测器组成(Agilent Technologies, Palo Alto, CA, USA);Zorbax SB-C18 色谱柱(4.6×250 mm, 5 μm,Agilent Technologies, Inc., Palo Alto, CA, USA);恒温磁力搅拌器(上海梅颖浦仪器仪表制造有限公司,中国); Nano-Zetasizer 动态光粒径测定仪(Malvern,UK);EL204-IC 电子天平(瑞 士 Mettler Toledo 公司);Allegra X-15R 离心机(Beckman,USA);冷冻干燥机(Coolsafe 110,Scanlaf,Denmerk);
原人参二醇 (纯度>98%,成都普菲尔生物技术有限公司),甲醇,乙腈(Merk,Germany);维生素E聚乙二醇琥珀酸酯TPGS (Sigma-Aldrich);丙酮购于天津凯通化学试剂公司;超纯水。
2 实验方法
2.1 原人参二醇纳米混悬液的制备
精密称取5 mg PPD溶解于1 mL丙酮中,在1 000 r/min条件下,注入到10 mL含0.015%(/)TPGS水相中,继续高速搅拌5 min,超滤法除有机溶剂,高速离心25 min,用等体积超纯水复溶,得到样品PPD纳米晶混悬液。
2.2 测定波长的选择
配置PPD甲醇溶液200 μg/mL, 通过HPLC 1200 全波长扫描,确定高效液相色谱法中PPD的测定波长。
2.3 流动相的优化
色谱柱:Zorbax SB-C18(250×4.6 mm, 5μm, Agilent);流速:1.0 mL/min;柱温:30 ℃;进样体积:20 μL;检测波长:210 nm;流动相:待优化。
2.4 标准曲线的绘制
精密称定5.77 mg PPD样品,甲醇溶解定容与5 mL 容量瓶中,得到浓度为1154 μg/mL 的PPD储备液。分别用移液管精密量取储备液,甲醇对半稀释,得到 1 154, 577,288.5,115.4,57.7,23.08μg/mL的标准液。按照2.2项下优化的色谱条件进样,PPD标准液的浓度(μg/mL)为横坐标,HPLC峰面积为纵坐标,进行线性回归,考察浓度与峰面积的线性关系。
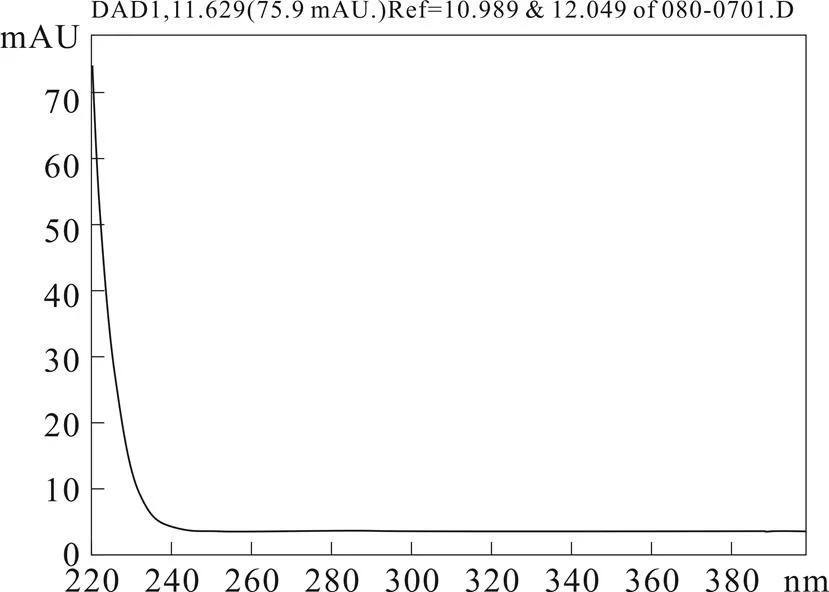
图1 PPD的全波长扫描图
2.5 精密度和准确度考察
分别取线性范围内的23.08, 284.48, 1 154 μg/mL高、中、低3个浓度的标准液,一天之内连续进样5次,连续进样3天,HPLC测定样品。将峰面积带入标准曲线,计算相应的标准液浓度,并与实际浓度进行比较,从而计算准确度,并且,以PPD测定浓度的相对标准偏差(RSD)评价日内与日间精密度。
2.6 稳定性试验
精密吸取“2.3”项下任意浓度作为供试品溶液,放置24 h,每隔2 h按照2.2项下优化的色谱条件进样3次,计算平均峰面积。
2.7 加样回收率试验
取已制备的PPD纳米混悬液1 mL(约含PPD 0.5 mg),分别加入80%,100%,120% 已配制完的PPD对照品溶液(0.512 4 mg/mL),按照2.2项下优化的色谱条件依次进样,平行测定3次,计算样品中含量。
2.8 原人参二醇纳米混悬液的冻干与重分散试验
取已制备完的 0.4 mg/mL 的 PPD 纳米晶混悬液,加入不同种类与浓度的冻干保护剂。样品搅拌加入冻干保护剂溶解后,放入-80 ºC 冰箱中预冻 12 h 以上, 后移入冷冻干燥机中冻干48 h以上,确保全部成为冻干粉。将冻干粉溶解于一定量超纯水中获得重分散体系。测定重分散后的混悬液的粒径和 PdI,筛选 出具有良好分散性的冻干保护剂。冻干 PPD 纳米晶混悬液候选保护剂如表1所示。
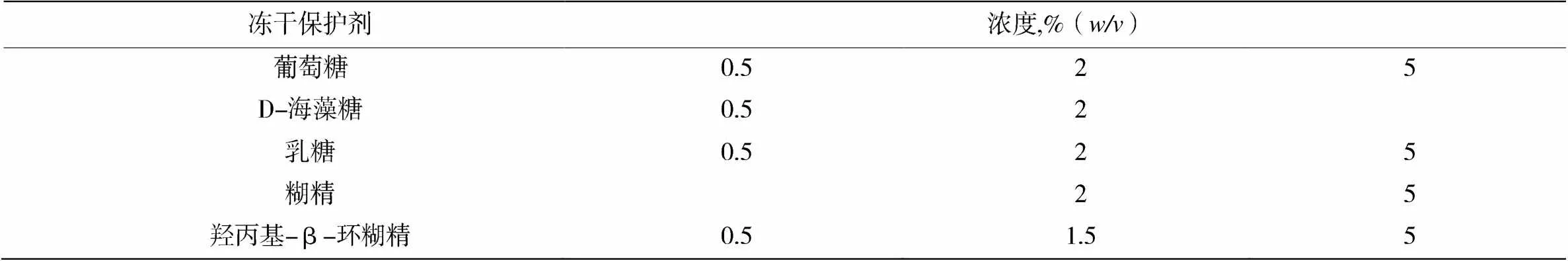
表1 不同种类冻干保护剂的浓度
3 结果与讨论
3.1 测定波长的选择
由HPLC1200得到原人参二醇在210~400 nm的全波长扫描图,如图1所示。
原人参二醇甲醇溶液在210 nm处有最大吸收,所以选择210 nm作为HPLC方法中的检测波长。
3.2 流动相的优化
调节乙腈与水的比例,得到的色谱结果如表2所示。实验结果表明,随着乙腈比例的增加,PPD的保留时间减小。为缩短分析时间,流动相比例确定为乙腈∶水(/)=90∶10 (/)。

表2 HPLC流动相比例优化
3.3 标准曲线的绘制
将PPD的浓度与对应的HPLC积分所得峰面积进行线性回归,得到的回归方程为:
=4.813 5-25.593(2=0.999 9)
式中:—积分所得峰面积;
—PPD浓度。
在23.08~1 154 μg/mL范围内线性良好,标准曲线见图2。
3.4 精密度和准确度的考察
该检测方法高、中、低浓度准确度以及日内、日间准确度如表3。结果表明,日内、日间精密度的RSD值均小于3%, 准确度在96%~103%之间,说明所建立的高效液相色谱方法的精密度和准确度均良好。

图2 PPD的标准曲线

表3 PPD的日间和日内准确度和精密度
3.5 稳定性试验
结果表明,24 h内测定的RSD值为1.45%, 说明PPD甲醇溶液稳定性良好。
3.6 加样回收率试验
该检测方法测定加样回收实验如表4。结果表明,加样回收率为100.84%,RSD值<3%,说明该高效液相色谱法的准确度良好。
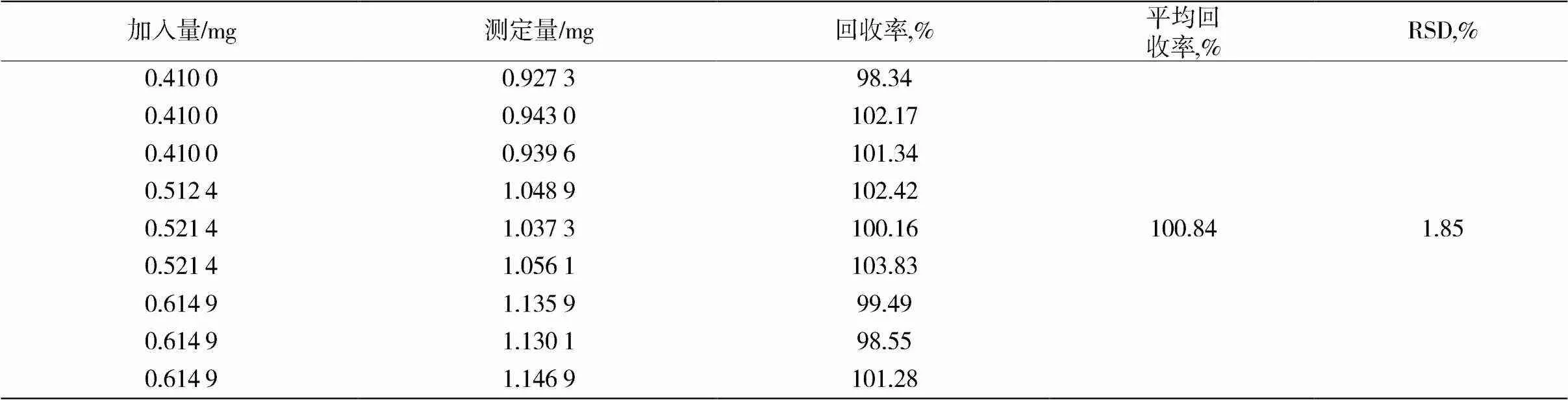
表4 PPD的加样回收率试验
3.7 原人参二醇纳米混悬液的冻干与重分散试验
从实验结果可见,冻干保护剂对PPD纳米混悬液的冻干后重分散的影响不同。当加入乳糖和糊精在PPD纳米混悬液冻干重分散时,有明显沉降发生,无法复溶。当使用不同浓度的葡糖、D-海藻糖和0.5% 羟丙基-β-环糊精时,虽然可以使PPD纳米混悬液重新分散,但是粒径较大,且不均一。当使用1.5%和5%浓度的羟丙基-β-环糊精时,复溶后,粒径没有明显变化,且PdI<0.3,体系较均一。在加入5%的羟丙基-β-环糊精时,由于浓度较高,在水中搅拌溶解时间较长。根据上述结果,因此最后确定以1.5%的羟丙基-β-环糊精作为PPD纳米混悬液的冻干保护剂。
4 讨论
本文曾以210 nm为波长,不同比例甲醇∶水作为流动相优化色谱条件,甲醇∶水=70∶30时,保留时间为29 min;甲醇∶水=80∶20时,保留时间为25 min;甲醇∶水=90∶10时,保留时间为18 min。尝试用乙腈∶水作为流动相梯度洗脱,但是由于其基线不稳,漂移且出现平峰、拖尾等问题,而最终选择以乙腈∶水=90∶10作为流动相,流速1 mL/min,效果较好。
[1] Liu, C.X. and P.G. Xiao, Recent advances on ginseng research in China[J]., 1992,36(1): 27-38.
[2]张均田. 人参研究的最新进展[J]. 江苏大学学报(医学版), 2009, 19(03): 185-191.
[3]Kitts, D. and C. Hu, Efficacy and safety of ginseng[J]., 2000, 3(4A): 473-85.
[4]Choi, K.T., Botanical characteristics, pharmacological effects and medicinal components of Korean Panax ginseng C A Meyer[J]., 2008, 29(9): 1109-18.
[5]张静静, 刘桂芹, 王庆鹏,李兰杰. 植物三七中皂苷类化学成分的研究进展[J]. 聊城大学学报(自然科学版), 2018, 31(02): 43-52+59.
[6]Liu, G.Y., et al., 20S-protopanaxadiol-induced programmed cell death in glioma cells through caspase-dependent and -independent pathways[J]., 2007, 70(2): 259-64.
[7]Zhang, Z., et al., TRAIL pathway is associated with inhibition of colon cancer by protopanaxadiol[J]., 2015, 127 (1): 83-91.
[8]Zhu, G.Y., et al., 20(S)-Protopanaxadiol, a metabolite of ginsenosides, induced cell apoptosis through endoplasmic reticulum stress in human hepatocarcinoma HepG2 cells[J]., 2011, 668(1-2): 88-98.
[9]Oh, H.A., et al., Anti-fatigue Effects of 20(S)-Protopanaxadiol and 20(S)-Protopanaxatriol in Mice[J]., 2015, 38(9): 1415-9.
[10]Xu, H., et al., Protective effect of Panax quinquefolium 20(S)-protopanaxadiol saponins, isolated from Pana quinquefolium, on permanent focal cerebral ischemic injury in rats[J]., 2014, 7(1): 165-170.
[11]Cooper, E.R., Nanoparticles: a personal experience for formulating poorly water soluble drugs[J]., 2010,141: 300-302.
[12]Junghanns, J.-U.A., M Li, S.L., Sun, E., Tan, X.B., Sechnology, drug delivery and clinical applications[J]., 3, 295.
Study on Determination of the In Vitro Content of Protopanaxadiol Nanosuspension and Its Lyophilized Protective Agent
,
(Liaoning Vocational College of Medicine, Liaoning Shenyang 113001, China)
Using 20 (S) -protopanaxadiol as research object, 20 (S) -protopanaxadiol nanosuspension was prepared by anti-solvent precipitation.An in vitro analytical method of protopanaxadiol by HPLC was established, and the liquid phase conditions were optimized as follows: the mobile phase acetonitrile and water(acetonitrile∶water=90∶10),the wavelength 210 nm.The standard curve, precision and accuracy were investigated. The results showed that the protopanaxadiol had good linearity in the range of 23.08~1 154 μg/mL,intra-day and inter-day precision RSD values were less than 3%,the accuracy was between 96%~103%, and the recovery rate was 100.84%.This method met the requirements for the in vitro determination of protopanaxadiol.At last,its lyophilized protective agents were screened, and 1.5% hydroxypropyl-β-cyclodextrin was finally determined as suitable lyophilized protective agent.
protopanaxadiol; content determination; lyophilized protective agent
2019-11-18
陈晨(1990-),女,助教,硕士,辽宁省沈阳市人,2016年毕业于澳门大学中药学专业,研究方向:药物分析。
孙倩(1985-),女,讲师,硕士,研究方向:药物分析。
O 657
A
1004-0935(2020)02-0140-04
