铁矿石中重铬酸钾滴定测TFe 分析方法优化研究
2020-03-27朱为民付海涛
李 娜,朱为民,付海涛
(江西新余钢铁股份有限公司,江西 新余 338001)
重铬酸钾氧化还原法测铁矿石中铁,用二氯化锡—三氯化钛还原三价铁为二价铁的分析方法时,钨酸钠为指示剂,当三氯化钛过量时可使钨酸钠中的六价钨还原成五价钨化合物,过量三氯化钛用稀重铬酸钾使溶液蓝色褪去。氧化“钨蓝”终点的观察为方法的关键。此举避免了剧毒汞盐的危害,但因氧化剂与滴定剂的同是重铬酸钾,操作稍有不慎都能使结果产生较大误差。因此,笔者就几种不同氧化还原分析方法做了比较分析后发现:汞盐法虽准确但因危害大不考虑。锌粉还原法需加装二氧化碳保护装置隔绝空气,操作繁琐。过量钛自然氧化法时间较长,不适合大批量生产操作。硫酸铜催化法灵敏快速,在控制好铜离子浓度消除干扰的情况下,可较好的用于生产分析[1]。
1 实验部分
1.1 主要试剂
(1)硫酸:ρ1.84g/mL。
(2)磷酸:ρ1.70g/mL。
(3)盐酸:ρ1.19g/mL。
(4)二氯化锡溶液(60g/L):称取6g 二氯化锡(SnCl2.2H2O)于150mL 烧杯中,加入20mL 盐酸(1.1.3),加热溶解至清亮,用水稀释至100mL,混匀。
(5)三氯化钛溶液(2+8):取20mL 三氯化钛,用盐酸(5+95)稀释至100mL,混匀。
(6)钨酸钠溶液(250g/L):钨酸钠溶液(250g/L)(有沉淀时需要过滤),使用时每100mL 加5mL 磷酸混匀。
(7)二苯胺磺酸钠指示剂溶液(2g/L)。
(9)硫酸铜溶液:0.5%。
1.2 实验方法
称取0.200g 试料(精确至±0.0001g),将试料置于300mL 锥形瓶中,加入5mL(2)磷酸、5mL(1)硫酸,加热至试料完全溶解,硫酸烟悬至瓶底1/3 处取下,冷却。缓慢加入10mL(3)盐酸,趁热滴加二氯化锡(4)溶液至呈浅黄色,冲入蒸馏水至体积60mL~80mL,加热至微沸,取下。 溶液冷至40℃~50℃时,加入10 滴钨酸钠(6)溶液,用三氯化钛(5)还原至蓝色,加硫酸铜溶液(9)2 滴,摇动4s~5s 至“钨蓝”恰好消失,加入6~8 滴二苯胺磺酸钠指示剂溶液(7),立即用重铬酸钾标准溶液(8)滴定至稳定的紫色为终点[2]。
1.3 分析结果的计算
按式(1)计算铁的百分含量。

V ——消耗重铬酸钾标准溶液的体积,mL;
m ——试料量,g。
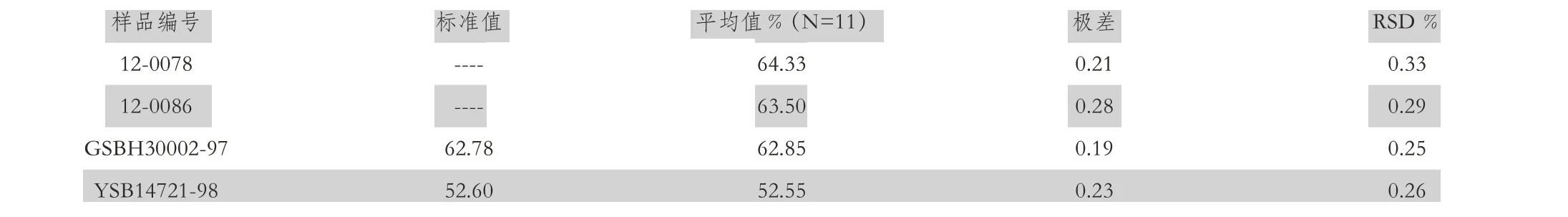
表1 准确度、精密度试验

表2 加标回收率试验
2 结果与讨论
2.1 铜离子对铁干扰的影响
硫酸铜催化法具有灵敏快速的优点,因铜离子的存在易使三氯化钛还原终点褪色,其量越高褪色越快。但铜离子易被三价钛还原为低价,同时又被重铬酸钾氧化,从而造成结果偏高(较高铜时)。另外铜氧化后又对亚铁起催化作用,又使铁的结果偏低。因此需控制好试样中硫酸铜浓度使其不干扰测定,一般理论上认为铜离子浓度大于0.5%即有干扰。经实验选择硫酸铜溶液浓度0.5%,2 滴。
2.2 硫酸铜还原温度的选择
在还原、氧化钨兰的这一步骤时,硫磷混酸溶样温度应控制50℃~60℃。主要原因是磷酸与钛盐络合作用,降低了“钨兰”终点的敏锐性,所以温度宜高些提高还原氧化时的灵敏度。温度低在硫酸铜氧化“钨兰”终点反应慢,氧化终点易返。温度高,反应快,温度太高,“钨兰”颜色浅,同时三氯化钛还原终点也易退色,另外,温度高时铜离子干扰增大,影响分析结果。
2.3 滴定溶液体积的选择
体积太大,由于酸度变小易引起钛盐水解;体积太小,由于盐酸比例大,终点黄色过渡色大,所以一般控制在加100ml 蒸馏水后再滴定。
2.4 准确度、精密度实验
由表1 可知,该方法对于铁矿石中铁的检测精密度和准确度都较好。
2.5 回收率实验
从表2 可知,加标回收率在98.%~100.%之间。
3 结论
硫酸铜催化法灵敏快速,在控制好溶液中铜离子浓度、温度、体积消除干扰的情况下,可较好的用于生产分析[3]。
