参麦注射液联合化疗治疗中晚期食管癌的近期效果观察
2020-03-26张健
张健
(常熟市第二人民医院胸外科 江苏 常熟 215500)
食管癌为我国发病率较高的恶性肿瘤,具有侵袭力强、早期扩散、易转移等风险,较多患者确诊时已经达到中晚期,无法实施手术治疗,需采取化疗治疗[1]。但是,部分中晚期食管癌患者化疗治疗效果不佳,且存在较高的毒副反应风险,患者依从性较差,亟待提升疗效及安全性。参麦注射液是中医治疗气阴两虚型之症的常用药物,对于化疗引发的虚症改善效果较好,但是其具体应用效果仍有待分析。为此,本次研究选取2017 年1 月—2019 年9月期间在本院行化疗治疗的48 例中晚期食管癌患者,对比了参麦注射液联合化疗治疗的近期效果,现总结报道如下。
1.资料与方法
1.1 一般资料
选取2017 年1 月—2019 年9 月在本院行化疗治疗的48 例中晚期食管癌患者,随机分为对照组(22 例)和参麦组(26 例)。参麦组,男18例,女8例,年龄52~76岁,平均64.17±12.03岁,病程3 ~12 个月,平均8.57±3.73 月。参麦组,男14 例,女8 例,年龄53 ~76 岁,平均64.51±11.52 岁,病程4 ~12 个月,平均8.29±3.82月。两组在一般资料比较,差异不显著(P >0.05),具有可比性。本研究经伦理委员会批准通过。
1.2 纳入与排除标准
纳入标准:病理学检查确诊为中晚期食管癌;放疗前血常规、肝肾功能等实验室检查指标基本正常;自愿参与本次研究,并签署知情同意书。排除标准:心肺肝肾功能不全者;远处转移者;食管瘘;预期生存期不足3 个月者;化疗禁忌症者等。
1.3 治疗方法
对照组采用化疗方案治疗:采用FP 方案,顺铂(注射用顺铂,国药准字H20056422,规格:20mg),20mg/m2,d1-5,静脉滴注;氟尿嘧啶注射液(国药准字H32022246,规格:10ml:0.25g)500 mg/m2,d1-5,静脉滴注。
参麦组在对照组基础上增加参麦注射液治疗:参麦注射液[国药准字Z51021263,每支装20ml(相当于红参、麦冬各2g)],60mL/次,与250ml5%葡萄糖配伍,静脉滴注,1 次d,d1~14,d29 ~42
1.4 观察指标
1.4.1 疗效评估 两组患者治疗前和治疗结束后1 个月,分别进行食道CT 及食道造影X 线摄片,参照《实体瘤近期客观疗效评价》(RECIST)评估近期疗效,分为完全缓解、部分缓解、稳定、进展共4 个项目(CR、PR、SD、PD);CR 为病灶基本消失;PR,病灶最长直径总缩小≥30%;SD,病灶最长直径总和缩小≥30%,或增大不足20%;PD:病灶最长直径总和增大≥ 20%,或出现新病灶者[2]。近期有效率 =(CR+PR)例数/样本数×100.0%。疾病控制率=(CR+PR+SD)例数/样本数×100.0%。
1.4.2 化疗毒副反应评估 密切观察患者化疗后是否出现胃肠道反应等,并监测白细胞、血小板、肝肾功能等指标变化,同时观察患者是否出现急性损伤情况,对比两组化疗毒副反应发生率。
1.4.3 生存质量评估 两组患者均采用卡式功能状态评分标准(Karnofsky,KPS)评估治疗前后患者生存质量情况,评分0~100 分,分值越高表明患者生存质量越好,对比两组治疗前、化疗结束后、随访3 个月生存质量评分情况[3]。
1.5 统计学方法
数据采用SPSS20.0统计学软件分析处理,计数资料采用率(%)表示,行χ2检验,计量资料用均数±标准差(±s)表示,行t 检验,P <0.05 为差异有统计学意义。
2.结果
2.1 两组近期疗效比较
参麦组近期有效率(57.69%)、疾病控制率(84.62%)显著高于对照组 (31.82%,68.18%),差异具有统计学意义(P <0.05),见表1。
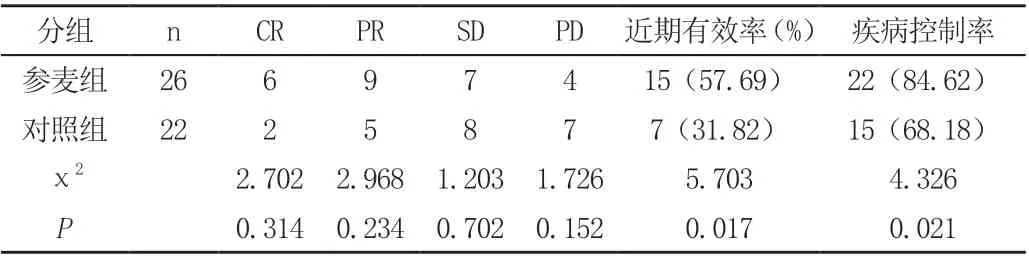
表1 两组近期疗效比较
2.2 两组化疗毒副反应比较
参麦组消化道不良反应、血液不良反应、疲乏衰弱、放射性肺炎、放射性食管炎、放射性皮炎和其他化疗毒副反应发生率均显著低于对照组,差异具有统计学意义(P <0.05),见表2。
2.3 两组治疗前后生存质量比较
两组治疗前生存质量KPS 评分比较,差异无统计学意义(P>0.05)。两组化疗结束后、生存质量KPS评分均显著低于治疗前,差异具有统计学意义(P <0.05);参麦组化疗结束后、随访3个月生存质量KPS 评分均显著高于对照组,差异具有统计学意义(P <0.05),见表3。
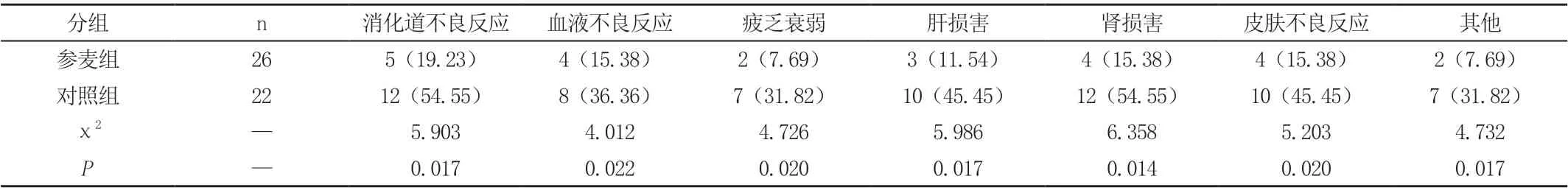
表2 两组化疗毒副反应比较[n(%)]
表3 两组治疗前生存质量KPS 评分比较(±s)
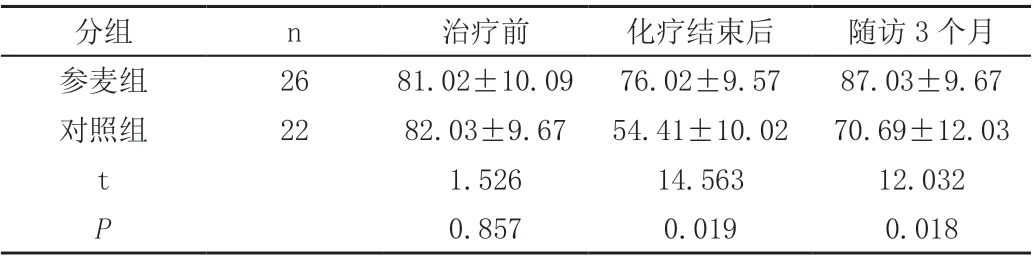
表3 两组治疗前生存质量KPS 评分比较(±s)
分组 n 治疗前 化疗结束后 随访3 个月参麦组 26 81.02±10.09 76.02±9.57 87.03±9.67对照组 22 82.03±9.67 54.41±10.02 70.69±12.03 t 1.526 14.563 12.032 P 0.857 0.019 0.018
3.讨论
食管癌早期无明显临床症状,因而较多患者错失早期治疗时机,确诊时已达到中晚期,无法实施手术治疗,或自愿放弃手术治疗,以化疗治疗为主,但是患者治疗期间极易出现多种毒副反应症状,影响治疗,患者生活质量下降显著,需提升治疗效果,降低毒副反应风险[4]。
参麦注射液为中药人参、麦冬的有效成分提取物,具有益气固脱,养阴生津、生脉之效,现代药理学研究发现,参麦注射液具有提高机体免疫力,促进受损组织再生、修复效果,有利于细胞活性提升,有利于减轻化疗引发的机体损伤[5]。恶性肿瘤临床治疗相关文献报道显示,参麦注射液与化疗药物联用时,可有效减轻患者化疗期间毒副反应,改善患者恶心呕吐、骨髓抑制、肝肾损害等毒副反应,多种毒副反应发生率可降低10%~60%,具有良好的“减毒”效果[6]。本次研究也发现参麦组消化道不良反应(19.23%)、血液不良反应(15.38%)、疲乏衰弱(7.69%)、放射性肺炎(11.54%)、放射性食管炎(15.38%)、放射性皮炎(15.38%)和其他化疗毒副反应发生率(7.69%)均显著低于对照组(54.55、36.36%、31.82%、45.45%、54.55%、45.45%、31.82%),可知联合参麦注射液可有效降低毒副反应风险。进一步追踪患者生存质量也显示,对照组化疗结束后、随访3 个月生存质量KPS 评分均显著低于治疗前,而参麦组化疗结束后、随访3 个月生存质量KPS 评分均显著高于对照组,可知参麦注射液改善了患者化疗后生存质量,预后改善效果可靠。此外,本次研究还发现,参麦组近期有效率(57.69%)、疾病控制率(84.62%)显著低于对照组 (31.82%,68.18%),提示联合参麦注射液治疗,有效提升了治疗效果,近期疗效可靠。
综上所述,化疗治疗中晚期食管癌基础上,联合参麦注射液治疗,可有效发挥“减毒增效”作用,具有临床应用价值。
