CaO对钛铁矿间接电解还原影响热力学研究
2020-03-26周忠仁
1 前言
在熔盐电解FeTiO3制备FeTi合金过程中,添加适量的CaO将有利于O2-的传输[1],进而加快阴极电脱氧速度。由于施加在电极两端的槽电压较大,熔盐中添加的CaO亦发生分解,并在阴极沉积出金属Ca。在高温下金属Ca能够还原阴极氧化物,促进阴极脱氧过程,该过程可以称为间接还原反应过程[2]。本文通过热力学计算着重分析CaO的加入对FeTiO3间接电解还原过程影响。
2 电解反应及热力学计算
钛铁矿在熔盐中生成的中间产物包括金属Fe、CaTiO3、Ti2O3、TiO、Ti、Fe2Ti和FeTi合金[3]。
为研究CaO的加入对FeTiO3的间接电解还原反应的影响,将熔盐中可能发生的电化学反应列入表1中,并将反应的吉布斯自由能和CaO活度的关系式列于表1中。
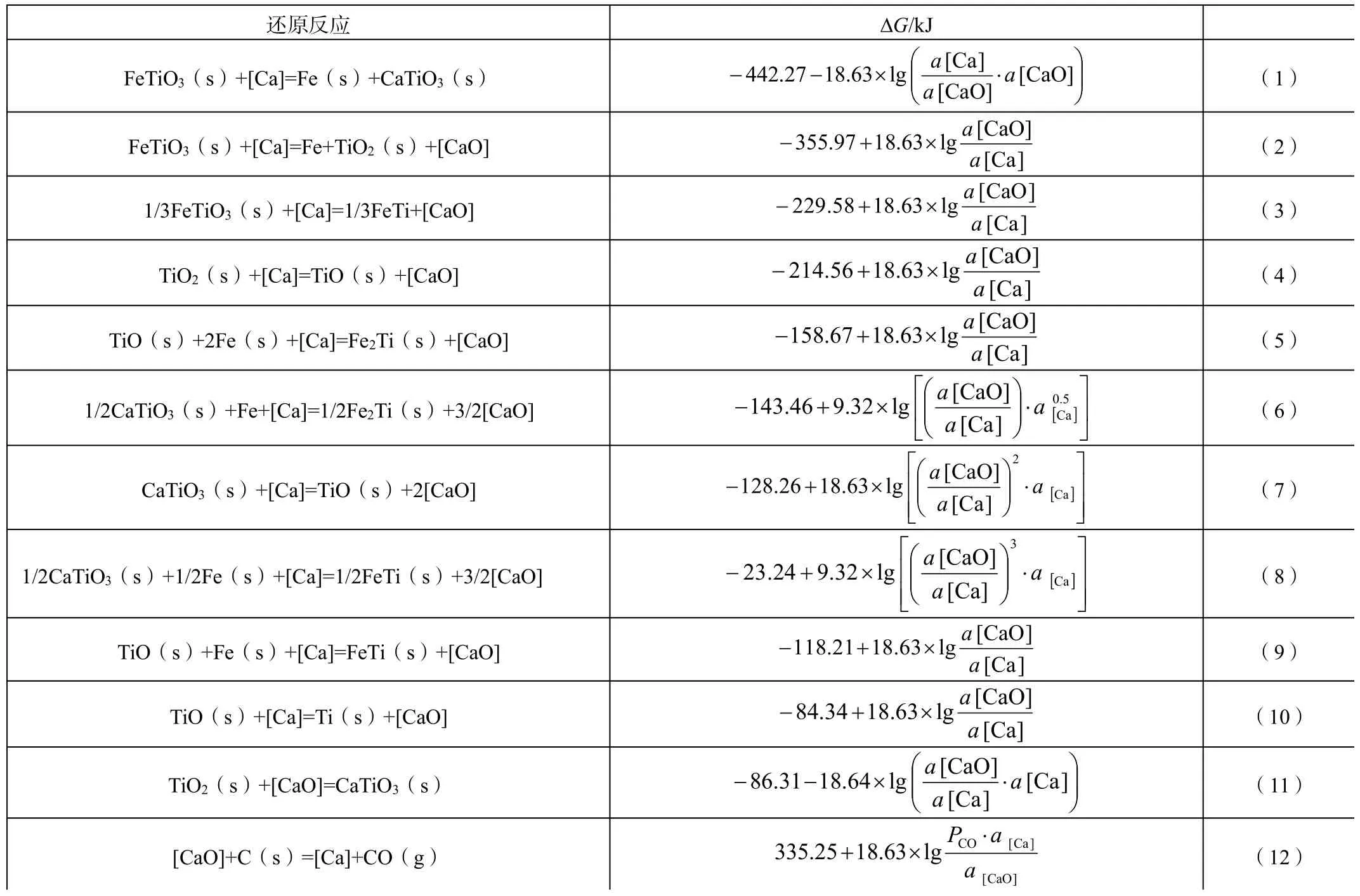
表1 间接原电极反应化学反应ΔG与CaO活度关系
3 结果与讨论
电解温度为699.85℃时,将钛铁矿间接电解还原过程中各中间产物的还原反应吉布斯自由能与CaO活度的关系列于表1。a[Ca]等于0.001时,反应吉布斯自由能ΔG与的关系如图1所示。假设阳极气体为CO,PCO=1。从图1可以看出,当a[Ca]等于0.001时,随着的增大,金属Ca还原FeTiO3生成单质Fe和CaTiO3的反应和TiO2与CaO反应生成CaTiO3反应的吉布斯自由能值为负,表明在此条件下更加容易生成CaTiO3,暗示了CaO活度的增大,有利于CaTiO3的生成。
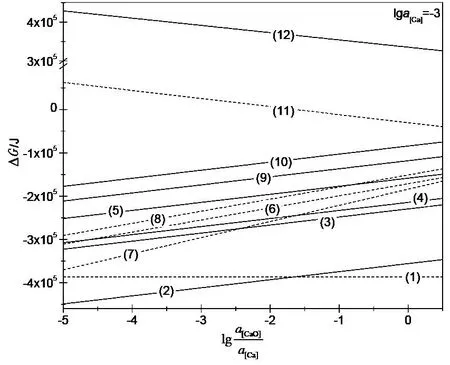
图1 当lga[Ca]为-3时,反应ΔG与的关系
对于CaTiO3的进一步电脱氧过程,随着的增大,图1中反应(6)~(8)的吉布斯自由能变得更正,说明CaTiO3的还原越难进行,其被金属Ca还原的趋势随着的增大而减弱。当增大后,CaO电解还原生成金属Ca的反应的吉布斯自由能负移,暗示了CaO的分解趋势更加明显。
4 结论
本文以CaCl2熔盐中电解还原FeTiO3制备钛铁合金(Fe2Ti和FeTi)为研究对象,分析了当熔盐中添加一定CaO后,CaO的电解脱氧对FeTiO3和中间产物CaTiO3电解还原反应吉布斯自由能的影响。根据热力学分析,随着CaO活度的增大,CaO的电脱氧生成金属Ca反应趋势增大,CaTiO3通过金属Ca还原FeTiO3生成的反应更容易进行,而金属Ca还原CaTiO3的反应趋势减弱。当增大熔盐中Ca的活度后,FeTiO3和CaTiO3的还原反应更容易。
