碳量子点/曙红Y比率型荧光探针测定L-抗坏血酸
2020-03-25武文波张越诚李承佳马红燕杨晓军
武文波, 张越诚, 李承佳, 马红燕, 杨晓军
(延安大学化学与化工学院 延安市分析技术与检测重点实验室, 陕西 延安 716000)
1 引 言
L-抗坏血酸(L-ascorbic acid,Ascorbic acid,AA)又称维生素C,是一种富含于水果和蔬菜中的水溶性维生素,也是维持机体正常生理功能的重要元素之一。AA在美白、组织修补、维持免疫功能、保持血管完整等过程中起着至关重要的作用,而长期缺乏AA则可能会引起败血症[1]。由于人体不能自身合成,只能从食物和药物中摄取,因此,对于食品药物中AA的分析具有重要意义[2]。目前,定量检测AA的方法有FTIR[3]、自动电位滴定[4]、HPLC[5]、紫外分光光度法[6]、动态比浊法[7]、伏安法[8]和荧光分析法[9]等。
碳量子点(CQDs)是一种新型的碳纳米功能材料,由于其显著的光学性能、低细胞毒性、良好的光稳定性、易于制备和环境友好等特性,在生物成像、光电催化、离子及药物检测等领域受到了广泛关注[10]。目前,基于CQDs的“关-开”型AA荧光探针已有课题组报道[11-12],但其信号仅基于单波长荧光强度信号检测。由于荧光强度易受外部环境(如温度、粘度)、仪器条件(如光散射、光漂白、背景光)等因素的影响,具有一定的波动性。而比率型荧光探针通常是将具有两种发射特性、不同发射波长的荧光材料构建成荧光探针,使用单一波长激发下的两个发射峰荧光强度比值的变化为信号,进行目标分析物的测定。两个峰的信号比值可以减小干扰从而提高分析的灵敏度和准确度[13-14]。因此,比率型荧光探针可广泛应用于化学传感、环境检测和生物分析等领域。目前,基于有机染料和半导体量子点比率荧光探针用于检测金属离子[15-16]、有机小分子[17]已有文献报道,但半导体量子点内在的细胞毒性、较差的水溶性和生物相容性限制了其进一步的发展和应用。CQDs的低毒性和环境友好性使其成为一种良好的替代品,但基于CQDs的比率型荧光分析法报道较少[18]。
本文以天然生物质去皮的蓖麻为碳源,只加入水,无需添加其他试剂,采用一步水热法合成了荧光性能良好的绿色蓖麻CQDs(CO-CQDs)。在紫外灯照射下,CO-CQDs的荧光发射峰位于405 nm处,呈蓝色荧光;而曙红Y(Eosin Y,EY)的荧光发射峰位于540 nm处,呈绿色荧光。CO-CQDs与EY可通过静电引力、疏水作用力与氢键作用紧密结合,形成具有双发射特性的CO-CQDs/EY比率型荧光探针,在紫外灯照射下,具有405 nm与540 nm两个发射峰。实验发现,Cr(Ⅵ)可显著猝灭CO-CQDs/EY复合物于540 nm/405 nm双发射峰处的荧光强度,而AA的加入仅可以使λem=540 nm处的荧光强度恢复,但λem=405 nm处的荧光强度基本不变。AA的浓度与该探针在540 nm/405 nm两处的荧光强度比值呈良好线性关系,可用于样品中AA含量的测定。
2 实 验
2.1 试剂与仪器
测试仪器:F-2700型荧光分光光度计(日本日立仪器有限公司);IR Prestige-21型傅里叶变换红外光谱仪(日本岛津仪器有限公司);HT7700型透射电镜(TEM)(日本日立仪器有限公司);FLSP920型瞬态稳态荧光光谱仪(英国爱丁堡仪器有限公司)。
EY(1.0×10-3mol/L):准确称取0.064 8 g EY,加入5.00 mL乙醇溶解,搅拌、超声后用水定容至100 mL容量瓶,置于冰箱 (4 ℃) 备用,使用时逐级稀释。
K2Cr2O7(6.0×10-3mol/L):准确称取0.176 5 g K2Cr2O7,加适量水溶解后转移至100 mL容量瓶,定容,摇匀,备用。
AA标准溶液(1.0×10-3mol/L):准确称取0.017 6 g AA标准品(广东光华科技股份有限公司),用水溶解,定容至100 mL容量瓶,置于冰箱 (4 ℃) 备用,使用时逐级稀释。
Na2HPO4-柠檬酸缓冲溶液(pH=4.00),蓖麻子去皮(市售),西红柿和柠檬采购于当地某农贸市场。
实验中所用水均是超纯水,所用试剂均为分析纯且没有进行任何后期处理。
2.2 CO-CQDs和CO-CQDs/EY复合物的合成
CO-CQDs的合成:将干净无杂质的蓖麻去皮、研碎,称取15.00 g置于50 mL有聚四氟乙烯内衬的高压釜中,加入30.00 mL水,180 ℃加热22 h。待高压釜冷却至室温,得到颜色为深棕色的CO-CQDs悬浮液,经滤纸、微孔滤膜(0.22 μm)依次过滤,定容至100 mL容量瓶,即得CO-CQDs溶液。稀释200倍得CO-CQDs工作液,备用。
CO-CQDs/EY复合物的制备:将7.00 mL CO-CQDs工作液和3.00 mL EY(5.0×10-5mol/L)溶液加入15.00 mL pH=4.00的Na2HPO4-柠檬酸缓冲溶液中,将混合物在室温下超声处理30 min后,即得CO-CQDs/EY复合物溶液。
2.3 基于CO-CQDs/EY比率型荧光探针的AA测定
向一系列10 mL比色管中依次加入1.00 mL CO-CQDs/EY复合物溶液、1.50 mL pH=4.00的Na2HPO4柠檬酸缓冲溶液、1.50 mL 6.0×10-3mol/L K2Cr2O7溶液以及不同浓度的AA溶液,用超纯水定容,摇匀,室温静置半小时,测定其在单一激发波长λex=320 nm下,λ405与λ540处的荧光强度,并计算其荧光强度比值I540/I405。
3 结果与讨论
3.1 CO-CQDs的性质表征
图1(a) CO-CQDs的透射电镜(TEM)图显示CO-CQDs呈规则的球形形态,平均粒径10 nm,且分散性好、无团聚现象。CO-CQDs的晶格形态可用XRD图谱(图1(b))表征,CO-CQDs在2θ为20.36°处有一个衍射宽峰,该峰为无定形态碳的特征峰,因此该CO-CQDs的晶型为无定型碳[19]。


图1 CO-CQDs的透射电镜图(a)和XRD谱(b),不同激发下的CO-CQDs的荧光发射谱(c)和红外光谱(d)。
Fig.1 Transmission electron micrograph(a), XRD spectrum(b), fluorescence emission spectra under different excitation(c) and FTIR spectra(d) of CO-CQDs.
3.2 基于AA测定的CO-CQDs /EY比率型荧光探针构建

随后,实验发现(图2),在320 nm的紫外光照射下,单独的CO-CQDs与EY的发射峰分别位于405 nm(黑线)与540 nm(红线)处。而CO-CQDs/EY复合物出现了两个发射峰(蓝线),分别位于405 nm与540 nm处,这分别显示出CO-CQDs和EY的特征峰,相较单一CO-CQDs与EY,CO-CQDs/EY复合物发射峰位置没变,荧光强度略有降低,进一步说明CO-CQDs与EY二者之间有相互作用发生。二者复合实现了用单一波长激发而得到两个荧光发射峰的设想。
进一步实验表明,于CO-CQDs/EY溶液中加入Cr(Ⅵ)时,Cr(Ⅵ)可以与CO-CQDs/EY复合物相结合,形成有效的电子转移[24],使CO-CQDs/EY 405 nm与540 nm处的荧光强度均显著降低(图2绿线),形成双猝灭。FLSP920型瞬态稳态荧光光谱寿命拟合结果显示,CO-CQDs/EY和CO-CQDs/EY-Cr(Ⅵ)的加权平均荧光寿命[25]分别为1.65 ns和1.69 ns,τ0/τ≈1,表明Cr(Ⅵ)与CO-CQDs/EY体系之间是以静态猝灭的方式相互作用的。

图2 不同物质结合的荧光发射谱
Fig.2 Fluorescence emission spectra of different component
于CO-CQDs/EY- Cr(Ⅵ)体系中加入AA后(图2粉线),EY的荧光逐渐恢复,而CQDs的荧光强度基本保持不变。图3(a)为Cr(Ⅵ)与AA作用的紫外-可见吸收光谱,由图可知,于Cr(Ⅵ)溶液中加入AA,Cr(Ⅵ)和AA之间可发生电子转移的氧化还原反应,使Cr(Ⅵ) 349 nm处的吸收峰消失。由于AA与Cr(Ⅵ)反应,AA可将Cr(Ⅵ)从CO-CQDs/EY复合物的表面脱落下来,阻隔了Cr(Ⅵ)与CO-CQDs/EY的反应。由于EY是包裹在CO-CQDs的周围,所以其表面的Cr(Ⅵ)首先脱落下来,EY荧光恢复,其恢复程度与AA浓度呈线性关系(图3(b)),而CQDs荧光强度不变,从而实现了用于检测AA的比率型荧光探针的构建。该方法的基本原理如图4所示。

图3 Cr(Ⅵ)-AA体系的紫外-可见吸收光谱(a)和CO-CQDs/EY与不同浓度AA溶液作用的荧光发射光谱(b)
Fig.3 UV-Vis absorption spectra of Cr(Ⅵ)-AA systems(a) and fluorescence emission spectra of CO-CQDs/EY interaction with different concentrations of AA solutions(b)

图4 CO-CQDs比率型荧光探针作用机理图
3.3 测定条件的优化
3.3.1 酸度、缓冲溶液的种类及用量的影响
在不同酸度环境中,CO-CQDs和EY有不同的形态和存在型体,因此酸度对其荧光性质有很大的影响。试验了不同酸度对CO-CQDs/EY体系的影响,如图5所示,其荧光强度比值I540/I405在pH为3.78~9.00的范围内保持恒定,因此,实验选择体系的酸度为4.00。此外,考察了HAc-NaAc、Na2HPO4-柠檬酸、柠檬酸-柠檬酸钠和BR等缓冲溶液种类和缓冲溶液的用量对体系I540/I405的影响。结果表明,加入1.50 mL pH=4.00的Na2HPO4-柠檬酸缓冲溶液时,I540/I405值最佳。

图5 CO-CQDs/EY、CO-CQDs/EY-Cr(Ⅵ)、CO-CQDs/EY-Cr(Ⅵ)-AA的pH值优化图。
Fig.5 pH optimization of CO-CQDs/EY, CO-CQDs/EY-Cr(Ⅵ), CO-CQDs/EY-Cr(Ⅵ)-AA.
3.3.2 Cr(Ⅵ)用量的影响
考察了Cr(Ⅵ)用量对体系的影响。结果表明,Cr(Ⅵ)用量太少,反应不完全,荧光响应值小;Cr(Ⅵ)用量过大,影响荧光恢复的效率。试验了Cr(Ⅵ)溶液用量在0.1~2.0 mL范围内对体系荧光强度比值I540/I405的影响,如图6所示,实验选择Cr(Ⅵ)溶液用量为6.0×10-3mol/L 1.50 mL。
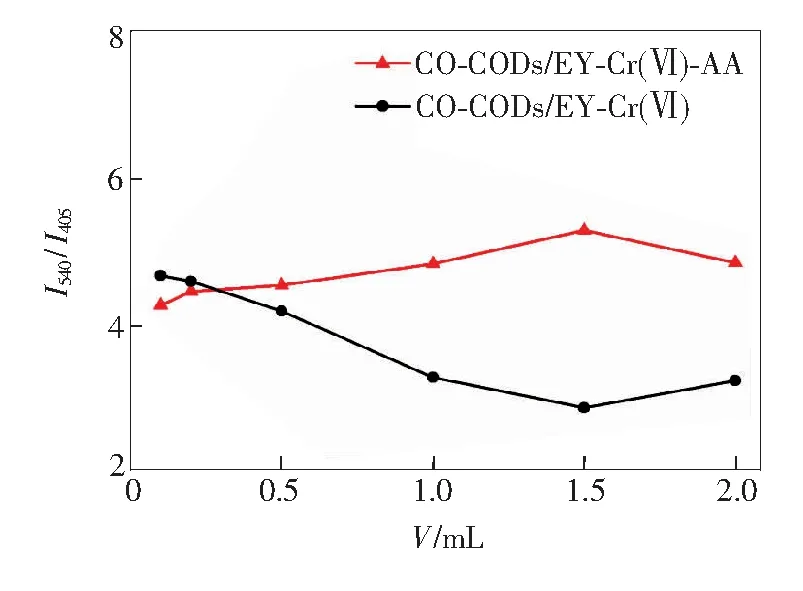
图6 Cr(Ⅵ)的用量对CO-CQDs/EY-Cr(Ⅵ)和CO-CQDs/EY-Cr(Ⅵ)-AA体系的影响
Fig.6 Effect of Cr(Ⅵ) amount on CO-CQDs/EY-Cr(Ⅵ) and CO-CQDs/EY-Cr(Ⅵ)-AA system
3.3.3 反应温度的影响
实验考察了不同温度对体系荧光强度比值I540/I405的影响,结果表明,加热对体系无任何增敏作用,实验选择不进行加热。
3.3.4 体系的稳定性
实验研究了不同的反应时间对体系荧光强度比值I540/I405的影响,如图7所示。结果表明,CO-CQDs/EY体系的荧光信号比值在室温下反应30 min可达稳定,且在7.5 h内保持不变。

图7 反应时间对体系的影响
3.4 检出限及线性范围
在优化的实验条件下,AA浓度在5.0×10-8~4.0×10-6mol/L范围内与CO-CQDs/EY体系位于两发射波长处荧光强度的比值I540/I405呈良好线性关系,线性方程为I540/I405=2.51+9.3×105c(mol/L),r=0.993 9,对浓度为1.0×10-6mol/L的AA进行5次平行测定,相对标准偏差为0.85%。
根据IUPAC规定,方法检出限σ=3S/K=3.7×10-8mol/L。
3.5 共存物质的影响

3.6 实际样品分析
3.6.1 药片中AA含量的测定
随机抽取同一批次的维生素C 10片(规格:0.1 g),研磨成粉,准确称取适量粉末(相当于0.017 6 g AA),加水溶解,超声后定容至100 mL容量瓶,摇匀、静置10 min后过滤。准确移取滤液适量,按照实验方法进行测定,同时进行加标回收实验。结果见表1。

表1 药片中AA测定及回收率实验(n=5)
注:1. 广东恒健制药有限公司,产品批号:H44021171;2. 西安利君制药有限责任公司,产品批号:1804176030。
3.6.2 水果和蔬菜中AA的测定
将新鲜蔬菜西红柿和水果柠檬去皮取果肉,分别称20 g置于研钵中,各加少许石英砂和20 mL 0.001% HCl充分研磨至匀浆,双层纱布过滤至50 mL容量瓶中,0.001% HCl反复浸洗残渣并滤入容量瓶,0.001% HCl定容[26],混匀,稀释100倍备用。取1.00 mL待测果蔬提取液,按照实验方法进行测定,同时进行加标回收实验,结果见表2。

表2 水果和蔬菜中AA的测定(n=5)
4 结 论
本文构建了一种基于AA高灵敏度检测的CO-CQDs/EY复合物比率型荧光探针。以天然生物质蓖麻为前驱体一步水热法合成了绿色荧光CO-CQDs,与荧光极强的卤代荧光素染料EY复合,二者形成了荧光发射峰相距较远的新型CO-CQDs/EY复合物。基于Cr(Ⅵ)的加入可使复合物405 nm/540 nm处的荧光发生双猝灭、而AA只使540 nm处的荧光有恢复作用的现象,实现了基于CO-CQDs/EY双发射比率型荧光探针对AA的测定。该体系简单、灵敏,有效消除了荧光测定的背景干扰,为AA测定提供了新方法,为碳量子点在分析化学领域的应用提供了新思路。
