水体中邻苯二甲酸酯的光催化降解
2020-03-25梁大鹏聂林春方媛萍
梁大鹏, 聂林春, 方媛萍, 姜 旭, 宁 杨
(吉林大学 地下水资源与环境教育部重点实验室, 新能源与环境学院, 长春 130012)
邻苯二甲酸酯(phthalate esters, PAEs)是一类人工合成的有机物, 在农业、 建筑和化工等领域应用广泛[1-2]. PAEs与基质中的聚合物以非共价键-键结合, 由氢键或范德华力连接, 在生产和使用过程中可从聚合物基质中浸出而进入环境, 导致环境污染, 损害生物和人体健康[3-5]. PAEs半衰期较长, 在环境中不易降解, 但目前其仍为市场上使用最广泛的塑化剂[6-8].
光催化氧化法可将有毒有害污染物去除或转化为低毒害物质, 是一种常用的污染去除方法. 其中TiO2是使用最广泛的光催化剂, 其价格低、 稳定性较好且可有效去除大多数污染物[9-10]. 与纯TiO2相比, TiO2复合材料具有更强的光催化性能, 在TiO2上负载少量Fe,Ag,Cu,Zn等重金属可使其具有更优异的性能[11-13].
目前, 催化剂的选择和用量、 光照条件和pH值等对PAEs光催化降解效果的影响研究报道较多, 对PAEs光催化降解机理及反应历程的研究报道较少. 基于此, 本文以地表水中检出量和检出率较高的4种邻苯二甲酸酯(邻苯二甲酸二甲酯(DMP)、 邻苯二甲酸二乙酯(DEP)、 邻苯二甲酸二丁酯(DBP)和邻苯二甲酸二(2-乙基己基)酯(DEHP))[14]为研究对象, 以含CuO质量分数为5.0%的TiO2(记为5.0%CuO/TiO2)为光催化剂, 用电喷雾萃取电离质谱法(EESI-MS)考察光照条件、 体系初始pH值、 光催化剂用量对PAEs降解效率的影响, 分析光催化最优反应条件及反应动力学模型, 并以产量最大、 使用最广泛的DBP[15]为例探讨其可能的光催化降解机理及反应历程.
1 材料与方法
1.1 仪器与试剂
高分辨率质谱仪(美国赛默飞公司), 配有Xcalibur 3.0数据处理系统; 电喷雾萃取电离离子源(吉林大学无机合成与制备国家重点实验室制备); 超声清洗器(KQ5200E型, 昆山市超声仪器有限公司); 控温磁力搅拌器(18-1型, 金坛市正基仪器有限公司); 马弗炉(RJX-5-13型, 天津实验炉厂); pH计(pHS-3C型, 上海仪电科学仪器股份有限公司).
邻苯二甲酸二甲酯(DMP)、 邻苯二甲酸二乙酯(DEP)、 邻苯二甲酸二丁酯(DBP)和邻苯二甲酸二(2-乙基己基)酯(DEHP)(均为分析纯, 上海国药集团化学试剂有限公司); 甲醇(色谱纯, 美国Fisher公司); 乙酸(色谱纯, 天津光复科技有限公司); TiO2(P-25, 德国Degussa公司); CuO(化学纯, 美国阿拉丁试剂公司); HCl和NaOH(化学纯, 北京化工厂).
1.2 方 法
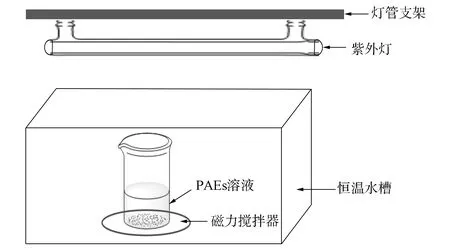
图1 光催化反应实验装置示意图
1.2.1 光催化反应实验 光催化反应实验装置如图1所示, 反应体系由烧杯、 紫外灯、 恒温水槽和控温磁力搅拌器组成. 实验过程中, 分别配制质量浓度为1 mg/L的4种PAEs水样各1 L, 用HCl和NaOH调节体系pH值, 加入适量光催化剂, 用磁力搅拌器使反应溶液充分混合. 反应过程中打开紫外灯, 每隔60 min取样一次, 用EESI-MS测定过0.45 μm微孔滤膜后的水样.
1.2.2 光催化剂制备 以TiO2为载体, CuO为前驱体, 用湿法浸渍法合成光催化剂[16]. 分别称取0.950 g TiO2粉末与0.05 g CuO粉末, 加入适量去离子水, 超声混合30 min使其分散均匀. 在烘箱中于110 ℃烘干6 h, 先将干燥后的产物研磨, 过200目筛, 再于马弗炉中500 ℃煅烧活化5 h, 即得含CuO质量分数为5.0%的TiO2光催化剂, 记为5.0%CuO/TiO2.
1.2.3 质谱检测条件 设置电喷雾萃取电离质谱的检测模式为正离子模式, 全扫描范围m/z为100~300/400. ESI电压为3.0 kV, 离子传输管温度为300 ℃, 雾化气体为体积分数99.999%的N2, 样品溶液流速为8 μL/min, 电喷雾溶液(V(甲醇)∶V(水)∶V(乙酸)=2∶2∶1), 流速为4 μL/min. 在定量分析时, 设置碰撞诱导解离(CID)实验的碰撞时间为30 ms, 能量为20%~30%, 其他参数由系统自动优化.
1.2.4 光催化降解机理实验 以DBP为例, 用EESI-MS检测DBP光催化降解0~5 h的样品溶液, 获得反应溶液的全扫描质谱数据. 将获得的数据用MATLAB软件归一化处理后, 用SIMCA软件进行偏最小二乘法判别分析(PLS-DA), 获得样品溶液的组分信息. 利用质谱数据库分析各质谱峰所代表的物质.
1.3 数据分析
用差减法计算PAEs的光催化降解率,t时刻PAEs的光降解率为
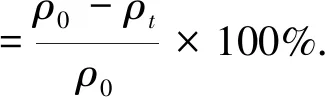
(1)
用一级动力学模型描述PAEs的降解过程[17], PAEs在t时刻的质量浓度和初始质量浓度与时间t的关系为
-ln(ρt/ρ0)=k×t,
(2)
其中:ρ0为PAEs初始的质量浓度;ρt为PAEs在t时刻的质量浓度;k为一级速率常数.
2 结果与讨论
2.1 CuO/TiO2催化剂表征

图2 5.0%CuO/TiO2复合材料的SEM照片
2.1.1 扫描电镜表征 湿法浸渍法合成5.0%CuO/TiO2光催化剂的扫描电子显微镜(SEM)照片如图2所示. 由图2可见, CuO/TiO2复合材料的形态为不规则且分散的细颗粒, 粒径约为50~100 nm.
2.1.2 X射线衍射表征 纯TiO2与5.0%CuO/TiO2复合材料的XRD谱如图3所示. 由图3可见, 纯TiO2最强的3个特征衍射峰分别位于25.48°,37.96°,48.2°处, 5.0%CuO/TiO2最强的3个特征衍射峰分别位于25.26°,37.74°,47.98°处, 复合材料与纯TiO2的特征衍射峰位置基本一致, 即掺杂CuO未改变纯TiO2的晶型结构, 推测CuO是以高分散状态覆盖在TiO2表面. 但掺杂CuO使锐钛矿型的TiO2峰强增加, 从而使其具有更高的光催化活性.
2.1.3 红外光谱表征 CuO/TiO2复合光催化材料的红外光谱如图4所示. 由图4可见, 湿法浸渍法合成的催化剂在523,620,1 627,3 401 cm-1处存在吸收峰, 分别由Cu—O,Ti—O,H—OH,O—H键的伸缩振动形成.

图3 TiO2与5.0%CuO/TiO2复合材料的XRD谱

图4 5.0%CuO/TiO2复合材料的红外光谱
2.2 影响PAEs光催化降解的因素
2.2.1 光照条件 紫外光(UV)及暗反应条件对PAEs去除率的影响如图5所示. 由图5可见: 在避光条件下, 仅DMP发生降解, 去除率为3.25%, DEP,DBP和DEHP几乎未降解; 在紫外光照条件下, 4种PAEs均发生降解. 因此, 4种PAEs在紫外光作用下远大于暗反应条件下的去除率.

图5 光照条件对PAEs去除率的影响
2.2.2 体系初始pH值 不同体系初始pH值对PAEs去除率的影响如图6所示. 由图6可见, 4种PAEs在中性偏酸的条件下去除率较好, 当pH=6时, 4种PAEs的去除率最高. 这是由于TiO2催化剂在弱酸性条件下可产生更多的活性基团, 提高了污染物的去除率[18]所致.
2.2.3 催化剂的质量浓度 CuO/TiO2催化剂质量浓度对PAEs去除率的影响如图7所示. 由图7可见, 在一定范围内增加催化剂的质量浓度可增大PAEs的去除率, 这是因为随着反应体系中催化剂质量浓度的增大, 溶液内分布的催化活性点位增多, 易产生活性基团, 进而促进了PAEs降解. 进一步增加催化剂的质量浓度, PAEs的去除率下降, 原因为: 1) 由于催化剂的质量浓度增大, 使其在溶液体系内发生团聚, 比表面积减小, 导致催化剂表面活性点位减少, 因此PAEs的去除率下降[19]; 2) 反应体系中分散催化剂的质量浓度增大, 使紫外光在反应体系中穿透能力下降, 导致PAEs去除率下降.

图6 不同体系初始pH值对PAEs去除率的影响
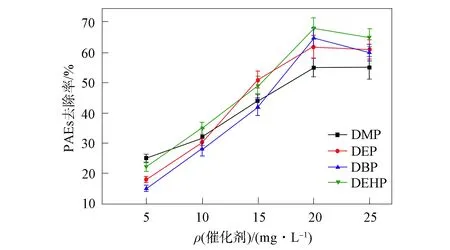
图7 光催化剂的质量浓度对PAEs去除率的影响
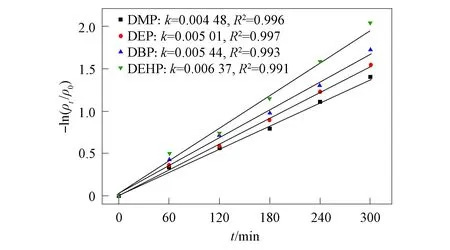
图8 PAEs光催化降解的伪一级动力学拟合方程
2.3 PAEs光催化降解动力学
4种PAEs的光催化降解动力学均可用一级动力学方程描述, 结果如图8所示, 其中一级反应动力学方程的斜率即为反应速率常数. 由图8可见, 4种PAEs的光催化降解反应速率随烷基链含碳数的增加而增大, 分子量越大的PAEs降解速率越快. 这是由于随着烷基链长度的增加, 酞酸酯对紫外光的稳定性下降所致.
2.4 DBP光催化降解机理及历程
用PLS-DA法处理数据, 对比DBP光催化降解0~5 h反应体系组分的变化. DBP光催化降解0~5 h质谱数据的PLS-DA分析结果如图9所示. 其中, 根据反应时间分别记为DBP0~DBP5, 每个样品平行3次实验, 分别记为DBPi-1~DBPi-3(i=0,1,…,5). 由图9可见, DBP光催化降解反应体系组分发生了显著变化. DBP光催化降解的中间产物列于表1. 其中VIP值可反映样品物质质荷比对样品区分的贡献大小, VIP值>1.0表示物质荷质比对样品区分的贡献较大. 由表1可见,m/z283.2,m/z223.1,m/z179.1,m/z167.1,m/z149.0,m/z123.1,m/z117.1等物质差异显著, 其中邻苯二甲酸单丁酯、 苯甲酸丁酯、 邻苯二甲酸和苯甲酸为主要中间产物. 本文比文献[20]给出了更详细的降解路径.
表1 DBP光催化降解的中间产物
Table 1 Intermediates of photocatalytic degradation of DBP
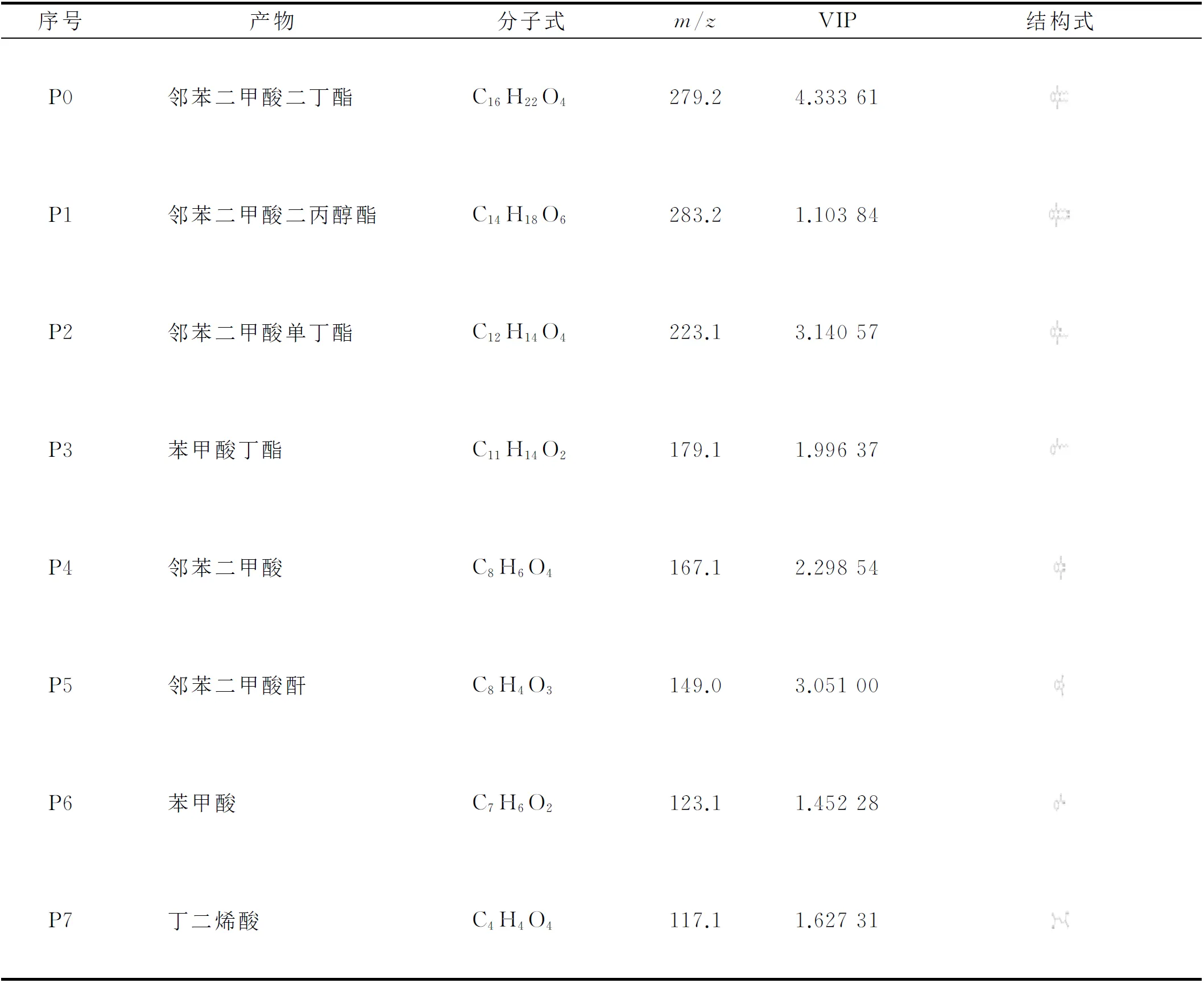

图9 DBP光催化降解的PLS-DA分析结果
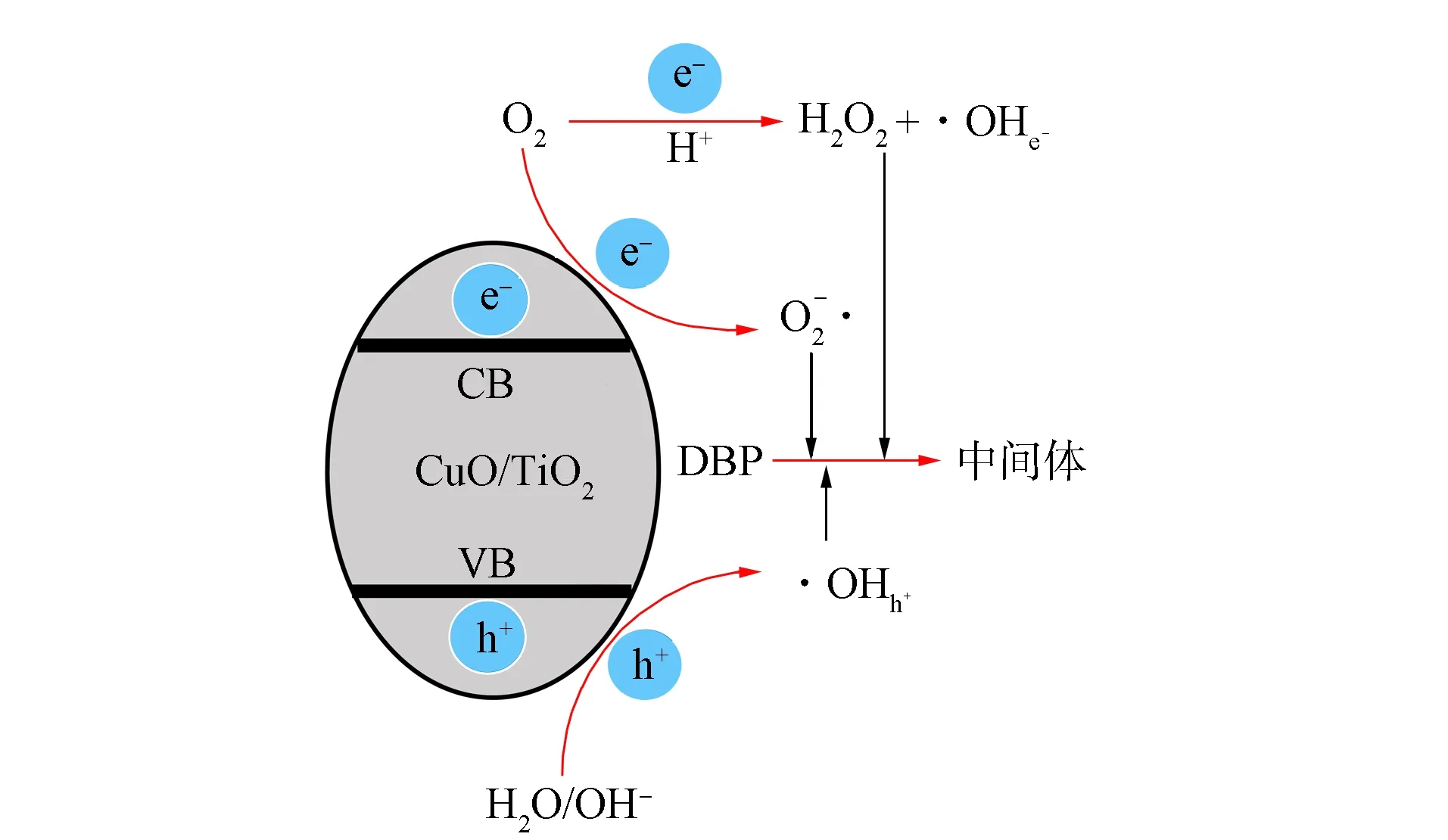
图10 DBP光催化降解的反应机理
在紫外光作用下, CuO/TiO2催化剂对PAEs的去除效果较好, 其反应机理如图10所示. 由图10可见: 在紫外光作用下, CuO/TiO2受激产生的电子-空穴对向表面迁移, 空穴与催化剂表面的H2O或OH-反应生成羟基自由基(·OHh+); 电子与表面吸附的O2反应生成超氧自由基(·O2-)或电子和O2与催化剂表面的H+反应生成过氧化氢(H2O2)和羟基自由基(·OHe-). 反应过程中生成的活性氧自由基基团均对DBP光降解具有催化氧化作用, 其光催化降解表达式为
由中间产物及反应机理推测DBP光催化降解的可能历程, 如图11所示. 在紫外光作用下, 首先催化剂产生的·OH等活性氧基团攻击DBP的长碳链, 生成邻苯二甲酸二丙醇酯(m/z283.2)、 邻苯二甲酸单丁酯(m/z223.1)和苯甲酸丁酯(m/z179.1); 然后中间产物(P1,P2,P3)被活性氧自由基基团氧化, 生成邻苯二甲酸(m/z167.1)、 邻苯二甲酸酐(m/z149.0)和苯甲酸(m/z123.1); 最后活性氧基团将邻苯二甲酸和苯甲酸等分解为小分子的丁二烯酸(m/z117.1).

图11 DBP光催化降解反应的历程
3 结 论
1) 湿法浸渍法合成的5.0%CuO/TiO2催化剂可有效降解4种PAEs, 在紫外光作用下, 当体系初始pH=6, 催化剂质量浓度为20 mg/L时, 降解效果最好.
2) PAEs的光催化降解反应可用一级反应动力学模型拟合, 且降解速率随烷基链增长和分子量的增大而加快.
3) DBP在紫外光作用下催化降解的产物包括邻苯二甲酸二丙醇酯、 邻苯二甲酸单丁酯、 苯甲酸单丁酯、 邻苯二甲酸、 苯甲酸、 邻苯二甲酸酐和丁二烯酸等.
