生物质碳点敏化超薄g-C3N4的表征及其对四环素的光催化降解1)
2020-03-25滕敏姜晓娜胡梦琴姚忠强李姣黄占华
滕敏 姜晓娜 胡梦琴 姚忠强 李姣 黄占华
(生物质材料科学与技术教育部重点实验室(东北林业大学),哈尔滨,150040)
四环素类抗生素(TCs)作为广谱抗生素,由于其具有促进动物生长和预防疾病等作用,被广泛应用于畜牧业以及水产养殖业。但TCs难以被动物肠胃吸收,高达90%的TCs以母体化合物形式通过尿液和粪便排出,通常直接释放到水环境中,对人体健康和生态系统平衡产生负面影响。四环素在不同的水体环境中的半衰期为4.5~180.0 d,在酸性条件下很稳定,因此,四环素会在重复施肥过程中发生累积,不仅会造成水体污染甚至引发抗生素耐药病原体的产生进而蛰伏威胁人类健康问题,所以开发低成本、高效率和高效益的处理技术迫在眉睫[1-2]。
目前处理TCs的方法主要有物理法、化学法和生物法。物理法中较为成熟的技术有离子交换法、膜技术及吸附法,其中离子交换法存在对TCs的去除率较低,膜技术和吸附法对TCs的处理不够彻底等问题[3-4];生物处理法以植物吸收TCs和微生物降解TCs为主要手段,贺德春等[5]研究发现小白菜和白萝卜等植物对四环素类抗生素的吸收积累特征,但吸收效果并不理想,在微生物作用下,抗生素残留物的结构和理化性质发生改变,从大分子化合物降解为小分子化合物,最终转变为水和二氧化碳,但是微生物培养过程复杂,成本较高;化学法主要包括络合法、氧化法和光催化降解等处理方法。其中,络合法处理过程不稳定,受初始浓度及环境酸碱性等因素的影响较大,而四环素类抗生素的强氧化降解往往受pH值和强氧化剂浓度的显著影响,且氧化剂不易回收,排放的强氧化剂会对环境造成破坏,所以,当前研究最广泛且最深入的是光催化降解TCs处理技术[1]。光催化降解技术中研究较为成熟的是以二氧化钛(TiO2)或氧化锌(ZnO)作为半导体催化剂来降解TCs,但ZnO(3.3 eV)和TiO2(3.2 eV)存在带隙较宽、太阳光利用率低(仅为4%)以及成本较高等缺点[6-7]。石墨比氮化碳(g-C3N4)更具有禁带狭窄(2.7 eV)、化学稳定性好、催化活性高以及廉价易得等优点,被认为是理想的光催化剂[8-9]。碳量子点的能带可调节、具有上转换发光和电子转移的特性,因此在光催化领域得到了广泛应用[10]。与贵金属纳米颗粒相比,碳量子点(CDs)作为一种新型的纳米碳,在具有良好的电子传递性能和广泛的光谱吸收性能[11-12],是光催化剂设计中的多功能组件。
本文以三聚氰胺、生物质碳量子点为原料通过简单的高温煅烧法合成了一种碳量子点敏化超薄氮化碳(CQDs/g-C3N4)复合材料,并将其用于光催化剂降解水中的TCs,来评价CQDs/g-C3N4复合材料的光催化活性和可见光光催化效率,并探索其光催化机理,以此为新型光催化材料的开发与利用提供理论基础数据。
1 材料与方法
主要试剂和仪器:生物质碳量子点(CQDs)(实验室自制);三聚氰胺、氯化铵、TC、L-赖氨酸。其它试剂皆为分析纯,实验室用水均为去离子水。紫外可见分光光度计(UV-vis)、X-射线衍射仪、傅里叶变换红外光度计(FT-IR)、透射电子显微镜(TEM)比表面积分析仪(BET)、氙灯光源系统。
1.1 CQDs/g-C3N4的合成
将三聚氰胺(C3H6N6)和氯化铵(NH4Cl)分别按照m(C3H6N6)∶m(NH4Cl)=1∶0、m(C3H6N6)∶m(NH4Cl)=12∶1、m(C3H6N6)∶m(NH4Cl)=6∶1、m(C3H6N6)∶m(NH4Cl)=4∶1、m(C3H6N6)∶m(NH4Cl)=3∶1和m(C3H6N6)∶m(NH4Cl)=2∶1的比例在一定温度下溶解共混,干燥后放入马弗炉中高温加热到550 ℃,煅烧4 h。冷却后,研磨得到不同制备条件的g-C3N4黄色粉末。将一定质量的CQDs加入到g-C3N4(m(C3H6N6)∶m(NH4Cl)=3∶1)中,将两者混合均匀,然后再进行干燥、高温煅烧,获得CQDs/g-C3N4光催化复合材料,记为CSN。
1.2 光催化活性试验
将0.1 g的光催化剂CSN加入到100 mL 20 mg/L的四环素(TC)水溶液中。采用300 W的Xe灯为光源,用滤光片过滤掉波长小于420 nm的紫外光,黑暗中搅拌30 min,以确保吸附平衡的建立。开灯后,在一定的时间间隔内提取3 mL的溶液,每次取出的样品用14 000 r/min的高速离心机离心分离20 min,将光催化剂CSN与溶液分离,取上层清液,采用紫外—可见分光光度计在335 nm处对上清液进行测定分析,根据吸光度来判断光催化剂CSN对TC溶液的降解效率。
1.3 光催化循环试验
将1.2试验中催化效果最理想的一组光催化剂CSN进行光催化性能循环试验测定,按上述光催化活性实验的步骤,将CSN进行重复使用用于光催化降解TC,共重复使用5次,记录每次光催化降解TC的实验结果,根据吸光度来计算催化剂CSN对TC溶液的重复降解效率并判断催化剂CSN的稳定性。
2 结果与分析
2.1 透射电子显微镜(TEM)分析
图1a为N-CQDs的TEM图。N-CQDs的纳米粒子均匀分布,在水相中有均匀的分散,粒径分布在2~5 nm,CQDs分布均匀和纳米颗粒的聚集[13-14]。N-CQDs较丰富的含氧官能团。加入NH4Cl后,g-C3N4形成了二维纳米多孔薄纱状类石墨烯结构(如图1b),这是因为NH4Cl在高温的分解过程中产生大量的氨气和HCl。连续折叠状结构变成小片状的薄纱结构,可能是体相g-C3N4的结构被破坏,并在气体的作用下进一步的剥离,形成体积较小的薄片结构[15-16]。N-CQDs分散在g-C3N4的薄片上(图1c),N-CQDs和g-C3N4形成异质结构,有利于界面电子的转移,增强光催化性能。
2.2 傅里叶变换红外光度计(FT-IR)分析
图2a为N-CQDs、g-C3N4,添加不同含量N-CQDs的CSN的FT-IR谱图。从图2a中可以看出g-C3N4在1 236(C—N)、1 312(C—N)、1 397(C—N)、1 412(C—N)、1 574(C=N)和1 636(C=N)cm-1处的振动峰对应典型的CN杂环的特征吸收峰[14,17]。在802 cm-1处的尖峰则是三嗪单元的拉伸振动峰,在3 200 cm-1的特征吸收峰是g-C3N4中—NH的拉伸振动峰。图2a中可以看出N-CQDs表面上存在一些特征官能团,包括—NH—基团的吸收峰(3 200 cm-1),—CH—拉伸振动的吸收峰2 869和2 937 cm-1,—CONH—基团特征吸收峰的1 651和1 567 cm-1,—CO—基团的特征吸收峰在1 376和1 022 cm-1,在1 709 cm-1处是C=O(羰基)的吸收峰,而在1 120 cm-1处是C—O—C(醚键)的吸收峰[18]。对比图2中各谱线可知,N-CQDs的特征峰值(3 200(N—H),1 651和1 567(—CONH—)cm-1)包含在CSN的特征峰值结构中,C=O(1 709 cm-1)和C—O—C(1 120 cm-1)的吸收峰被CSN中其它特征峰掩盖,表明了N-CQDs与g-C3N4成功地进行了复合。
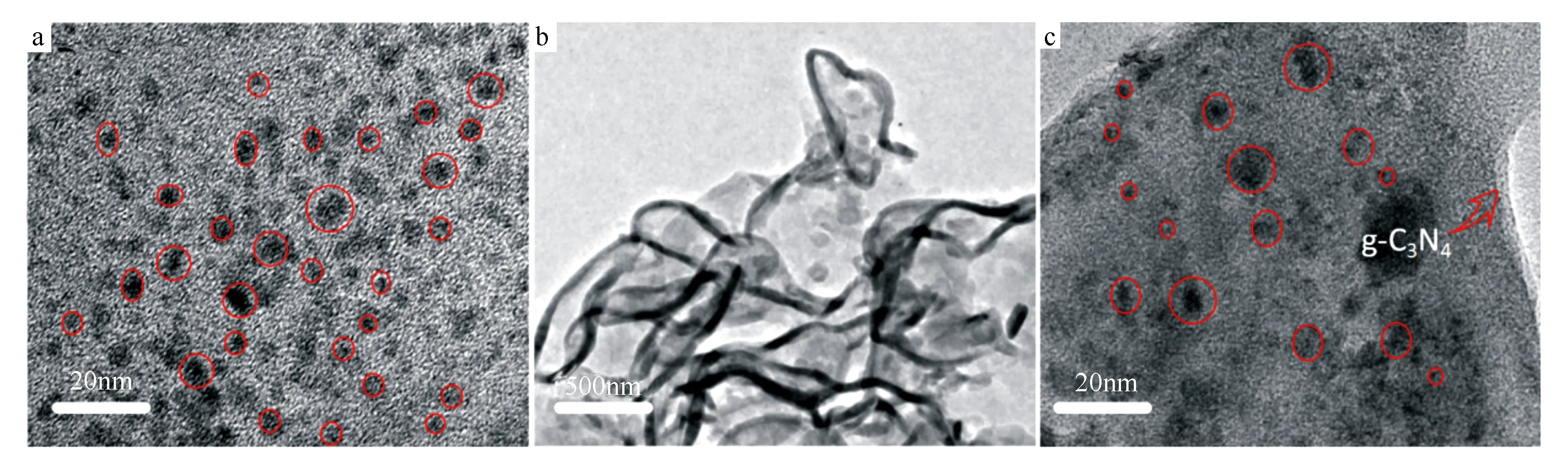
a.N-CQDs b.g-C3N4c.0.5% CSN。
图1各样品的TEM图
2.3 X-射线衍射(XRD)分析
图2b为g-C3N4和不同N-CQDs质量分数的CSN复合材料的样品XRD图。13.1°和27.3°是g-C3N4的特征衍射峰(JCPDS#87-1526)[19-20]。在2θ=13.1°处的衍射峰与g-C3N4的三嗪环单元的平面结构层(110)对应。而27.3°处的峰型尖锐且峰窄,与g-C3N4为层状堆叠结构(002)晶面的衍射峰一致。N-CQDs的衍射峰在2θ=21.7°处较尖锐,不同质量分数的N-CQDs的加入,并没有引起g-C3N4的晶型结构[20-22]。通过谱图可以看出,CSN在21.7°处有衍射峰,说明N-CQDs已经成功加入到g-C3N4中。随着N-CQDs质量分数的增加,(100)和(002)的衍射峰减弱,可能是N-CQDs的加入有效的阻止了三聚氰胺的聚合g-C3N4纳米片的堆积。同时,在CSN的XRD图谱中,CQDs的衍射峰较弱,这可能是由于N-CQDs纳米粒子质量分数较低引起的。
2.4 紫外可见分光光度(UV-vis)分析
由图2c可知,所有样品具有相似的光吸收光谱,经N-CQDs修饰后,样品在可见光区吸收增强。g-C3N4的光吸收截止波长约456 nm处,与文献报道结果相似[14]。与g-C3N4相比,0.5% CSN的光吸收有轻微的红移,显著增强了光谱响应能力,拓宽了对可见光的吸收范围。通过Kubellka-Munk公式[23]:
(αhv)1/n=A(hv-Eg)。
(1)
其中,α为吸光系数,h为普朗克常数,v为频率,A为常数,Eg能带间隙,n代表过渡半导体的类型(直接半导体n=1/2;间接半导体n=2)。经过计算后,g-C3N4的带隙为2.72 eV,0.5% CSN的带隙为2.69 eV。半导体的价带和导带计算公式[24]:
ECB=X-Ee-0.5Eg。
(2)
EVB=ECB+Eg。
(3)
其中,EVB是价带的氧化还原电势,ECB导带的氧化还原电势,X是半导体材料的绝对电负性,Ee是常数,相对于标准氢电位,取值4.50 eV,Eg是半导体材料能带间隙。通过计算知,g-C3N4和0.5% CSN的能带分别是(-1.21,+1.51)eV和(-1.205,+1.485)eV。这可能是由量子限制和超薄g-C3N4纳米片诱导作用导致的。此外,当N-CQDs均匀地沉积在0.5% CSN表面上时,CSN呈现更高的可见光吸收范围且多孔的结构增加了g-C3N4的表面缺陷,导致能带结构发生改变,这可能归因于入射光在纳米片孔隙内的多次反射、散射作用增强了入射光的吸收和传递,0.5% CSN比g-C3N4具有更好的光捕集能力,同时也说明了N-CQDs的掺杂可促进产物对光的吸收范围。
2.5 比表面积(BET)分析
催化剂的比表面积和孔隙结构在有机污染物降解过程中起着重要作用,因为它们有利于有机分子的吸附和扩散,可以提供更多的反应位点,从而提高降解速率。图2d为样品的氮吸附—解吸和孔隙大小分布曲线。根据IUPAC组织物理吸附等温线分类,g-C3N4和CSN样品的氮吸附—解吸曲线为IV型等温线,H3型迟滞回线,孔隙大小分布都显示为介孔结构[25-26]。利用等温线脱附分支的Barrett-Joyner-Halenda(BJH)方法估计了孔径分布,结果见表1。表中所示与煅烧过程中加入NH4Cl可增加g-C3N4的BET表面积,当C3H6N6和NH4Cl的质量比为3∶1时,所得g-C3N4的比表面积最大,可达134.294 1 m2·g-1,具有较大的孔径及孔隙率,NH4Cl的加入增加了比表面积,多孔的纳米结构增加了光的吸收,增加了入射光的折射和散射,从而提高了入射光的利用率。多孔的g-C3N4更有利于增加有机分子的吸附和扩散,增加了有机分子在光催化剂的表面的浓度,增加了反应活性位点,更有利于多孔的g-C3N4吸附和降解。
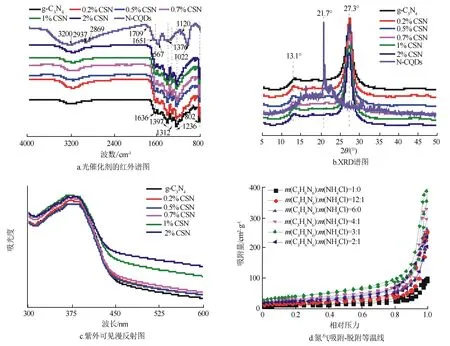
图2 样品结构表征图像
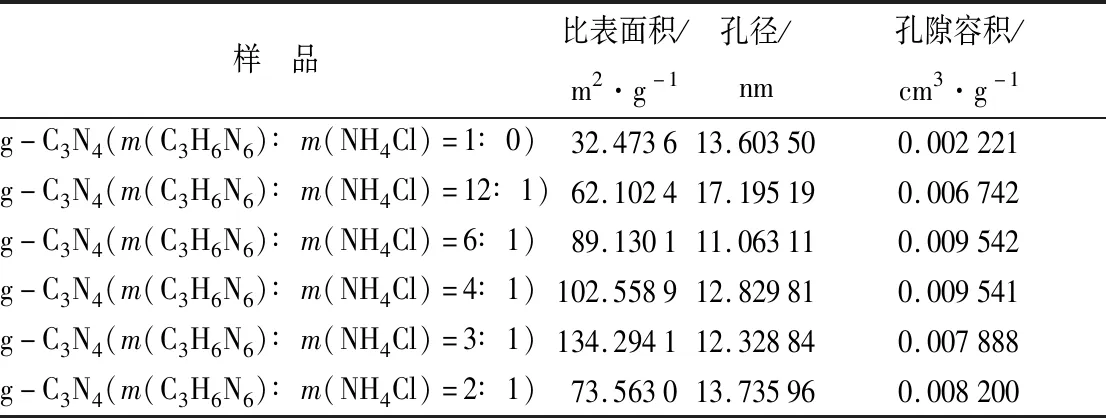
表1 样品的比表面积、孔径和孔体积
2.6 光催化性能分析
如图3a不同样品在可见光照射下对TC的光催化降解效果。未添加催化剂时,TC在60 min内下降很少,表明TC的自光解效果是很差。同时,g-C3N4在降解TC中作用也不是特别明显,仅为28%。可能由于g-C3N4的电子—空穴能够快速的重组,降低了光催化活性。N-CQDs的加入增强了光催化活性,提高了光催化降解能力。当N-CQDs的质量百分比增加到0.5%时,N-CQDs/g-C3N4复合光催化剂对降解TC光催化活性最高(在60 min内降解速率几乎达到100%)。当进一步增加N-CQDs的加入量到2%时,TC的降解速率降到了75%,可能的原因是由于碳基材料的屏蔽效应导致的。0.5% CSN具有较强的光谱响应性,能够吸收更多的能量,增强光催化制剂的氧化还原能力。
图3b中揭示了不同样品在可见光照射下光催化降解TC动力学曲线。采用一阶动力学模型进行数据拟合,公式如下[27]:
ln(C0/C)=kt。
(4)
其中:t为时间,C0和C分别是TC溶液的初始浓度和不同时刻下TC溶液的质量浓度,斜率k是反应速率常数。所有催化剂的k值都高于g-C3N4(图3e),0.5% CSN具有最大降解速率常数为0.069 69 min-1是g-C3N4降解速率常数的12倍。
在实际应用中,光催化剂的稳定性是光催化反应中的关键问题之一。图3c为0.5% CSN光催化降解TC的循环实验效果图,用来考察光催化剂的稳定性和重复使用性。经过5次循环光催化降解TC实验发现,0.5% CSN对TC的降解效果几乎没有改变,60 min内降解几乎达到100%。循环使用实验说明该催化剂性质稳定,可重复使用多次,具有良好的循环稳定性。
2.6 光催化降解机理探究
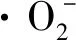
g-C3N4+hv→g-C3N4(h++e-)
0.5% CSN+hv→g-C3N4(h+)+N-CQDs(e-)
g-C3N4(h+)+TC→g-C3N4+
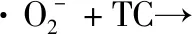
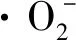
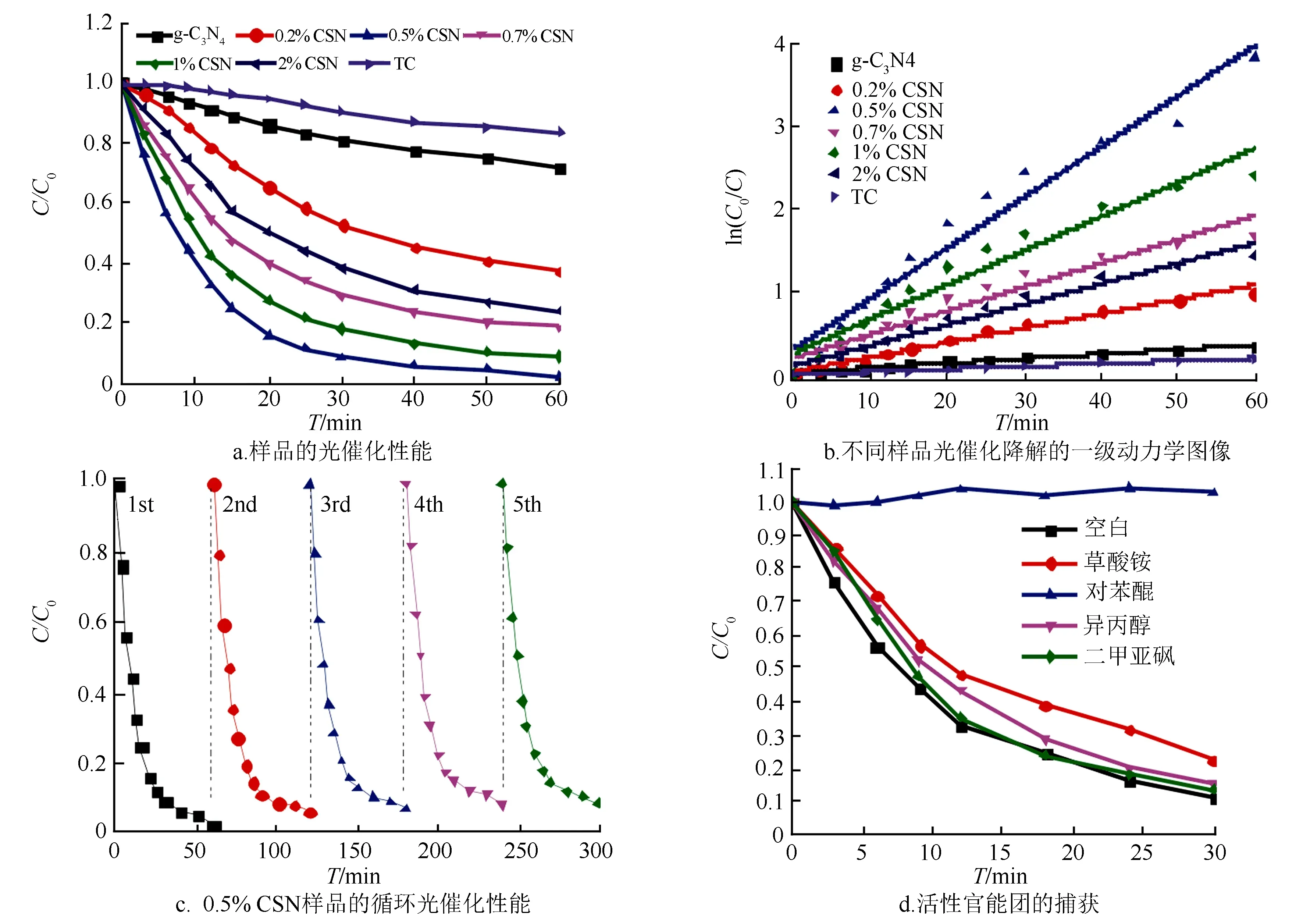
图3 样品光催化性能测试图
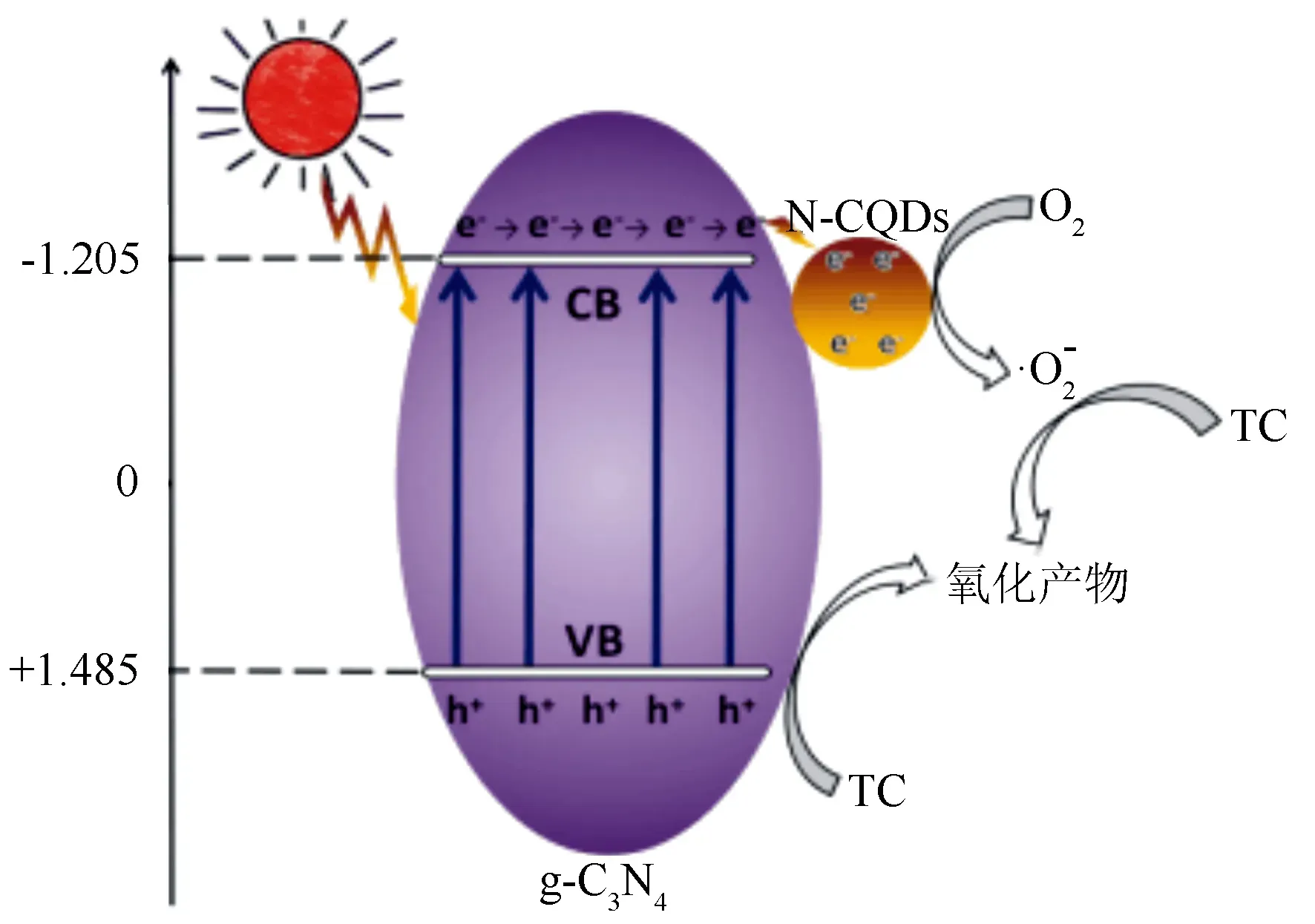
图4 N-CQDs/g-C3N4光催化降解原理
3 结论
本研究采用高温煅烧法将N-CQDs复合于超薄片层状g-C3N4表面,制备了N-CQDs/g-C3N4复合光催化剂。通过FT-IR、XRD、TEM和UV-vis DRS等多种手段对其微观形貌、能带结构等进行表征。结果表明:N-CQDs与超薄片状g-C3N4间通过杂化作用形成了复合物,N-CQDs均匀的分布在片状g-C3N4上。将g-C3N4与修饰的CQDs结合。当加入N-CQDs的质量百分比为0.5%时,N-CQDs/g-C3N4复合光催化剂降解TC光催化活性最高,其降解速率常数是g-C3N4的12倍,较大程度上提高了0.5% CSN的光催化活性。在进行5次循环试验后,对TC的降解效率仍可达到99.2%,N-CQDs/g-C3N4复合材料具有优异的光稳定性和可回收性。在环境净化修复方面具有较大的潜在应用价值。光催化复合材料的制备,一方面可以有效促进电子的转移,降低光催化材料中电子空穴复合率,提高其光量子效应;另一方面可以形成光催化吸附协同效应,其表面光催化反应活性位点增多,从而显著提高其光催化性能。
