聚乙二醇干扰素α-2a治疗HBeAg阳性慢性乙型肝炎部分应答患者序贯替比夫定治疗疗效观察*
2020-03-23丁俊琪
丁俊琪,张 偲,张 彬
慢性乙型肝炎(chronic hepatitis B,CHB)是一个危害世界的健康问题。据统计,全球约20亿人曾感染过乙型肝炎病毒(hepatitis B virus,HBV)。一项血清学调查结果显示,全球目前仍有2.5亿人是HBV携带者[1]。关于CHB的治疗,国际指南建议使用有限疗程的聚乙二醇干扰素或长期给予核苷(酸)类似物治疗[2,3]。研究显示,聚乙二醇干扰素α-2a较核苷酸类似物具有较高的HBeAg血清学转换率[4,5],但其疗程一般较长,且治疗费用较高,长期使用易加重患者的不良反应和经济负担。因此,在干扰素治疗结束后,对于未能实现血清学转换的部分应答患者后续是停药观察还是改用核苷酸类药物继续治疗,有学者认为干扰素治疗存在延迟应答效应,因此可以停药进行随访观察,但亦有学者认为改用核苷酸类药物继续治疗能够提高应答率。相对于其他核苷酸类药物,替比夫定具有较高的HBeAg血清学转换率。据报道,HBeAg阳性的CHB患者经替比夫定治疗2年后,HBeAg血清学转换率约为29%~41.6%[6]。CHB患者常伴有慢性肾脏疾病,目前临床应用的所有核苷及核苷酸类药物都是以原型的形式从肾脏排泄,导致抗病毒治疗过程中有可能引起肾功能不全,对药物代谢产生影响,甚至加重患者肾损伤。资料显示,替比夫定能够改善CHB伴有轻度肾损伤患者的肾功能[7]。本研究旨在探讨干扰素治疗结束后序贯替比夫定治疗HBeAg阳性CHB患者的临床疗效及安全性,现将结果报道如下。
1 资料与方法
1.1 一般资料 2016年1月~2017年2月我院感染病科收治的HBeAg阳性CHB患者63例,男性35例,女性28例;年龄20~43岁,平均年龄为(30.0±5.9)岁。符合中华医学会肝病学分会和感染病学分会制定的《慢性乙型肝炎防治指南(2015年更新版)》的诊断标准[8]。纳入标准:①连续使用聚乙二醇干扰素α-2a治疗48周;②48周疗程结束时呈部分应答;③无精神类疾病,能正常沟通。排除标准:①合并心肺肾等重要脏器疾病;②既往曾使用过核苷酸类似物治疗;③妊娠及哺乳期妇女;④合并甲型、丙型肝炎或人类免疫缺陷病毒感染者;⑤临床确诊为肝硬化、肝癌或其他系统恶性肿瘤者;⑥合并自身免疫性、遗传性肝病或药物性肝损伤;⑦酗酒、吸毒者。本研究经本院医学伦理委员会批准,所有参与患者及其家属对本研究内容均知情,并签署知情同意书。
1.2 方法 将63例CHB患者分为序贯治疗组31例和对照组32例。在序贯治疗组,在停止干扰素治疗后,给予替比夫定继续治疗48周;在对照组,在停止干扰素治疗后,随访观察48周。部分应答定义为在干扰素治疗48周末,血清HBV DNA较基线下降超过2 lg copies/mL,但未阴转,血清ALT未复常,未出现HBeAg血清学转换[16]。
1.3 血清检测 使用全自动生化分析仪(AU5800,美国Beckman)检测血生化指标(上海生物工程有限公司);采用PCR法检测血清HBV DNA(上海生物工程有限公司);采用化学发光法检测血清HBsAg、抗-HBs、HBeAg和抗-HBe(北京佰桥瑞景生物科技有限公司)。
1.4 统计学方法 应用SPSS 19.0软件处理和分析,计量资料以(±s)表示,采用t检验,率的比较采用x2检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 两组临床疗效比较 见表1和表2。

表1 两组临床疗效(%)比较
表2 两组疗效(±s)比较
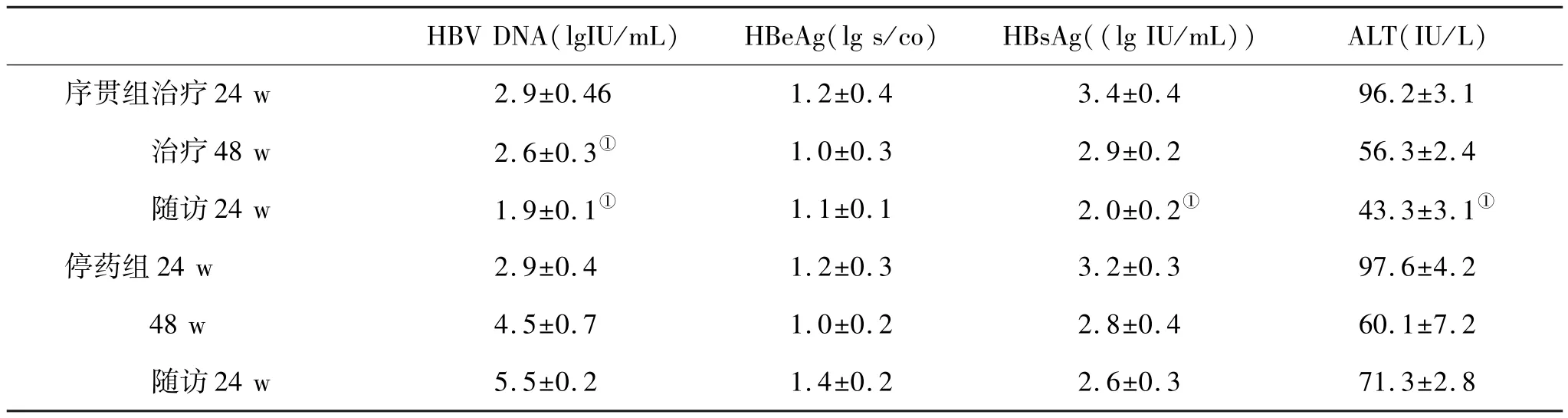
表2 两组疗效(±s)比较
与停药观察组比,①P<0.05
HBV DNA(lgIU/mL) HBeAg(lg s/co) HBsAg((lg IU/mL)) ALT(IU/L)序贯组治疗24 w 2.9±0.46 1.2±0.4 3.4±0.4 96.2±3.1治疗48 w 2.6±0.3① 1.0±0.3 2.9±0.2 56.3±2.4随访24 w 1.9±0.1① 1.1±0.1 2.0±0.2① 43.3±3.1①停药组24 w 2.9±0.4 1.2±0.3 3.2±0.3 97.6±4.2 48 w 4.5±0.7 1.0±0.2 2.8±0.4 60.1±7.2随访24 w 5.5±0.2 1.4±0.2 2.6±0.3 71.3±2.8
2.2 安全性比较 序贯治疗组在48周治疗期间,无患者出现需更改治疗方案的情况,其中9例(29.0%)患者在服用替比夫定期间出现血清肌酸激酶升高现象,在治疗10~13周后下降至正常水平。
3 讨论
治疗CHB患者的最终目标是最大限度地抑制乙型肝炎病毒的复制,从而减轻肝细胞坏死及肝纤维化,减缓及减少肝功能衰竭等并发症的发生。抗病毒治疗是CHB患者治疗的关键,所有患者都应接受规范化的抗病毒治疗。抗病毒药物的选择对CHB患者的治疗至关重要。目前,临床常用的抗病毒药物主要为α-干扰素和核苷酸类似物。聚乙二醇干扰素-α是治疗CHB患者的主要抗病毒药物之一,但仍有部分患者在疗程结束后未能达到理想的治疗效果。研究显示,α-干扰素治疗疗程延长,会在一定程度上增加患者不良反应发生率及经济负担[9,10]。α-干扰素与核苷酸类似物的抗病毒作用机制不同。因此,对于α-干扰素治疗不完全应答的患者,序贯使用核苷酸类似物继续进行治疗,不仅能够提高治疗效果,且一般不会产生不良反应[11]。临床上多以是否出现HBeAg血清学转换作为治疗效果的观察标准。研究结果显示,对于聚乙二醇干扰素α-2a治疗不完全应答的患者序贯替比夫定继续进行治疗,较之其他抗病毒药物而言,能够获得更加理想的HBeAg转换率,且安全性更高[12]。究其原因,可能是由于两者均具有调节免疫应答的作用,序贯使用可能使免疫调节作用叠加或协同发挥,从而增加了患者HBeAg血清学转换率。研究发现,经聚乙二醇干扰素-α治疗结束后部分应答患者及时加用替比夫定继续治疗,能够使替比夫定与干扰素的后续作用联合而增强,加强了抗病毒效果[13]。
CHB与慢性肾病关系密切,目前所用的核苷及核苷酸类似物有可能诱发肾脏损伤。但研究发现,替比夫定具有持续改善CHB患者肾功能的作用,尤其是对于伴有肾功能受损的慢性乙型病毒感染患者效果更为明显[14]。
研究结果证实,经聚乙二醇干扰素-α治疗48周部分应答的HBeAg阳性CHB患者序贯替比夫定治疗具有较好的HBeAg血清学转换率及良好的耐受性[15]。本研究对63例经聚乙二醇干扰素-α治疗结束后未获得完全应答患者分别进行序贯替比夫定治疗或停药观察48周,观察结果显示,在替比夫定继续治疗24周、48周和随访24周,序贯治疗组患者血清HBeAg转阴率分别为22.5%、25.8%和35.4%,均显著高于停药观察组(分别为0.0%、3.2%和3.2%),在治疗48周和随访24周,序贯治疗组血清HBV DNA转阴率分别为90.3%和87.0%,显著高于停药观察组的34.3%和18.7%,结果显示序贯治疗组血清HBeAg和HBV DNA转阴率均显著高于停药观察组,与有关报道[16]结果一致。据报道,对经α-干扰素治疗部分应答的患者序贯使用替比夫定继续进行进一步治疗能够加强患者免疫应答及病毒清除率[17-20]。当出现HBeAg血清学转换、HBV DNA转阴且血清ALT恢复正常时,即获得了联合应答。本研究结果显示,在α-干扰素治疗48周结束为获得应答反应的患者,序贯治疗组获得了更高的血生化学和病毒学应答率,显著优于停药观察组。序贯治疗组ALT复常率显著高于停药观察组,且序贯治疗组HBeAg和HBV DNA血清转阴率均显著高于停药观察组,说明序贯治疗组患者联合应答率明显高于停药观察组。
有研究指出,替比夫定能够引起相关性肌病和周围神经病变,因此本研究对序贯治疗组患者血清肌酸激酶水平和其他不良反应进行了监测,结果显示,序贯治疗组在48周治疗期间,无患者出现需更改治疗方案的情况,其中9例患者在服用替比夫定一段时间后出现血清肌酸激酶水平升高现象,但均在治疗13周内下降至正常水平。在替比夫定继续治疗的48周内,两组患者均未出现肾功能损害、周围神经病变、肝功能失代偿等严重不良反应,说明序贯使用替比夫定治疗具有较高的安全性。本研究纳入病例数有限,故在分析疗效过程中可能存在一定的偏差,且观察时间也比较短,有待后续加大样本量进行深入探讨和分析。
综上所述,在应用聚乙二醇干扰素α-2a治疗HBeAg阳性CHB患者标准疗程后部分应答患者序贯给予替比夫定继续治疗是大多数干扰素治疗失败患者当然的补救治疗方法,短期观察发现能够有效地提高患者血清HBeAg血清学转换率和HBV DNA转阴率,且具有较高的安全性[21-23]。对这些患者长期核苷(酸)类治疗过程中疗效和观察和耐药患者的及时发现和更换新的治疗方法,是当前需要认真研究的课题。
