(NH4)2SO4溶液中CaSO4·2H2O溶解速率增长特性及机制
2020-03-21刘仕忠朱家骅夏素兰
刘仕忠,朱家骅,夏素兰,葛 敬
(四川大学 化学工程学院,四川 成都 610065)
磷石膏是湿法磷酸生产过程中的富钙副产物[1],其中含有质量分数约为90%的二水硫酸钙,以及二氧化硅、五氧化二磷、氟化物等其他杂质[2]。全球每年产生磷石膏 100 ~ 280 Mt[3],目前只有约14%的磷石膏被回收利用,且大部分用作水泥缓凝剂[4],58%的磷石膏堆积在自然界中,甚至还有28%被注入水域,造成了严重的环境问题[5],磷石膏回收利用显得十分重要。磷石膏主要成分为CaSO4·2H2O,可利用其在NH3作用下矿化CO2,实现CO2减排和磷石膏处理为一体的以废治废、变废为宝的绿色低碳技术路线[6]。主要反应式为:
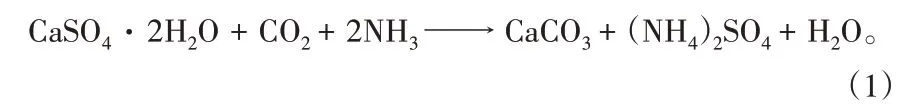
该矿化反应的速率控制步骤是二水硫酸钙的溶解[7]:
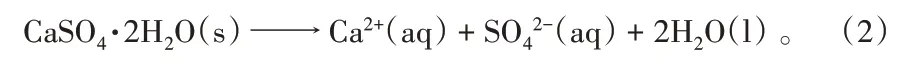
二氧化碳矿化磷石膏工业系统中,母液含有大量硫酸根离子[8]。由于同离子效应以及盐效应的相互影响,硫酸根离子的存在会改变CaSO4·2H2O 的溶解度[9],即平衡浓度ceq。平衡浓度是影响溶解推动力的重要因素,对溶解速率有很大的影响。
纯水体系中二水硫酸钙的溶解动力学已有大量研究[10-12],而对盐溶液体系中二水硫酸钙溶解行为的研究较少。PACHON-RODRIGUEZ E A等[13]利用全息干涉法研究了石膏在酒石酸、硼酸、氨羧络合剂等溶液中的溶解速率,发现硼酸等对石膏溶解的抑制主要是因为其与表面钙离子的螯合作用阻碍了钙离子从石膏表面释放。GOBRAN G R 等[14]研究了石膏在 NaCl、MgCl2、Na2SO4、MgSO4溶液中的溶解速率,发现不同盐溶液对石膏溶解具有不同的影响机制。KUNKUL A 等[15]测定了钠硼解石在0.10、0.25、0.50、1.00 mol/L(NH4)2SO4溶液中的溶解速率,实验结果显示随着硫酸铵浓度的增大,钠硼解石的溶解速率呈增加趋势。然而,(NH4)2SO4溶液中,二水硫酸钙的溶解速率将会发生怎样的变化,截至目前仍缺少这方面的研究。
“直接矿化磷石膏联产硫基复合肥”新工艺结合了碳减排与磷石膏综合利用,提高磷石膏颗粒的溶解速率是提高工艺效率的核心。笔者以二水硫酸钙块材为研究对象,在温度(25 ℃)、搅拌转速(180 r/min)恒定的条件下,研究(NH4)2SO4溶液中二水硫酸钙的溶解规律。探究溶解推动力、扩散阻力对溶解速率的影响,为工业应用中反应器的设计提供基础数据和理论指导。
1 实验
1.1 实验试剂
天然二水石膏(湖北荆门石膏粉厂,w(CaSO4·2H2O)大于98%,将其加工为统一大小的块状,每次实验前均用砂纸打磨光滑);硫酸铵(AR)。
1.2 实验步骤
在2 000 mL 烧杯中加入硫酸铵溶液1 800 mL进行溶解实验,搅拌转速控制在180 r/min,水浴温度保持在25 ℃。在石膏溶解过程中,每隔一定时间取反应液5 mL,通过电感耦合等离子体原子发射光谱法(ICP-AES)检测溶液中的Ca2+浓度。通过式(3)计算溶解速率:

式中,r为二水硫酸钙的溶解速率,mol/(cm2·min);V为溶液的体积,mL;S为石膏的表面积,cm2;c为钙离子浓度,mol/L;t为溶解时间,min。
2 结果与讨论
2.1 CaSO4·2H2O在硫酸铵溶液中的溶解速率
溶解速率方程可表示为溶解推动力与溶解速率常数的乘积[16-17],即:

式中,k为溶解速率常数,m/s;ceq为钙离子平衡浓度,mol/L。
由溶解速率方程式(4)可知,溶解速率主要受2 个方面影响,一个是溶解推动力,一个是溶解阻力(溶解速率常数的倒数)。
CaSO4·2H2O 溶解初始,体系中的钙离子浓度较低,推动力较大,钙离子浓度呈线性迅速增加。随着溶解时间的延长,钙离子浓度不断增加,溶解推动力逐渐减小,钙离子浓度缓慢增加直至趋于饱和,溶解速率逐渐降低(见图1、图2)。
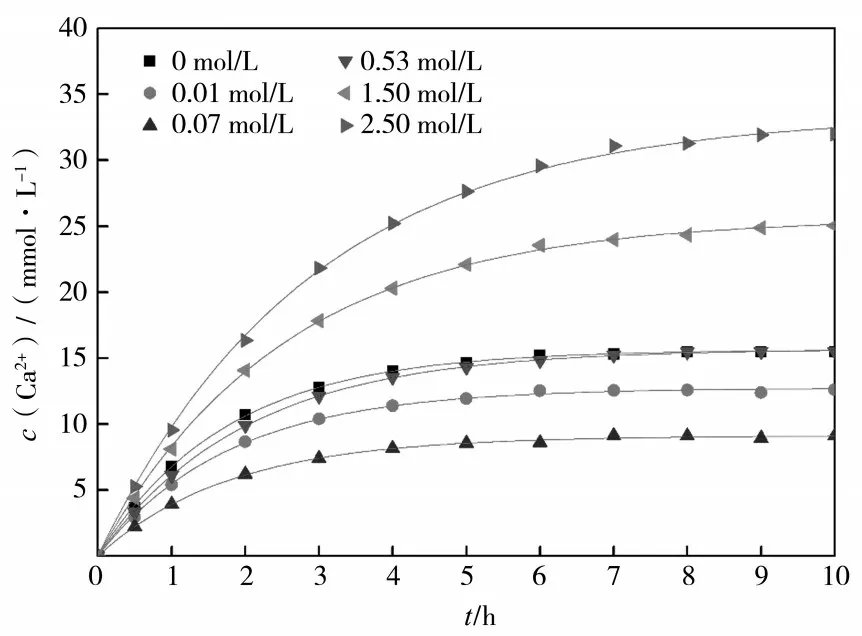
图1 不同浓度硫酸铵溶液中钙离子浓度与时间的关系
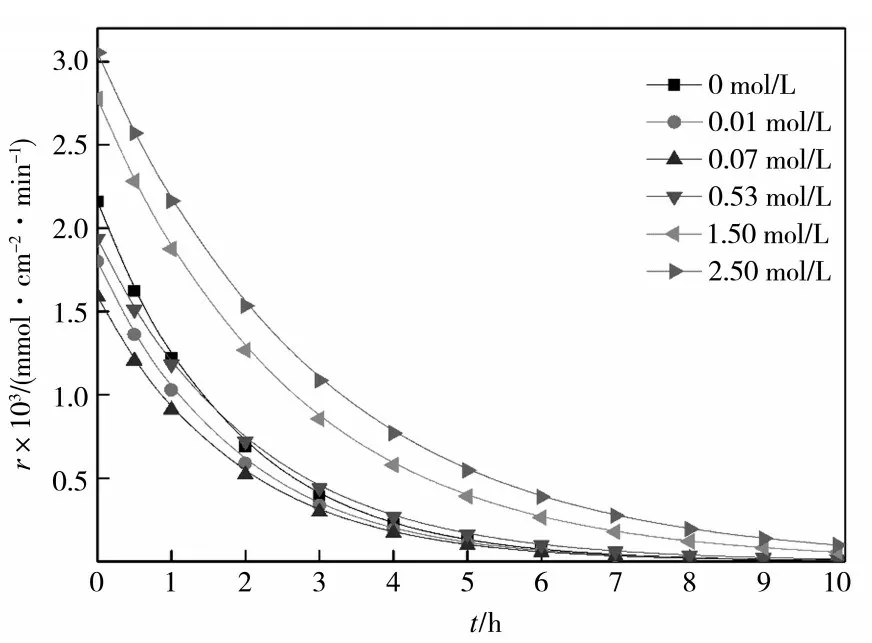
图2 不同浓度硫酸铵溶液中CaSO4· 2H2O溶解速率与时间的关系
不同硫酸铵浓度下,钙离子浓度呈现相似的增长趋势。二水硫酸钙的溶解速率随着(NH4)2SO4浓度的增大先下降后升高。低(NH4)2SO4浓度下(小于0.07 mol/L 时),(NH4)2SO4浓度越高,二水硫酸钙的溶解速率越慢;(NH4)2SO4浓度高于一定值(0.07 mol/L)后,(NH4)2SO4浓度越高,二水硫酸钙溶解速率越快。(NH4)2SO4浓度在0.07 mol/L 时,CaSO4·2H2O 的溶解速率达到最小。(NH4)2SO4浓度达到2.50 mol/L 时,CaSO4·2H2O 的平均溶解速率达到纯水中的2 倍。
通过对式(4)积分可得:

其中:

式(5)所描述的钙离子浓度与时间的函数关系和图1 所描述的规律一致。用式(5)的函数式对图1 的数据进行拟合,每条曲线的拟合度均在99.8%以上。
2.2 硫酸铵溶液中二水硫酸钙的溶解推动力
溶解推动力为溶液中Ca2+的平衡浓度与溶液中Ca2+浓度的差值,即ceq-c。因此,溶解推动力决定于溶液中Ca2+的平衡浓度ceq。二水硫酸钙的溶解度(平衡浓度)随着硫酸铵浓度的增加呈现出先降低后升高的趋势(见图3)。硫酸铵浓度为0.07 mol/L时,二水硫酸钙的溶解度最低,为0.009 8 mol/L。硫酸铵浓度低于0.07 mol/L 时,随着硫酸铵浓度的增加,二水硫酸钙的溶解度迅速降低。当硫酸铵浓度高于0.07 mol/L 时,随着硫酸铵浓度的增加,二水硫酸钙的溶解度呈现上升趋势,在硫酸铵浓度为0.53 mol/L 时,二水硫酸钙的溶解度接近于在纯水中的溶解度,为0.015 2 mol/L;硫酸铵浓度为2.50 mol/L 时,二水硫酸钙的溶解度达到在纯水中溶解度的2 倍以上,为0.032 0 mol/L,即溶解初始推动力为纯水中的2 倍。但由图2 可知,硫酸铵浓度为2.50 mol/L 时,相比于纯水,溶解推动力虽增加了1 倍,但溶解初始瞬时速率并没有增加1 倍。原因是溶解速率还受到溶解速率常数,也即是溶解阻力的影响。
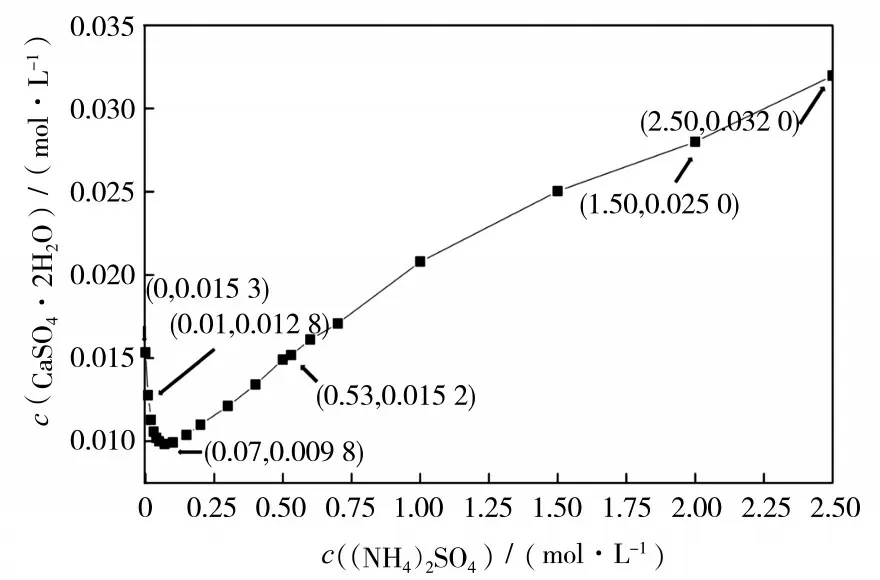
图3 25 ℃下不同浓度硫酸铵溶液中CaSO4· 2H2O 的溶解度
2.3 硫酸铵溶液中二水硫酸钙的溶解速率常数
以对数形式表示式(5)可得:

不同浓度硫酸铵溶液中,石膏溶解的表面积S和溶液体积V之比的变化在1.0%以内,可以忽略。溶解反应前5 h内,ln[ceq/(ceq-c)]与时间t的关系如图4 所示,数据点呈现良好的线性关系,与式(7)所描述的一样,溶解反应符合一级反应动力学。
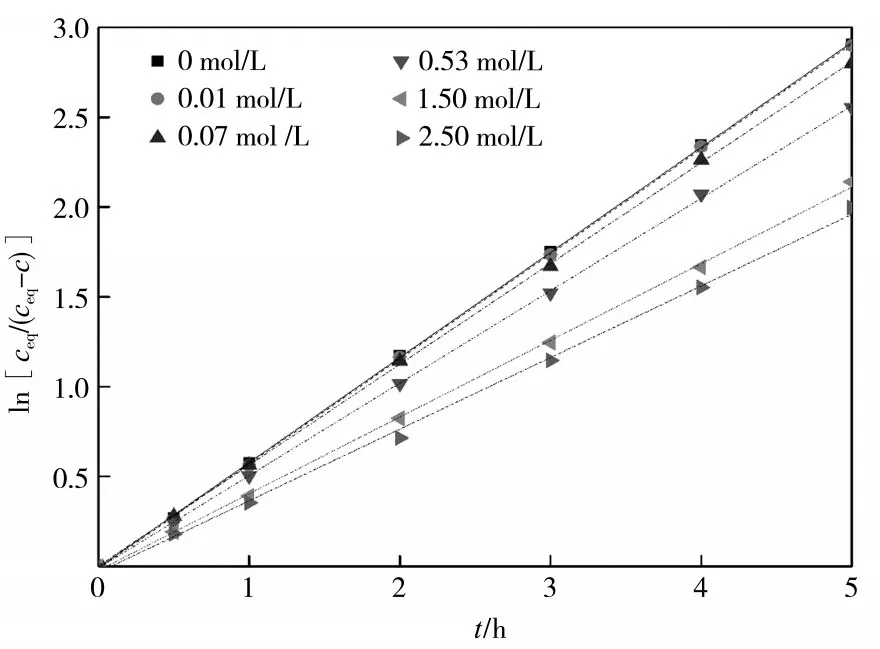
图4 不同浓度硫酸铵溶液中ln[ceq/(ceq-c)]与时间t的关系
溶解速率常数k可通过图4 直线的斜率计算得出。二水硫酸钙在0、0.01、0.07、0.53、1.50、2.50 mol/L 的(NH4)2SO4溶液中的溶解速率常数k分别为 2.923×10-5、2.921×10-5、2.805×10-5、2.573 ×10-5、2.134×10-5、1.993×10-5m/s。随着硫酸铵浓度的增加,溶解阻力增大,溶解速率常数降低,在一定程度上阻碍了溶解速率的加快。所以溶解初始,2.50 mol/L(NH4)2SO4溶液中二水硫酸钙的溶解速率并没有达到纯水中的2倍,只是纯水中的1.4倍左右。
将溶解速率方程式(4)以饱和度形式表示。
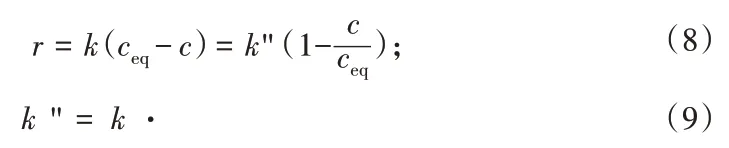
不同浓度硫酸铵溶液中溶解速率与c/ceq的关系见图5。
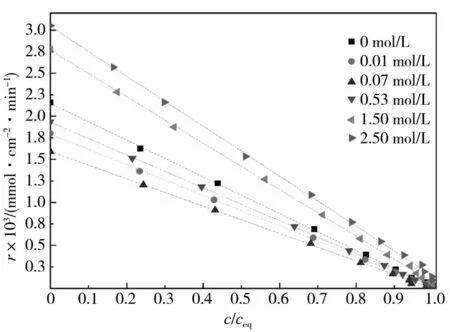
图5 不同浓度硫酸铵溶液中溶解速率与c/ceq的关系
根据图5 可知,当饱和度c/ceq小于0.94 时,溶解速率r与c/ceq几乎呈线性关系,即该反应符合一级反应动力学。c/ceq大于0.94,Ca2+浓度接近平衡浓度时,溶解速率呈非线性规律。这与JESCHKE A A等[18]对石膏在纯水中的溶解速率研究具有类似的结论。
2.4 溶液黏度对溶解速率常数的影响
CaSO4· 2H2O 溶解过程为先在晶体表面分解,然后钙离子穿过液膜扩散到主体溶液中(见图6)。
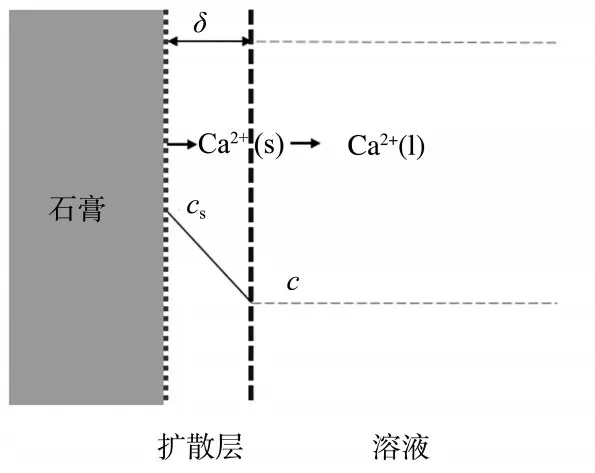
图6 溶解过程示意
在稳态情况下,固体溶解过程扩散速率等于表面反应速率[19],即:
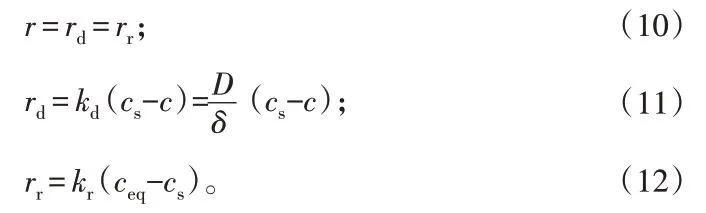
式中,rd为扩散速率,mol/(cm2· min);rr为表面反应速率,mol/(cm2·min);kd为扩散传质系数,m/s;D为扩散系数,m2/s;kr为反应传质系数,m/s;cs为石膏表面钙离子的浓度,mol/L;δ为扩散膜厚度,cm。通过上述3个方程可解出:
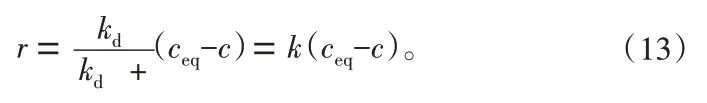
所以:

根据式(14)可知,溶解速率常数k受扩散传质系数kd和反应传质系数kr的影响。根据阿仑尼乌斯公式[20],反应传质系数kr基本上不变。所以扩散传质系数kd决定了溶解速率常数k的大小。
根据Stokes-Einstein 方程,物质A 在物质B 中的扩散系数DAB可表示为:

式中,rA为溶质A分子的半径,m;μB为溶剂B的黏度,Pa·s;kB为玻尔兹曼常量;T为热力学温度,K。扩散系数与黏度成反比,而扩散传质系数为:

扩散液膜厚度δ与溶液黏度成正相关[21]。实验测得溶液黏度随着硫酸铵浓度的增加而增大,如图7 所示。因此,溶解速率常数k随着硫酸铵浓度的增加而减小。
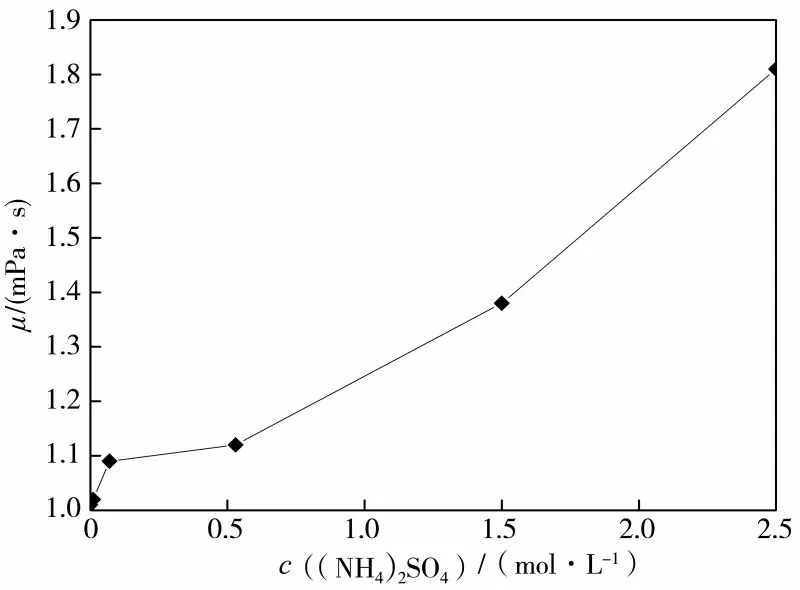
图7 溶液黏度随硫酸铵浓度的变化
3 结论
(1)二水硫酸钙溶解是CO2矿化反应体系的控速步骤,二水硫酸钙的溶解行为受硫酸铵溶液浓度的影响显著。数据显示:c((NH4)2SO4)>0.07 mol/L后,二水硫酸钙溶解速率与c((NH4)2SO4)呈正相关。随着硫酸铵浓度的增加,二水硫酸钙的溶解度增加,溶解推动力显著增加,但伴随着溶液黏度的增加,传质阻力也相应增大;整体上随着硫酸铵浓度的增加,二水硫酸钙溶解速率呈现显著增长趋势。
(2)在反应5 h内,饱和度c/ceq<0.94时,二水硫酸钙溶解反应为一级反应,溶解速率与饱和度呈线性关系。二水硫酸钙在0、0.01、0.07、0.53、1.50、2.50 mol/L 的(NH4)2SO4溶液中的溶解速率常数k分别为 2.923×10-5、2.921×10-5、2.805×10-5、2.573 ×10-5、2.134×10-5、1.993×10-5m/s。饱和度c/ceq>0.94 时,钙离子浓度接近平衡浓度,溶解速率呈现出非线性规律。
(3)本研究为CO2矿化反应器优化设计提供了依据,若反应器设计液相硫酸铵浓度>2.5 mol/L,则其控速步骤比纯水中快1 倍,从动力学角度物料停留时间及反应器有效容积均可相应缩减。
