芦荟大黄素在石墨烯/聚多巴胺/金复合纳米材料修饰电极上的电化学行为及检测
2020-03-20吴其国蓝伦礼庄晨曦
阳 敬 兰 慧* 吴其国 蓝伦礼 庄晨曦 赵 佳
(1.红河卫生职业学院云南蒙自 661199;2.安庆医药高等专科学校安徽安庆 246052;3.桂林医学院广西桂林 541100)
芦荟大黄素(Aloe Emodin)是中药大黄中的有效成分,它广泛存在于百合科芦荟、豆科决明子及蓼科植物大黄中,具有抗菌、消炎、杀虫、抗癌、抗衰老等功效[1]。芦荟大黄素主要用于保健食品添加剂和食品染色剂。目前,对芦荟大黄素的分析方法主要有高效液相色谱法[2]、分光光度法[3]及薄层色谱法[4]等。这些分析方法虽然应用广泛,但其设备昂贵,前处理复杂。电化学方法因其仪器设备简单,操作简便灵活,低成本和灵敏度高并且不需要复杂的前处理,已被广泛应用于实际样品的检测[5-7]。而采用电化学方法分析研究芦荟大黄素报道较少。
纳米材料具有良好的导电性及生物相容性,已经应用于生物传感器的构建中。石墨烯(GNs)具有大的比表面积、优良的导电性、良好的电化学活性,有特殊的结构和优异的力学、电学、光学及催化性能,在纳米电子学、微电子学、储能材料以及复合材料等领域具有广泛的应用前景。同时,由于这种碳纳米材料具有良好的导电性及生物相容性,已经被广泛应用于生物传感器的制备及电催化领域。GNs已广泛应用于电分析化学领域[8,9]。GNs基复合材料借助不同材料的协同作用,具有更快的电子迁移率、更大的比表面积和更好的生物相容性[10]。近年来,以GNs合成复合材料应用于电化学和生物传感领域的报道已经很常见。例如:ZnO-GNs[11]、TiO2-GNs[12]、WO3-还原氧化石墨烯(RGO)[13]等。但是GNs的片与片之间有较强的范德华力,容易聚集,这给GNs的研究和应用造成了极大的困难。因此,对其进行有效的功能化修饰非常重要[14]。聚多巴胺(PDA)是贝壳、蚌等生物分泌的粘性蛋白的主要成分,具有极强的粘附性,能稳定地固定在各种基质上。Lee等[15]以多巴胺(DA)为单体,通过简单的自聚合反应在各种基质表面形成了仿生PDA膜,该膜不仅具有良好的粘附性,同时保持了原有单体良好的生物相容性。PDA薄膜被广泛地用于对Au和Pt纳米颗粒、碳纳米管、GNs氧化物的表面修饰。DA特有的还原性可以作为氧化石墨烯(GO)的还原剂。PDA良好的粘附性和生物相容性又可以作为GNs的保护剂。
本文合成石墨烯/聚多巴胺/金(GNs/PDA/Au)复合纳米材料,采用紫外-可见吸收光谱、X射线衍射(XRD)、扫描电镜(SEM)对合成的材料进行表征,并将制备的材料构建电化学传感器用于检测芦荟大黄素。GNs大的比表面积有利于PDA的负载,PDA的引入既可以很好的改善RGO的水溶性,又可作为一个良好的连接剂,能够很好的负载Au纳米粒子,Au纳米粒子负载的GNs/PDA复合纳米材料中Au纳米粒子具有良好的电化学活性,有利于电化学检测性能的提高[16]。本研究采用循环伏安法(CV)和差分脉冲伏安法(DPV)对影响芦荟大黄素检测的pH值、富集时间进行优化,最佳条件为pH=5.72,富集时间280 s。方法可用于检测大黄中的芦荟大黄素,为进一步检测此类药品及保健食品的有效成分提供一条有效途径。
1 实验部分
1.1 仪器与试剂
CHI660E电化学工作站(上海辰华仪器(上海)有限公司);DZF-60S0真空干燥箱(DZF-60S0上海科学仪器有限公司);CP224C电子天平(奥豪斯仪器(上海)有限公司);HH-4水浴锅(金坛市大地自动化仪器厂);SK5200HP超声波清洗器(上海科特超声仪器有限公司);AM1202-H数显电动搅拌机(上海昂尼仪器);TG18-WS离心机(上海岛析实业有限公司)。
芦荟大黄素对照品(批号:20140814)购自国药集团上海化学试剂有限公司,大黄对照药材(批号:20130909)购自国药集团上海化学试剂有限公司;石墨烯(GNs)(阿拉丁试剂有限公司,8 000目);HCl、柠檬酸三钠、NaNO2、KMnO4、NaBH4、H2SO4、H3PO4、HAc、HAuCl4、三羟甲基氨基甲烷(Tris)、甲醇、NaOH、30%H2O2均为分析纯。水为二次蒸馏水。
1.2 石墨烯/聚多巴胺(GNs/PDA)复合材料的制备
采用Hummers’方法[17]制备氧化石墨烯(GO),取60 mg GO溶于80 mL水中,超声分散2 h后,加入40 mg DA,冰浴超声30 min,搅拌下加入40 mL pH=8.5的12.5 mmol/LTris-HCl缓冲溶液,于80 ℃反应48 h,用水离心清洗数次,直到除去多余的DA,产物溶于水中[18]。为了对比,本文还参考文献方法制备了RGO纳米材料[19]。
1.3 GNs/PDA/Au复合材料的制备
参考文献报道的方法[20]制备GNs/PDA/Au复合纳米材料,具体方法如下:取1 mL 10 mg/mL GNs/PDA纳米复合物,加入10 mg HAuCl4(0.5 mL 20 mg/mL)和14.705 mg柠檬三酸钠,整个溶剂的体积为40 mL,冰浴超声30 min,冰浴中加入0.6 mol/L NaBH4,搅拌30 h,用水离心清洗后,备用。
1.4 传感器构建
先将玻碳电极(GCE,直径为3 mm)依次用1.0、0.3和0.05 μm/L的Al2O3粉末在麂皮上抛光成镜面,然后分别在1.0 mol/L HNO3、无水乙醇和水中各超声清洗1 min,室温晾干。移取7 μL制备好的GNs/PDA/Au溶液滴涂在GCE表面,室温晾干后,保存备用。
1.5 电化学测试
采用三电极体系,以修饰GCE为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,整个实验在0.04 mol/L的H3PO4、H3BO4和HAc缓冲溶液中进行,循环伏安法实验的电位扫描区间为-0.8~0.2 V,扫描速率为50 mV/s。
1.6 样品提取
取大黄粉末0.5 g,加甲醇100 mL,浸泡1 h,过滤。取滤液25 mL,蒸干,残渣加水50 mL使其溶解,再加5 mL HCl,加热回流30 min,立即冷却。用乙醚分两次振摇提取,每次20 mL,合并乙醚层,蒸干,用三氯甲烷溶解后,置于50 mL容量瓶中,用三氯甲烷稀释至刻度,摇匀,置于4 ℃下[21]保存。
2 结果与讨论
2.1 紫外-可见吸收光谱表征
采用紫外-可见分光光度计分别对GO、GNs、DA、GNs/PDA和GNs/PDA/Au进行光谱表征。如图1所示,GO在波长230 nm处有最大吸收峰(曲线b),GNs的吸收峰较GO的红移了33 nm(曲线c),表明GO已被成功的还原为GNs。从图中曲线a可以看出DA在280 nm处有最大吸收峰,GNs/PDA在267 nm处有一个强的吸收峰(曲线d),这是由于GNs与PDA之间的相互作用所致。GNs/PDA/Au在562 nm处出现了一个新的吸收峰(曲线e),这个峰是Au纳米粒子的吸收峰。表明成功制备了GNs/PDA/Au。
2.2 X射线衍射分析
采用pert3 powder型X射线衍射仪对GNs、GNs/PDA和GNs/PDA/Au进行X射线衍射(XRD)表征。从图2a可以看出GNs在2θ=22.19° 附近出现一个新的宽衍射峰,这是由于化学还原后,移除了GO表面大量的含氧功能基团,使得层与层之间的晶面间距减小。同时GNs的衍射峰变宽,峰强度大大减弱,这是由于还原后片层尺寸更加缩小,晶体结构完整性进一步被破坏,无序度增加。图2b是GNs/PDA的XRD图,可以看到在2θ=24.9°处出现一个宽的衍射峰,与单纯GNs的衍射峰形类似,表明GNs表面已成功的被PDA膜包裹。图2c为GNs/PDA/Au的XRD图,衍射峰位置分别为:2θ=38.20°、44.46°、64.56°、77.52°和81.70°,分别对应Au纳米粒子的(111)、(200)、(220)、(311)和(222)晶面。这个结果与文献报道的Au纳米粒子的XRD特征峰吻合[9],表明Au的前驱液HAuCl4已被NaBH4成功还原成Au纳米粒子。GNs/PDA/Au的XRD峰中GNs/PDA的XRD特征峰很不明显,可能是因为Au纳米粒子在GNs/PDA的表面负载密度太高,而掩盖了GNs/PDA的峰。

图1 DA(a)、GO(b)、GNs(c)、GNs/PDA(d)和GNs/PDA/Au(e)的紫外-可见(UV-Vis)光谱图Fig.1 UV-Vis spectra of DA(a),GO(b),GNs(c),GNs/PDA(d) and GNs/PDA/Au(e)

图2 GNs(a)、GNs/PDA(b)和GNs/PDA/Au(c)的X射线衍射(XRD)图Fig.2 XRD patterns of GNs(a),GNs/PDA(b) and GNs/PDA/Au(c)
2.3 GNs/PDA/Au的扫描电镜表征
图3A为GNs/PDA/Au复合纳米材料的扫描电镜(SEM)图,可以看出Au纳米粒子均匀分散在GNs/PDA表面,只有少量Au纳米粒子有团聚现象。这可能是由于PDA作为一个良好的保护剂和连接剂有利于金纳米粒子的均匀负载。图3B为GNs/PDA/Au复合纳米材料的透射电镜(TEM),可以看出Au纳米粒子平均粒径约为40 nm。表明成功地制备了GNs/PDA/Au复合纳米材料。
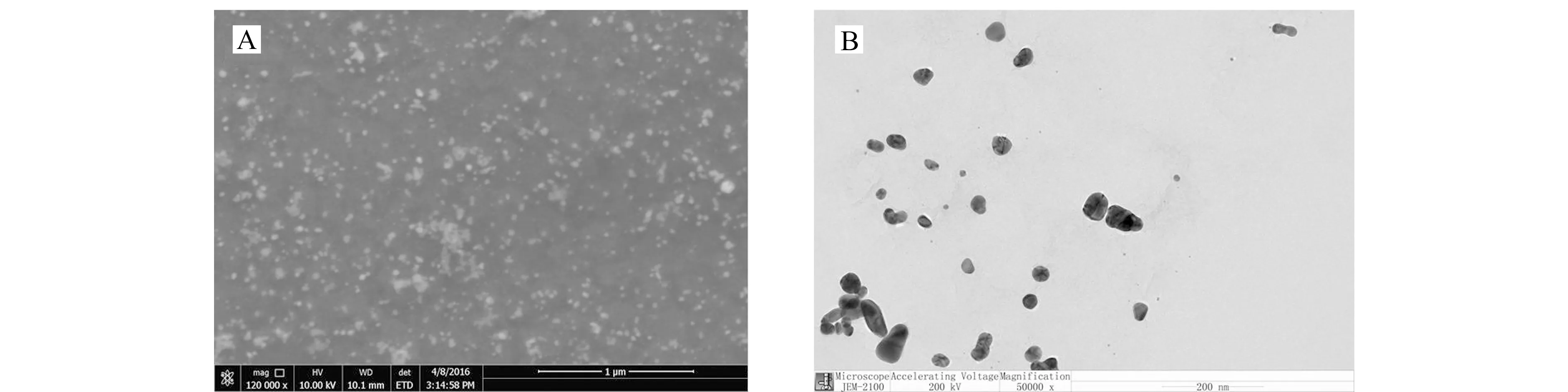
图3 GNs/PDA/Au的扫描电镜(SEM)(A)和透射电镜(TEM)(B)图Fig.3 SEM image(A)and TEM image(B)of GNs/PDA/Au
2.4 芦荟大黄素的电化学行为
考察不同材料修饰的电极在含有22.2 μmol/L芦荟大黄素的B-R缓冲溶液(pH=5.72)中的循环伏安行为(图4)。从图中可以看出,GNs/GCE(a)和GNs/PDA/GCE(b)在含芦荟大黄素的B-R缓冲溶液中无电化学响应,GNs/PDA/Au/GCE(c)在-0.6~-0.3 V之间有一对较好的可逆氧化还原峰,还原峰电位为-0.372 mV,氧化峰电位为-0.557 mV,其电位差ΔEp为185 mV。结果表明在阴极扫描过程中,芦荟大黄素被还原成蒽氢醌化合物,然后又立刻被溶液中的溶解氧氧化为芦荟大黄素,接着又在电极上被还原,从而形成一个催化循环[22]。从图中还可以看出GNs/PDA/Au复合纳米材料修饰后峰电流明显增大,这表明GNs/PDA/Au不仅增大了电极的有效表面积,而且对芦荟大黄素的氧化还原具有电催化作用。这可能是由于GNs的优异的性能,以及Au纳米粒子良好的电化学活性所致,可以加速芦荟大黄素与电极表面之间电子的传递,从而显著增加了氧化还原峰电流,提高了芦荟大黄素电化学检测性能。
2.5 pH的选择
考察了B-R缓冲溶液pH对芦荟大黄素检测的影响。从图5可知,随着pH增大芦荟大黄素的峰电流先逐渐增加,在pH=5.72时达到最大值,但继续增加pH时,峰电流反而下降。选择pH=5.72的B-R缓冲溶液为最佳检测溶液。
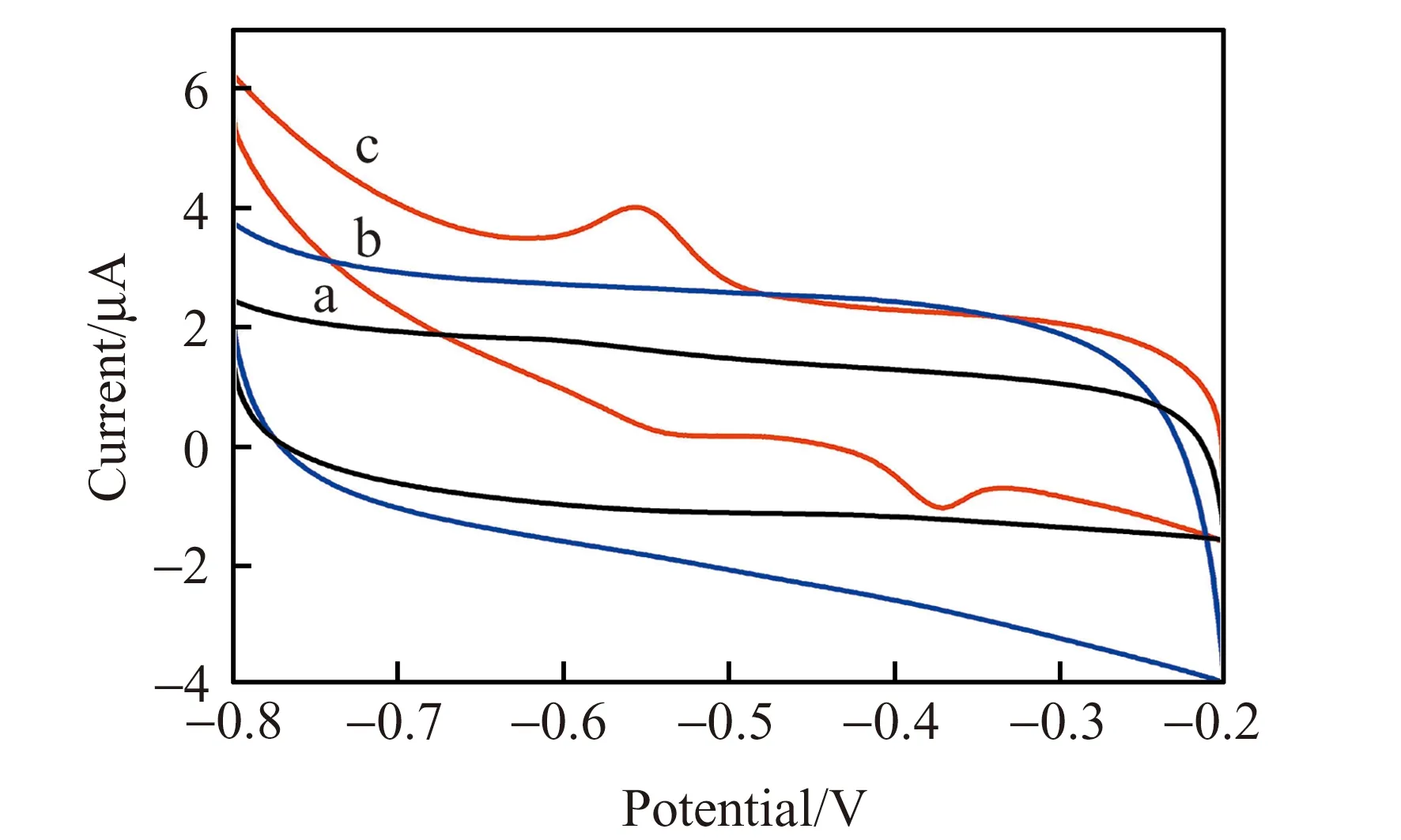
图4 芦荟大黄素在不同修饰电极上的循环伏安图Fig.4 Cyclic voltammograms of aloe emodin at different modified electrodesa:GNs modified glassy carbon electrodeb:GNs/PDA modified glassy carbon electrode;c:GNs/PDA/Au modified glassy carbon electrode.pH=5.72,t=280 s,scan rate:50 mV/s.
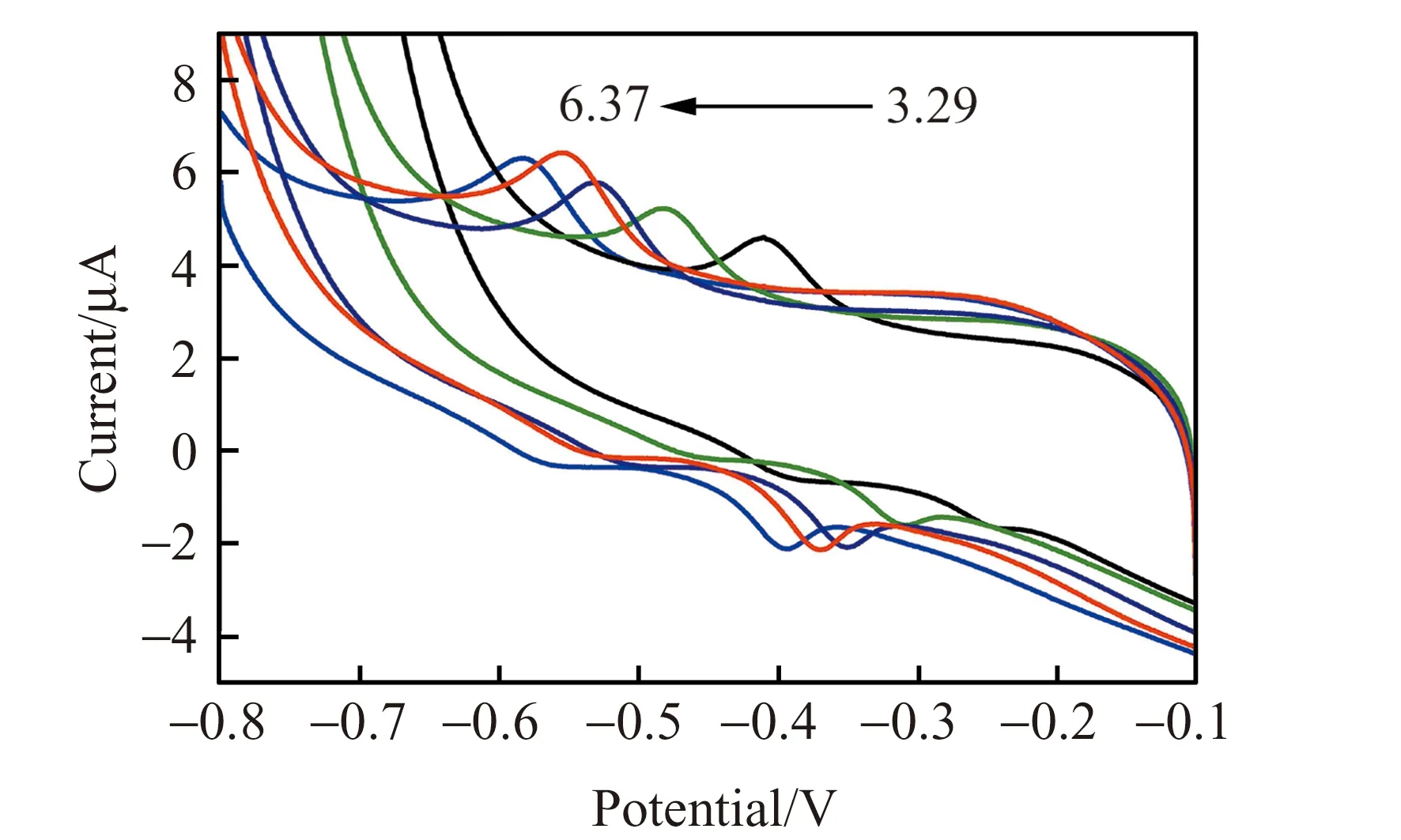
图5 芦荟大黄素GNs/PDA/Au上于不同pH B-R缓冲溶液中的循环伏安图Fig.5 Cyclic voltammograms of aloe emodin at GNs/PDA/Au in different pH B-R solutionpH:3.29、4.56、5.33、5.72、6.37.t=300 s,scan rate:50 mV/s,peak potential:-0.8--0.1 V.
2.6 富集时间的选择
考察了GNs/PDA/Au/GCE在pH=5.72的B-R缓冲溶液中,采用差分脉冲伏安法(DPV),对芦荟大黄素富集时间的影响。结果表明,在60~280 s范围内,随着富集时间的增加,峰电流依次增加,继续增大富集时间到320 s,峰电流反而减小。这可能是由于芦荟大黄素在GNs/PDA/Au/GCE表面达到了饱和状态,继续增加富集时间,会有部分芦荟大黄素非特异性吸附在电极表面,阻碍电子的传递,导致峰电流降低。选择280 s作为芦荟大黄素的最佳富集时间。
2.7 修饰电极检测芦荟大黄素的重现性和稳定性
在上述最佳条件下,采用DPV法检测芦荟大黄素。由图6知,在pH=5.72的B-R缓冲溶液中,芦荟大黄素在GNs/PDA/Au/GCE上的峰电流与其浓度在2.96~128.5 μmol/L范围内呈现良好的线性关系,线性回归方程为:Ip(μA)=0.78c(μmol/L)+5.62,线性相关系数是0.9928,线性检测范围是16.03~125.8 μmol/L,检测限为4.82 μmol/L。本文方法与邹洪等[23]报道的方法相比(线性范围为3.0~28.6 mg/L,检测限为0.06 mg/L),检测限更低,线性范围更宽。
采用DPV法研究了GNs/PDA/Au/GCE的重现性和稳定性,在pH=5.72的B-R缓冲溶液中,对浓度为24.67 μmol/L的芦荟大黄素用同一支修饰电极连续测定6次,还原峰电流的相对标准偏差(RSD)为2.4%,将修饰电极放置于冰箱中保存,2周后测定上述溶液,响应峰电流变为原来电流的89.5%,表明该GNs/PDA/Au/GCE修饰电极具有很好的重现性及稳定性。
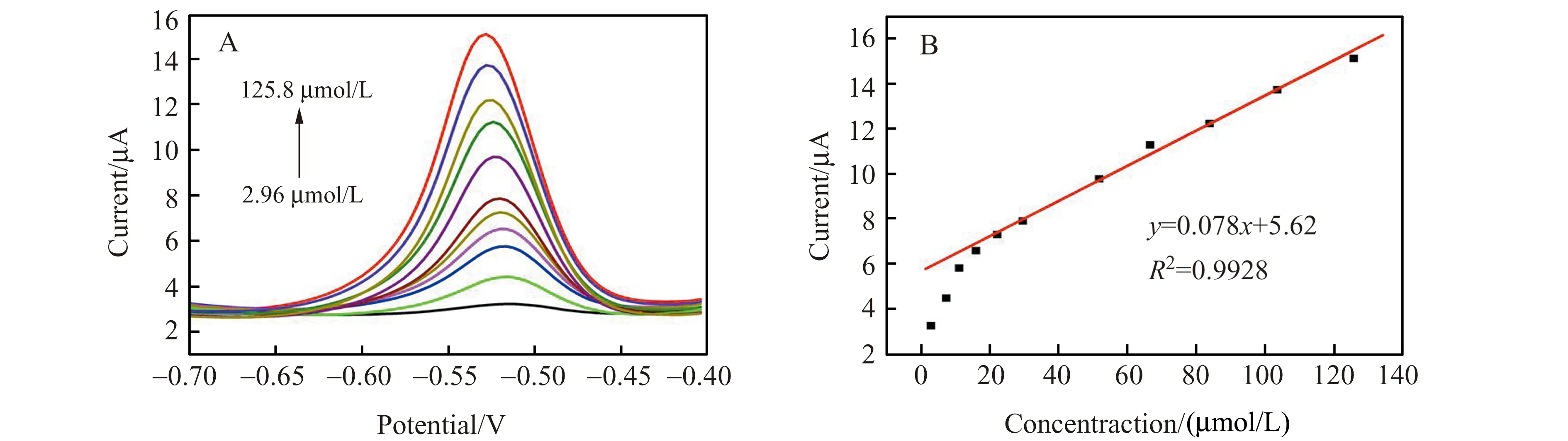
图6 (A)芦荟大黄素在GNs/PDA/Au修饰电极上的差分脉冲伏安图;(B)峰电流与芦荟大黄素浓度的线性响应曲线Fig.6 (A)Differential pulse voltammograms of different concentrations of aloe emodin at GNs/PDA/Au modified electrode;(B)Linear response curve between peak current and aloe emodin concentrationc:2.96,7.4,11.1,16.03,22.2,29.6,51.8,66.6,83.87,103.6 and 125.8 μmol/L;pH=5.72,t:280s.scan rate:50 mV/s.
2.8 样品分析及回收率
在pH=5.72的B-R缓冲溶液中,采用DPV法测定了大黄药材中芦荟大黄素的含量。取“1.6”中提取的样品溶液进行测定,结果见表1。由表可得,用GN/PDA/Au/GCE修饰电极检测到大黄药材中芦荟大黄素的含量平均为1.6 mg/g,与高效液相色谱法[24]测定的1.555 mg/g结果相一致。采用加标回收法对样品进行测定,回收率为98.6%~102.1%。表明方法准确度较高,完全满足实际样品测定需求。

表1 芦荟大黄素样品的加标回收测定Table 1 Standard recovery results of aloe emodin in samples
3 结论
本实验成功制备了GNs/PDA/Au复合纳米材料,并用紫外-可见吸收光谱、X射线衍射、扫描电镜对合成的材料进行表征。将GNs/PDA/Au复合纳米材料构建电化学传感器,用于对芦荟大黄素进行检测。采用循环伏安法(CV)和差分脉冲伏安法(DPV)对影响芦荟大黄素电化学行为的pH、富集时间进行优化。实验结果表明最佳pH为5.72,最佳富集时间为280 s。在最佳条件下,芦荟大黄素检测的线性范围为16.03~125.8 μmol/L,检测限为4.82 μmol/L,可用于药物制剂中芦荟大黄素的定量测定。该电化学检测方法适用于对实际样品的检测,可应用到药物分析中。
