慢性乙型肝炎初治后转换恩替卡韦干预的耐药及疗效观察
2020-03-13马春明张锁才史罗明吴剑明周根法郑剑
马春明 张锁才 史罗明 吴剑明 周根法 郑剑
恩替卡韦属2’-戍环脱氧鸟嘌呤核苷类似物,抑制HBV聚合酶活性较阿德福韦、拉米夫定高。据报道,恩替卡韦可抑制HBV DNA多聚酶启动及正链合成与复制、自mRNA前基因组反转录负链,对初治者治12个月时无耐药,6年仅1.3%[1]。本研究观察慢性乙型肝炎患者采用阿德福韦酯+拉米夫定初始联合治疗后转换为恩替卡韦干预的疗效及耐药性,报道如下。
资料与方法
一、 一般资料
2012年10月至2015年12月常州市第三人民医院收治的慢性乙型肝炎患者124例,获我院医学伦理委员会批准。纳入标准:(1)参照《慢性乙型肝炎防治指南(2010年版)》[2],慢性HBV感染;HBsAg阳性或阴性;(2)年龄>18岁;(3)均已接受阿德福韦酯+拉米夫定初始联合抗病毒治疗>12个月,无相关药物禁忌证;(4)获知情同意。排除标准:(1)伴失代偿性肝硬化临床表现,凝血酶原活动度<60%,血清总胆红素>35 μmol/l,白蛋白<35 g/L;(2)既往有腹水、食管胃底静脉曲张破裂出血、肝性脑病;(3)恶性肿瘤;(4)自身免疫性、药物性、酒精性肝病等所致肝功能异常者;(5)糖尿病、高血压;(6)伴甲、丙、丁、戊型肝炎及其他病毒感染;(7)伴严重心脑血管、内分泌、呼吸、血液、泌尿系统等原发疾病或精神病患;(8)妊娠期或哺乳期妇女。按照抽检随机对照法,将所有患者分为两组,各62例,两组临床资料比较差异均无统计学意义(P>0.05)。见表1。
二、 方法
(一) 治疗方法 对照组仍按原方案治疗,予阿德福韦酯(江苏正大天晴药业)10 mg,1次/d;拉米夫定(苏州葛兰素史克制药)100 mg,1次/d[3]。观察组治疗方案替换为恩替卡韦干预,即口服恩替卡韦(中美上海施贵宝制药)0.5 mg,1次/d。两组均治疗3年。
(二) 检测方法 HBV血清标志物使用电化学发光法检测,试剂购自美国雅培公司;采用荧光定量PCR仪(ABI7000型,美国ABI公司),行定量检测,治疗后HBV DNA阴性设定为<103 IU/mL,试剂购自杭州艾康生物技术有限公司;HBV耐药突变位点检测使用采用直接测序法,试剂购自上海基因科技股份有限公司。运用全自动分析仪(瑞士罗氏公司,COBAS 8000型),以免疫比浊法测定尿β2-微球蛋白、尿视黄醇结合蛋白;肾小球滤过率估计值按公式计算,即肾小球滤过率估计值=175×血肌酐1.234×年龄0.179(女性×0.79),当肾小球滤过率低于50 mL·min-1·(1.73 m2)-1时,则判断为肾功能损害。相关指标正常参考范围:尿β2-微球蛋白为0~0.025 g/mol,尿视黄醇结合蛋白为0~0.025 g/mol。
三、 观察指标
所有患者均采用门诊复查方式随访3年,每隔3个月门诊复查一次,观察两组随访1、2、3年时病毒学应答及基因耐药率、血肌酐、肾小球滤过率、尿视黄醇结合蛋白、尿β2-微球蛋白变化。
四、 统计学方法

结 果
一、 两组不同时间段病毒学应答及基因耐药率比较
观察组随访3年时HBV DNA转阴率显著高于随访1年(P<0.05),对照组随访3年时基因耐药发生率显著高于随访1年(P<0.05);观察组随访2、3年HBV DNA转阴率显著高于对照组(P<0.05),基因耐药发生率显著低于对照组(P<0.05)。见表2。
二、 两组各时点血肌酐、肾小球滤过率对比
对照组随访1、2、3年血肌酐有不同程度升高,肾小球滤过率有不同程度下降,其中随访2、3年时血肌酐显著高于随访1年(P<0.05),随访3年时肾小球滤过率显著低于随访1、2年(P<0.05);而观察组血肌酐、肾小球女滤过率基本保持基线水平。观察组随访1、2、3年血肌酐均显著低于对照组(P<0.05),肾小球滤过率均显著高于对照组(P<0.05),见表3。观察组随访2、3年时血肌酐较基线上升>50 μmol/L的比例显著低于对照组(P<0.05),随访1、2、3年时肾小球滤过率较基线下降30%的比例显著低于对照组(P<0.05),见表4。
三、 两组各时点尿视黄醇结合蛋白、尿β2-微球蛋白对比
随访2、3年,观察组尿视黄醇结合蛋白及尿β2-微球蛋白异常率显著低于对照组(P<0.05),见表5。

表1 两组一般资料比较
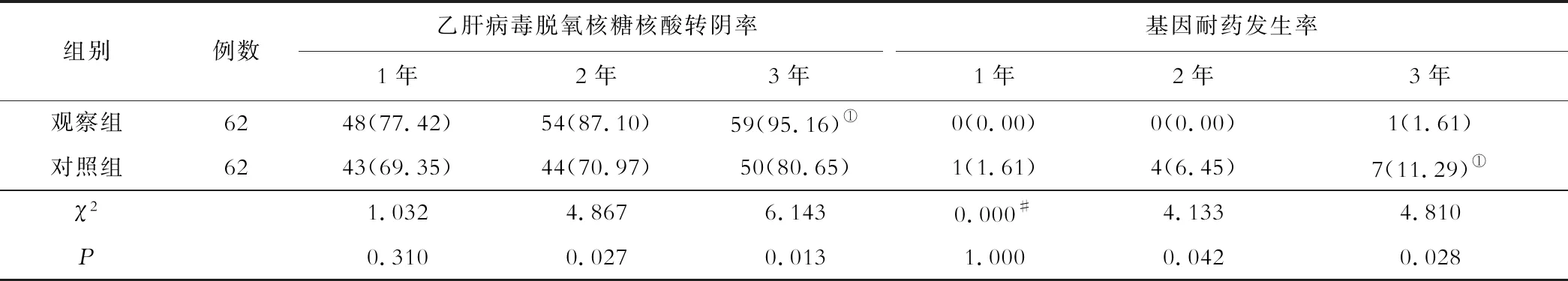
表2 两组不同时间段病毒学应答及基因耐药率比较[n(%)]
注:#取校正检验卡方值;与同组1年比较,①P<0.05

表3 两组各时点血肌酐、肾小球女滤过率对比(±s)
注:与同组1年比较,①P<0.05;与同组2年比较,②P<0.05
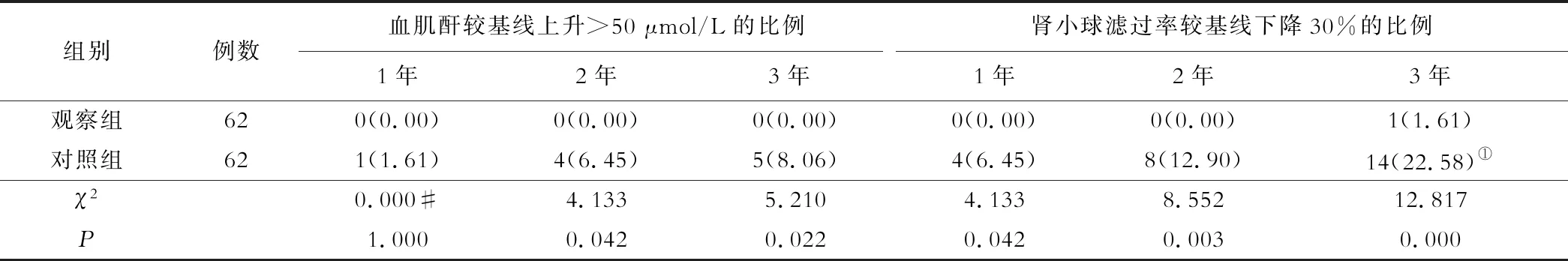
表4 两组各时点血肌酐、肾小球滤过率对比[n(%)]
注:#取校正检验卡方值;与同组1年比较,①P<0.05

表5 两组各时点尿视黄醇结合蛋白、尿β2-微球蛋白对比[n(%)]
讨 论
本研究发现,观察组随访2、3年HBV DNA转阴率明显高于对照组,基因耐药发生率明显低于对照组,证实慢性乙型肝炎患者阿德福韦酯+拉米夫定初治后转换为恩替卡韦干预,能有效提高病毒学应答率,降低耐药发生率,与Seto等[4]研究一致。赖玺杰等[5]也证实,慢性乙型肝炎患者初始阿德福韦酯+拉米夫定联合治疗方案替换恩替卡韦单药治疗,能提高病毒学应答率,减少耐药发生率。相较于恩替卡韦,核苷类似物(如阿德福韦酯、拉米夫定等)临床耐药发生率较高,与rtL180M/rtM204(I/V)位点突变相关。笔者认为,在阿德福韦酯+拉米夫定初始联合治疗未出现基因突变前,转换为恩替卡韦干预,能预防耐药发生;而本研究中,两组均出现阿德福韦酯临床耐药,其中观察组治疗方案替换为恩替卡韦干预,病毒学应答率明显提高。
本研究发现,随访1、2、3年,对照组血肌酐有不同程度升高,肾小球滤过率有不同程度下降;而观察组血肌酐、肾小球滤过率基本保持基线水平,提示患者阿德福韦酯+拉米夫定初治后转换为恩替卡韦干预,能降低肾功能损害发生率。长期使用阿德福韦酯,不良反应较多,多表现为肾毒性。有报道发现,长期接受阿德福韦酯+拉米夫定联合抗病毒治疗的292例慢性乙型肝炎患者随访16、36个月时,肾功能损害发生率分别为9.6%、7.5%,随访5年时,肾功能损害发生率达10.5%,而阿德福韦酯是诱发肾功能损害关键因素[6]。Shimizu等[7]也报道长期使用阿德福韦酯,会导致患者肾小球女滤过率降低、血肌酐升高,诱发肾小管损伤,具体机制尚未明确。笔者推测其可能机制如下:(1)肾近端小管阴离子转运蛋白-1对阿德福韦酯的亲和力相对较强,使肾近端小管细胞内易发生药物聚集;(2)阿德福韦酯对线粒体存在一定毒性作用,易诱发线粒体变形、肿胀,减少线粒体DNA,诱导肾小管对视黄醇结合蛋白、β2-微球蛋白等尿微量蛋白重吸收明显减少,引起肾功能损害。慢性乙型肝炎患者每3~6个月行肾功能复查,但肾小管功能检查并不包括在内,部分患者各项复查结果虽处于正常状态,实际上肾功能已出现损害;而临床检查发现血肌酐升高或肾小球滤过率降低时,往往预示患者肾功能损害已比较严重。
本研究发现,观察组随访2、3年尿视黄醇结合蛋白及尿β2-微球蛋白异常率较对照组低,提示示恩替卡韦对阿德福韦酯长期使用致肾功能损害具有预防作用,与Craig等[8]研究相似。尿视黄醇结合蛋白、尿β2-微球蛋白属阿德福韦酯相关性肾损害早期评估指标,长期接受阿德福韦酯+拉米夫定联合治疗者复查血常规等时,需复查尿微量蛋白,观察肾小管功能,以便及时调整治疗方案,预防肾功能损伤。
综上,对已接受阿德福韦酯+拉米夫定初始联合抗病毒治疗的慢性乙型肝炎患者替换成恩替卡韦,能提高病毒学应答,减少耐药发生率,预防长期使用阿德福韦酯致肾功能损害。但本研究样本量偏小,观察时间短,远期疗效并不明确,有待今后深入探讨。
