离子液体[Mmim][DMP]与DMSO/乙腈二元体系的密度和黏度
2020-03-10王薪薪周清张晓春张志博吕兴梅张锁江
王薪薪,周清,2,张晓春,张志博,吕兴梅,2,张锁江,2
(1 中国科学院过程工程研究所离子液体清洁过程北京市重点实验室,北京100190; 2 中国科学院大学化学工程学院,北京100049)
引 言
离子液体(ILs)作为一种绿色溶剂,在生物质预处理过程中显示出优异的性能,尤其是用在从天然植物中分离纤维素或木质素过程。2002 年美国R.D. Rogers 教授率先发现离子液体可用于纤维素溶解,由此掀起了离子液体应用于生物质预处理的研究热潮,并且将溶剂从常规离子液体逐渐拓展至功能化离子液体[1-5]。研究报道显示,当阴离子含有卤离子(F-,Cl-,Br-,I-)、磷酸根([R1O(R2O)PO2]-,[R1O(R2)PO2]-,[R1R2PO2]-)、羧 酸 根([XCOO]-, X=—R,—CH2OH,—CH2C6H5,—CH2NH2,—CH2SH)或者硫氰酸根([SCN]-)时,能够促进纤维素的溶解和分离。这是因为这些阴离子和纤维素之间可以形成氢键[6-10],从而导致纤维素之间的氢键断裂,促进了纤维素的溶解[11-12]。
一般来说,当离子液体用于纤维素溶解过程中时,随着溶解时间的延长和溶解物质含量的增加,体系的黏度迅速增大,从而导致溶解过程难以继续进行。众所周知,添加有机溶剂可以显著降低离子液体的黏度,有利于溶解过程中的传质[13-14]。因而目前预处理生物质的研究多侧重于离子液体多组分体系或分步分离。但有关离子液体溶解生物质体系的物理化学性质的报道相对来说比较少。因此,对生物质分离离子液体体系的物理化学性质,特别是生物质预处理过程及规模装置进行设计所必需的密度和黏度数据进行测定和拟合,具有重要的应用价值。
离子液体1,3-二甲基咪唑磷酸二甲酯([Mmim][DMP]),是用于纤维素预处理过程时具有良好效果的溶剂之一[15-24]。对于其混合体系的物理化学性质的研究目前报道却比较少,主要包括:醇/甲苯+己烷/庚烷/乙酸甲酯+ [Mmim][DMP]和苯+ 环己烷+[Mmim][DMP]体系的液-液平衡[25-30],醇类+水/乙酸甲酯/丙酮/氯仿/乙腈+ [Mmim][DMP]体系的汽液平衡,水/甲醇/乙醇/1-丙醇/2-丙醇+[Mmim][DMP]二元体系的蒸气压[31-37],水/乙醇/甲醇+ [Mmim][DMP]二元体系的热容[38],烷烃、烯烃、烷基苯在[Mmim][DMP]中的无限稀释活度系数[39]等。截止到目前为止,只有五篇文献报道了[Mmim][DMP]与水、乙醇、甲醇、1-丙醇、2-丙醇二元体系和[Mmim][DMP] +MDEA + H2O、LiNO3+ [MMIM][DMP] + H2O 三元体系的密度和黏度[40-44]。但是,除了水体系之外,上述研究中涉及的其他体系并未用于生物质预处理。传统的有机溶剂,如二甲基亚砜(DMSO)和乙腈,由于其良好的溶解性,在生物和化学过程中得到了广泛应用。例如,有研究报道了离子液体与DMSO 和乙腈二元体系在生物质分离中的应用[45-57]。然而,目前的文献中仍然没有[Mmim][DMP]与DMSO 或乙腈的二元体系的物理化学性质数据。
由此,本文测定了293.15~323.15 K,全浓度组成范围内离子液体[Mmim][DMP]与DMSO、乙腈二元体系的密度、黏度,并且进一步计算了体系的超额摩尔体积(VE)、表观摩尔体积(Vϕ)、无限稀释表观摩尔体积(V∞ϕ)、偏摩尔体积(-V)以及黏度偏差(Δη),并从分子间作用力、结构影响上对二元体系的超额摩尔体积、黏度偏差结果进行了讨论。
1 实验材料和方法
1.1 原料与试剂
DMSO、乙腈均为色谱纯(国药集团化学试剂厂,纯度>99%);乙醚为分析纯(天津市西华特种试剂厂,纯度>99%)。合成离子液体的原料甲基咪唑、磷酸三甲酯均为分析纯(Alfa Aesar公司,纯度>98%)。
1.2 实验装置
溶液配置采用电子天平Sartorius Scientific Instrument Co. Ltd.,BS124S,精确度为±0.0001 g,溶液的摩尔分数精确度为±0.0001;密度测量采用Anton Paar DMA 5000 振动管密度计,精确度为±5×10-6g·cm-3,温度精确度为±0.001 K;黏度测量采用Anton Paar AMVn 全自动落球式黏度计,精确度为±0.005 mPa·s,温度精确度为±0.01 K,黏度测量中所用到的四个测量管直径分别是1.6、1.8、3.0、4.0 mm,对应的钢球直径分别为1.5、1.5、2.5、3.0 mm。
1.3 离子液体1,3-二甲基咪唑磷酸二甲酯([Mmim][DMP])的合成
离子液体1,3-二甲基咪唑磷酸二甲酯([Mmim][DMP])采用之前的方法合成[44],合成步骤如下:

图1 离子液体[Mmim][DMP]的合成Fig.1 Synthesis of[Mmim][DMP]
按摩尔比1∶1 称取甲基咪唑(1.15 mol,94.4 g)和磷酸三甲酯(1.15 mol,161.1 g),将其混合于圆底烧瓶中,使用恒温加热磁力搅拌器控制反应温度为423.15 K,并在烧瓶上部通循环水冷凝,反应10 h,停止反应后,倾倒出所得液体,冷却至室温,然后用等体积量的乙醚对反应产物进行反复洗涤4次。洗涤结束后,将产物转移至圆底烧瓶,在343.15 K下旋转真空蒸发3 h,除去乙醚,接着将真空干燥箱的温度设为343.15 K,将所得产物放在里面干燥三到四天。最后得到浅黄色的液体。
将所得到的离子液体分别进行核磁、红外的表征以及水分的测定,所得结果与文献[44]报道的结果是一致的,离子液体的纯度>99%。
1.4 纯离子液体、溶剂密度和黏度的测量
为了验证所用密度计和黏度计的准确性和试剂的纯度,对所得到的纯离子液体、DMSO、乙腈进行密度、黏度测量并与文献进行比较,结果列于表1中。从表1 结果可以看出,密度值偏差<0.002,黏度值偏差<0.1。以上实验值与文献值的偏差值均在合理范围内,验证了实验设备与实验数据的准确性。
1.5 二元混合体系密度和黏度的测量
不同浓度的二元体系混合物选用容量瓶称重法进行配制,所用电子天平(ML204)的精度为±0.0001 g。配制称量时采用的是一次性滴管快速称量。然后将瓶盖迅速密封,摇匀,等待测量。所配溶液的摩尔分数的精度为±0.0001。
[Mmim][DMP]与DMSO 或乙腈的二元体系的密度(ρ)通过Anton Paar DMA 5000 密度计测量。在测量二元体系之前,用超纯水和干燥空气在大气压下校准密度计。样品溶液测量结束后,继续向振动管中推入待测样品溶液,进行重复测量,三次求平均值,使其更逼近真实值。实验重复性较好,三次测量值非常接近,在误差允许范围内。测完一种样品溶液后,要排出样品溶液,选用无水乙醇进行冲洗,洗完后,连接好循环管,打开泵循环对管吹扫、干燥。关闭泵循环后对空气的密度进行测量,并与标准值进行比较,如果差别比较大,重新清洗,直到接近标准值。黏度(η)通过Anton Paar AMVn 黏度计获得。温度范围为293.15~323.15 K,由内置的精确Peltier 恒温器控制,精度为±0.01 K。测量系统由四根毛细管(直径分别为1.6、1.8、3.0 和4.0 mm)和直径匹配的球(直径分别为1.5、1.5、2.5 和3.0 mm)组成。每个样品测量三次,实验重复性较好,三次测量值非常接近,在误差允许范围内,结果取三次平均值。测完一种样品溶液后,直接把样品吸出,再用无水乙醇清洗三遍管路,通风吹扫。

表1 纯物质的密度、黏度实验值与文献值比较Table 1 Comparison of measured with literature values of densities and viscosities of pure compounds
1.6 量子化学计算
通过Gaussian 09 软件,采用B3LYP/6-311++G**基组对[Mmim][DMP]、DMSO、乙腈、单独阴阳离子与DMSO、单独阴阳离子与乙腈,以及离子对与DMSO 和离子对与乙腈的结构进行了优化。优化构型后,通过检查振动频率不存在“虚频”来确定得到的构型是稳定构象。
2 结果与讨论
2.1 密度
实验测定了293.15~323.15 K 温度范围内二元体系[Mmim][DMP]+DMSO 和[Mmim][DMP]+乙腈溶液的密度[结果参见开放科学(资源服务)标识码(OSID)中表S1],密度和温度的关系由式(1)进行关联拟合[43]

式中,ρ为密度,g/cm3;A为拟合参数,g·cm-3;B为拟合参数,g·cm-3·K-1。拟合结果列于表2中。
密度随温度的变化如图2 所示。从图2 可以看出,相同浓度时,随着温度的升高,[Mmim][DMP]体系的密度略微减小。这是因为当温度升高时,体系内离子液体和溶剂分子的热运动加快、分子间的缔合作用减弱,导致不同分子之间的分子间距增大,从而使二元体系的体积增大,所以体系的密度减小。并且同一浓度下[Mmim][DMP]+乙腈体系的密度随温度减小得更多。这是因为相对于DMSO体系来说,乙腈体系的自由体积效应随温度的变化更明显,分子间的缔合作用减弱得更多。从表2 可以看出体系的密度随温度的升高是线性减小的,并且在所有组成下都显示出非常好的线性相关性(R2≈1)。这与纯离子液体的密度随温度的变化规律是一致的[43]。
离子液体二元体系的密度随浓度的变化如图3所示。从图3可以看出,相同温度时,两种体系的密度均随着离子液体摩尔分数的增大而增大,这是因为随着离子液体浓度的增大,离子液体和溶剂之间的离子对相互作用增强。从图中还可以看出,体系的密度在离子液体浓度较低时随着离子液体浓度的增大而急剧增大,而在较高的离子液体浓度下,密度的增大趋势变缓。这是因为纯离子液体的密度比DMSO 和乙腈大很多,当离子液体加入到溶剂里时,会迅速提高体系的密度,而随着离子液体浓度的增加,这种趋势会逐渐变缓,并慢慢接近纯离子液体的密度。

表2 方程(1)拟合参数A和B的值Table 2 Fitted values of empirical parameters A and B for densities of binary mixtures based on Eq.(1)
2.2 表观摩尔体积
表观摩尔体积一般被认为是溶液中溶质和溶剂的摩尔体积。与纯物质的摩尔体积的不同在于,表观摩尔体积可以体现体系中同种分子和不同分子之间的相互作用,比如离子-离子、溶质-溶剂以及溶剂-溶剂之间的相互作用。二元体系[Mmim][DMP] + DMSO 和[Mmim][DMP] + 乙腈溶液的表观摩尔体积Vφ,i(i=1,2)可由式(2)、式(3)计算得出[63]
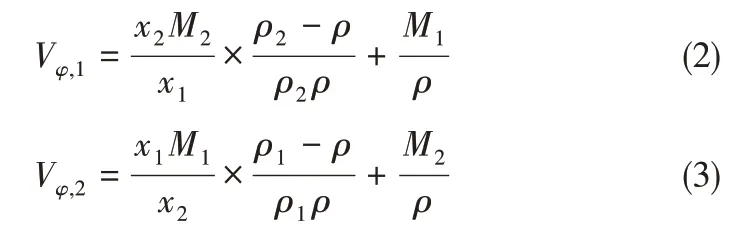
式 中,Vφ,i、xi、Mi、ρi(i=1,2)分 别 代 表[Mmim][DMP]和有机溶剂的表观摩尔体积、摩尔分数、摩尔质量和密度,ρ代表二元体系的密度。不同温度下[Mmim][DMP]和有机溶剂的表观摩尔体积值参见开放科学(资源服务)标识码(OSID)中表S2。

图2 [Mmim][DMP]二元体系的密度随温度的变化Fig.2 Densities for[Mmim][DMP]binary systems as a function of temperature at different mole fractions of IL
不同温度下[Mmim][DMP]体系的表观摩尔体积随组成的变化如图4 所示。由图4 可以看出,离子液体的表观摩尔体积随着温度和离子液体摩尔分数的增加而增大。温度较低时,离子液体在DMSO中表观摩尔体积受温度和浓度的变化比在乙腈中更明显,温度较高时,二者差距不大。从图中还可以看出,同一浓度下,离子液体的表观摩尔体积随温度的升高呈线性增大。从图4 可以看出,离子液体浓度较低时,离子液体在DMSO 中的表观摩尔体积比在乙腈中的大,而离子液体浓度较高时,二者差别很小。这是因为离子液体浓度较低时,离子液体周围被溶剂分子包围,而离子液体的阴阳离子与DMSO 之间的相互作用更弱。而在离子液体浓度较高时,溶液中的主要作用是离子液体阴阳离子之间的相互作用,所以二者的表观摩尔体积差别很小。

图3 [Mmim][DMP]二元体系的密度随组成的变化Fig.3 Densities for[Mmim][DMP]binary system as a function of mole fractions of IL at different temperatures
当离子液体的浓度接近0 时,阴阳离子被溶剂分子所包围,阴阳离子之间的相互作用变得很小,可以忽略不计。无限稀释表观摩尔体积(Vϕ∞)可以排除离子-离子相互作用的影响,用来表示离子-溶剂之间的相互作用强度。其可以通过Redlich-Mayer type[式(4)]计算得出[64]
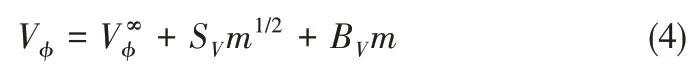
式 中,SV和BV是 经 验 参 数;m是 离 子 液 体 在DMSO 或者乙腈中的质量浓度。不同温度下离子液体的Vϕ∞值列于表3。从表中数据可以看出,Vϕ∞值都是正的,这主要是因为离子液体的浓度接近0时,阴阳离子的内在体积增大,离子-溶剂间的作用增大[63]。而且还可以看出,离子液体在DMSO 中的无限稀释表观摩尔体积比在乙腈中更大,这同样是由于离子液体的阴阳离子与DMSO之间的相互作用更弱。从表中数据还可以看出,离子液体在DMSO 中的Vϕ∞值与温度呈正相关,但在乙腈中却呈现不一样的趋势。这说明随着温度的升高,离子液体与DMSO 的相互作用减弱,但在乙腈中相互作用是增强的。

图4 不同温度下[Mmim][DMP]二元体系的表观摩尔体积随组成和温度的变化Fig.4 Apparent molar volume versus mole fractions and temperatures of[Mmim][DMP]binary system
2.3 偏摩尔体积
偏摩尔体积被认为是一定量溶质溶在1 mol 溶液中所引起的体积变化,与溶液浓度相关。与表观摩尔体积一样,偏摩尔体积也可以体现同种分子和不同分子间的相互作用。离子液体和有机溶剂的偏摩尔体积可由式(5)、式(6)计算得出[65-66]

2.4 黏度
实验测定了293.15~323.15 K 温度范围内二元体系[Mmim][DMP]+DMSO 和[Mmim][DMP]+乙腈溶液的黏度[结果参见开放科学(资源服务)标识码(OSID)中表S3]。同一浓度下,温度对体系黏度的影响可以采用Vogel-Fulcher-Tammann 方程式(7)进行关联拟合[67-68]
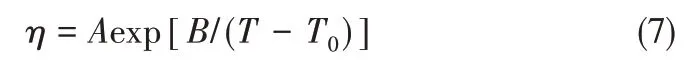

表3 293.15~323.15 K下[Mmim][DMP]的无限稀释表观摩尔体积(V ϕ∞)Table 3 Apparent molar volume at infinite dilution(V ϕ∞)of[Mmim][DMP]at temperatures from 293.15 to 323.15 K
式中,η为黏度,mPa·s;A为拟合参数,mPa·s;B为拟合参数,K;T0为玻璃化转化温度,K[58-59,69]。拟合结果列于表5中。
从表5 可以看出,离子液体与DMSO 和乙腈混合体系的黏度在各个浓度下与VFT 方程符合得很好(R2≈1)。从图5可以看出,同一浓度下,当温度从293.15 K 升至323.15 K 时,体系的黏度急剧下降。而且可以清楚地看出,相对于密度受温度的影响,温度对黏度的影响更大。这主要是由于随着温度的升高,离子液体阴阳离子之间的相互作用减弱,降低了离子液体内部的流动阻力,使其体系的黏度降低。不同温度下,二元体系的黏度随组成的变化如图6 所示,随着[Mmim][DMP]摩尔分数(x1)的降低,黏度开始急剧的减小,当x1<0.4时,黏度减小缓慢。这与密度随组成的变化规律是一致的。随着溶剂在溶液中摩尔分数的增加,越来越多的溶剂将离子液体中的阴阳离子溶剂化,导致离子间库仑力减小,致使溶液的黏度减小;而从微观上看,溶剂分子较离子液体分子体积小,溶剂的增多,使大分子流动性增加,所以导致黏度降低。从图中还可以看出,同一条件下,离子液体-DMSO 体系的黏度比离子液体-乙腈体系的黏度更大,这是由于DMSO比乙腈的黏度更大以及离子液体的阴阳离子与DMSO可以形成更强的氢键(图7、图8)导致的。

图5 [Mmim][DMP]二元体系黏度在不同组成下随温度的变化Fig.5 Viscosity for[Mmim][DMP]binary system as a function of temperature at different mole fractions of IL(The composition x1 was the mole fraction of[Mmim][DMP]in DMSO and acetonitrile,respectively)
2.5 量子化学计算的相互作用
采用量子化学计算方法优化获得的[Mmim]阳离子与乙腈、[Mmim]阳离子与DMSO 的结构见图7。由图可知,乙腈和DMSO 与[Mmim]阳离子均存在氢键作用。其中,乙腈上的N 原子与[Mmim]阳离子C2位上的H 原子形成氢键,键长为2.109 Å(1 Å=0.1 nm)。DMSO 上的O 原子与[Mmim]阳离子C2位上的H 原子形成的氢键键长为1.903 Å。另外,DMSO 上的O原子与[Mmim]阳离子甲基基团上的H原子也形成氢键,键长为2.358 Å。
表4 293.15~323.15 K下[Mmim][DMP](1)+DMSO(2)和[Mmim][DMP](1)+乙腈(2)体系的偏摩尔体积Table 4 Partial molar volumes()of mixtures of[Mmim][DMP]with DMSO and acetonitrile at temperatures from 293.15 to 323.15 K

表4 293.15~323.15 K下[Mmim][DMP](1)+DMSO(2)和[Mmim][DMP](1)+乙腈(2)体系的偏摩尔体积Table 4 Partial molar volumes()of mixtures of[Mmim][DMP]with DMSO and acetonitrile at temperatures from 293.15 to 323.15 K
注:x1为[Mmim][DMP]的摩尔分数; 为[Mmim][DMP]的偏摩尔体积; 为DMSO 或乙腈的偏摩尔体积;标准不确定度u,u(T)=0.01 K,u(x)=0.0001;相对扩展不确定度Ur,U(r)=0.005 cm3·mol-1。
-V1/(cm3·mol-1)-V2/(cm3·mol-1)x1 293.15 K 298.15 K 303.15 K 308.15 K 313.15 K 318.15 K 323.15 K 293.15 K 298.15 K 303.15 K 308.15 K 313.15 K 318.15 K 323.15 K[Mmim][DMP](1)+DMSO(2)0 0.1002 0.1997 0.2998 0.4000 0.5008 0.6023 0.7014 0.7996 0.8964 1.0000[Mmim][DMP](1)+乙腈(2)0 0.0901 0.2010 0.3001 0.4013 0.5005 0.5984 0.6978 0.8007 0.8995 1.0000 201.93 195.17 190.64 187.30 184.77 182.71 181.05 179.69 178.55 177.57 176.65 202.85 195.49 190.62 187.08 184.42 182.26 180.55 179.19 178.07 177.12 176.15 203.78 196.29 191.34 187.74 185.05 182.85 181.12 179.72 178.57 177.62 176.64 204.73 197.09 192.07 188.40 185.70 183.42 181.67 180.24 179.07 178.10 177.12 205.68 197.90 192.79 189.07 186.32 184.01 182.23 180.78 179.59 178.60 177.60 206.64 198.72 193.52 189.74 186.95 184.60 182.79 181.32 180.11 179.10 178.09 207.61 199.55 194.26 190.41 187.58 185.20 183.36 181.86 180.63 179.60 178.57 70.63 68.31 66.72 65.58 64.66 63.97 63.41 62.96 62.58 62.17 61.77 70.94 68.58 66.97 65.81 64.88 64.18 63.59 63.14 62.77 62.36 61.94 71.26 68.86 67.23 66.07 65.08 64.39 63.79 63.32 62.95 62.55 62.12 71.58 69.14 67.48 66.30 65.30 64.60 63.99 63.51 63.13 62.72 62.28 71.90 69.42 67.74 66.54 65.52 64.81 64.19 63.71 63.31 62.90 62.45 72.23 69.71 67.99 66.78 65.74 65.02 64.39 63.90 63.50 63.08 62.62 72.55 69.99 68.25 67.02 65.96 65.23 64.59 64.09 63.68 63.26 62.80 53.51 45.81 41.10 38.79 37.25 36.11 35.36 34.74 34.24 33.62 32.99 283.98 243.49 219.19 206.58 198.07 192.11 187.65 184.11 181.12 178.72 176.65 285.95 243.74 218.63 205.63 196.96 190.97 186.56 183.17 180.37 178.11 176.15 287.96 245.05 219.59 206.43 197.66 191.60 187.16 183.72 180.88 178.64 176.64 290.02 246.39 220.55 207.23 198.36 192.23 187.74 184.26 181.40 179.14 177.12 292.11 247.74 221.53 208.04 199.07 192.88 188.34 184.82 181.92 179.65 177.60 294.25 249.10 222.55 208.85 199.78 193.55 188.93 185.38 182.45 180.17 178.09 296.43 250.48 223.61 209.67 200.50 194.22 189.54 185.95 182.99 180.70 178.57 51.50 44.40 40.07 37.88 36.38 35.35 34.65 34.06 33.48 33.05 32.45 51.81 44.62 40.24 38.02 36.52 35.48 34.76 34.17 33.63 33.14 32.55 52.14 44.85 40.41 38.18 36.65 35.61 34.88 34.28 33.74 33.25 32.64 52.48 45.07 40.59 38.33 36.79 35.74 35.00 34.39 33.86 33.34 32.72 52.82 45.30 40.76 38.48 36.94 35.86 35.12 34.50 33.98 33.44 32.81 53.16 45.56 40.93 38.64 37.10 35.98 35.24 34.62 34.11 33.53 32.90
优化获得的[DMP]阴离子与乙腈、[DMP]阴离子与DMSO的结构见图8。由图可知,乙腈和DMSO和[DMP]阴离子均形成了氢键。其中,乙腈甲基上的2个H 原子与[DMP]阴离子上的2 个O 原子分别形成了键长为2.331 和2.334 Å 的氢键。DMSO 甲基上的2 个H 原子与[[DMP]阴离子上的O 原子分别形成了键长为2.138和2.144 Å的氢键。
优化获得的[Mmim][DMP]与DMSO、[Mmim][DMP]与乙腈的结构见图9。由图可知,乙腈与阴阳离子均形成了氢键,其中,乙腈上的N 原子与[Mmim]阳离子甲基基团上的H 原子形成了氢键,键长为2.578 Å,乙腈甲基基团上的H 原子与[DMP]阴离子上的O 原子形成了氢键,键长为2.147 Å。DMSO 与阴阳离子也均形成了氢键,其中,DMSO 上的O原子与[Mmim]阳离子甲基基团上的H原子形成的氢键键长为2.206 Å,DMSO 甲基基团上的H 原子与[DMP]阴离子上的O 原子形成的氢键键长为2.129 Å。
2.6 超额摩尔体积与黏度偏差
超额摩尔体积(VE)和黏度偏差(Δη)可分别由密度和黏度的实验数据计算所得,是非常重要的热力学数据,表明了混合物与理想混合物之间的差异,也可以体现分子间的相互作用。混合体系的超额摩尔体积和黏度偏差分别由式(8)和式(9)计算得到[58-60]

表5 VFT方程拟合参数A,B和T0的值Table 5 Fitted values of empirical parameters,A,B and T0 for viscosity based on VFT equation

式中,ρ1、ρ2和ρ分别为离子液体、溶剂与离子液体和溶剂二元体系的密度,g·cm-3;M1和M2分别是离子液体和溶剂的摩尔质量,g·mol-1;x1和x2分别是离子液体和溶剂的摩尔分数。η1、η2和η分别为离子液体、溶剂和二元体系的黏度,mPa·s。其计算结果参见开放科学(资源服务)标识码(OSID)中表S4。
华安说,你跑后,欧阳橘红在保卫科反省了一个月,写了五万多字检讨。她怕过不了关,把思想深处点点滴滴的活思想都挖了出来。包括和雷志雄不和谐的性生活也和盘托出,把与你的关系上升到世界观的高度加以批判。在保卫科反省一个月后就接受群众批斗。批斗大会上,欧阳橘红胸前挂一串破鞋,两小时的批斗,她的眼睛都盯在自己的脚尖上,眼神不敢朝台下瞄。厂门前,有个大批判专栏,题目是《把欧阳橘红的腐朽思想批深批臭》。大批判办命令她,每天上班前二十分钟,站在批判栏前,把每一篇批臭她的文章,读二遍以上,不少于四十分钟。那时正是上班高峰,又是上班的必由之路,大家看猴似的,看她读批臭自己的文章。
超额摩尔体积VE和黏度偏差Δη可采用Redlich-Kister方程[式(10)]进行关联拟合[58-60]:

式中,参数Ai和标准偏差σ结果列于表6 中。式(11)为标准偏差的计算公式[58-60]:
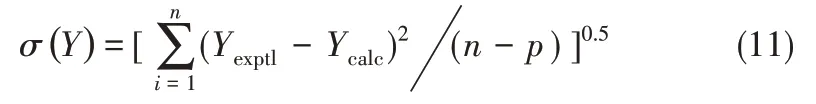

图6 [Mmim][DMP]二元体系的黏度不同温度下随组成的变化Fig.6 Viscosity for[Mmim][DMP](1)+DMSO binary system as a function of mole fractions of IL at different temperatures
式中,n为实验数据的个数;p为参数的个数;下角标exptl和calc分别是实验值和计算值。从表6中可以看到,超额体积用Redlich-Kister 方程关联较好,计算得到的标准偏差均小于0.05。

图7 B3LYP/6-311++G**基组优化的[Mmim]阳离子与乙腈和DMSO的结构Fig.7 Optimized structures of[Mmim]-acetonitrile and[Mmim]-DMSO obtained at the B3LYP/6-311++G**level(Hydrogen bonds are indicated by dotted lines,and distances are in angstroms)


图8 B3LYP/6-311++G**基组优化的[DMP]阴离子与乙腈和DMSO的结构Fig.8 Optimized structures of[DMP]-acetonitrile and[DMP]-DMSO obtained at B3LYP/6-311++G**level(Hydrogen bonds are indicated by dotted lines,and distances are in angstroms)
离子液体与溶剂二元体系黏度偏差如图11 所示,黏度偏差在所有组成下均为负值,并且在相同浓度下,体系的黏度偏差随着温度的升高是逐渐减小的。根据文献可知,体系的黏度偏差主要受分子间相互作用、分子形状和大小的影响。当混合物之间范德华力占主导地位时,黏度偏差为负。当溶剂与溶质之间的特殊作用力,例如氢键占主导地位时,黏度偏差为正。所以黏度偏差的正负可以通过混合物中存在的氢键与范德华相互作用的强弱来解释。在本文中,离子液体黏度比溶剂黏度大,而且在离子液体中,离子之间产生的离子键作用要远远大于分子之间作用力。同时,当溶剂加入到离子液体内,溶剂对离子液体的阴阳离子进行包裹,形成溶剂化作用,促使离子液体黏度急剧下滑,从而产生负偏差,而离子液体摩尔分数在0.6~0.7 之间时,溶剂对离子液体溶剂化的效应最大,黏度偏差产生最小值。
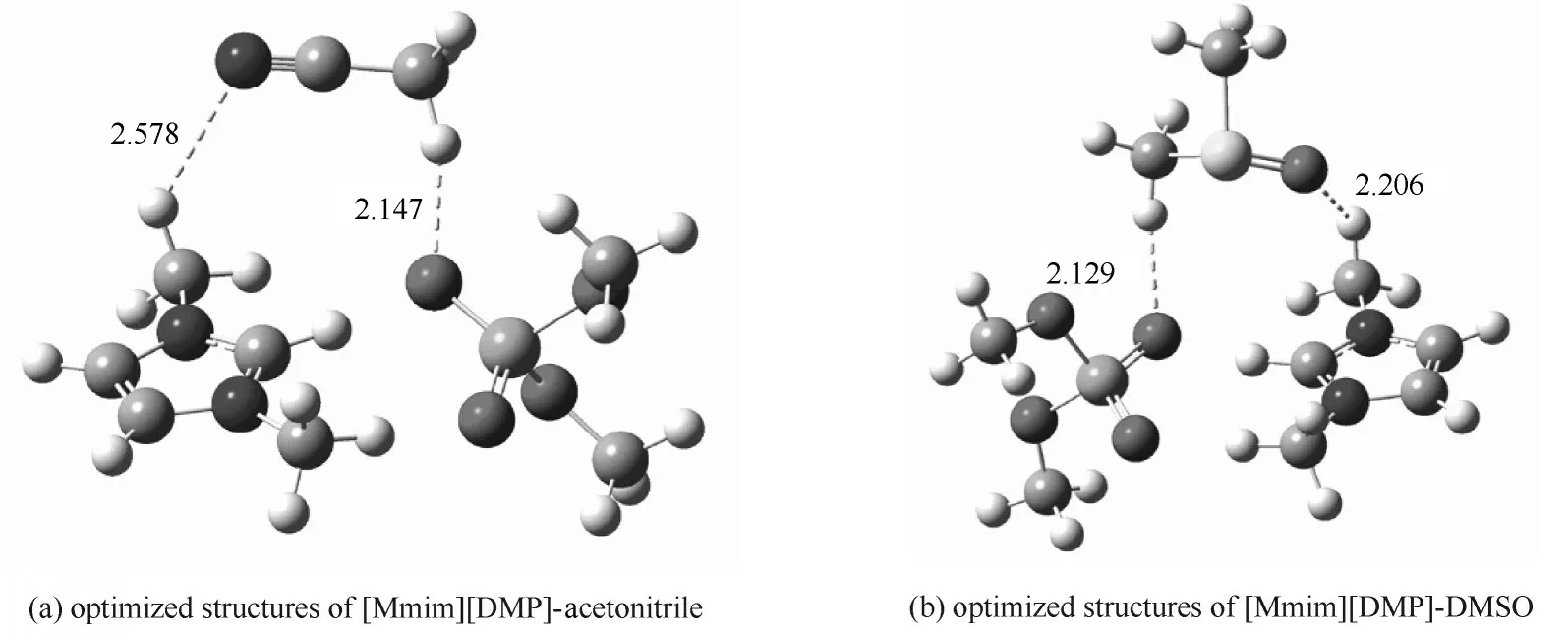
图9 B3LYP/6-311++G**基组优化的[Mmim][DMP]与乙腈和DMSO的结构Fig.9 Optimized structures of[Mmim][DMP]-acetonitrile and[Mmim][DMP]-DMSO obtained at the B3LYP/6-311++G**level(Hydrogen bonds are indicated by dotted lines,and distances are in angstroms)

图10 [Mmim][DMP]二元体系的超额摩尔体积不同温度下随组成的变化Fig.10 Excess molar volumes for mixtures of[Mmim][DMP]binary system as a function of mole fractions of IL at different temperatures(The solid curves are calculated with Redlich-Kister equation,and symbols represent experimental values)

图11 [Mmim][DMP]二元体系的黏度偏差不同温度下随组成的变化Fig.11 Viscosity deviations for mixtures of[Mmim][DMP]binary system at different temperatures(The solid curves are calculated with Redlich-Kister equation,and symbols represent experimental values)

表6 二元混合体系VE和Δη的回归系数及标准偏差Table 6 Coefficients of standard deviation and Redlich-Kister equation for VE and Δη for two mixtures of[Mmim][DMP]with DMSO and acetonitrile
3 结 论

(1)二元混合溶液的密度随着温度的升高而线性减小,而混合溶液的密度随着离子液体含量增加而非线性增加。二元混合溶液的黏度随着温度的升高呈非线性减小,同一温度下随着离子液体摩尔分数的增加,黏度也呈非线性减小。
(2)离子液体的表观摩尔体积和无限稀释表观摩尔体积、偏摩尔体积都是正值,其中,表观摩尔体积随着温度和离子液体摩尔分数的增加呈现大致升高的趋势,偏摩尔体积随着温度的升高而增大,随着离子液体摩尔分数的升高而减小。
(3)分子模拟结果表明离子液体的阴阳离子分别可与DMSO和乙腈形成氢键。
(4)VE和Δη均为负值,其中,VE在组成0.3~0.4之间有最小值,Δη在组成0.6~0.7 之间时有最小值。同一组成下,VE和Δη均随着温度的升高而减小。
符 号 说 明
A——多项式方程拟合参数,g·cm-3
Ai——Redlich-Kister拟合参数
B——多项式方程拟合参数,g·cm-3·K-1
BV——经验参数,kg·m-3
M1,M2——分别为离子液体和溶剂的摩尔质量,g·mol-1
m——离子液体在溶剂中的质量浓度,mol·kg-1
n——实验值个数
p——实验参数
R2——线性相关系数
SV——经验参数,mol·kg-1
T——温度,K
T0——玻璃化转化温度,K
Ur——相对扩展不确定度
u——标准不确定度
VE——超额摩尔体积,cm3·mol-1
Vφ,1,Vφ,2——分别为离子液体和溶剂的表观摩尔体积,cm3·mol-1
V10,V20——分别为离子液体和溶剂的摩尔体积,cm3·mol-1
x1,x2——分别为离子液体和溶剂的摩尔分数
Y——VE或Δη
η1,η2,η——分别为离子液体、有机溶剂和二元体系的黏度,mPa·s
Δη——黏度偏差,mPa·s
ρ1,ρ2,ρ——分别为离子液体、有机溶剂和二元体系的密度,g·cm-3
σ——标准偏差
下角标
calc——计算值
exptl——实验值
