颅内动静脉畸形患儿血管内栓塞术后出血的危险因素分析
2020-03-09
(徐州市儿童医院SICU,江苏 徐州 221000)
颅内动静脉畸形(cerebral arteriovenous malformation,cAVM)是一种先天性血管畸形,颅内异常发育的血管团不经毛细血管床而直接连接动脉和静脉,形成动静脉短路,导致血流动力学紊乱[1]。cAVM虽然在儿童中的发病率较低,却是儿童颅内自发性出血最常见的原因,儿童cAVM的出血率为2.6%,病死率高达37%[2]。随着介入技术的发展,血管内栓塞术成为治疗儿童cAVM的主要方法,其通过栓塞主干动脉达到封闭畸形通道、缩小异常血管团的目的。栓塞术的主要优势在于创伤小、术后并发症少,但处理不当也会发生颅内出血等严重并发症[3]。本研究回顾性分析经血管内栓塞术治疗的cAVM患者发生术后出血的相关危险因素,以期为栓塞术后出血的防治提供参考。
1 资料与方法
1.1 临床资料
纳入2013年8月至2018年8月于我院诊断为cAVM并行血管内栓塞治疗的患者180例。其中,男98例,女82例;年龄4~17岁,平均(10.4±2.3)岁;颅内出血起病138例(76.7%),反复抽搐17例(9.4%),反复头痛14例(7.8%),逐渐加重的神经功能缺损11例(6.1%)。纳入标准:年龄3~18岁;经影像学或全脑数字减影血管造影(digital subtraction angiography,DSA)确诊;首次血管内治疗且未接受过显微外科或放射治疗;入院时GCS≥10分。排除生命体征不稳定、脑疝及合并其他颅内病变患者。
1.2 方法
1.2.1 手术方法 患者取仰卧位,全身麻醉,经股动脉插管行全脑DSA初步评估畸形血管位置、长度和直径,明确后使用肝素抗凝,保持国际标准比率(International Standard Ratio,INR)为2.0~2.5。将0.035#导丝插入患侧颈内动脉/椎基底动脉系统,根据造影显示结果选择相应型号的漂浮导管插入畸形血管团,在DSA指导下注入栓塞剂,出现返流则停止注射,行双面正侧位造影观察栓塞情况。术后血压管理:有高血压病史的患者将血压控制在基础血压1/3水平以下,无高血压病史的患者控制在术前水平以下。于麻醉复苏后行神经系统体格检查,疑似神经功能损害者复查头颅CT或MRI。
1.2.2 资料收集 查阅相关文献,收集患者基本资料、脑动静脉畸形特点、手术情况及术后管理等15项可能影响栓塞术后出血的指标。患者基本资料:性别、年龄、出血史、癫痫史、高血压史;脑动静脉畸形特点:畸形血管位置(功能区/非功能区,幕上/幕下)、畸形血管直径(大:>6 cm;中:3~6 cm;小:<3 cm)、S-M分级(Ⅰ~Ⅳ级)、是否有深静脉引流、是否合并动脉瘤;手术情况:栓塞时间(>60 min或≤60 min)、栓塞体积(≥36.5%或<36.5%)、是否引流静脉栓塞(静脉中是否有栓塞剂填充);术后管理:血压是否达标、是否使用脱水剂。资料中所涉及的造影结果均由两名5年以上经验的医师做双盲阅片得到。
1.3 栓塞术后颅内出血诊断标准
栓塞术后颅内出血诊断标准为,术后1周内患者有新发的神经功能缺损症状、原有症状加重、伴或不伴意识状态改变、影像学检查出现新发出血灶。
1.4 统计学方法
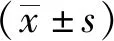
2 结果
2.1 栓塞术后颅内出血发生情况
纳入研究的180例患者,术后148例(82.22%)未发生颅内出血,32例(17.78%)发生颅内出血,多发生在术后3 d内。其中脑实质出血20例,蛛网膜下腔出血8例,脑室出血4例。颅内出血S-M分级:Ⅰ级8例、Ⅱ级16例、Ⅲ级6例、Ⅳ级2例。
2.2 cAVM栓塞术后颅内出血相关指标单因素分析
单因素分析结果显示,高血压史、出血史、畸形血管直径、深静脉引流、合并动脉瘤、栓塞体积、引流静脉栓塞及术后血压未达标是影响栓塞术后颅内出血的危险因素(P<0.05);而性别、年龄、癫痫史、畸形血管位置、S-M分级、栓塞时间及术后使用脱水剂与术后出血无关(P>0.05),见表1。
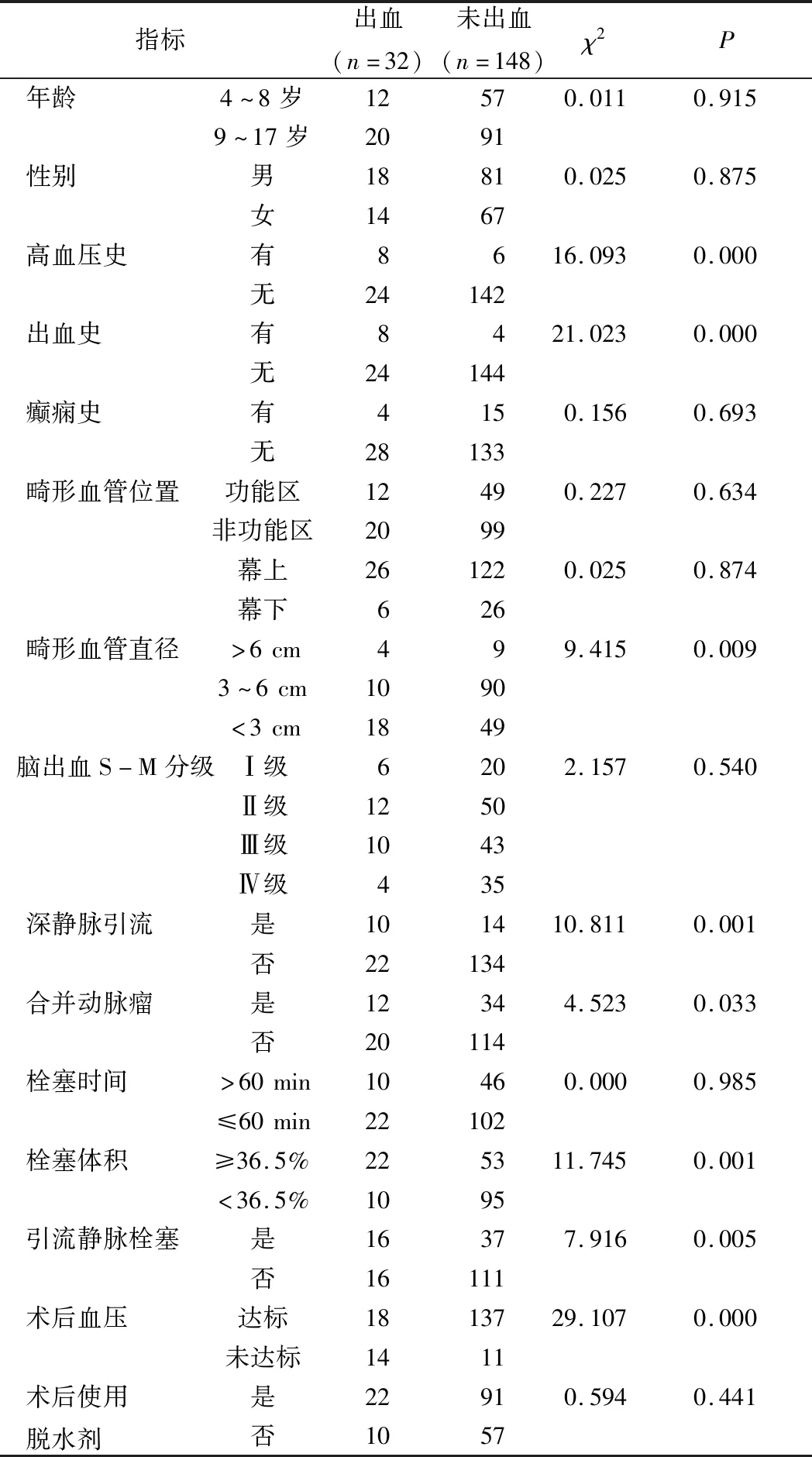
表1 cAVM栓塞术后颅内出血相关指标的单因素分析(例)
2.3 多因素Logistic回归分析
多因素Logistic回归分析显示,出血史、深静脉引流及引流静脉栓塞是血管内栓塞术后颅内出血的独立性危险因素(P<0.05),见表2。
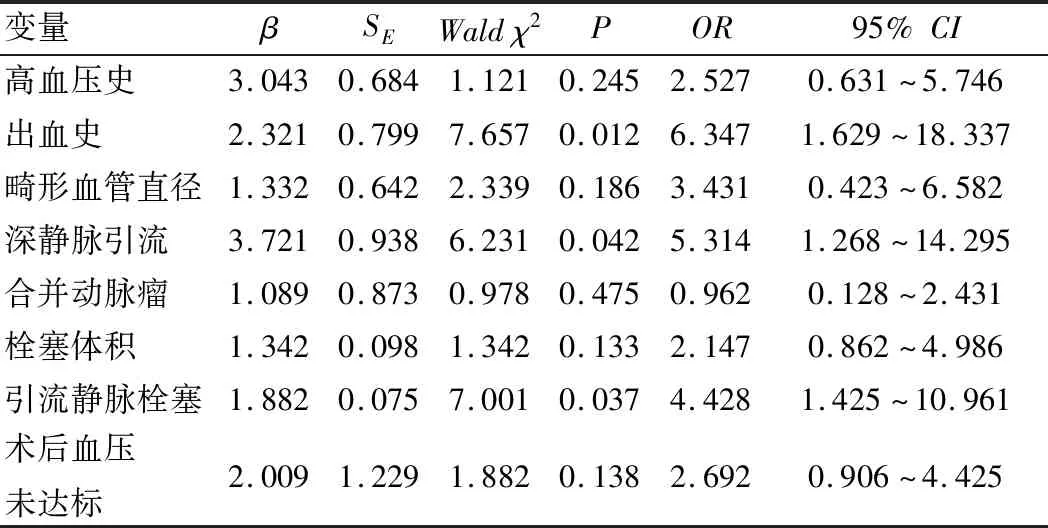
表2 cAVM栓塞术后颅内出血危险因素Logistic回归分析
3 讨论
cAVM是一种先天颅内血管发育畸形,胚胎3周时动静脉间的正常毛细血管床发育失败,形成异常血管团直接连接主干动静脉,导致局部脑组织血流分布异常、低动脉流入压、高静脉流出压、脑组织灌注不足,从而引发各种神经系统症状[4]。临床上可以自发性出血、抽搐、头痛或神经功能缺损等多种形式起病,其中自发性出血最常见[5]。据统计,儿童cAVM以颅内自发性出血起病的比例高达2%~4%,高于成人的1%~2%[6]。此外,由于儿童cAVM发生在幕下的比例较高(儿童23%,成人15%),出血后造成的神经功能损伤更重、病死率更高[7]。
随着微创技术的不断发展,血管内栓塞治疗凭借风险低、创伤小、术后恢复快等优势成为治疗cAVM的重要手段[8]。尤其对病变广泛、位于重要区域、出血严重、手术切除难度大或手术后可能引发过度灌注综合征者,栓塞治疗是首选方法[9]。但该方法最大的问题是术后颅内出血,这是血管内栓塞最严重也是最常见的并发症,是影响手术效果和患者生活质量的主要因素[10]。目前国内外文献中有关栓塞后颅内出血的危险因素说法不一。国外学者对215例行栓塞后放射治疗的cAVM患者进行了回顾性研究,术后出血发生率为 6.7%,认为畸形血管位置、直径、栓塞难度及深静脉引流是出血发生的主要危险因素[11];有研究显示,出血史和高血压史也增加了栓塞后出血的风险[12]。国内学者认为,栓塞体积≥36.5%、引流静脉中栓塞剂填充这两大栓塞术中的危险因素应该引起高度重视[13]。本研究收集了180例行栓塞治疗的cAVM患者,术后出血发生率为17.78%,单因素分析显示,高血压史、出血史、畸形血管直径、深静脉引流、合并动脉瘤、栓塞体积、引流静脉栓塞及术后血压未达标是术后出血的影响因素;多因素分析显示,出血史、深静脉引流及引流静脉栓塞是术后出血的独立性危险因素。
出血史作为栓塞术后出血的危险因素也有较多文献报道,有文献对158例术后出血患者进行了Logistic分析,结果显示出血史、脑动静脉畸形分级和深静脉引流为栓塞术后出血的三大危险因素,且出血史是最重要的危险因素。推测原因为多次出血的畸形血管壁薄弱,栓塞治疗引起血流动力学突然改变,局部栓塞区域血流量降低,非栓塞区域血流量增加,压力增大,进而导致本就薄弱的血管壁破裂出血[14]。Gobin等[15]的研究显示,脑动静脉畸形Ⅱ~Ⅴ级患者术后出血发生率与畸形血管团大小、是否位于功能区和深静脉引流有关。本研究显示,血管团直径和深静脉引流是术后出血的影响因素,其中深静脉引流为独立危险因素,但血管团是否位于功能区并未对出血造成影响,推测可能与样本偏倚有关。关于引流静脉栓塞作为术后出血的危险因素的文献报道较少见,但有研究证实引流静脉栓塞与术后高灌注损伤密切相关[14-16]。Gondar等[17]对52例行栓塞治疗的cAVM患者进行了观察,发现所有引流静脉保留者术后均未出现高灌注损伤,栓塞1条以上者13.7%术后发生高灌注损伤,所有引流静脉均栓塞者发生高灌注损伤达45.6%,证实了保留引流静脉对减轻高灌注损伤的意义。本研究显示,引流静脉栓塞是cAVM栓塞后出血的独立性危险因素,除了与高灌注损伤有关外,还有可能由于引流静脉还引流部分正常脑组织血液,栓塞后导致部分正常脑组织血液回流受阻,引起静脉性出血。此外,在本研究中单因素分析有意义的高血压史和术后血压控制未达标被许多研究证实是成人cAVM术后出血的危险因素,对于儿童而言,由于高血压病史短,血压对血管壁损伤程度轻,血管弹性好,高血压对术后出血的影响相对较小,但若联合其他危险因素,则可能导致出血风险大大增加,不容忽视[18]。需要特别注意的是cAVM直径与术后出血的关系,直径小的cAVM更易发生出血,一方面由于直径越小,引流静脉越小,栓塞造成的高灌注损伤越严重;另一方面有学者认为,低分化、发育差的畸形血管团直径偏小,血管壁更薄弱[19]。结合本研究结果,在临床选择栓塞治疗cAVM时,需要警惕上述影响因素,若有无法改变的影响因素存在,在手术中可采取一些防范措施,如适当减小栓塞体积,将深静脉引流改为双向引流,保留引流静脉等。
综上所述,出血史、深静脉引流及引流静脉栓塞是cAVM栓塞术后出血的独立性危险因素,正确认识并在手术过程中采取相应的防范措施有利于降低栓塞出血并发症的发生率。
