枸杞中原花青素和总黄酮的抗氧化活性研究
2020-03-07黄婷周璐梅婵徐慧
黄婷,周璐,梅婵,徐慧
(江苏省理化测试中心,江苏南京 210042)
原花青素和黄酮是枸杞中最主要的两类活性成分,二者最显著的活性为抗氧化活性。目前常使用的抗氧化方法分为两类:一类为基于H原子转移的方法(HAT),包括ORAC法、TRAP法、脂质过氧化法等;另一类为基于电子转移的方法(SET),主要包括FRAP法、ABTS法、DPPH法等,这些方法多采用分光光度计测定颜色的变化,使用简单快速[1]。本实验中评价原花青素和黄酮的抗氧化活性采用FRAP法及DPPH法,以研究枸杞中原花青素和黄酮的抗氧化活性。
1 材料与方法
1.1 材料与仪器
枸杞(特级黑枸杞,宁夏);原花青素标准品(阿达玛斯贝塔(上海)化学试剂有限公司);芦丁(总黄酮)标准品(阿达玛斯贝塔(上海)化学试剂有限公司);TPTZ(阿达玛斯贝塔(上海)化学试剂有限公司);DPPH(阿达玛斯贝塔(上海)化学试剂有限公司);ABTS(阿达玛斯贝塔(上海)化学试剂有限公司)。
KQ-400KDE型高功率数控超声波清洗器(昆山市超声仪器有限公司);TGL-16B高速台式离心机(上海安亭科学仪器厂);A-1000S水流抽气机(上海爱朗仪器有限公司);OSB-2100油浴锅(上海爱朗仪器有限公司);UV-2102PC分光光度计(龙尼柯(上海)仪器有限公司);HH-1系列数显恒温水浴锅(上海江星仪器有限公司)。
1.2 枸杞中生物活性物质含量的测定
1.2.1 原花青素含量测定
称取原花青素标准品10.00 mg,加入甲醇并用超声溶解,定容至 10 mL,分别吸取 0 mL、0.10 mL、0.25 mL、0.50 mL、1.00 mL、1.50 mL,用甲醇定容至10 mL 容量瓶中,制得含量为 0.0~150.0 μg/mL 的系列标准溶液。将正丁醇与盐酸按95∶5的体积比配制成300 mL混合溶液,储存备用。将枸杞样品研成粉末,密封置于阴暗处储存。称取粉末样品0.50 g,用30 mL乙醇溶解,并用超声处理约20 min,用乙醇定容至50 mL,摇匀,必要时离心或放置澄清后取上清液。于10 mL具塞试管中分别加入6 mL正丁醇盐酸溶液、1 mL系列标准管溶液和样品溶液、2 mL硫酸铁铵溶液(用2 mol/L盐酸配成2%的溶液),混匀,同步做空白实验。将所有试管置于沸水中精确反应40 min 后,立即放在冰水中 15 min。在 546 nm 处,用甲醇调零,测定标准系列溶液和样品的吸光度。
1.2.2 总黄酮含量测定
称取总黄酮标准品20.00 mg,并用80%乙醇溶解定容至100 mL容量瓶中。分别吸取上述溶液2.5 mL、5.0 mL、7.5 mL、10.0 mL、12.5 mL、15.0 mL、17.5 mL、20.0 mL 于 25 mL 容量瓶,用 80% 乙醇准确定容至刻度,摇匀,制得20.0~160.0 μg/mL的系列标准溶液。吸取0.5 mL上述系列标准溶液,依次加入1.5 mL 95% 的乙醇溶液、0.1 mL 10% 的 AlCl3溶液、0.1 mL 1 mol/L 的乙酸钾溶液以及 2.8 mL 蒸馏水,混匀。将所有标准系列溶液于室温下静置30 min。在415 nm处,用蒸馏水调零,测定标准溶液的吸光度。根据测定结果绘制总黄酮吸光度曲线。称取0.50 g枸杞粉末样品于烧杯中,加入少量甲醇溶液并超声后定容至50 mL容量瓶中,摇匀过滤,用旋转蒸发器将上层清液于45 ℃旋转蒸发至干后,加入20 mL 80%乙醇溶液溶解。按照上述方法测定样品溶液吸光度。
1.3 生物活性物质的抗氧化性研究
1.3.1 FRAP法评价抗氧化活性
FRAP 工作液的制备:称取 5.1 g CH3COONa,加入20 mL乙酸溶解,并用蒸馏水准确定容至250 mL,得到300 mmol/L的CH3COONa缓冲溶液备用;称取0.270 5 g FeCl3·6H2O,用蒸馏水定容至 50 mL,得到20 mmol/L 的氯化铁溶液备用;称取 0.031 2 g TPTZ 用10 mL 40 mmol/L 的 HCl溶液溶解备用。将上述 3 种溶液按体积比10∶1∶1均匀混合,得到FRAP工作溶液。
抗氧化活性测定:吸取0.2 mL样品提取液、6 mL FRAP工作液、0.6 mL蒸馏水,混合摇匀后于37 ℃水浴20 min;在593 nm处,用无水乙醇调零,测吸光度,VE溶液作阳性对照[2]。
FeSO4标准曲线制作:用无水乙醇配制FeSO4溶液(浓度梯度为 200~6 000 μg/mL),按照上述方法测定标准系列溶液的吸光度,得到曲线方程。FRAP值换算:在FeSO4标准曲线中,以样品吸光度找到相对应的FeSO4溶液的浓度,当FeSO4溶液的浓度为1 000 μg/mL 时,FRAP 值为 1。
1.3.2 DPPH法评价抗氧化活性
DPPH 溶液的配制:称取 0.019 7 g DPPH,用无水乙醇溶解(必要时超声或加热处理帮助溶解)并定容至250 mL,得到浓度为2×10-4mol/L的DPPH溶液[3]。
抗氧化活性测定:分别吸取2 mL样品提取液和2 mLDPPH溶液、2 mL样品的无水乙醇溶液和2 mL无水乙醇、2 mL无水乙醇和2 mLDPPH溶液于3只试管中,混合摇匀,在黑暗环境下放置30 min,在 517 nm波长处,用无水乙醇调零后,测其吸光度。VE溶液作阳性对照。
2 结果与分析
2.1 生物活性物质的含量
如图1所示,原花青素的标准曲线在10~150 μg/mL浓度范围内与吸光度有良好的线性关系,其回归方程为:y=0.004 6x+0.010 6,R2=0.999 4。100 g 枸 杞 样品中原花青素含量为4.26 g,实验的重现性较好。
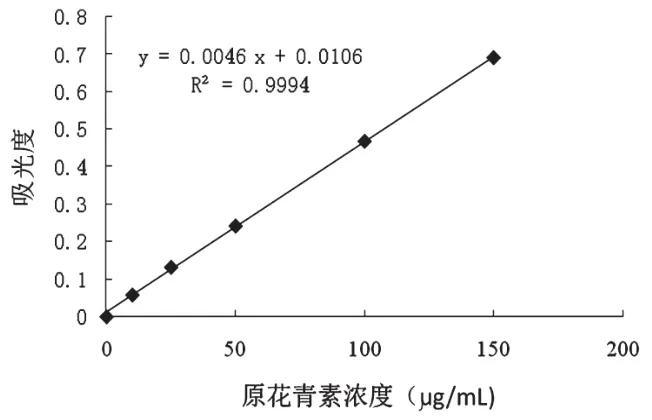
图1 原花青素的标准曲线
总黄酮的标准曲线在20~160 μg/mL浓度范围内与吸光度有良好的线性关系,其回归方程为:y=0.006 4x-0.023 3,R2=0.999 1。100 g 枸杞样品中总黄酮含量为0.68 g,实验的重现性较好,实验结果见图2。

图2 总黄酮的标准曲线
2.2 原花青素抗氧化活性测定
2.2.1 FRAP法对枸杞样品中原花青素抗氧化活性测定结果
FRAP法测定原花青素抗氧化能力的结果如图3所示。由图可知,FRAP法测定抗氧化性时有剂量依赖关系,在测试的浓度范围内,FRAP值随着原花青素浓度增加而增大,即原花青素浓度越高,FRAP值越大,反应体系中被还原成Fe2+-TPTZ的含量越高,样品浓度与FRAP值呈正相关关系。另外,在测试浓度范围内,样品的FRAP值远高于阳性对照VE。因此,样品有很强的Fe3+还原能力。

图3 原花青素的Fe3+还原能力
2.2.2 DPPH法对样品中原花青素抗氧化活性测定结果
DPPH法测定原花青素抗氧化能力的结果如图4所示。随着样品量的逐渐增加,原花青素浓度增加,在测试浓度范围内,原花青素对DPPH自由基的清除能力逐渐增强,当添加量在6~10 μg/mL浓度范围内时,清除率的增加趋势变缓,当浓度达到一定水平,清除率将不在增加,而趋于平稳。另外,在测试浓度范围内,样品的清除率远高于阳性对照VE。因此,样品有很强的DPPH自由基消除活性。

图4 原花青素的DPPH自由基清除率
2.3 总黄酮抗氧化活性测定
2.3.1 FRAP法对样品中黄酮抗氧化活性评价结果
FRAP法测定总黄酮抗氧化能力的结果如图5所示。由图可知,在测试的浓度范围内,FRAP值随着总黄酮浓度增加而增大,呈正相关关系。当总黄酮浓度达到一定程度后,FRAP值增加缓慢。另外,样品的FRAP值远高于阳性对照VE。因此,样品有很强的Fe3+还原能力。
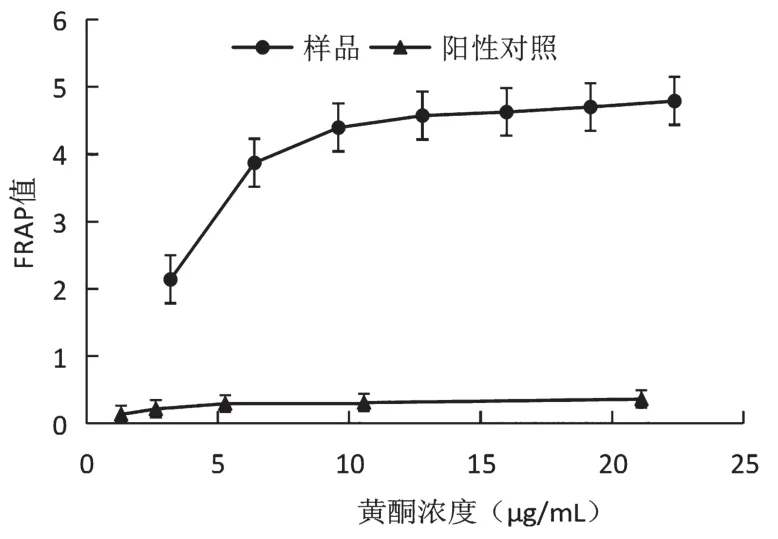
图5 黄酮的Fe3+还原能力
2.3.2 DPPH法对样品中黄酮抗氧化活性评价结果
DPPH法测定黄酮抗氧化能力的结果如图6所示。由图知,随着样品量的逐渐增加,黄酮浓度增加,黄酮含量与DPPH自由基的清除能力之间呈正相关关系,当添加浓度达到16 μg/mL之后,清除率的增加趋势变缓,清除率已经接近100%。另外,在测试浓度范围内,样品的自由基清除率高于阳性对照VE,而且清除率增加趋势随着阳性对照VE浓度升高而变缓。因此,样品有很强的DPPH自由基消除活性。
3 结论
本实验对枸杞中原花青素和总黄酮的含量进行了测定,同时采用了DPPH法和FRAP法对原花青素和黄酮的抗氧化活性进行评价。实验表明,原花青素和黄酮的抗氧化性均高于阳性对照VE。随着黄酮和原花青素浓度的增高,FRAP值和DPPH自由基的清除率增大,并且逐渐接近100%,可见总黄酮和原花青素的抗氧化性在这两种方法评价中,存在剂量依赖关系。对比原花青素和总黄酮的抗氧化能力,可发现原花青素对DPPH自由基的清除能力以及Fe3+的还原能力均高于黄酮。

图6 黄酮的DPPH自由基清除率
