乙酰苯胺制备实验的教学实践与探索
2020-03-06祝梦琴
陈 静,祝梦琴,胡 威
(四川文理学院化学化工学院,四川 达州 635000)
由于磺胺类化合物具有杀菌、抗病毒活性的良好效果,在感染性疾病的治疗当中有着不可替代的作用[1]。研究发现经化学结构修饰后含有对氨基苯磺酰胺母体的多种产物表现出广泛的生物活性,显示出巨大的药用潜力和开发价值,因此许多研究致力于磺胺类化合物的深入开发[2]。对氨基苯磺酰胺的合成可以使用乙酰苯胺,经过氯磺化、氨处理和水解三步得到。其中原料乙酰苯胺可由苯胺与乙酸或乙酸酐反应制备,氨基上的氢原子被取代生成酰胺用于氨基的保护,然后在酸或碱的催化下脱去乙酰基。乙酰苯胺是用途广泛的化工原料,主要应用于医药、日用化工等诸多领域。结合近几年实验课程的教学现状,从以下三个方面进行了探索和实践,使学生能够深刻理解专业知识,增强综合实验操作技能和创新意识。
1 实验预习与基础课程内容紧密结合,加深对理论知识的理解
在有机化学课程[3]的学习中学生已经了解到氨基与脂肪烃基相连组成脂肪胺,与芳香环相连组成芳香胺。氨基属于化学性质比较活泼的基团,基团中的氮有孤对电子,使其具有碱性和亲核性,容易发生氧化、酰化和烃基化等反应。当氮原子上连有一个或几个烃基时,可使用兴斯堡反应来鉴别与分离伯、仲、叔胺。乙酰苯胺的制备是有机化学反应当中保护氨基的一种简便方法,在合成当中通常使用酰化试剂与伯胺反应,降低氨基的反应活性。下一步合成中由于乙酰基的空间效应通常选择性的生成对位产物,最后可水解脱去乙酰基。乙酰苯胺是容易结晶的固体,有一定的熔点容易从水溶液中结晶析出。制备方法目前有分馏法、回流法、微波加热以及射频辐射等[4]。回流法使用冷凝管来加热回流制备乙酰苯胺,反应时间对产品产率的影响较大,而且反应体系中生成的水不能及时除去,最终影响反应物的产率[5]。目前有机化学实验教学当中使用苯胺和乙酸为原料采取分馏法来制备乙酰苯胺[6]。该反应属于固体有机化合物的合成,其目的是通过实验操作让学生熟练掌握苯胺乙酰化反应原理及分馏和重结晶的操作方法。乙酸与苯胺的反应较慢,且反应是可逆的,所以一般使用过量的乙酸或者利用适当的方法及时将反应中生成的水从反应体系中除去从而提高产率。
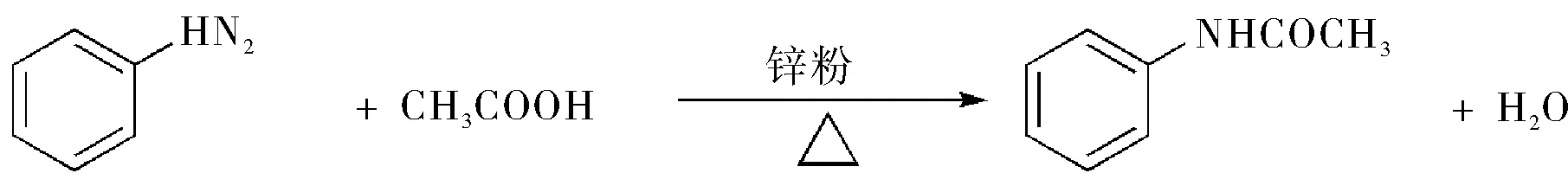
(1)
2 乙酰苯胺制备实验教学方法的实践与探索
2.1 明确实验步骤,熟悉各种仪器的使用及组装方法
实验操作开始前先讲解具体步骤:首先在烧瓶中加入苯胺、乙酸和少量锌粉,安装装置,加热。待温度计示数稳定后又开始下降或烧瓶中出现白色雾气时停止加热,然后将烧瓶中的溶液倒入烧杯冷却结晶、抽滤,将得到的粗产品转移至烧杯中加适量水,加热完全溶解,稍冷后加入活性炭煮沸5~10 min,过滤、冷却结晶,抽滤得重结晶的产物即乙酰苯胺。在介绍需要使用的实验仪器和药品时演示各部分仪器的组装和使用方法,强调实验过程中的注意事项。整个分馏装置由圆底烧瓶、分馏柱、蒸馏头、温度计、温度计套管、冷凝管、尾接管及接收瓶组成。在实验当中使用分馏柱有填充式分馏柱和韦氏分馏柱,填充式分馏柱内可装入不参与化学反应的玻璃珠,要求填充的玻璃珠均匀分布,有一定的空隙。实验用的玻璃珠有几种大小,在使用玻璃珠填充分馏柱的过程中,部分学生没有注意选择合适的玻璃珠,使其容易从分馏柱的底部掉出或者在加热过程中坠入反应烧瓶内。因此在填充分馏柱时要求学生注意玻璃珠的大小或者在分馏柱的尾部填充少量棉花后再加入玻璃珠避免操作失误。此外,分馏柱内填充的玻璃珠过多或过少都会影响加热分馏的效果。
2.2 细心观察实验现象,控制加热分馏的时间和温度
分馏的原理与蒸馏相似,通过分馏柱内多次冷凝和气化分离沸点相近的混合物。在实验过程中如果使用电热套快速加热升温,接收瓶内很快有液体馏出,由于柱内温度梯度较小,导致水和乙酸的分离效率不高,而且加热温度过高容易使反应体系中的乙酸被蒸出来,导致反应物的比例失调。另外高温下苯胺自身容易被氧化使反应不完全,因此得到制备产物产率较低。提醒学生在反应过程中注意加热温度的调节,仔细观察分馏柱内的反应现象,控制馏出液的速度。加热分馏的时间可以通过观察温度计的读数变化,当温度由98 ℃附近开始下降或者反应瓶中出现白色雾气时反应结束。各个实验小组的实验进展不一致,缩短加热时间直接进行下一步反应,会导致产品产率不理想或者没有产物生成。
2.3 掌握正确的重结晶操作,训练良好的实验技能
加热完成后抽滤得到粗产品需要重结晶,学生初次制备乙酰苯胺得到产品产量有多有少,重结晶当中使用的溶剂用量也不相同,应当根据粗产品产量加入适量的溶剂。加热使乙酰苯胺溶解,如果有不溶解的油珠可以添加少量水[7]。在实际操作当中,部分学生按照教材内容一次性加入100 mL水导致溶剂量过多,最后冷却析出的结晶很少或者没有结晶析出。出现这种情况后可适当延长加热时间,使溶剂蒸发掉一部分,其次把得到的滤液分成两份分别冷却结晶。加入活性炭煮沸后过滤操作中乙酰苯胺晶体容易析出在附着在滤纸上和漏斗下端,造成产品的损失。可以使用减压装置来抽滤,快速除去活性炭尽量减少产品的损失。从实验结果来看,各个实验小组的精制产品产量在0.5~3 g左右,重结晶后产品产率降低。
3 引导学生对实验过程进行探索与改进
为了培养学生的实验技能和创新思维能力,充分调动学生的学习积极性、发挥自身特长,让理论内容和实际应用更好地结合起来,引导学生对乙酰苯胺的反应条件进行了探索和改进。首先让学生利用学校的资源自主查阅文献,认真分析实验当中的出现问题,找出具体的改进方向。其次根据文献资料[8]整理设计合成路线的改进方法。主要对以下三个方面进行探讨:(1)乙酸用量对乙酰苯胺产率的影响。实验课程当使用乙酸和苯胺的量分别为7.5 mL及5 mL,由于反应是可逆,而且在加热分馏的过程中会损失部分乙酸,因此一般使用过量乙酸来参与反应。为了探究乙酸与苯胺用量比对产物产率的影响,在不改变其他条件的情况下进行对比实验。随着冰乙酸用量的增加,乙酰苯胺的产率也增大,实验结果显示在用量比为2:1时产品产率最高,再增加乙酸的用量会使合成产物产率降低。(2)催化剂对乙酰苯胺产率的影响。单质碘作为催化剂具有较高的选择性、反应条件相对温和,可用于亲电及亲核反应,在合成当中应用广泛[9-10]。在反应中加入少量碘,其他条件保持不变的情况下观察反应现象和结果。当加入的碘催化剂用量为1.5 g时,产物产率有明显增加。(3)半微量实验制备乙酰苯胺。微型化学实验是近年来迅速发展的绿色化学实验新方法,可以减少化学试剂的用量、节省实验经费,降低污染物的排放[11]。采用半微量即常量的50%进行实验操作,发现分馏和重结晶的时间缩短,由于反应物用量少后期处理得到产品的损失比例较大,产率有所下降。因此实验过程中要求学生集中精力、细心操作,培养严谨的科学态度,提高综合实验能力。

表1 乙酰苯胺实验条件的改进
4 结 语
化学实验是对理论课程内容的验证,使学生通过实际操作充分理解抽象的原理,也是课堂教学的延伸。在乙酰苯胺的实验教学过程中注重具体实验操作的讲解和演示、及时指导和纠正让学生掌握正确的操作技能并得到满意的实验结果,激发他们进一步学习和钻研的兴趣。让学生自主查阅文献尝试从不同角度的分析和归纳问题,改进实验方法、观察实验现象并总结实验结果,有助于增强学生的综合实验操作技能和创新意识,培养学生的动手能力、设计与科研创新能力,达到良好的教学效果。
