NiCo2S4多孔核壳微球作为锂氧气电池阴极催化剂的应用研究
2020-03-05张耀文尹建军
张耀文 尹建军

摘 要:采用简单的两步溶剂热法成功地制备了NiCo2S4多孔核壳微球。将此NiCo2S4多孔核壳微球作为阴极催化剂组装非水系锂氧气电池,在电流密度为0.1 mA/cm2的条件下,首次放电比容量为2 683 mA·h/g,并且在同样的电流密度,截止容量为500 mA·h/g的条件下,NiCo2S4电极能够稳定循环80圈,远超过同样条件下的导电炭黑Super P电极性能,表现出了出色的充放电循环稳定性,这主要是由于NiCo2S4多孔核壳微球相对于Super P具有更高的电催化氧还原和氧析出的活性,同时多孔核壳球形貌具有更多的空间容纳放电产物Li2O2的沉积,进而避免了阴极的体积变化造成的电池性能衰减。
关 键 词:NiCo2S4;多孔核壳微球;锂氧气电池;阴极催化剂
中图分类号:TM911.41 文献标识码: A 文章编号:1671-0460(2020)01-0091-04
Application of NiCo2S4 Porous Core-Shell Spheres as
Cathode Catalyst in Lithium-Oxygen Batteries
ZHANG Yao-wen, YIN Jian-jun
(Lanzhou University of Technology, Gansu Lanzhou 730050, China)
Abstract: NiCo2S4 porous core-shell spheres were synthesized by two-step solvothermal method. Non-aqueous lithium-oxygen battery was assembled with the NiCo2S4 porous core-shell spheres as cathode catalyst, and its initial discharge specific capacity was up to 2 683 mA·h/g and the cycle stability reached 80 cycles under the limited specific capacity of 500 mA·h/g at 0.1 mA/cm2. The performance of NiCo2S4 cathode was better than that of Super P cathode, because it had efficient electrocatalytic activities of the NiCo2S4 for oxygen reduction and evolution reactions, and the morphology of porous core-shell spheres could accommodate more discharge products and avoid the performance degradation due to volumetric variation.
Key words: NiCo2S4; Porous core-shell spheres; Lithium-oxygen battery; Cathode catalyst
近些年來,非水系锂氧气电池因其具有超高的理论能量密度逐渐成为储能电池领域的研究热点,吸引着越来越多研究人员的关注[1-4]。然而,锂氧气电池中阴极迟滞的氧化还原反应动力学、阴极较大的放电产物体积形变、电解液的不稳定性等问题导致了非水系锂氧气电池实际放电比容量不高、充放电循环寿命短的状况,这些问题都限制了锂氧气电池的实际应用。因此,开发一种高效稳定的催化剂用于提高锂氧气电池阴极反应活性迫在眉睫[5-8]。
目前,大多数的导电炭材料都能够对氧化还原反应具有较好的催化效果,但对氧析出反应催化效果却不佳,这是因为放电产物导电性差,难以分解[9]。过渡金属硫化物具有催化氧气还原和氧析出双重功能[10,11],并且相对于过渡金属氧化物具有更高的导电性[12],因此过渡金属硫化物有希望用于锂氧气电池,以期降低电池反应过电势,提高电池的循环寿命。首先通过溶剂热法制备了NiCo-甘油酸盐前驱体,然后再通过离子交换反应的硫化过程成功制备了NiCo2S4多孔核壳微球。循环伏安测试表明了NiCo2S4多孔核壳微球作为阴极催化剂具有优异的氧还原和氧析出催化性能;所制备的NiCo2S4多孔核壳微球用于Swagelok型非水系锂氧气电池,在电流密度为0.1 mA/cm2,截止容量为500 mA·h/g 的条件下,NiCo2S4电极能够稳定循环80圈,远远超过Super P电极的循环性能。
1 实验部分
1.1 NiCo2S4多孔核壳微球的制备
将一定量的硝酸钴和硝酸镍分散在400 mL异丙醇中搅拌均匀,然后一边搅拌一边向上述溶液加入一定量的甘油后转移至水热釜中,恒温180 ℃反应6 h,待冷却至室温后产物用无水乙醇洗涤过滤多次后得到NiCo-甘油酸盐前驱体,80 ℃烘干备用。称取一定量上述所制备的前驱体,并将其均匀分散到400 mL无水乙醇中,然后加入一定量的硫代乙酰胺搅拌分散均匀后转移至水热釜中,180 ℃反应10 h,待反应完成并冷却至室温后用无水乙醇将产物洗涤过滤多次后收集沉淀,并80 ℃真空干燥12 h,最终得到NiCo2S4多孔核壳微球。
1.2 氧电极的制备和电池的组装
将Super P、NiCo2S4多孔核壳微球和PTFE黏结剂以质量比6∶2∶2混合研磨,然后将此浆料擀制成片,80 ℃真空干燥8 h,将其用压片机压在不锈钢网上,80 ℃真空干燥24 h后转入手套箱备用。Super P与PTFE黏结剂以质量比8∶2相同的方法制备成极片作为对照组。本实验采用的是Swagelok电池,金属锂片作负极,玻璃纤维膜作隔膜,电解液为1 M LiTFSI in TEGDME。所有的电池组装都是在Ar气保护的手套箱内进行操作。
1.3 测试与表征
采用美国BRUKER AXS公司生产的D8 ADVANCE型X射线衍射仪上测定材料晶型,制备的样品形貌通过美国FEI Tecnai G2 F20型场发射透射电子显微镜来表征的,同时用配套的EDS能谱仪来分析所合成材料的元素分布情况,材料的元素组成及价态通过日本岛津-Kratos公司的AXIS Ultra DLD型X射线光电子能谱仪来确定,通过场发射扫描电子显微镜FESEM(S-4800,Hitachi)来观察放电产物的形貌。通过Bio-Logic电化学工作站(SP-300)测试氧电极的循环伏安曲线(扫描电压范围为2.0~4.2 V,扫描速率为0.1 mV/s),采用武汉蓝电电池测试系统(LANHE CT2001A)对电池的进行充放电测试。
2 结果与讨论
2.1 NiCo2S4多孔核壳微球的结构和形貌表征
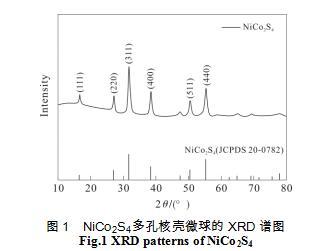
图1为制备的NiCo2S4多孔核壳微球的X射线衍射(XRD)谱图。从图中可以看到尖锐衍射峰的出现,证明材料的结晶度高。衍射峰位置16.34°,26.83°,31.58°,38.31°,50.46° 和 55.33°分别对应NiCo2S4(111),(220),(311),(400),(511)和(440)晶面,与NiCo2S4的标准卡片一一对应[13],证实成功的合成了立方尖晶石NiCo2S4,并且没有出现其他的杂相峰,说明所合成样品纯度很高。
通过场发射透射电镜(FETEM)对NiCo2S4形貌进行表征,如图2a、2b所示。通过TEM图片可以看到所制样品为均匀分布的多孔核壳微球,这为電池的固态放电产物提供了较多的存储空间,同时这些NiCo2S4微球的多孔核壳结构有利于O2传输和Li+扩散。图2c为Ni、Co和S三种元素EDS能谱图,可以看出三种元素在核壳结构中分布均匀,再一次证实成功合成制备了NiCo2S4多孔核壳微球。
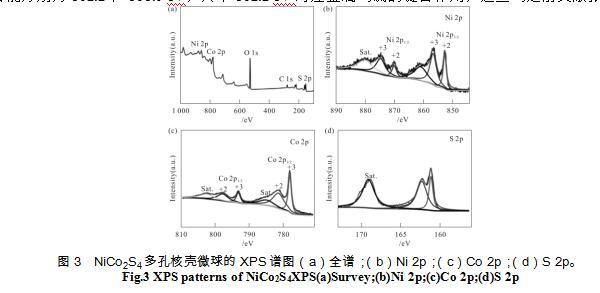
采用X射线光电子能谱技术(XPS)对NiCo2S4样品元素组成以及价态进行表征,结果如图3所示。由XPS总谱(图3a)可以证实,合成的NiCo2S4样品中除了含有Ni,Co,S三种元素,还含有C和O元素,这两种元素来自制备时所用前驱体的残留。其中,Ni 2p3/2和Ni 2p1/2谱图可以用两个自旋轨道双线进行拟合,结合能在869.9和852.7 eV附近的峰对应着Ni2+,结合能在874.5和856.6 eV附近的峰对应Ni3+,同样Co 2p3/2和Co 2p1/2谱图也可以用两个自旋轨道双线进行拟合,结合能在797.8和781.5 eV附近的峰对应着Co2+,结合能在793.2和778.2 eV附近的峰对应Co3+。图3d为S 2p能谱,S 2p1/2和S 2p3/2轨道结合能分别为162.2和161.0 eV,其中162.2 eV对应金属与硫的键合作用,这些与之前文献报道的结果基本符合[14]。
2.2 NiCo2S4多孔核壳微球的电化学性能表征
图4是基于Super P和NiCo2S4的锂氧气电池的循环伏安曲线。在氩气气氛中下,两个电极都没有氧化还原峰,说明这两种材料在2.0~4.2 V电压窗口区间能够保持稳定;当在O2气氛中,在负扫过程中二者都有明显的氧还原峰,说明二者都具有良好的ORR催化活性,值得注意的是,NiCo2S4电极的还原峰电流比SP电极要高,说明NiCo2S4具有比Super P更高的电催化氧还原活性;而在正扫过程中,NiCo2S4电极的氧析出起始电压在3.0 V,接近理论氧化还原电位(2.96 V),而且NiCo2S4电极的氧化峰电流也要比SP电极高,说明NiCo2S4具有比Super P更高的电催化氧析出活性。循环伏安测试表明了NiCo2S4电极具有良好的电催化氧还原和氧析出的活性。
为了探究阴极催化剂材料对锂氧气电池充放电性能的影响,将Super P电极和NiCo2S4电极组装成锂氧气电池进行恒电流充放电测试。在电流密度为0.1 mA/cm2,充放电电压窗口2.0~4.3 V的条件下,电池首圈充放电曲线如图5a所示,由NiCo2S4电极组装的电池放电比容量为2 683 mA·h/g,高于Super P电极放电比容量(2 439 mA·h/g),而且NiCo2S4电极的首圈库伦效率为87%远高于Super P电极的14%。如图5b所示,基于NiCo2S4的锂氧气电池的充电电压平台远远低于Super P电极,这是由于NiCo2S4比Super P具有更优异的催化氧析出的性能,并且NiCo2S4的多孔核壳结构有利于氧气传输和锂离子扩散。
在截止容量为500 mA·h/g,电流密度为0.1 mA/cm2的条件下,锂氧气电池的充放电循环性能测试如图5c和5d所示。基于NiCo2S4电极组装的锂氧气电池能够稳定循环80圈,远远高于基于Super P电极的电池循环20圈;如图5e所示为在截止容量为500 mA·h/g的条件下,两个电池放电终止电压随循环圈数的变化图,Super P电极循环至第20圈时终止电压急剧下降,而对于NiCo2S4电极循环至第80圈时终止电压逐渐下降为2.13 V,这表明相对于Super P电极NiCo2S4電极具有良好的循环稳定性。
为了进一步研究锂氧气电池的充放电行为,对电池在充放电前后的电极片分别进行SEM表征(图6),在电池放电到截止电压2.0 V时,NiCo2S4电极出现膜状放电产物Li2O2(图6c),这可能是由于NiCo2S4的多孔核壳结构能提供更多的反应位点,有利于放电产物的沉积从而使得反应产物的形成更均匀而表现为膜状,同时能有效地传输氧和锂离子,而Super P电极的表面出现了环状线圈形的放电产物Li2O2(图6d),这都跟文献报道的放电产物Li2O2的形貌一致[15-17]。值得注意的是,膜状Li2O2产物能够在较低的充电电压下分解,这有利于电池的循环性能,这也对应符合了前面的充放电测试结果。在完全充电之后,NiCo2S4电极表面看不到产物(图6e),与初始极片基本一致(图6a),说明产物已经完全分解;但Super P电极在完全充电之后其表面仍有一些环状产物没有完全分解(图6f),再一次证实了NiCo2S4优异的电催化产物分解(即氧析出)的性能,因此NiCo2S4的引入能够使放电产物Li2O2完全分解,有助于提高锂氧气电池的电化学性能。
3 结论
采用简便的两步溶剂热的方法成功制备了NiCo2S4多孔核壳微球,NiCo2S4多孔核壳微球作为非水系锂氧气电池阴极催化剂表现出了优异的电催化氧析出性能,在截止容量为500 mA·h/g,电流密度为0.1 mA/cm2的条件下,基于NiCo2S4的锂氧气电池能够稳定循环80圈,这主要是因为NiCo2S4具有较高的电催化氧还原和氧析出的双功能活性,并且NiCo2S4的多孔核壳结构有利于放电产物的存储避免了充放电过程中阴极的体积变化,同时有利于氧气和锂离子的传输扩散。因此,NiCo2S4多孔核壳微球作为在锂氧气电池阴极催化剂具有良好的应用前景,并且这对于开发其他的新型多孔核壳结构双金属硫化物材料应用于锂氧气电池具有良好的借鉴意义。
參考文献:
[1] Armand M, Tarascon J M. Building better batteries[J]. Nature, 2008, 451(7179): 652-657.
[2] Bruce P G, Freunberger S A, Hardwick L J, et al. Li-O2 and Li-S batteries with high energy storage[J]. Nature Materials, 2011, 11(1): 19-29.
[3] Luo W-B, Gao X-W, Chou S-L, et al. Investigation of Promising Air Electrode for Realizing Ultimate Lithium Oxygen Battery[J]. Advanced Energy Materials, 2017, 7(24).
[4] 辛森, 郭玉国, 万立骏. 高能量密度锂二次电池电极材料研究进展[J].中国科学:化学, 2011, 41 (08): 1229-1239.
[5] Eftekhari A, Ramanujam B. In pursuit of catalytic cathodes for lithium–oxygen batteries[J]. Journal of Materials Chemistry A, 2017, 5(17): 7710-7731.
[6] Yu T, Fu J, Cai R, et al. Nonprecious Electrocatalysts for Li-Air and Zn-Air Batteries: Fundamentals and recent advances[J]. IEEE Nanotechnology Magazine, 2017, 11 (3): 29-55.
[7] 路琦,赵强,张红明,等.空心微球聚苯胺二次锂氧电池正极材料研究[J].高分子学报, 2013, 08: 1080-1084.
[8] 雷鸣,曹勇,林晓东,等.MnO/氮掺杂石墨烯复合正极材料在锂空气电池中的高效催化性能研究[J].中国科学:化学, 2017, 47(05): 663-670.
[9] Zhang Y L, Cui Q H, Zhang X M, et al. Amorphous Li2O2: Chemical Synthesis and Electrochemical Properties[J]. Angewandte Chemie- International Edition, 2016, 55 (36): 10717-10721.
[10]Liu Q, Jin J, Zhang J. NiCo2S4@graphene as a bifunctional electrocatalyst for oxygen reduction and evolution reactions[J]. ACS Appllied Materials Interfaces, 2013, 5 (11): 5002-5008.
[11]Zhang Z, Wang X, Cui G, et al. NiCo2S4 sub-micron spheres: an efficient non-precious metal bifunctional electrocatalyst[J]. Nanoscale, 2014, 6 (7): 3540-3544.
[12]Yu D J, Yuan Y F, Zhang D, et al. Nickel cobalt sulfide Nanotube Array on Nickel Foam as Anode Material for Advanced Lithium-Ion Batteries[J]. ElectrochimicaActa, 2016, 198: 280-286.
[13]Wang J-G, Jin D, Zhou R, et al. One-step synthesis of NiCo2S4 ultrathin nanosheets on conductive substrates as advanced electrodes for high-efficient energy storage[J]. Journal of Power Sources, 2016, 306: 100-106.
[14]Du W, Wang Z, Zhu Z, et al. Facile synthesis and superior electrochemical performances of CoNi2S4/graphene nanocomposite suitable for supercapacitor electrodes[J]. Journal of Materials Chemistry A, 2014, 2 (25): 9613-9619.
[15]Cui Q, Zhang Y, Ma S, et al. Li2O2 oxidation: the charging reaction in the aprotic Li-O2 batteries[J]. Science Bulletin, 2015, 60 (14): 1227-1234.
[16]Yang C, Wong R A, Hong M, et al. Unexpected Li2O2 Film Growth on Carbon Nanotube Electrodes with CeO2 Nanoparticles in Li-O2 Batteries[J]. Nano Letters, 2016, 16 (5): 2969-2974.
[17]Liu B, Xu W, Zheng J, et al. Temperature Dependence of the Oxygen Reduction Mechanism in Nonaqueous Li–O2 Batteries[J]. ACS Energy Letters, 2017, 2 (11): 2525-2530.
