显微镜下颅内动脉瘤夹闭术与血管介入动脉栓塞术治疗前循环出血性颅内动脉瘤患者的对比研究
2020-03-05
(河南省南阳南石医院,河南 南阳 473000)
颅内动脉瘤指颅内动脉管壁局限性异常膨出,多发于40~60岁女性,是引起蛛网膜下腔出血的重要原因。而前循环颅内动脉瘤所占比例最高,达85%左右,若破裂出血会出现头痛、颈强直、眼眶疼、昏迷等,严重威胁患者生命安全[1]。显微镜下颅内动脉瘤夹闭术是一种微创手术,可有效制止脑血管出血,疗效显著,但术后易出现并发症。而血管介入动脉栓塞术创伤小,安全性高,受到临床广泛关注。本研究以我院前循环出血性颅内动脉瘤患者为研究对象,行显微镜下颅内动脉瘤夹闭术与血管介入动脉栓塞术,对比两者手术效果,报告如下。
1 资料及方法
1.1一般资料 选取2016年4月~2019年1月我院84例前循环出血性颅内动脉瘤患者,按照手术方法分组,各42例。介入组男16例,女26例;年龄25~58岁,平均(41.62±5.49)岁;Hunt-Hess分级[2]:Ⅲ级17例,Ⅳ级19例,Ⅴ级6例。显微组男17例,女25例;年龄26~57岁,平均(41.48±5.36)岁;Hunt-Hess分级:Ⅲ级16例,Ⅳ级20例,Ⅴ级6例。两组基线资料(性别、Hunt-Hess分级、年龄)均衡可比(P>0.05),本研究经我院医学伦理委员会批准。
1.2入选标准 ①纳入标准:发病时间<72 h;经数字减影血管造影(DSA)、CT血管成像(CTA)检查确诊;患者家属签署知情同意书。②排除标准:其他脑部疾病,凝血功能障碍,恶性肿瘤,肝肾功能不全,精神异常,传染性疾病。
1.3方法
1.3.1介入组 行血管介入动脉栓塞术,建立静脉通路,泵注尼莫地平,气管插管全麻,采用Seldinger技术穿刺股动脉,对颈动脉、椎动脉等部位行DSA检查,观察动脉瘤形态、部位、充盈等情况,更换导引导管,全身肝素化,微导丝经导管进入动脉瘤,选合适微弹簧圈介入,进行栓塞操作,核查栓塞,无问题后完成栓塞,保证载瘤动脉血流顺畅,再行DSA检查,动脉瘤中无造影剂后,可拔除导引导管、微导管,术后6 h拔鞘,按压股动脉,无出血后包扎。
1.3.2显微组 行显微镜下颅内动脉瘤夹闭术,气管插管全麻,经翼点入路,显微镜下分开外侧裂,释放脑脊液,暴露载瘤动脉、动脉瘤瘤颈,缓慢分离瘤颈。根据情况可阻断载瘤动脉,时间<5 min,选择合适动脉瘤夹夹闭动脉瘤颈,无出血后缝合脑膜,出现严重水肿者行去骨瓣减压术治疗。两组术后静滴尼莫地平、低分子肝素,术后1 d下肢制动。
1.4观察指标 ①对比两组术后Hunt-Hess分级,Ⅰ级:无症状或症状轻微;Ⅱ级:颅神经麻痹,颈项强直、头痛;Ⅲ级:嗜睡,意识模糊,轻微神经功能缺损;Ⅳ级:神经功能障碍,偏侧不全麻痹,早期去大脑强直;Ⅴ级:去大脑强直,深度昏迷。②采用改良Rankin量表(mRS)评分评价两组术后3个月日常生活能力[3],总分5分,评分越低,日常生活能力越强。③对比两组术后并发症(颅内感染、血管痉挛、脑积水、再出血)发生率。
1.5统计学方法 采用SPSS 22.0统计软件分析数据,计数资料(并发症发生率)用n(%)表示,采用χ2检验,等级资料(Hunt-Hess分级、mRS评分)比较采用Ridit分析,P<0.05为差异有统计学意义。
2 结果
2.1术后Hunt-Hess分级 介入组术后Hunt-Hess分级与显微组对比,差异无统计学意义(P<0.05),见表1。

表1 两组术后Hunt-Hess分级分布对比
注:表内计数资料数据用[n(%)]表示;两组比较,χ2=1.749,P=0.626
2.2术后mRS评分 介入组术后3个月mRS评分与显微组对比,差异无统计学意义(P>0.05),见表2。
2.3术后并发症发生率 介入组术后并发症发生率较显微组低,复发率较显微组高(P<0.05),见表3。
2.4典型病例 病例1,女性,45岁。左侧后交通动脉瘤,首次出血后2 d手术,图A:术前CT示左颞叶小血肿;图B:术前CTA示后交通动脉瘤。行动脉瘤夹闭术,图C:术中夹闭动脉瘤;图D:术后3D-CTA复查。见图A~图D。病例2,女性,52岁,前交通动脉瘤,出血1 d内手术,图E:术前CT示蛛网膜下腔出血:图F:3D-CTA示前交通动脉瘤。行动脉栓塞术,图G:填塞致密,出血消失,图H:术后3D造影示动脉瘤消失。见图E~图H。

表2 两组术后mRS评分分值分布对比
注:表内计数资料数据用[n(%)]表示;两组比较,χ2=2.782,P=0.734

表3 两组术后并发症发生率对比
注:表内计数资料数据用[n(%)]表示
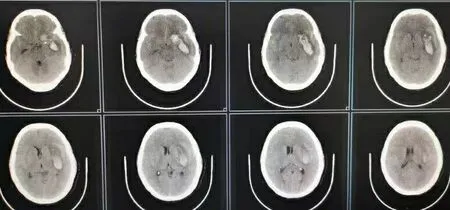
图A 术前CT示左颞叶小血肿

图B 术前CTA示后交通动脉瘤 图C 术中夹闭动脉瘤 图D 术后复查3D-CTA示动脉瘤不显影
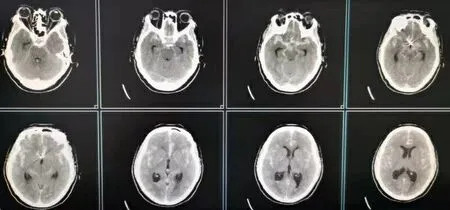
图E 术前CT示蛛网膜下腔出血

图F 3D-CTA示前交通动脉瘤 图G 术中动脉瘤致密填塞 图H 术后3D造影示动脉瘤消失
3 讨论
颅内动脉瘤具体病因不明,可能与先天脑动脉发育不良、感染、动脉硬化、血流动力学冲击有关[4-5]。颅内动脉瘤多发于Willis环前循环,动脉瘤破裂会形成瘤壁渗血,压迫周围血管、神经组织,威胁患者安全,并易出现严重后遗症。
临床常采用外科手术治疗前循环出血性颅内动脉瘤,传统采用开颅夹闭术可有效制止出血,清除蛛网膜下腔积血、颅内血肿,减轻脑动脉痉挛,避免动脉瘤再破裂,但手术创伤大,术后易发生并发症,不利于患者术后康复[6-7]。显微镜下颅内动脉瘤夹闭术是在开颅夹闭术基础上进行改进,于显微镜下进行颅内动脉瘤夹闭术,有利于减小手术创伤,但对深部动脉瘤操作困难,可能出现严重并发症。而血管介入动脉栓塞术对脑血管、周围组织损伤小,适用于深部动脉瘤、手术耐受力差的患者[8-9]。刘小雷等[10]研究显示,血管内介入术与显微外科夹闭术均可有效治疗中青年颅内动脉瘤,改善患者生活能力,但血管内介入术并发症发生率为18.37%,比显微外科夹闭术的38.64%低,具有较高的安全性。同时,Meta分析资料显示,介入栓塞治疗破裂颅内动脉瘤,不良事件发生率、再出血发生率低于手术夹闭,而两种术式术后血管痉挛、缺血性脑梗死发生率、术后1年病死率无显著差异[11]。本研究结果显示,介入组术后Hunt-Hess分级、mRS评分与显微组对比,差异无统计学意义,说明显微镜下颅内动脉瘤夹闭术与血管介入动脉栓塞术治疗前循环出血性颅内动脉瘤患者,手术效果相当,可减轻患者病情,增强患者日常生活能力。
前循环出血性颅内动脉瘤并发症主要为脑积水、脑血管痉挛、再出血、颅内感染等,是导致患者术后残疾、死亡的重要原因。血管介入动脉栓塞术可预防再出血发生,防止血红蛋白刺激脑血管发生痉挛,并能抑制蛛网膜阻塞、蛛网膜黏连等,降低脑积水等并发症发生率[12-13]。本研究还显示,介入组术后并发症发生率较显微组低,复发率较显微组高,可见,与显微镜下颅内动脉瘤夹闭术相比,血管介入动脉栓塞术治疗前循环出血性颅内动脉瘤患者,可减少术后并发症发生,但术后易复发。对载瘤动脉严重迂曲、血管严重痉挛等患者,微导管较难抵达瘤腔,故血管介入动脉栓塞术不太适合治疗以上患者,应根据患者病情选择合适的手术方式[14-15]。
综上所述,显微镜下颅内动脉瘤夹闭术与血管介入动脉栓塞术治疗前循环出血性颅内动脉瘤患者,手术效果相当,可减轻患者病情,增强患者日常生活能力,血管介入动脉栓塞术可减少术后并发症发生,但术后易复发,需谨慎选择术式。
