头孢泊肟酯片的处方工艺及质量研究
2020-03-04杨宏硕李敏马亚松贾玉捷孙燕
杨宏硕 李敏 马亚松 贾玉捷 孙燕
(华北制药河北华民药业有限责任公司,河北 石家庄 050000)
0 引言
头孢泊肟酯是第三代头孢菌素,口服后经肠管壁酯酶迅速水解成抗菌活性体头孢泊肟进入血液循环,饭后给药较空腹给药时吸收良好。头孢泊肟酯除有第三代口服头孢菌素的优点外,尚有以下优点:(1)多数第三代头孢菌素,对GP菌中的葡萄球菌属细菌感染的疗效不够理想,而头孢泊肟酯抗菌谱更广,对葡萄球菌属也有中度的抗菌活性,临床对葡萄球菌感染能取得较佳疗效。(2)它是前体药物,在肠胃道不起作用,经非特异性酯酶水解后进入血液变成活性体,副作用小。(3)餐后服用血药浓度高,吸收率高。(4)半衰期长,药物耐受性好。(5)一天两次,服用方便,费用低。(6)适宜儿童使用。
1 仪器和试药
1.1 仪器
高效液相色谱仪(Agilent-1100);电子分析天平(岛津AUW120D);智能溶出仪(天津大学ARS-8G);湿法混合制粒机(中航工业HLSH2-6A);恒温干燥箱(上海爱斯佩克LC-213);压片机(上海天和制药机械有限公司TDP单冲型);包衣机(宝鸡诺凯技术开发有限公司B200/400-B型)。
1.2 药品和试剂
头孢泊肟酯原料药(自制,130102);头孢泊肟酯对照品(中国国食品药品检定研究院,130517-200802);头孢泊肟酯片(日本第一三共株式会社,0295)乳糖;羟丙基纤维素;羧甲淀粉钠;羟丙甲纤维素(E5);十二烷基硫酸钠;二氧化硅;硬脂酸镁;包衣预混剂。
2 方法和结果
2.1 头孢泊肟酯片的制备
(1)头孢泊肟酯片的处方筛选 参比制剂辅料组成:乳糖、羧甲基纤维素钙、羟丙纤维素、羟丙甲纤维素、十二烷基硫酸钠、胶体二氧化硅、滑石粉、硬脂酸镁、二氧化钛。根据头孢泊肟酯原料药的性质,选用片剂常用辅料,根据辅料常用量和参比制剂规格及片重设计处方,并以休止角、溶出度、吸湿增重等作为控制指标,以溶出行为对处方进行优化。按照片剂常规工艺步骤进行操作,即原辅料预处理、预混、制软材、制粒、干燥、整粒、总混、压片、包衣。根据成型工艺、溶出度、溶出曲线、含量、有关物质等考察项目对处方进行筛选并优化和重复。具体通过单一辅料用量变化考察并筛选处方。处方1~13的筛选情况参见表1~表3。通过助流剂、表面活性剂及崩解剂用量筛选最终确定为处方13。

表1 处方筛选表1-5
(2)头孢泊肟酯片的影响因素试验 以处方13按照工艺步骤进行操作制备片剂。取参比制剂和自制品进行高温(40℃)和(60℃),强光照射(光照强度4500±500Lx),高湿(RH75%)和(RH92.5%)的影响因素试验,10天后取样检测,结果见表4、表5。结果表明,头孢泊肟酯片高温高湿的条件对产品质量有明显影响,因此制剂工艺应注意避免高温、高湿,产品应选防潮且密封性优良的包装材料。

表2 处方筛选表6-9
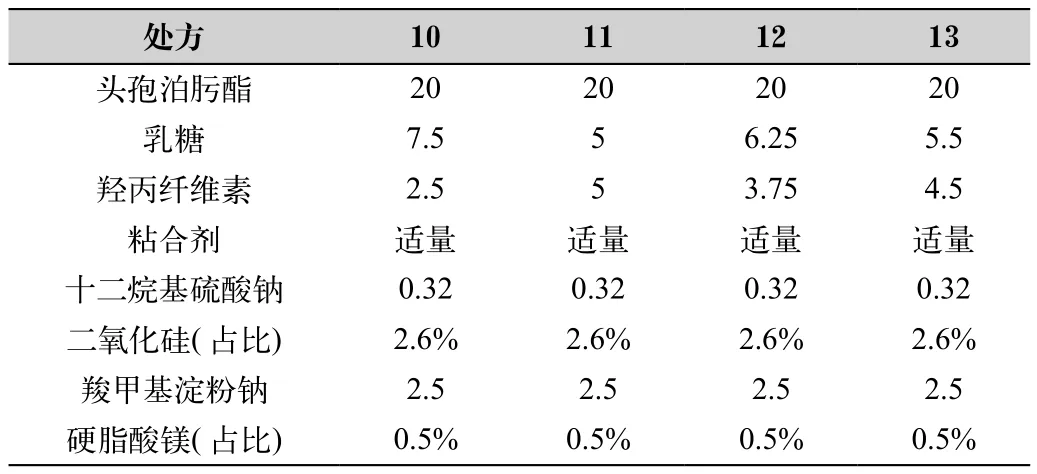
表3 处方筛选表10-13
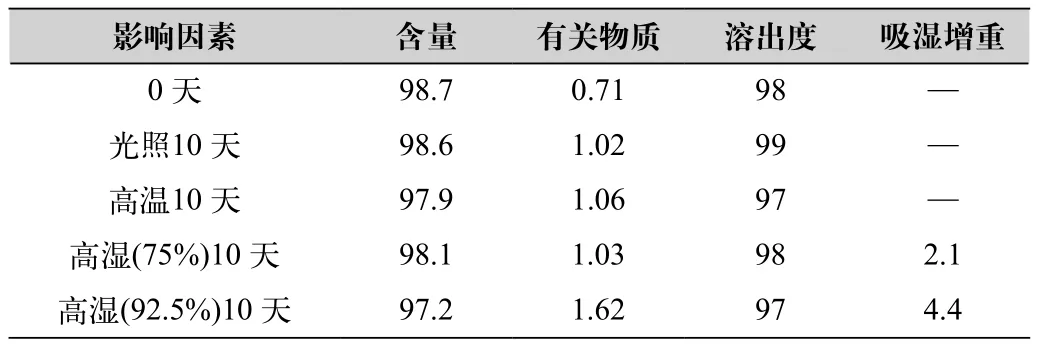
表4 影响因素试验结果(自制产品)

表5 影响因素试验结果(参比制剂)
2.2 含量测定
色谱条件:十八烷基硅烷键合硅胶为填充剂;流动相甲醇/水=45/55;检测波长240nm;流速0.8ml/min;柱温40℃。精密称取头孢泊肟酯(约相当于头孢泊肟21mg),置50mL量瓶中,用适量甲醇溶解并用流动相稀释至刻度,摇匀,过滤,精密量取续滤液10μL注入液相色谱仪。另取头孢泊肟酯对照品适量,同法测定。按外标法以头孢泊肟酯异构体I和Ⅱ峰面积和计算供试品中C15H17N5O6S2的含量。本品含头孢泊肟酯按头孢泊肟计应为标示量的90.0%~110.0%。
2.3 有关物质检查
色谱条件:十八烷基硅煸键合硅胶为填充剂:以A(无水甲酸:甲醇:水=1:400:600),以D(无水甲酸:甲醇:水=1:950:50)为流动相;检测波长254nm;流速0.6ml/min。柱温20℃。分别精密量取供试品溶液和对照溶液。注入液相色谢仪,供试品溶液色谱图中所有色谱峰的相对保留以头孢泊肟酯异构体Ⅱ为参照:杂质B异构体1的相对保留为0.68,头孢泊肟翻异构体1的相对保留为0.74,杂质C的相对保留为0.82,杂质B异构体的相对保留为0.85,杂质D(两个峰)的相对保留大约为0.88和1.13,杂质H(两个峰)的相对保留大约在1.9和2.3之间。供试溶液色谱图中杂质B的峰面积不得过对照溶液中两主峰面积和的0.5倍(0.5%);杂质C的峰面积不得过对照溶液中两主峰面积和的3.0倍(3.0%);杂质D、H的峰面积不得过对照溶液中两主峰面积和的1.0倍(1.0%);其他单个杂质的峰面积不得过对照溶液中两主峰面积和的0.2倍(0.2%);所有杂质的峰面积和不得过对照溶液中两主峰面积和的6.0倍(6.0%);任何小于对照溶液中两主峰面积和0.05倍(0.05%)的杂质峰可忽略不计。
2.4 溶出度试验
溶出度:取本品,照溶出度与释放度测定法,制备甘氨酸氯化钠盐酸溶液(pH3.0):[取甘氨酸54.5g和氯化钠42.6g,置1000ml量瓶中,加水500ml溶解,缓慢加人盐酸14.2ml,放冷,用水稀释至刻度,摇匀,作为贮备液。取贮备液50ml,加水至900ml]为溶出介质,转速为每分钟75转,依法操作。经30分钟时,取溶液适量,过滤,精密量取滤液适量,用溶出介质定量稀释制成每1ml中约含头孢泊肟11μg的溶液,照紫外-可见分光光度法,在259nm的波长处测定吸光度;另精密称取头孢泊肟酯对照品适量,加甲醇适量溶解并用溶出介质定量稀释制成每1ml中约含头孢泊肟11μg的溶液,同法测定。计算每片的溶出量。限度为标示量的70%,应符合规定。
3 结果与讨论
按照处方13制备3批头孢泊肟酯片,铝塑包装后进行加速试验。温度(30±2℃),湿度(75%±5%)。结果:三批自制供试品及参比制剂12个月后,各项考察指标有所变化,但均在限度范围内,符合要求。
4 结语
头孢泊肟酯片重点关注指标为药物溶出度和有关物质含量的变化,对药物溶出释放,崩解剂羟丙基纤维素钠和羧甲基淀粉钠联合使用达到了较理想的效果。通过影响因素试验考察,片剂的稳定性受外部温度、湿度的影响较大,应严控储藏条件。该处方的头孢泊肟酯片有较好的溶出度和稳定性,可进一步研究开发,进行临床试用。
