我国仿制药一致性评价工作进展及其在儿童专科医院的应用潜力*
2020-02-11闵丽婷张笑天徐步龙施芳红张顺国
闵丽婷,张笑天,李 浩△,徐步龙,郑 美,施芳红,张顺国
(1.上海交通大学医学院附属上海儿童医学中心药剂科,上海 200127; 2.上海市虹口区市场监督管理局,上海 200083; 3.上海交通大学医学院附属仁济医院药剂科,上海 200127)
仿制药是指与原研药具有相同的药物活性成分,并在剂型、规格等方面与原研药品保持一致,并具有相同适应证、给药方式和用法用量的药品[1-3]。仿制药为我国人民的健康和有效的医疗保障作出了重要贡献[4]。截至2016年,仿制药处方占美国总药物处方的89%,但仅占药物总支出的27%[4]。仿制药一致性评价是快速提升我国仿制药研制水平的质量提升工程[1,5],科学地对仿制药品进行评价,不仅可提高药物政策制订的准确性,也可提高决策效率[5-7]。同时,仿制药的生物等效性评价、一致性评价等工作为促进我国临床药物可及性作出了重要贡献[8]。2017年起,我国加速推进仿制药一致性评价工作。截至2019年3月,我国已发布20批仿制药参比制剂目录和5批通过一致性评价的药品目录。本研究中通过对20批仿制药参比制剂和5批通过一致性评价的药品的详细情况进行统计分析,并与样本儿童医院药品供应目录进行交叉对比,以期为我国仿制药一致性评价工作及仿制药在儿童专科医院应用提供参考。现报道如下。
1 资料与方法
1.1 资料收集
收集2017年1月1日至2019年3月1日我国原食品药品监督管理总局官方发布的仿制药参比制剂及通过仿制药一致性评价的药品信息。以上海交通大学医学院附属上海儿童医学中心为样本医院,将样本医院药品供应目录与收集的仿制药参比制剂及通过一致性评价的药品信息进行交叉对比分析。
1.2 项目与方法
我国仿制药参比制剂发布情况:根据收集的仿制药参比制剂信息,分析各批次仿制药参比制剂的发布数量和发布时间分布,判断我国仿制药一致性评价工作进展。
仿制药参比制剂的剂型分布情况:分析收集的仿制药参比制剂的剂型,探讨不同剂型的仿制药在总体药品信息中所占的结构比例,同时分析各种剂型的详细分类情况。
仿制药参比制剂的主要药理学归类情况:根据汇总的仿制药参比制剂目录,依据《新编药物学》第17版中对药品的药理学分类情况进行归类,对于药品的主要成分涉及多种药理学归类的药品,根据药品的剂型及实际使用情况进行准确归类,判断我国仿制药参比制剂的品种分布情况。
仿制药参比制剂目录中同种化合物出现频次:提取仿制药参比制剂目录中的药物主要成分信息,分析同种化合物出现频次及药品仿制的热点化合物分布情况。
样本医院院内供应药品与仿制药参比制剂目录及通过一致性评价的药品目录对应情况:将收集的仿制药参比制剂信息及通过仿制药一致性评价的药品信息,与样本医院药品供应目录进行交叉对比,分析仿制药一致性评价工作在儿童专科医院的应用潜力,同时分析我国仿制药一致性评价工作在未来儿童药物可及性中的应用前景。
2 结果
2.1 我国仿制药参比制剂发布情况
自2017年3月17日第1批仿制药参比制剂目录发布至2019年1月15日第20批仿制药参比制剂发布以来,我国仿制药参比制剂共发布20批目录共涉及1 176个药品品规。2017年7月至2018年1月是仿制药参比制剂品种及目录发布的高峰时期;2018年1月至2019年年初,我国仿制药参比制剂发布速度放缓,仿制药参比制剂目录趋于成熟。详见图1和表1。
2.2 仿制药参比制剂的剂型分布情况
1 176种仿制药参比制剂中,全部为口服剂型,主要包括片剂、胶囊剂、颗粒剂、混悬剂等。详见表2。915种片剂品种中,以普通片剂为主,其次为缓释片。194种胶囊剂中,以普通胶囊剂为主,其次为缓释胶囊。1 176种仿制药参比制剂中,泡腾片、分散片、软胶囊、颗粒剂、混悬剂、混悬液、混悬凝胶、干糖浆、散剂、细粒剂是适合儿童使用的口服剂型,共涉及91种(7.74%)药物。
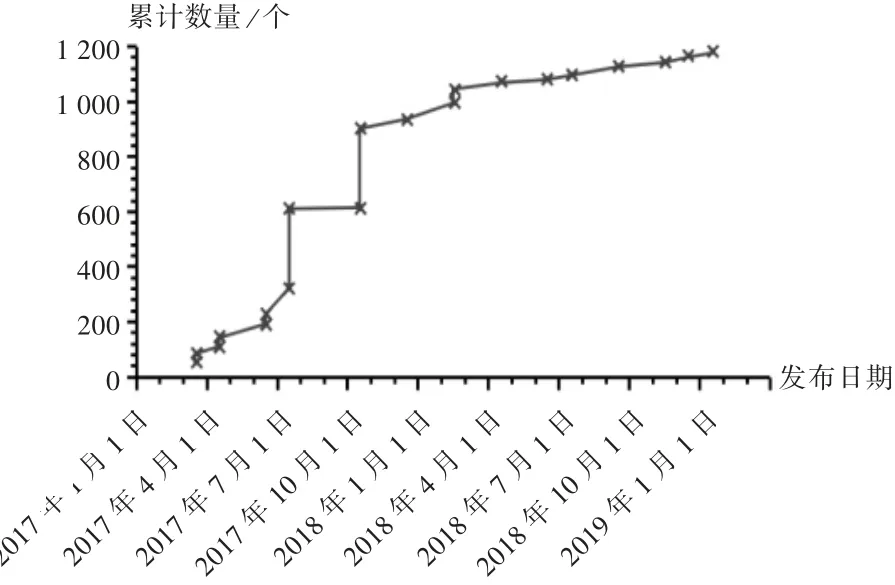
图1 我国仿制药参比制剂发布情况
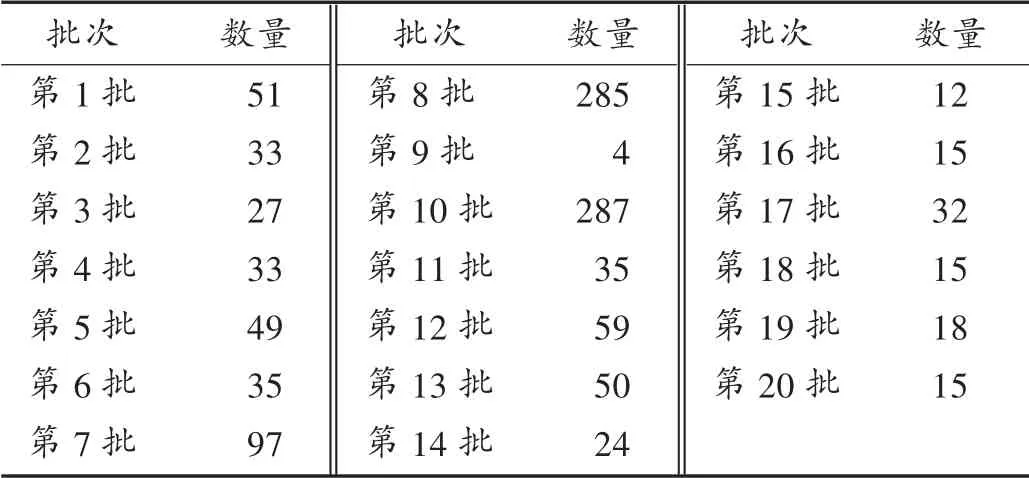
表1 我国20批仿制药目录数量(个)
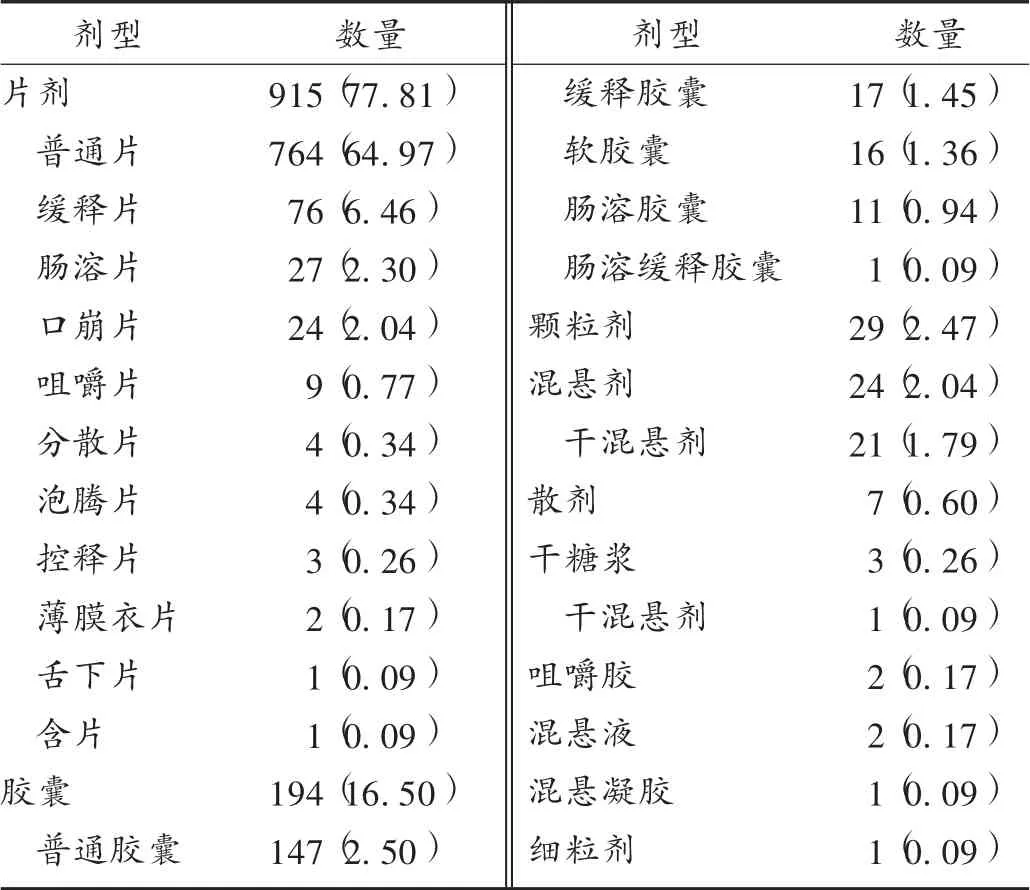
表2 1 176种仿制药参比制剂的剂型分布情况[种(%),n=1 176]
2.3 仿制药参比制剂的主要药理学归类
1 176种仿制药参比制剂以主要作用于中枢神经系统的药物为主,其次为抗感染药物和主要作用于心血管系统的药物。1 176种药物的主要药理学归类覆盖《新编药物学》第17版中的13个药理学归类篇章,但其中175种药物未被该书收录,故无药理学归类。药理学归类分析结果显示,我国仿制药品的参比制剂涉及面广,目录内容已逐渐趋于成熟。详见表3。
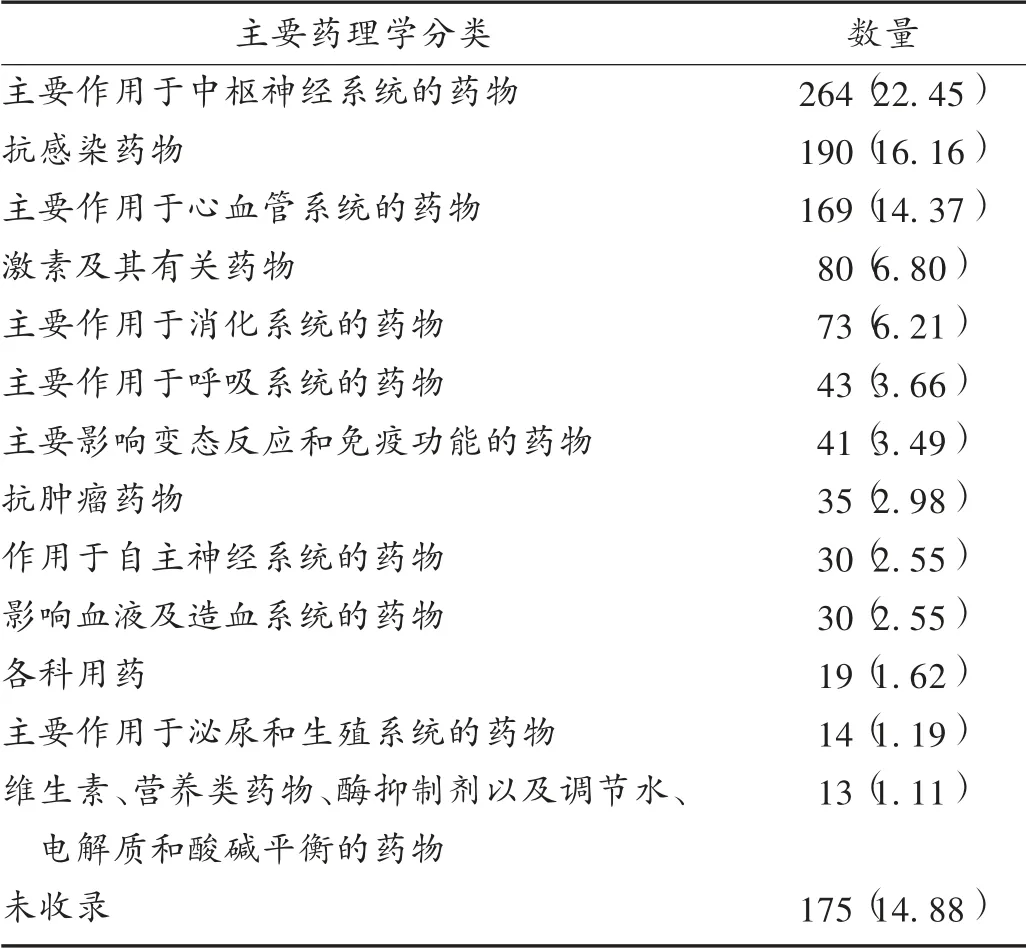
表3 1 176种仿制药参比制剂的主要药理学归类[种(%),n=1 176]
2.4 仿制药参比制剂目录中同种化合物分布情况
1 176种仿制药参比制剂中,共5种药物成分的参比制剂信息超过10条,其中布洛芬、喹硫平的仿制药参比制剂信息为12条;利培酮和双氯芬酸钠的仿制药参比制剂信息为11条;羟考酮的仿制药参比制剂信息为10条。这5种药物主要用于解热镇痛或用于治疗精神类疾病。此外,阿莫西林、单硝酸异山梨酯和美托洛尔的仿制药参比制剂信息为9条。结合仿制药参比制剂的主要药理学归类情况,我国仿制药的研究热点主要集中于神经系统领域。
2.5 样本医院院内供应药品与仿制药参比制剂目录及通过一致性评价的药品目录对应情况
我国通过5次信息发布,公布了5批已批准通过仿制药质量和疗效一致性评价的品种目录,共涉及57个药品品种[1]。结合已发表的1 176种药品,与样本儿童医院供应的药品目录进行交叉对比分析。结果显示,样本医院供应药品中口服的药品共313种,其中175种药品(55.91%)2种目录均未收录;8种药品(占2.56%)为通过仿制药一致性评价的药品;37种药品(占11.82%)与仿制药参比制剂相同,且在目录中;93种药品(占29.71%)的主要成分存在于仿制药参比制剂目录中,但非原参比制剂或非通过仿制药一致性评价的药物。我国仿制药一致性评价及仿制药在儿童专科医院中的应用发展仍有较大空间。
3 讨论
3.1 仿制药一致性评价的历史背景和工作进展
2012年2月,国务院印发《国家药品安全“十二五”规划》,提出应全面提高仿制药质量,逐步开展仿制药一致性评价工作;2013年3月,原国家食品药品监督管理总局发布《关于开展仿制药一致性评价工作的通知(国食药监注[2013]34号)》,提出2020年全面完成基本药物的质量一致性评价;2015年8月,国务院发布《关于改革药品医疗器械审评审批制度的意见(国发[2015]44号)》,提高仿制药质量成为5大改革目标之一;2016年3月,国务院办公厅印发《关于开展仿制药质量和疗效一致性评价的意见(国办发[2016]8号)》,将仿制药一致性评价工作提升至国家层面;2017年8月,总局发布《总局关于仿制药质量和疗效一致性评价工作有关事项的公告》(2017年第100号),为仿制药一致性评价过程中涉及的各项信息清晰明了地提出了指导意见,仿制药一致性评价体系逐步趋于完善。自2017年3月第1批仿制药参比制剂目录发布后,至2019年1月15日共发布仿制药参比制剂目录20批共涉及1 176个药品品规。此外,5批仿制药通过一致性评价,涉及57个品规、30个药品生产企业[1]。
3.2 仿制药一致性评价工作侧重点
本研究结果显示,我国仿制药一致性评价工作主要侧重于经口服用的仿制药品的一致性评价工作。1 176种仿制药参比制剂品规中,均为口服制剂,以片剂为主、其次为胶囊剂,而其他剂型的仿制药参比制剂较少。缺乏注射剂型等仿制药品参比标注。在仿制药生物等效性试验备案信息平台数据库中,注射制剂的占比仅为0.7%[9]。提示我国未来应进一步侧重注射制剂的仿制药一致性评价工作[10]。
对于药物的药理学分类,仿制药参比制剂主要集中在中枢神经系统药物、抗感染药物和作用于心血管系统的药物,这与目前临床常用的药物品种分类保持一致。1 176种仿制药参比制剂品规中,5种药物成分的参比制剂品规信息超过10条,3种药物的参比制剂信息为9条,这与仿制药参比制剂的主要药理学分布情况保持一致,研发热点主要集中在解热镇痛、精神疾病治疗、抗感染治疗和心血管疾病治疗方面。但目前我国对于低价药、独家药的仿制药一致性评价工作开展较缓慢,如对儿童专用的短缺品种缺乏相应的鼓励和保障机制[11]。
3.3 仿制药一致性评价在儿童专科医院的应用潜力
本研究结果显示,1 176种仿制药参比制剂中,仅泡腾片、分散片、软胶囊、颗粒剂、混悬剂、混悬液、混悬凝胶、干糖浆、散剂、细粒剂是适合儿童使用的口服剂型,共涉及91种药物,仅占发布的药品总数的7.74%。交叉分析结果显示,在57种通过仿制药一致性评价的品规中,仅8种存在于样本医院药品供应目录中,37种药品存在于仿制药参比制剂目录中。93种药物的主要成分存在于仿制药参比制剂目录中,但这些药物并非国家发布的仿制药参比制剂或通过一致性评价的药物。此外,175种药物均不存在2种目录中,表明我国仿制药一致性评价工作目前尚未在儿童专科医院进行延伸,93种药品主要成分存在于仿制药参比制剂的目录中的药品,具有逐步替换为仿制药或参比原研药的潜力,以逐步降低医药费用,并同时加强对仿制药的疗效和安全性的科普宣传和用药教育[12-14]。仿制药一致性评价工作可能是未来逐步解决我国儿童专属药品短缺,提升儿童用药可及性的重要措施。我国应逐步推进儿童专用药品仿制药参比制剂的遴选工作,探讨无法采用参比制剂进行评价的儿童常用药品的一致性评价策略[15-18]。
我国仿制药一致性评价工作正逐步趋于成熟。仿制药在儿童专科医院的应用较少,未来在确证仿制药疗效和安全性后,应逐步推进仿制药在儿童专科医院的应用。
