CSF1R基因突变致遗传性弥漫性球体细胞白质脑病1例☆
2020-01-14成红江赵豆豆王国印许丽娜杨丰兵贾龙斌
成红江 赵豆豆 王国印 许丽娜杨丰兵 贾龙斌○☆
遗传性弥漫性球体细胞白质脑病 (hereditary diffuse leukoencephalopathy with spheroids,HDLS)是一种罕见的成年发病的常染色体显性遗传脑白质病,外显率较高,临床表现多变,包括性格和行为改变、痴呆、抑郁、帕金森综合征、癫痫发作、运动障碍等[1-2],其病理特点主要为广泛的髓鞘丢失、轴突破坏及轴突球样体等[1,3]。据相关文献报告[4],集落刺激因子受体-1(colony-stimulating factor 1,CSF1R)为该病致病基因。该病发病罕见,现将我院首诊的1例HDLS报告如下,以期增加临床医生对本病的认识。
1 临床资料
1.1 发病情况患者女,26岁,主因“右上肢乏力1年,言语不利、记忆力减退5个月余,右下肢乏力2个月”于2017年9月13日入我院。患者于1年前无明显诱因在使用电脑打字过程中发现右上肢乏力,主要表现为右手活动欠灵活,但右上肢上抬可,持物无影响,不伴肢体麻木,不伴言语不利、饮水呛咳,不伴头痛、恶心、呕吐等,日常生活影响不明显,未在意。5个月余前被家属发现其言语不利,伴记忆力减退,以近事记忆为著,反应略迟钝,仍未予以注意。2个月前在外旅游时不慎摔倒,行相关检查未发现骨折,此后始终感觉右下肢乏力,走路拖拽,以足部活动为著,不伴肢体麻木、大小便障碍等,为求进一步诊治入住我院。既往体健。否认手术、输血、中毒史。非早产、难产。父母、弟弟、女儿健康状况良好。否认神经精神疾病家族史。
1.2 体格检查体温36.2℃,脉搏78次/min,呼吸20次/min,血压110/82 mmHg。心律齐,双肺呼吸音清,未闻及干湿性啰音,腹软无压痛,双下肢无水肿。神经系统查体:神志清楚,言语欠流利,记忆力、计算力减退,伸舌略右偏,余颅神经(-),左侧肢体、右上肢肌力5级,右手握力差,右手指活动欠灵活,右下肢轻瘫试验阳性,右侧肢体腱反射(+++),左侧肢体腱反射(++),双侧肌张力适中,双侧Hoffman's征(+),右侧Babinski's征(+),左侧Babinski's征(-),右侧指鼻及跟膝胫试验欠稳准,左侧稳准,脑膜刺激征(-),步态为偏瘫步态。
1.3 辅助检查头颅MRI平扫+增强(本院,2017年9月14日,如图1):脑内多发异常信号;未见明显强化。脑脊液:压力160 mmH2O,常规、生化未见异常。AQP-4-Ab+NMOIgG血清及脑脊液均为阴性。余血常规、急诊生化、甲状腺功能、肿瘤系列、传染病系列、风湿免疫指标等均为阴性。
1.4 诊断、治疗与随访
1.4.1 诊断与治疗 诊断为脱髓鞘病。入院后予以完善相关检查,给予静脉滴注甲强龙500 mg/d×3 d,240 mg/d×3 d,120 mg/d×3 d,醋酸泼尼松片60 mg/d×3 d,后右侧肢体乏力症状略改善,仍欠佳,于2017年10月11日出院。(出院时建议醋酸泼尼松片30 mg/d继续口服,1个月后复查)。
1.4.2 随访 患者于2017年11月28日因症状好转不明显就诊于北京某三甲医院。行头颅MRI平扫+增强示“中脑左侧大脑脚、左侧内囊后肢、左侧脑室前后角旁、胼胝体压部、两侧放射冠、半卵圆中心及左侧额顶叶皮层下可见多发斑、片状异常信号,T1WI上为等/稍低信号,T2WI/FLAIR上为高信号,DWI上为高/稍高信号,无占位效应。增强后脑内未见明显异常强化”。肌电图+诱发电位:VEP:双侧P100潜伏期及波形未见异常;BAEP:听阈:左15 dB,右25 dB,各波均未见异常;SEP:刺激右正中神经,各波均未见异常。刺激右胫神经:皮层波幅偏低,余未见异常。余心脏彩超、胸部CT未见异常。实验室化验:肿瘤系列:血清骨胶素CYFRA21-1 5.06 ng/mL(0.1~3.3 ng/mL),肿瘤相关抗原CA19-9 39.4 U/mL(0.01~37 U/mL),余指标未见异常。余甲功全项、电解质、肝肾功、脑脊液生化+常规、脑脊液细胞学、脑脊液免疫球蛋白(IgG、IgM、IgA)、脑脊液找抗酸杆菌、脑脊液墨汁染色找隐球菌、脑脊液涂片找细菌、脑脊液抗Amphiphysin抗体、AQP-4-Ab+NMO-IgG(脑脊液及血清)、自身免疫性脑炎相关抗体(脑脊液及血清)、神经系统副肿瘤综合征相关抗体(脑脊液及血清)、脑脊液蛋白电泳、中枢神经系统脱髓鞘疾病(抗NMO抗体IgG、抗MBP抗体IgG、抗MOG抗体IgG)、脑脊液TORCH8项、代谢脑病六项、极长链脂肪酸检测及风湿免疫相关指标(风湿三项、免疫五项、抗核抗体谱、抗中心粒细胞胞浆抗体谱、抗β2-糖蛋白1抗体IgA/G/M、抗心磷脂抗体IgA/G/M、血沉)均为阴性。入院考虑“原发性中枢神经系统血管炎可能”,予醋酸泼尼松片20 mg/d晨起顿服,静脉滴注血栓通注射液300 mg/d、复方脑肽节苷脂注射液20 mL/d、七叶皂苷钠20 mg/d及补钙(碳酸钙片0.75 g,每天3次)、补钾(氯化钾缓释片1 g,每天2次)等治疗。症状缓解不明显,于2017年12月12日出院,出院诊断“脑白质病变 特发性炎性脱髓鞘病?原发性中枢神经系统血管炎?”,建议院外继续口服醋酸泼尼松片20 mg/d,每周减2.5 mg。患者出院后逐渐出现情感淡漠、抑郁等精神症状,言语不利及肢体乏力症状进行性加重,于2018年6月6日就诊于上海某三甲医院,行脑白质病相关基因检测(北京金准基因科技有限责任公司,明睿Focus-脑白质病,2018年7月8日)示该患者在第5号染色体CSF1R基因第19号外显子区域(chr5:149435609)存在一处杂合突变:c.2534T>C(胸腺嘧啶>胞嘧啶),导致氨基酸改变p.L845p(亮氨酸>脯氨基),因其为常染色体显性遗传,理论上此杂合突变可能致病(如图2)。HGMDpro数据库报道情况:突变位点c.2534T>C报道为致病基因突变(DM,报道疾病:Leukoencephalopathy with cerebral calcifications and cysts[5],27895249)。最后确诊为遗传性弥漫性球体细胞白质脑病。患者于2018年9月27日在我科门诊复诊,仍情感淡漠,不愿讲话,伴反应迟钝、言语含糊,走路为偏瘫步态,较前明显加重,需在家人搀扶下行走。复查头颅MRI(当地县医院,2018年9月25日)示“颅内多发异常信号”(如图3)。2019年4月11日于我院门诊以患者(Ⅱ2)为先证者,完善家系调查,基因结果(北京金准基因科技有限责任公司,2019年4月21日)显示:其父亲(Ⅰ1)、母亲(Ⅰ2)、弟弟(Ⅱ1)、丈夫(Ⅱ3)均未携带该异常基因,其女(Ⅲ1,3岁,未发病)存在相同的杂合突变位点(家系图如图4)。
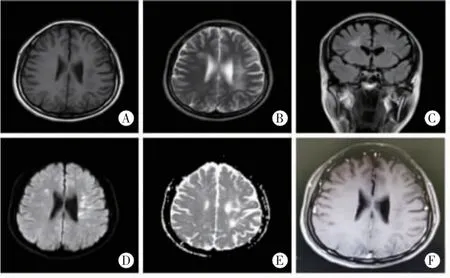
图1 患者2017年9月14日头颅MRI结果。A~F:显示双侧侧脑室旁及半卵圆中心多发斑、片状异常信号,T1WI(A)上为等/稍低信号,T2WI/FLAIR(B/C)上为高信号,DWI(D)上为高/稍高信号,ADC(E)为等、稍高或高信号,增强(F)未见明显异常强化

图2 该患者在chr5-149435609处存在一处杂合突变:c.2534T>C(箭头)

图3 患者2018年9月25日头颅MRI结果。a~f:颅内多发异常信号(较前明显增多)。T1WI(b)上为等/稍低信号,T2WI(a)/FLAIR(c和d)上为高信号,DWI(e和f)上为高/稍高信号。前后两次头颅MRI对比可见持续进展T2WI/FLAIR高信号,DWI为持续性高信号

图4 患者家系调查图
2 讨论
HDLS由AXELSSONR等[1]于1984年最先报告。2011年,RADEMAKERS等[4]运用全基因组连锁分析和外显子测序确定位于5q32的CSF1R基因是该病的致病基因。在大脑中,小胶质细胞是对神经细胞具有吞噬和营养作用的巨噬细胞,CSF1R基因突变会造成小胶质细胞增殖分化受阻,使HDLS患者发病[6,7-11]。显微镜下,HDLS主要病理表现为脑白质疏松、空泡化,以及有髓纤维丢失,星形细胞增生,含脂巨噬细胞及弥漫性小胶质细胞的活化,尤其在皮层病灶可见轴索球样变,其可能为HDLS特征性病理学表现[12-14]。
HDLS的临床表现主要与受累部位有关,具有显著个体化差异,包括执行能力下降,记忆力下降,人格改变,运动障碍,癫痫发作,额叶症状等[2,14]。需同额颞叶痴呆[15]、多发性硬化[16]或CADASIL[17]相鉴别。其临床表现复杂多样,无特异性,很难与其他脑白质病相鉴别。在影像学方面,其特征性表现,可能会对其诊断提供一定帮助。HDLS典型的头颅MRI表现为双侧额叶或额顶叶皮层下、脑白质深部、脑室周围、胼胝体或皮质脊髓束等部位T2WI/FLAIR高信号,T1WI低信号,不断加重的脑白质损害导致脑室扩大和继发性脑萎缩改变,一般没有灰质、脑干的萎缩,多无脑实质的异常增强及小脑的异常改变[18-19]。早期多为非对称性,表现为斑片样或局限性损害,随着病程进展逐渐呈对称性损害。持续进展的脑白质DWI高信号可能为HDLS重要的影像学特征[20]。其DWI高信号可能与T2穿透效应有关[21]。本例患者头颅MRI示颅内多发长T1、长T2信号,DWI为高信号,增强无强化,随着病情进展,T2WI/FLAIR高信号病灶进行性增多,DWI呈持续进展性高信号,其分布范围除侧脑室旁外,额顶叶皮层下、半卵圆中心、胼胝体、中脑等多部位均受累,形态各异,较大处为融合性病灶,左侧脑实质略萎缩,脑室略大,最具特征性的是三次复查DWI均为高信号,符合HDLS影像学特征。而多发性硬化一般为侧脑室旁多发类圆形异常信号,T1WI上为等或低信号,T2WI/FLAIR上为多灶性不同程度的高信号,其长轴与侧脑室或大脑长轴垂直,且有一狭窄正常信号带将病灶与侧脑室分开,较大的活动性病灶时DWI上可显示弥散受限,增强可有强化[22],该患者影像学特点与其明显不符,血清及脑脊液NMO-IgG两次复查均为阴性,激素冲击治疗无效,基本除外此诊断。CADASIL影像学以颞叶及外囊白质损害为特点,与HDLS分布特点不符[23-24]。故结合其特征性影像学特点及基因检测结果HDLS诊断明确。
本例患者为基因确诊病例,目前国内已有第18和20号外显子错义突变报道[25-27],本例为第19号外显子突变,属国内首例。HDLS作为一种遗传病,确诊方法主要是基因检测,或病理证实。目前尚无特效治疗,以支持对症治疗为主,包括营养支持与抗癫痫、抗感染治疗等。最常见的死亡原因是肺炎及其他继发性感染。
综上,如果患者发病年龄较轻,出现进行性神经功能缺损症状,头颅核磁提示双侧脑白质病变时,特别是持续进展DWI高信号,不能用常见疾病解释时,要高度警惕HDLS的可能,尽早完善CSF1R基因检测,从而确诊或除外HDLS。对于确诊病例,我们建议患者家属进行遗传学检测,以期降低其后代的患病风险。
