壳聚糖/β-环糊精复合物的制备及应用
2020-01-13刘佳鑫王思琪周悦王西赵文珍赵珺
刘佳鑫,王思琪,周悦,王西,赵文珍,赵珺*
1. 长春大学食品科学与工程学院(长春 130022);2. 郑州市城区河道管理处(郑州 450000)
生活中腌制品、纺织品、化妆品等行业大量排放含Cl-废水[1],由于Cl-具有强腐蚀性,排入江河湖海中会污染水质,会使动植物不能正常生长,造成生态环境危害[2-3]。刘伟佳[4]研究表明水中的氯离子和硫酸根离子()会污染地下水且氯离子对地下水的污染要明显高于SO42-。李春云等[5]研究表明,高浓度的造纸废水不利于灌溉盐碱化芦苇湿地,其会使Cl-在土壤中下层出现积累,不利于芦苇对钠离子(Na+)的吸收。目前,我国去除水中Cl-的常用方法有石灰铝盐沉淀、离子交换、膜分离、电吸附、电渗析等[6],但这些方法存在着操作复杂、易产生大量固体废弃物、成本和能耗较高等问题。近年来,壳聚糖和β-环糊精天然产物由于具有吸附作用且不会造成水的二次污染,常被用于处理含重金属离子、染料、酚类、有机物等生活和工业废水。例如用四氧化三铁和β-环糊精改性过的磁性壳聚糖微球,对亚甲基蓝有很高的吸附量和去除率[7]。而采用反相悬浮法将壳聚糖与β-环糊精复合,对葛根素的去除效果比单一壳聚糖好[8],然而目前关于壳聚糖交联β-环糊精聚合物对水中Cl-去除研究还鲜见报道。
壳聚糖是唯一一种天然碱性多糖,是甲壳素经脱乙酰作用的产物[9],难溶于水和碱性溶液,但溶于酸[10]。其分子链上存在大量的氨基、羟基及一些N-乙酰氨基,可在酸性溶液中形成阳离子电解质,对阴离子具有吸附能力[11-13]。β-环糊精具有特殊的空腔结构,能有效包裹一些有机分子、无机离子、水分子、卤化氢和稀有气体等形成包络物客体,将其从环境中提取出来,从而降低污染。而通过改性制成的β-环糊精聚合物,既保持了β-环糊精的包络及识别作用,又兼有较好的机械强度和稳定性[14]。将β-环糊精聚合物交联至壳聚糖分子链上,得到环糊精修饰的壳聚糖衍生物,用以处理含Cl-废水,以降低废水中Cl-的含量。
1 材料和方法
1.1 材料与仪器
β-环糊精(上海惠世生化试剂有限公司);壳聚糖(脱乙酰度80.0%~95.0%,国药集团化学试剂有限公司);柠檬酸、磷酸二氢钠(北京化工厂);聚乙二醇400、戊二醛、基准氯化钠(天津市光复精细化工研究所);蒸馏水、盐酸、氢氧化钠、乙醇、柠檬酸(均为分析纯)。
AM-3250 A型磁力搅拌恒温器(上海硕光电子科技有限公司);HH-ZK1型恒温水浴锅(巩义市予华仪器有限责任公司);GZX-9070 MBE型电热鼓风干燥箱(上海博迅实业有限公司医疗设备厂);AUW 120型电子天平(日本岛津仪器有限责任公司);PHS-3C型pH剂(上海仪电科学仪器股份有限公司);TDL-50 B型低速离心机(上海安亭科学仪器厂);NTS-4000 B型恒温振荡水槽(日本东京理化械株式会社);Nicolet iS5型傅里叶红外光谱仪(日本岛津仪器有限责任公司);JSM-6510 LA扫描电镜(日本电子株式会社);JJ-1 BA型搅拌器(常州润华电器有限公司)。
1.2 方法
1.2.1β-环糊精聚合物的制备[15-16]
将2 g柠檬酸、1 g聚乙二醇400、0.25 g磷酸二氢钠、10 gβ-环糊精放入烧杯中,加入蒸馏水并加热,使其充分溶解。将溶液放在恒温鼓风干燥箱中烘干,取出烧杯,冷却。将生成的产物在瓷乳钵中仔细研磨,然后用蒸馏水、无水乙醇充分洗涤、抽滤、烘干。最后,将干燥的产物仔细研磨,即得β-环糊精聚合物。
1.2.2 壳聚糖/β-环糊精复合物的制备及制备条件优化
1.2.2.1 壳聚糖/β-环糊精复合物的制备[17]
称取壳聚糖于盐酸溶液中,同时称取β-环糊精聚合物于蒸馏水中,将两种溶液倒入烧杯中混匀,加热升温至60 ℃后向烧杯中缓慢滴加25%戊二醛溶液,开始恒温搅拌,待反应结束后将沉淀过滤,用乙醇、蒸馏水洗涤、抽滤,滤出物于45 ℃下烘至恒质量,得到棕色粉末状壳聚糖/β-环糊精复合物。
1.2.2.2 壳聚糖/β-环糊精复合物制备条件优化
分别设定壳聚糖与β-环糊精聚合物质量比、反应温度、反应时间、戊二醛添加量的不同水平进行单因素试验,制备出壳聚糖/β-环糊精复合物,制备条件如表1所示。
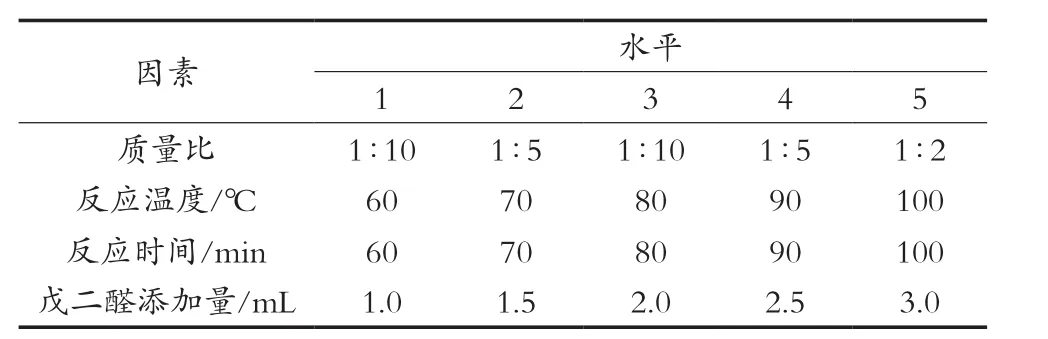
表1 壳聚糖/β-环糊精复合物制备单因素试验设计
1.2.3 吸附试验及壳聚糖/β-环糊精复合物最优制备条件确定
按照腌制品行业脱盐处理后废水中氯离子含量配制0.15% Cl-模拟废水[18]。
称取一定质量不同制备条件下获得的壳聚糖/β-环糊精复合物,加入到0.15% Cl-模拟废水中,调节pH为4,在100 r/min转速下恒温振荡2 h,离心并取上层清液。
Cl-含量采用硝酸银滴定法进行测定。Cl-吸附率按式(1)计算,Cl-吸附量按式(2)计算。
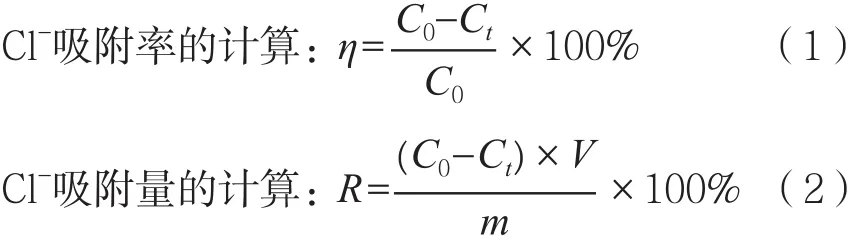
式中:C0为Cl-的初始浓度,mg·L-1;Ct为恒温振荡2 h后的剩余浓度,mg·L-1;V为Cl-溶液的体积,L;m为吸附时所用壳聚糖/β-环糊精复合物质量,g。
以不同制备条件下壳聚糖/β-环糊精复合物对氯离子的吸附量和吸附率作对比,筛选出最优壳聚糖/β-环糊精复合物制备条件。
1.2.4 傅里叶变换红外光谱表征
将壳聚糖、β-环糊精、β-环糊精聚合物、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物分别经溴化钾压片,用傅里叶变换红外光谱仪进行测定,扫描范围为4 000~500 cm-1[19-20],分析各物质红外光谱以判断合成及吸附前后样品表面基团的变化。
1.2.5 扫描电镜表征
将壳聚糖、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物放在铜台上喷金,在加速电压5.0 kV、电流10 mA的条件下对壳聚糖、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物进行形貌观察。
2 结果与分析
2.1 壳聚糖/β-环糊精复合物制备时质量比对Cl-吸附量和吸附率的影响
由图1可知,Cl-吸附量和吸附率随着壳聚糖与β-环糊精聚合物质量比的增加而不断上升,当质量比达到1︰5时,Cl-吸附量、吸附率达到最高,分别为19.6 mg·g-1和26.2%;之后随着壳聚糖与β-环糊精聚合物质量比的增大,吸附量和吸附率逐渐减小。这是因为随着质量比的不断增加,复合物与Cl-结合位点不断增多,吸附量和吸附率不断增加,但达到一定质量比时,过量的壳聚糖会与交联剂发生反应,使壳聚糖与β-环糊精聚合物反应降低,导致吸附率和吸附量下降,由此确定制备最佳壳聚糖与β-环糊精聚合物质量比为1︰5。

图1 壳聚糖、β-环糊精聚合物质量比对Cl-吸附量和吸附率的影响
2.2 壳聚糖/β-环糊精复合物制备时反应温度对Cl-吸附量和吸附率的影响
由图2可知,Cl-吸附量和吸附率随着反应温度的升高而增加,当反应温度达到80 ℃时,吸附量、吸附率达到最高,分别为27.41 mg·g-1和38.7%;之后随着温度升高,吸附量和吸附率逐渐降低,这是因为温度过高使部分产物发生分解,导致吸附量和吸附率下降,由此确定制备最佳反应温度为80 ℃。
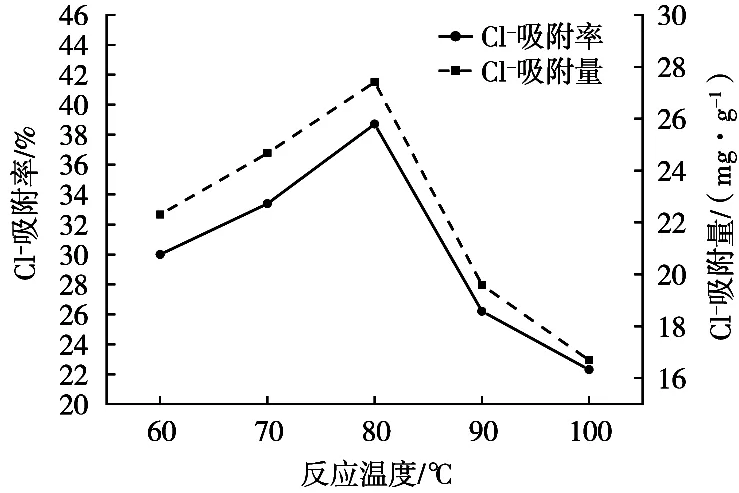
图2 反应温度对Cl-吸附量和吸附率的影响
2.3 壳聚糖/β-环糊精复合物制备时反应时间对Cl-吸附量和吸附率的影响
由图3可知,Cl-吸附量和吸附率随着反应时间的延长而增加,当反应时间达到90 min时,吸附量、吸附率达到最高,分别为29.75 mg·g-1和40.2%,之后随着时间延长吸附量和吸附率并无太大变化,这是因为在90 min时壳聚糖与β-环糊精聚合物已反应完全,之后没有壳聚糖/β-环糊精复合物的生成,导致吸附量和吸附率不再变化。由此确定制备最佳反应时间为90 min。
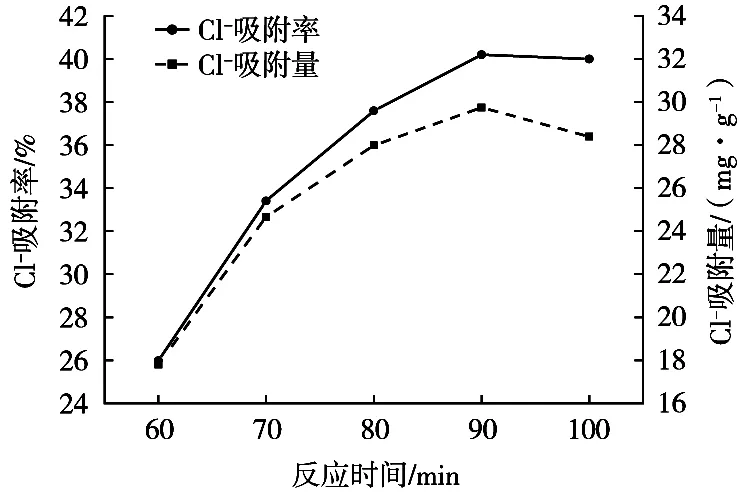
图3 反应时间对Cl-吸附量和吸附率的影响
2.4 壳聚糖/β-环糊精复合物制备时戊二醛添加量对Cl-吸附量和吸附率的影响
由图4可知,Cl-吸附量和吸附率随着戊二醛添加量增加而逐渐增加,在1.5 mL时吸附量、吸附率达到最大值,分别为30.34 mg·g-1和40.78%;之后随着添加量的增加,Cl-吸附量和吸附率反而减小。这是因为过量的戊二醛交联剂自身也会发生交联,导致壳聚糖和β-环糊精聚合物不能得到完全的交联反应,由此确定最佳交联剂戊二醛添加量为1.5 mL。
2.5 β-环糊精、β-环糊精聚合物红外光谱图分析
由图5可知,β-环糊精和β-环糊精聚合物红外光谱中特征吸收峰大致相同,均在3 400 cm-1附近处出现由于—OH键的伸缩振动产生的强而宽的吸收峰,在937.65和860.63 cm-1处分别出现α-(1, 4)糖苷键和α-(1, 4)吡喃葡萄糖的吸收特征峰。而β-环糊精聚合物的红外光谱中,除保留了β-环糊精分子中葡萄糖单元的特征吸收峰及—OH的伸缩振动产生的吸收峰外,在1 708.33 cm-1处出现了酯基的吸收峰,由此推测,柠檬酸上的羧基与β-环糊精上的羟基反应生成了酯键[21-22],合成了β-环糊精聚合物。

图4 戊二醛添加量对Cl-吸附量和吸附率的影响

图5 β-环糊精、β-环糊精聚合物的红外光谱
2.6 壳聚糖、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物红外光谱图分析
由图6可知,3 426.79 cm-1是壳聚糖O—H及N—H的伸缩振动吸收峰,895.72 cm-1是壳聚糖β-(1, 4)糖苷键的特征峰;由图5β-环糊精聚合物红外光谱图可知,在937.65和860.63 cm-1处分别是β-环糊精聚合物上的α-(1, 4)糖苷键和α-(1, 4)吡喃葡萄糖吸收特征峰;与壳聚糖和β-环糊精聚合物红外光谱图对比可知,壳聚糖/β-环糊精复合物在895.72 cm-1处特征峰是壳聚糖的β-(1, 4)糖苷键的特征峰,946.49和860.32 cm-1处分别是β-环糊精聚合物上的α-(1, 4)糖苷键和α-(1, 4)吡喃葡萄糖吸收特征峰。由于壳聚糖和β-环糊精聚合物有很多相同的基团,当二者交联后,壳聚糖会掩盖住β-环糊精聚合物,由此可推断β-环糊精聚合物与壳聚糖发生了交联,合成了壳聚糖/β-环糊精复合物。
吸附Cl-后壳聚糖/β-环糊精复合物红外光谱图与吸附前壳聚糖/β-环糊精复合物相比,3 384.62 cm-1处O—H及N—H伸缩振动吸收峰迁移到3 416.09 cm-1处;壳聚糖/β-环糊精复合物在1 641.9和1 600.6 cm-1处N—H变形和N—H弯曲振动峰,吸附Cl-后伸缩到1 637.22和1 577.29 cm-1处,由此推断,壳聚糖/β-环糊精复合物上氨基参加了反应,吸附后壳聚糖/β-环糊精复合物在946.49和860.32 cm-1处吸收峰消失,也可推断复合物上的β-环糊精聚合物和Cl-同样也发生反应,此外其他特征吸收峰没有明显变化。因此合成了壳聚糖/β-环糊精复合物,且壳聚糖/β-环糊精复合物与Cl-发生了反应。

图6 壳聚糖、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物红外光谱
2.7 壳聚糖、壳聚糖/β-环糊精复合物、吸附Cl-后壳聚糖/β-环糊精复合物扫描电镜分析
由图7可知,壳聚糖呈片状结构,表面光滑无褶皱,壳聚糖/β-环糊精复合物呈固体颗粒结构,且表面紧密粗糙,比表面积较壳聚糖大,吸附位点增多。吸附Cl-后壳聚糖/β-环糊精复合物的表面更加粗糙,由此推测其表面聚集了众多氯聚集体。
3 结论与讨论
为了确定壳聚糖/β-环糊精复合物最优制备条件,考察了壳聚糖与β-环糊精聚合物质量比、反应温度、反应时间、戊二醛添加量对废水中Cl-吸附量和吸附率的影响。研究结果显示:当壳聚糖与β-环糊精聚合物质量比为1︰5、反应温度为80 ℃、反应时间为90 min、戊二醛添加量为1.5 mL时,Cl-的吸附量和吸附率达到最佳,分别为30.34 mg·g-1和40.78%。经红外图谱分析表明,产物在1 708.33 cm-1处出现了由柠檬酸上的羧基与β-环糊精上的羟基反应生成的酯基吸收峰,因此证明合成了β-环糊精聚合物;壳聚糖/β-环糊精复合物红外光谱图上分别在895.72,946.49和860.32 cm-1处出现了壳聚糖的β-(1, 4)糖苷键、β-环糊精聚合物α-(1, 4)糖苷键、α-(1, 4)吡喃葡萄糖吸收特征峰,壳聚糖与β-环糊精聚合物发生了交联反应,说明合成了壳聚糖/β-环糊精复合物;吸附Cl-后壳聚糖/β-环糊精复合物红外光谱图与吸附前壳聚糖/β-环糊精复合物相比,一些特征峰消失或发生了位移,这与吸附到Cl-有一定的关系。经扫描电镜分析表明,壳聚糖/β-环糊精复合物表面紧密粗糙,比表面积较壳聚糖大,吸附位点增多,吸附率增加;吸附后的壳聚糖/β-环糊精复合物由于表面聚集了众多氯聚集体而变得更加粗糙。
壳聚糖和β-环糊精是天然产物,制备成壳聚糖/β-环糊精复合物对其进行吸附是既利用壳聚糖对阴离子吸附能力又利用β-环糊精的空腔结构,其操作简单、成本低廉。试验尝试在β-环糊精聚合物的基础上,生成壳聚糖/β-环糊精复合物,并对废水中的Cl-进行吸附研究,吸附效率明显高于壳聚糖和β-环糊精直接生成的复合物,而吸附量和吸附率也可进一步通过优化吸附工艺得以提高。
