NaSal/2SHNC对R14HTAB体系自组装行为的影响机制
2020-01-10孙浩玉李嘉伟张英男燕友果
孙浩玉, 张 琰, 高 阳, 李嘉伟, 张英男, 燕友果, 张 军
(1.中国石化胜利石油工程有限公司钻井工艺研究院,山东东营 257000; 2.中国石油大学(华东)材料科学与工程学院,山东青岛266580; 3.中国石油新疆油田公司勘探开发研究院,新疆克拉玛依 834000)
表面活性剂作为一种基本的组装基元,由于其特殊的两亲分子结构,在体相溶液中,表面活性剂具有逃离水相的趋势,可自发地组装形成各种形貌的胶束结构,例如球形、蠕虫状、囊泡、片层等。蠕虫状胶束因其特殊的黏弹性被广泛应用于油气田开发、减阻、生活用品等领域[1-3]。蠕虫状胶束的构筑方法众多,例如:无机盐/表面活性剂混合构筑法[4]、有机盐/表面活性剂混合构筑法[5]、阴阳复配体系构筑法[6]、聚合物/表面活性剂混合构筑法[7]、纳米颗粒/表面活性剂混合构筑法[8]等。其中有机盐/表面活性剂混合构筑蠕虫状胶束的基本原理是:有机盐通过屏蔽带电头基间的静电斥作用,使表面活性剂头基靠得更紧密,从而增加体系端部能量;同时有机盐的疏水尾链插入到胶束内核与表面活性剂的疏水尾链增强了疏水缔合作用;这两种作用共同促使胶束的形成[9]。此外有机盐类型是影响蠕虫状胶束结构和性能的重要因素之一,魏西莲等[10]采用实验方法研究有机盐类型对表面活性剂体系流变性能的影响,推测不同的有机盐在胶束表面吸附量不同,从而调控蠕虫状胶束的形貌,进而影响体系的零剪切黏度。蠕虫状胶束体系的研究大多采用实验手段,通过流变仪表征体系的剪切黏度、黏性弹性模量等宏观流变性能,通过小角度中子散射(SANS)、动态光散射(DLS)、低温透射电子显微镜(Croy-TEM)等[11-14]表征胶束尺寸、自组装形态等微观形貌,但难以观测蠕虫状胶束自组装形成的微观过程,无法定量表征分子之间的相互作用强度。分子动力学模拟[15]尤其是粗粒化分子动力学和耗散粒子动力学,可以构建分子间的相互作用模型,用于考察微米、微秒量级空间和时间尺度内的表面活性剂自组装过程,通过提取构型参数、相互作用等参量揭示自组装机制,并通过抗拉强度计算揭示其黏弹性等力学性能。相关模拟能够弥补实验中无法观察微观过程并揭示分子原子间相互作用的不足。Noriyoshi等[16]采用耗散粒子动力学(DPD)的方法研究表面活性剂自组装形成蠕虫状胶束的过程,揭示了蠕虫状胶束的自组装的过程可分为成核、球形胶束形成及长大、椭球型胶束形成及蠕虫状胶束形成与长大4个过程;Maiti等17]研究低聚表面活性剂的聚合度和联接基团长度对自组装结构的影响,发现随着聚合度的增加,表面活性剂自组装形貌由球形转变为蠕虫状结构;Sangwai等[18-19]研究水杨酸钠(NaSal)对CTAC胶束形貌转变的影响,发现水杨酸钠诱导球形胶束转变为棒状胶束的两种方式,一是水杨酸根插入到胶束内部改变胶束形貌,二是水杨酸根的插入改变胶束表面的Zeta电位,促使胶束融合,促进蠕虫状胶束的形成。笔者采用粗粒度分子动力学模拟的方法,以有机盐水杨酸钠(NaSal)和2-羟基萘-3-羧酸酯(2SHNC)两种有机盐为研究对象,研究两种有机盐类型对阳离子表面活性剂3-烷氧基-2-羟丙基三甲基卤化铵(RnHTAB,n=14)体系自组装行为以及对组装体中蠕虫状胶束黏弹性能的影响。
1 模型及模拟方法
采用Gromacs 4.5.5程序包[20],模拟表面活性剂体系为200 Å×200 Å×200 Å盒子,设置盒子具有三维周期性边界条件,采用NPT系综,温度设定为300 K,压强为0.1 MPa,模拟的时间步长为20 fs,系统的控温方法采用Berendsen[21],控压方法采用Berendsen。非键相互作用截断半径设定为12 Å,采用Gromacs标准移位函数分段处理的方法,对在标准移位半径0.9 nm到截断半径1.2 nm之间的范德华相互作用加入移位函数,静电相互作用在0~1.2 nm之间。所有的构型均模拟了1 μs来获得其平衡稳定结构。构型的可视化采用VMD(Visual Molecular Dynamics)软件[22]实现。
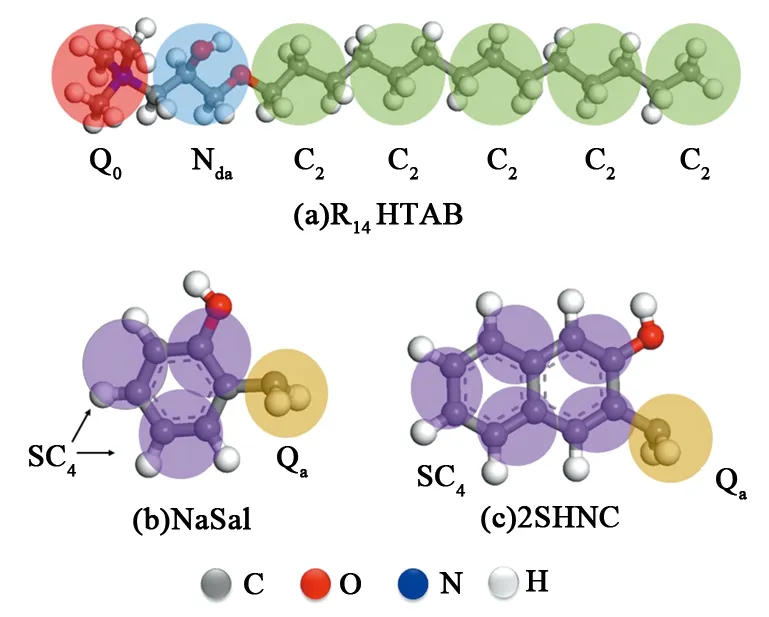
图1 全原子结构粗粒化示意图Fig.1 Full-atomic coarsegraining models
模拟中采用Martini[23]力场,根据分子结构和力场珠子的划分规则,图1给出了R14HTAB、NaSal、2SHNC的粗粒化示意图。其中R14HTAB的疏水尾链由5个C2珠子组成,C2珠子包含了3个疏水C原子及与其成键的氢原子,亲水头基为Q0和Nda两个珠子,其中Q0带正电;NaSal由3个SC4珠子和一个带负电的Qa珠子构成[24];2SHNC由5个SC4珠子和一个带负电的Qa珠子构成。粗粒化的水珠子由4个水分子组成,体系中包含两种类型的水珠子,一种正常的水珠子W,另外一种是水珠子BW,采用两种水珠子的目的是为了打破溶液粒子统一大小的晶格参数,防止水形成有序晶体结构,BW珠子占全部水珠子的10%。
为考察有机盐浓度对表面活性剂R14HTAB自组装的影响,模拟中固定盒子中R14HTAB的个数为900(浓度为180 mmol/L),调控NaSal与2SHNC的浓度分别为0、36、72、108、144、180 mmol/L,与表面活性剂R14HTAB对应的物质的量比Rc(有机盐∶表面活性剂)分别为:0、0.2、0.4、0.6、0.8、1.0。
2 结果分析
2.1 不同复配下胶束的自组装过程
图2给出了两种有机盐浓度逐渐增加时表面活性剂的自组装平衡构型。对于NaSal,随着浓度的增加,其胶束形貌经历了从球形到蠕虫再到枝状的转变。当Rc从0增加至0.4时,球形胶束个数逐步减少,胶束尺寸逐渐增大,说明NaSal能够加速胶束的融合;当Rc=0.6时,球形胶束融合形成短棒状的蠕虫状胶束;当Rc=0.8时,蠕虫状胶束继续生长变长,胶束个数继续减少;当Rc=1.0时,蠕虫状胶束融合形成树枝状胶束。

图2 体系平衡构型Fig.2 Equilibrium configuration of system
对于2SHNC,随着浓度的增加,其胶束形貌经历了从球形到蠕虫再到囊泡的转变。当Rc从0增加到0.2时,球形胶束个数逐渐减少,胶束尺寸逐渐增大,说明2SHNC同样可以加速球形胶束的融合;当Rc=0.4时,球形胶束融合形成短棒状蠕虫胶束;当Rc=0.6时,蠕虫状胶束继续生长变长,胶束个数继续减少;当Rc=0.8和1.0 时,胶束卷曲形成圆盘状胶束后继续卷曲形成囊泡。
对比两种有机盐的影响,复配体系形成蠕虫状胶束时所需要的有机盐2SHNC数量更低,且随着2SHNC个数的增加其胶束形貌转变更快。如2SHNC在Rc=0.2 时已经促使球形胶束转变为棒状的蠕虫状胶束,而NaSal则在Rc=0.4时才有这样的转化;另外,2SHNC添加到Rc=0.8后会获得囊泡胶束,但NaSal在相同浓度时不能得到。上述对比说明了2SHNC具有更强的促进胶束融合的能力。
2.2 不同形貌胶束的自组装过程
表面活性剂在水溶液中形成不同形貌的胶束,其动态形成过程有助于了解胶束的生长动力学。在不同的有机盐添加浓度下,可以获得球形、蠕虫和囊泡3种胶束结构,通过提取3种蠕虫形貌形成过程中不同时刻的构型揭示其生长行为。
2.2.1 球形胶束形成过程
图3给出了球形胶束形成过程中最大胶束聚集数(Nm)的变化,可用于表征胶束融合过程中包含表面活性剂数目的变化。从图中可以看出:起初,随机分布在水溶液中的表面活性剂快速聚集形成许多小的球形胶束(时间小于50 ns),对应的Nm较小;随后,临近的球形胶束融合形成较大的球形胶束(时间小于100 ns),Nm逐渐增大;当融合完成后,获得几个体积较大的稳定球形胶束(时间大于100 ns),对应的Nm不再变化,Nm对应数值为200。
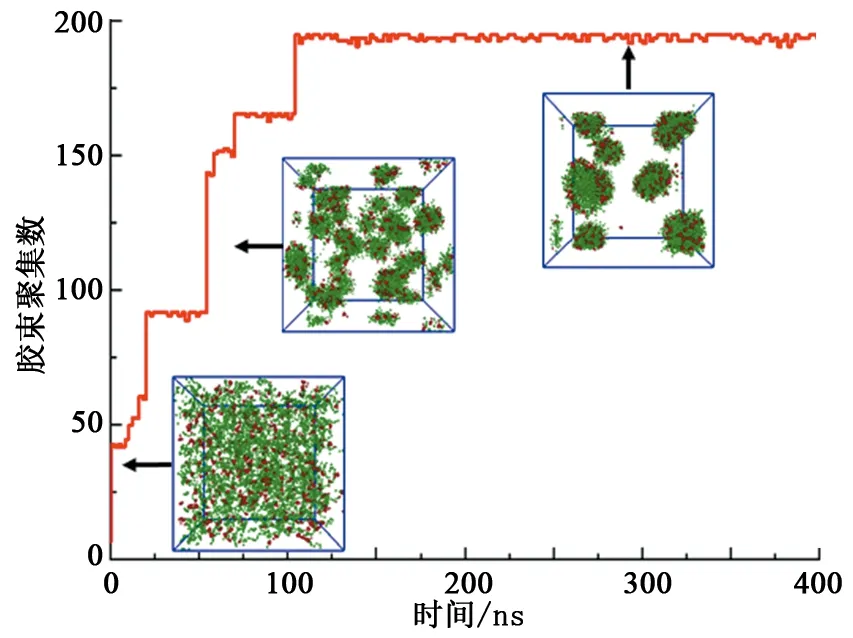
图3 球形胶束形成过程中Nm变化及对应的典型构型Fig.3 Evolution of Nm and corresponding typical configuration during formation of spherical micelles
2.2.2 蠕虫状胶束形成过程
图4给出了蠕虫的形成过程中Nm的变化曲线。在初始阶段,随机分布的表面活性剂形成大量小的球形胶束(时间小于50 ns),对应的Nm较小;然后,这些球形胶束继续融合,Nm曲线中多个台阶表明发生了多次融合(耗时较长,时间小于250 ns);球形胶束融合后最终形成了稳定的蠕虫状胶束(时间大于250 ns),Nm对应数值为300,大于形成稳定球形胶束的数值(200)。

图4 蠕虫状胶束形成过程中Nm变化及对应的典型构型Fig.4 Evolution of Nm and corresponding typical configuration during formation of worm-like micelles
2.2.3 囊泡形成过程
图5给出了囊泡形成过程中Nm的变化。同上述球形和蠕虫胶束类似,起初随机分布的表面活性剂形成了大量小的球形胶束;随后这些球形胶束会融合形成几条蠕虫状胶束;随后这些蠕虫状胶束融合转化为一个巨大的层状结构,然后这层状结构弯曲并闭合形成囊泡。与前面两种结构相比,囊泡的形成经历了蠕虫到层状结构转变然后弯曲闭合的复杂过程,该结构的形成需要更强的融合能力,对应在高浓度的有机盐2SHNC环境下形成。

图5 囊泡形成过程中Nm变化及对应的典型构型Fig.5 Evolution of Nm and corresponding typical configuration during formation of vesicle micelles
2.3 胶束融合能力及蠕虫胶束力学性质
2.3.1 NaSal和2SHNC体系的胶束融合能力
为了阐明NaSal、2SHNC促进胶束融合的能力,选取蠕虫状胶束作为对比。采用伞形抽样的方法分别计算两类有机盐体系中蠕虫状胶束在形成过程中的融合自由能(图2)。对于NaSal,盐离子与表面活性剂摩尔浓度比Rc为0.6和0.8时形成了蠕虫;对于2SHNC,Rc为0.4和0.6时形成了蠕虫。分别计算Rc为0.4、0.6、0.8时胶束的融合自由能,结果见图6,其中融合自由能为负值表明胶束有自发融合趋势,绝对值越大表明融合能力越强。从图6看出,NaSal在Rc=0.6时胶束的融合能力最大,2SHNC在Rc=0.4时胶束的融合能力最大。另外,2SHNC在胶束间距小于65 Å时融合自由能开始小于0,开始发生融合;NaSal需要胶束间距小于55 Å时融合自由能开始小于0,融合才可以发生。相比NaSal,2SHNC在更低的浓度更远的距离就可以促进胶束的融合。因此2SHNC具有更强的促进胶束融合的能力。进一步分析两种有机盐融合能力不同的原因,可能是2SHNC具有两个苯环,而NaSal只有一个苯环,导致2SHNC与表面活性剂R14HTAB的疏水尾链具有更强作用,能够更有效地促进了胶束的融合,这一模拟结果与已有的实验研究结果是一致的[25]。
2.3.2 黏弹性能差异
蠕虫状胶束的长度和稳定性是其黏弹性能的重要评价指标之一。溶液中的蠕虫状胶束处于动态平衡,经历着断裂—融合的可逆过程。通过蠕虫状胶束断裂过程中的分离能间接评价可以形成蠕虫状胶束的长度及其稳定性。断裂需要的分离能越大意味着融合后的胶束不容易断裂,可以形成长度大且稳定的蠕虫状胶束,对应的黏弹性能较好。通过计算蠕虫状胶束单轴拉伸过程中受力的变化曲线(图7)评价胶束断裂的分离能。采用的是NaSal和2SHNC在Rc=0.6获得的蠕虫状胶束。拉伸过程中受力的积分定义为单个蠕虫状胶束的分离能[25]。图7表明:一方面,相比于NaSal,2SHNC的蠕虫状胶束可以拉伸的长度更大而保持不断裂;另一方面,2SHNC的蠕虫状胶束在拉断过程中需要施加的力显著高于NaSal的蠕虫状胶束。在图7中通过对两条拉力曲线积分可以得到蠕虫状胶束的分离能,2SHNC的分离能要远大于NaSal的分离能,说明2SHNC促进更长、黏弹性更好的蠕虫状胶束形成。

图6 蠕虫状胶束形成过程中融合自由能的变化Fig.6 Variation of fusion free energy in formation of worm-like micelles
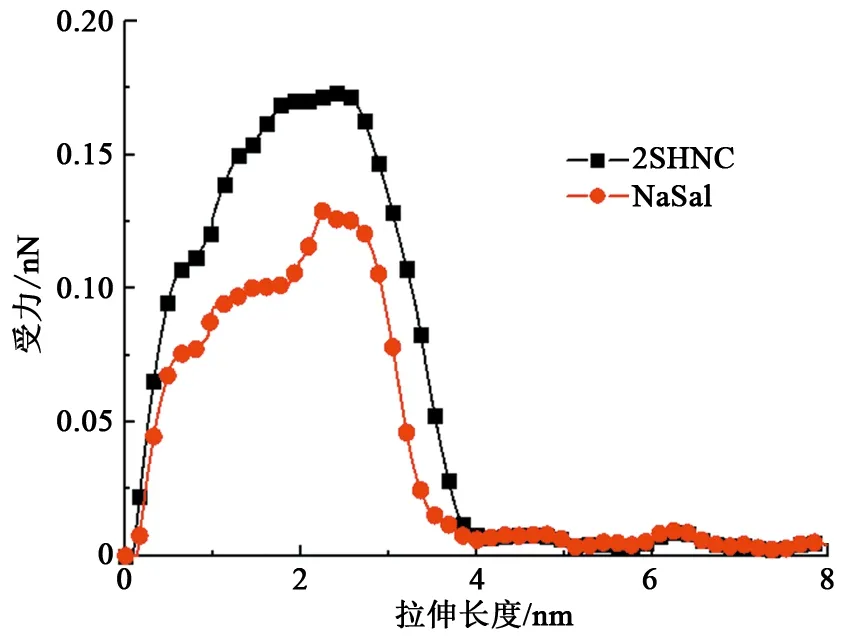
图7 蠕虫状胶束在非轴向拉伸过程中受力的变化Fig.7 Variations of force in stretching of worm-like micelle
3 结 论
(1)NaSal/R14HTAB和2SHNC/R14HTAB两种混合体系随着浓度的增加可以获得球形、蠕虫、囊泡3种胶束形貌,与实验观察结果一致。球形胶束融合形成棒状胶束,棒状胶束转变形成层状胶束并卷曲闭合是蠕虫状胶束和囊泡形成的关键环节。
(2)相比NaSal,2SHNC具有更强的促进胶束融合的能力,在更低的浓度下就可以诱导蠕虫状胶束的形成,而且可以获得形貌更加复杂的囊泡胶束。
(3)2SHNC可以促进更长且稳定的蠕虫状胶束形成,具有更优异的黏弹性能。
