基于UPLC- Q- TOF- MS对野马追内酯F在大鼠体内代谢产物的分析
2020-01-09秦伟瀚王云红宋小仙
秦伟瀚,刘 翔,王云红,宋小仙,阳 勇,李 卿
重庆市中药研究院,重庆 400065
野马追为菊科植物轮叶泽兰(EupatoriumlindleyanumDC.)的干燥地上部分[1]。又名白鼓钉、化食草等。除新疆以外广泛分布于全国各地,其中江苏省盱眙县为该药材的道地产区[2,3]。早在1988年江苏省地方药材标准就已有收载,现收录于2015年版《中华人民共和国药典》[4]。本品味苦、性平,归肺经,具有化痰、止咳、平喘之功效,常用于治疗痰多、咳嗽、气喘等病症[5,6]。随着对野马追药材研究的不断深入,新近药理报道还指出其具有降血脂、抗动脉粥样硬化等作用[7- 13]。课题组前期通过对野马追提取物研究发现,其降血脂效果与辛伐他汀相当,部分药理检测指标还优于辛伐他汀,但起效物质和起效过程尚不明确,阻碍了其进一步开发和应用。
随着高分辨质谱在中药化学领域的快速普及和发展,多重质量亏损过滤(MMDF)技术在海量数据挖掘过程中优势逐渐显现,对于目标化合物筛查、药物代谢及天然产物鉴定等方面具有越来越大的应用空间。借助超高效液相色谱- 飞行时间质谱联用(UPLC- Q- TOF- MS)技术,分析中药复杂成分和中药代谢[14],能够省略分离纯化过程的同时鉴定痕量的药物及其代谢产物;同时,在药物代谢物筛选与表征过程中,具有去除背景离子干扰,排除假阳性,提高分析效率等诸多明显优势。倍半萜内酯是野马追的主要特征性成分,野马追内酯F(eupalinolide F)在倍半萜成分中含量较高,故本研究以探究大鼠血浆中野马追内酯F的代谢产物为目标,采用高分辨质谱,基于多重质量亏损和动态背景扣除技术,系统分析了野马追内酯F在大鼠体内的生物转化过程,为明确野马追药材的药效物质基础及深入开发利用提供科学依据。
1 材料与方法
1.1 仪器及试药
1.1.1 仪器
LC- 30A型超高效液相色谱仪(日本,岛津公司):二元高压泵、自动进样器、柱温箱;Triple TOFTM4600型四极杆串联飞行时间高分辨质谱仪(美国,AB公司):Analyst 1.6工作站、PeakView 1.2.0.3数据处理软件、MetabolitePilot 1.5.0.8532代谢产物鉴定软件;DW- 86L486型超低温冰箱(中国,中科美菱公司);Microfuge 20R型超高速离心机(美国,贝克曼库尔特公司)。
1.1.2 实验动物
SD大鼠,SPF级,10只,雄性,体重200±20 g,由重庆市中药研究院实验动物研究所提供,实验动物生产许可证号SCXK(渝)2012- 0006,动物合格证号0003054。动物饲养于重庆市中药研究院药化所,动物实验环境(温度20~25 °C,湿度50%~65%),自由摄食和饮水;并按实验动物使用的“3R”原则给以人道主义关怀。
1.1.3 药材与试剂
野马追内酯F对照品为自制,经高效液相色谱(HPLC)归一化法测定,纯度>95%。乙腈、甲醇、水(色谱纯级,德国Merck公司);甲酸(色谱纯级,美国ACS公司);乙醇(分析纯,重庆川东化工公司)。
1.2 野马追内酯F灌胃给药
取SPF级SD大鼠10只,饲养3天后禁食12 h,自由饮水。按照10 mg/kg体重剂量灌胃,分别于给药后30、60、90、120、180、240 min眼眶静脉丛取血0.5 mL于装有肝素钠的EP管中,于10 625×g离心10 min取上层血浆,- 80 °C冰箱保存,备用。
1.3 样品采集与处理
按照采血时间点,精密吸取10只大鼠血浆样品各50 μL于1.5 mL EP管中,加入色谱甲醇600 μL后涡旋混匀2 min,于10 625×g离心10 min,分别吸取上清液和空白对照液2 μL进样,进行UPLC- Q- TOF- MS分析。
1.4 实验条件
1.4.1 色谱条件
色谱柱:Phenomenex Luna- C18(2 mm×100 mm,3 μm);流动相:A为0.1%甲酸水溶液,B为乙腈;梯度程序:0~2.0 min,6%B;2.0~10.0 min,6%~80%B;10.0~12.0 min,80%B;12.0~12.1 min,80%~6%B;12.1~15.0 min,6%B;流速:0.2 mL/min,柱温:30 °C,进样量:2 μL。
1.4.2 质谱条件
电喷雾离子源(ESI),负离子模式采集数据,喷雾电压(IS):- 4 500 V;雾化气压力(GS1):50 Psi;气帘气压力(CUR):15 Psi;辅助气压力(GS2):45 Psi;离子源温度(TEMP):600 oC;簇裂解电压(DP):55 V;碰撞能量(CE):40 V;碰撞能量滚动区间(CES):15 V;检测模式为IDA(信息关联采集模式),多重质量亏损(MMDF)和动态背景扣除(DBS)为触发二级的条件,满足该条件优先进行二级扫描。
1.5 代谢产物分析鉴定
查阅野马追化学相关文献,采用ChemDraw软件建立野马追内酯F的mol格式文件,导入PeakView软件,结合Formula Finder、Mass Calculators等功能,对野马追内酯F标准品和血浆样品进行定性分析,并将上述结果代入MetabolitePilot软件,对该化合物产生的所有代谢产物进行分析鉴定。
2 结果与讨论
2.1 野马追内酯F质谱鉴定分析
采用UPLC- Q- TOF- MS对野马追内酯F标准品和血浆样品进行分析。如图1B、图2所示,野马追内酯F在ESI负离子模式中的母离子[M- H]-的质荷比为m/z419.173 4,经质谱电离裂解作用分别脱去116.051 7、176.072 3、220.063 4、264.089 1、304.133 3 Da生成质荷比为m/z303.121 7、243.101 1、199.110 0、155.083 4、115.040 1的碎片离子,利用PeakView软件的Mass Calculators功能计算出C5H8O3、C7H12O5、C12H12O4、C14H16O5、C17H20O的理论值分别为116.046 8、176.067 9、220.073 0、264.099 2、304.130 5 Da,与脱去碎片的实际值之差均小于0.01 Da。通过上述对二级碎片裂解规律的分析并结合化合物结构特点,判定该化合物应为野马追内酯F。
将野马追内酯F分子式(C22H28O8)代入PeakView软件的XIC Manager筛查表中对该化合物保留时间、强度等质谱参数进行提取处理;由图1A、1C可知,有效部位在5.872 min处有超过200 000 cps响应,而血浆样品在5.888 min处有接近10 000 cps响应,进一步对其MS/MS碎片进行比较分析(如图1B、1D),发现两者的裂解碎片质荷比基本一致,据此判断血浆样品中含有野马追内脂F。由初步的量时曲线(图3)可以看出,采血时间为灌胃后30 min时,血浆样品中野马追内酯F离子强度为8 773 cps;

图1 野马追内酯F的提取离子图和二级质谱图Fig.1 Extraction ionogram and secondary mass spectrogram of eupalinolide F注:A.对照品提取离子图;B.对照品二级质谱图;C.血浆样品提取离子图;D.血浆样品二级质谱图。Note:A.XIC of effective fraction;B.MS/MS of effective fraction;C.XIC of plasma;D.MS/MS of plasma.
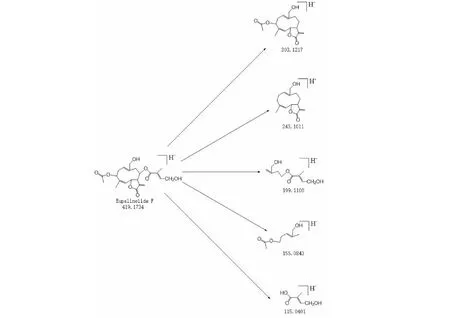
图2 野马追内酯F裂解规律图Fig.2 Pyrolysis chart of eupalinolide F
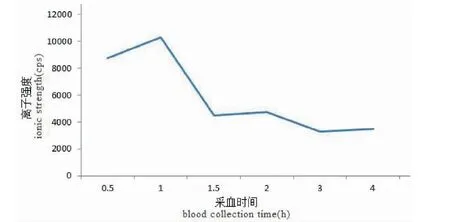
图3 野马追内酯F量时曲线图Fig.3 Mass spectrometric response intensity and time curve of eupalinolide F
当采血时间为60 min时,野马追内酯F的血药浓度达到最大值;之后直到240 min,血浆样品中野马追内酯F离子强度逐渐降低。由上述数据分析结果可知,入血后野马追内酯F的离子强度可以达到标准品的1/20,可能与该药物吸收代谢特性以及血浆样品的基质效应等因素相关。
2.2 野马追内酯F在大鼠体内代谢转化分析
采用ChemDraw软件建立野马追内酯F的mol格式文件,导入MetabolitePilot软件中,获取该化合物理论裂解参数,再将标准品的Q- TOF数据作为血浆样品的参比对照导入该软件,以2.2项下的保留时间、二级碎片等分析结果对野马追内酯F实际质谱信息进行筛选匹配,建立该化合物的质谱数据库;MetabolitePilot软件会自动对以野马追内酯F为母核的所有代谢产物进行分析处理,再结合相应代谢产物的二级碎片裂解规律进行补充鉴定,代谢产物鉴定结果见表1、图4。
通过大鼠体内生物转化分析研究,以野马追内酯F为原型共鉴定出了55个代谢产物,其中I相代谢包括氢化、氧化、酯键水解、成酮、脱氧、甲基化、去甲基等12种反应类型;II相代谢包括葡萄糖苷结合、葡萄糖醛酸结合、乙酰化、磷酸酯化、硫酸酯化、谷胱甘肽结合、半胱氨酸结合、谷氨酰胺结合、硫磺酸结合等10种反应类型;发生两次以上代谢过程均包含水解反应,与化合物原型含有两个酯键和一个内酯的结构特征相符;I相代谢中氧化反应较多,可以是单纯加氧或成酮,而还原反应以不饱和双键加氢为主;单独的II相反应只有谷胱甘肽结合(M9)、葡萄糖醛酸结合(M10)和乙酰化(M12),其余17个发生了结合反应的II相代谢产物均伴随了I相水解反应。由此可见I相反应过程通过氧化、还原、水解在野马追内酯F分子结构中引入或脱去功能基团从而发挥药效活性或失去活性;II相反应则通过与内源性物质经共价键结合,生成极性大、水溶性高的结合物,经尿液排泄。

表1 野马追内酯F代谢产物鉴定结果
续表2(Continued Tab.2)
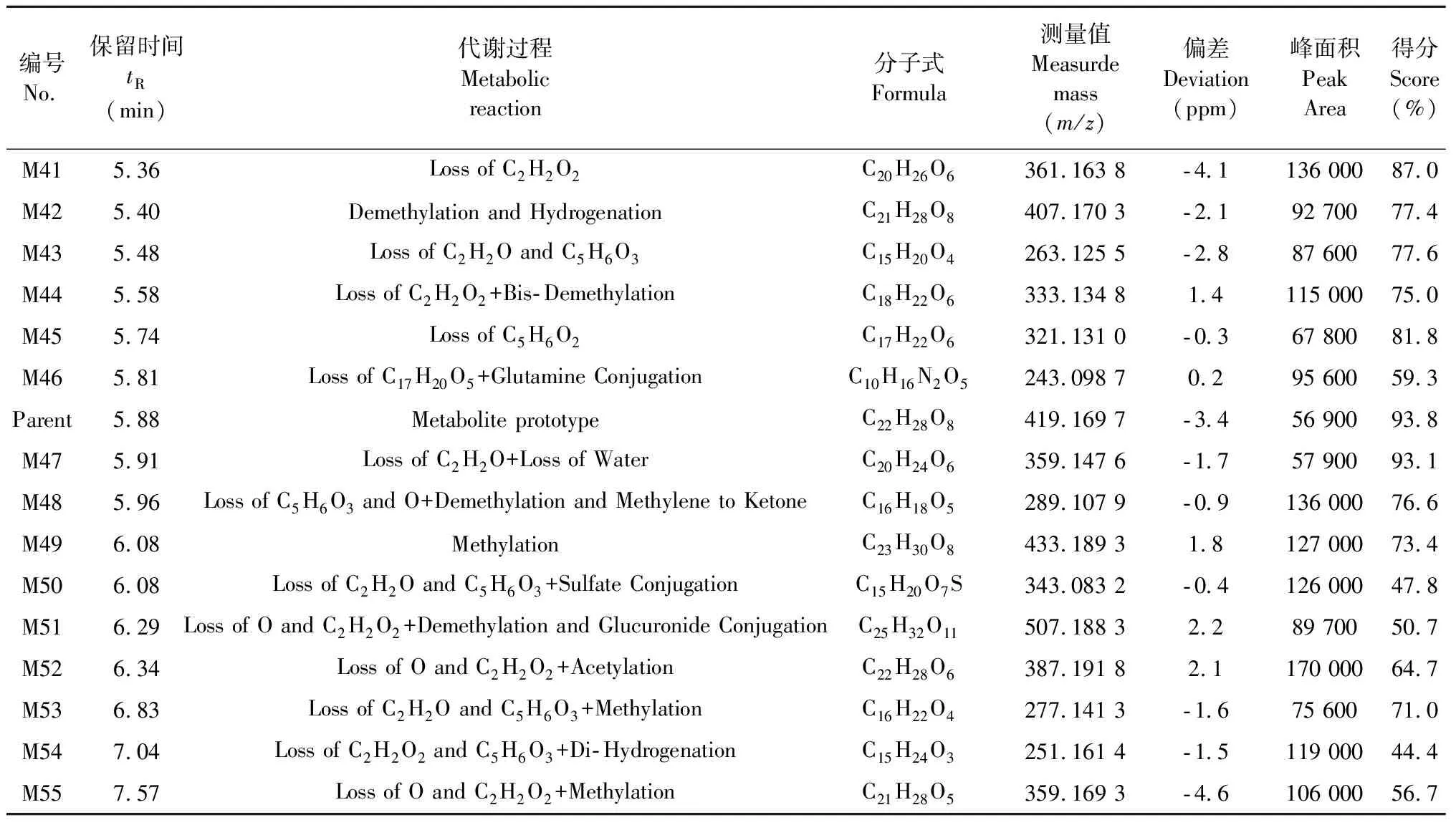
编号No.保留时间tR(min)代谢过程Metabolic reaction分子式Formula测量值Measurde mass (m/z)偏差Deviation(ppm)峰面积Peak Area得分Score(%)M415.36Loss of C2H2O2C20H26O6361.163 8-4.1136 00087.0M425.40Demethylation and HydrogenationC21H28O8407.170 3-2.192 70077.4M435.48Loss of C2H2O and C5H6O3C15H20O4263.125 5-2.887 60077.6M445.58Loss of C2H2O2+Bis-DemethylationC18H22O6333.134 81.4115 00075.0M455.74Loss of C5H6O2C17H22O6321.131 0-0.367 80081.8M465.81Loss of C17H20O5+Glutamine ConjugationC10H16N2O5243.098 70.295 60059.3Parent5.88Metabolite prototype C22H28O8419.169 7-3.456 90093.8M475.91Loss of C2H2O+Loss of WaterC20H24O6359.147 6-1.757 90093.1M485.96Loss of C5H6O3 and O+Demethylation and Methylene to KetoneC16H18O5289.107 9-0.9136 00076.6M496.08MethylationC23H30O8433.189 31.8127 00073.4M506.08Loss of C2H2O and C5H6O3+Sulfate ConjugationC15H20O7S343.083 2-0.4126 00047.8M516.29Loss of O and C2H2O2+Demethylation and Glucuronide ConjugationC25H32O11507.188 32.289 70050.7M526.34Loss of O and C2H2O2+AcetylationC22H28O6387.191 82.1170 00064.7M536.83Loss of C2H2O and C5H6O3+MethylationC16H22O4277.141 3-1.675 60071.0M547.04Loss of C2H2O2 and C5H6O3+Di-HydrogenationC15H24O3251.161 4-1.5119 00044.4M557.57Loss of O and C2H2O2+MethylationC21H28O5359.169 3-4.6106 00056.7

图4 野马追内酯F代谢过程图Fig.4 Metabolic process diagram of eupalinolide F
3 结论
本研究进行了野马追内酯F的大鼠体内生物转化分析,共鉴定出了55个代谢产物,其中I相水解反应是主要代谢过程;在血浆中检出的野马追内酯F离子强度可以达到灌胃标准品的1/20,表明该化合物的吸收程度较高,但该化合物起效过程和起效机制尚不明确,课题组拟后续通过血浆蛋白结合率、药代动力学、P450酶体外代谢等实验进行深入探讨。野马追的主要化学成分包括黄酮、萜、生物碱、甾醇等类成分[15,16],其中野马追内酯F是属于吉马烷型倍半萜类的一种,是野马追主要特征有效成分,据笔者统计,野马追萜类成分包括二萜、倍半萜和三萜,该类化合物共计38种之多[17],而市面上销售的纯品仅野马追内酯A、野马追内酯B和野马追内酯H,想要对该类化合物的体内代谢产物进行逐一分析鉴定,存在着较大困难,本研究基于前期对野马追内酯F进行的分离、纯化工作,在利用高分辨质谱对野马追内酯F化学结构进行定性解析基础上,采用MetabolitePilot软件对野马追内酯F的所有代谢产物进行快速分析鉴定,为明确野马追的体内起效物质基础提供了新思路,也为野马追的新药开发及临床应用等提供科学参考。
