黄芪- 苍术改善糖尿病肾病糖脂代谢的网络药理学研究
2020-01-09吴巧敏黄超颖王箴仪周逸钧张美芳陈洁文
王 鑫,吴巧敏,黄超颖,王箴仪,施 敏,周逸钧,张美芳,陈洁文
上海交通大学医学院附属第九人民医院临床营养科,上海201900
流行病学调查显示,2013年中国18岁以上成年人的糖尿病患病率为10.4%,患病人数位居全球首位[1]。糖尿病肾病(diabetic kidney disease,DKD)是糖尿病最主要的微血管并发症之一,也是导致终末期肾病的主要原因之一[2],近年来我国DKD的患病率也呈增长趋势。DKD早期发病隐匿,难以及时发现,发展至临床后期通常难以逆转,最终需接受透析或肾移植治疗,严重影响患者生活质量,因此对DKD进行早期干预治疗具有重要意义[3]。但DKD的发病机制目前尚不完全清楚,研究认为其可能与高血糖引起的氧化应激、糖脂代谢紊乱、细胞因子表达异常、肾组织炎症反应增加、肾脏血流动力学变化等有关[4,5]。DKD临床诊断为:糖尿病引起的慢性肾脏病,主要包括肾小球滤过率(GFR)低于60 mL/min/1.73 m2或尿白蛋白/肌酐比值(ACR)高于30 mg/g持续超过3个月[6]。西医治疗DKD主要关注控制血糖、血压、血脂、改善尿蛋白等方面,但这并不能完全阻断DKD的发生发展。
中医认为DKD属于“消渴”、“水肿”、“虚劳”等范畴,临床证型为脾肾两虚、湿瘀互阻型[7]。近年来,中医药在防治DKD发生发展、延缓肾功能等方面显示出较大的优势。中药具有抗氧化、调节免疫、降脂降糖等多种药理学特性。黄芪及其成分改善肾脏疾病的机制可能是通过抗过氧化作用、调节内皮素、改善血小板功能、调节糖代谢。研究表明,黄芪通过下调肾组织脂联素表达降低糖尿病肾病大鼠血糖和减少尿蛋白[8]。黄芪甲苷可能通过抑制内质网应激及影响TGF-β/SMADS信号通路发挥改善糖尿病肾病作用[9]。苍术具有抑制糖原生成、抗缺氧、抗炎、调节糖脂代谢等作用[10]。研究表明,苍术多糖对STZ诱导大鼠的血糖、血脂具有调节作用,主要通过抑制糖类消化酶活性,降低肠道糖类吸收[11]。研究发现,芪术颗粒(主要成分为黄芪、苍术)可通过回调DKD糖代谢、脂代谢及氨基酸代谢等过程中的代谢中间产物显著改善DKD糖脂代谢紊乱、尿蛋白水平,保护肾脏功能,延缓病情进展[12,13]。鉴于中药具有多成分、多靶点等特点,目前黄芪- 苍术改善DKD糖脂代谢的分子作用机制尚未完全阐明。
网络药理学(network pharmacology)是由英国药理学家Hopkins在2007年提出,基于系统生物学理论,运用各种组学、高通量筛选、网络分析等技术揭示“药物- 靶点- 疾病”间的复杂网络关系,打破既往单成分- 单靶点- 单疾病的研究模式,对预测中药多成分、多靶点、多途径的作用机制具有重要意义[14]。因此,本研究从网络药理学出发,对黄芪- 苍术改善糖尿病肾病糖脂代谢的有效成分、作用靶点及信号通路进行探索,根据GO和KEGG信号通路富集分析其潜在作用机制,为进一步实验及临床研究提供理论依据。
1 方法
1.1 黄芪- 苍术活性成分筛选
以黄芪、苍术作为研究对象,依托中药系统药理学数据库及分析平台(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)分别筛选出与黄芪、苍术相关的所有化学成分,排除其中相同的化学成分[15]。口服生物利用度(oral bioavailability,OB)是药物吸收、分布、代谢、排泄中最重要的药动学参数之一,表示口服药物的有效活性成分被吸收后到达体循环的速度和程度。OB值表示活性成分的类药性(drug- likeness,DL),值越高表明类药性越好。参考文献报道,根据药代动力学参数确定以OB≥30%,DL≥0.18作为化合物有效活性成分的筛选条件[16]。
1.2 黄芪- 苍术活性成分靶点预测及构建“活性成分- 靶点”网络图
根据TCMSP平台筛选出的化学成分,以及候选化学成分的蛋白质潜在靶点。用Uniprot数据库(http://www.uniprot.org/)中的Uniprot KB搜索功能,输入靶点名称并设定物种为人,将检索到的所有蛋白靶点得到相应的基因名称(official symbol)[17]。再采用网络图像化软件Cytoscape 3.6.1(http://www.cytoscape.org/)构建“活性成分- 靶点”网络图。网络中节点(node)表示活性成分和基因靶点。若某一活性成分作用于该靶点,则以边(edge)相连。
1.3 糖尿病肾病相关靶点检索
本研究通过将“diabetic nephropathy”、“nephropathy,diabetic”、“diabetic kidney disease”作为检索词在人类基因组数据库GeneCards(http://www.genecards.org/)、TTD(http://bidd.nus.edu.sg/group/cjttd/)、DrugBank(https://www.drugbank.ca/)、OMIM(http://www.omim.org/)等公认的疾病靶点数据库进行检索,获得目前已报道的与DKD相关的靶点。将药物活性成分对应的靶点与疾病相关靶点取交集。
1.4 蛋白质- 蛋白质相互作用网络图及药物活性成分- 靶点- 疾病网络图构建
运用STRING(https://string- db.org/)和Metascape(http://metascape.org/)数据库,导入上述取交集的靶点,设定物种为人,进行蛋白相互作用分析,构建蛋白质- 蛋白质相互作用关系(protein- protein interaction,PPI)网络图。
1.5 Pathway富集分析
通过DAVID(https://david.ncifcrf.gov/)富集分析上述获得的关键靶点,人种设定为人,富集分析GO(gene ontology)生物学过程(生物过程、分子功能、细胞组成)和KEGG(KEGG pathway analysis)信号通路,总结研究黄芪- 苍术改善糖尿病肾病糖脂代谢相关信号通路。
2 结果
2.1 筛选黄芪- 苍术的有效活性成分
截至2019年4月,通过查找中药化学成分数据库及相关文献,共收集到黄芪的化学成分87种,苍术的化学成分49种,汇总去掉重复化学成分,共有136种,其中同时满足OB≥30%和DL≥0.18的化学成分共有29个(见表1)。
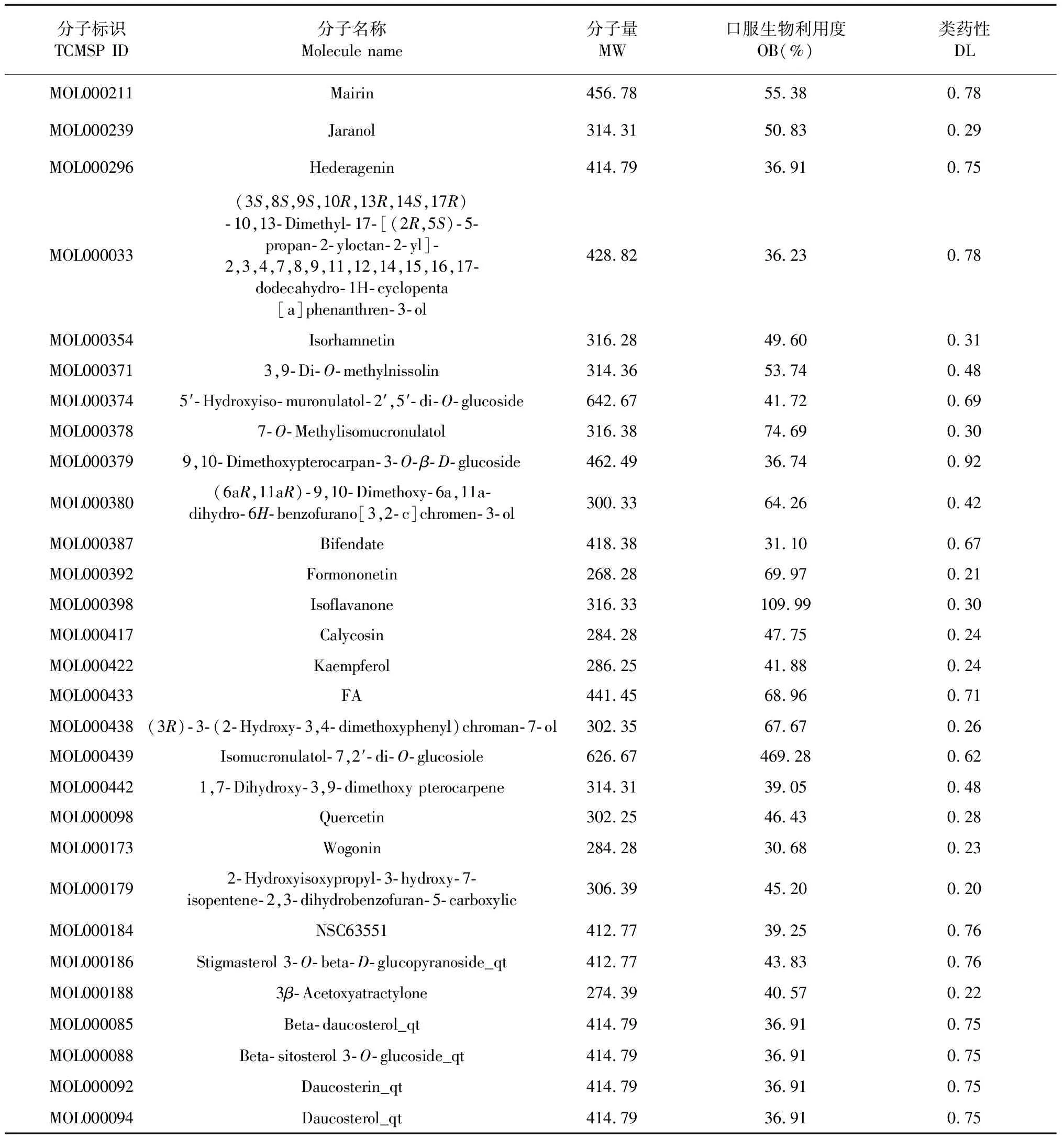
表1 黄芪和苍术的有效活性成分
2.2 黄芪- 苍术作用靶点预测及“活性成分- 靶点”网络构建分析
在TCMSP数据库中筛选出黄芪活性成分的潜在靶点446个,删除重复靶点后剩余213个;筛选出苍术活性成分的潜在靶点66个,删除重复靶点后剩余57个。两者汇总删除重复后剩余218个靶点。利用Cytoscape软件构建活性成分- 靶点网络(如图1),该网络中有506条边,代表活性成分和靶点的相互作用关系,有9个化合物无对应靶点。其中,槲皮素(quercetin)有最多的潜在靶点共154个,其次为山奈酚(kaempferol)有63个潜在靶点。其它如汉黄芩素(wogonin)、异鼠李素(isorhamnetin)、常春藤皂甙元(hederagenin)、芒柄花素(formononetin)对应靶点也较多,分别为22、37、24、15个。

图1 黄芪和苍术有效活性成分- 靶点图Fig.1 Active component- target network between S.membranaceus and A.lancea注:圆圈:靶基因;菱形:化合物。Note:Circle:target gene;Diamond:compound.
2.3 DKD相关潜在靶点预测
通过检索TCMSP、Drugbank、TTD、OMIM、GeneCards等数据库,共获得目前与DKD发生发展密切相关的靶点基因1 412个,将其与活性成分对应靶点取交集,共得到97个靶点。表明这97个靶点可能是黄芪- 苍术治疗DKD的关键靶点。
2.4 黄芪和苍术活性成分对应潜在靶点网络图
根据STRING和Metascape分析得出,黄芪和苍术活性成分对应潜在靶点之间的PPI网络图主要为丝裂原活化蛋白激酶(MAPK)、转化生长因子(TGFB1)、表皮生长因子(EGFR)、胰岛素样生长因子结合蛋白(IGFBP3)等相互作用(如图2和图3)。

图2 黄芪和苍术活性成分对应靶点的PPI网络图(STRING数据库)Fig.2 PPI network of target proteins in S.membranaceus and A.lancea from STRING database
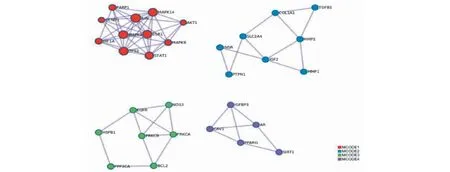
图3 黄芪和苍术活性成分对应靶点的PPI网络图(Metascape数据库)Fig.3 PPI network of target proteins in S.membranaceus and A.lancea from Metascape database
2.5 黄芪- 苍术改善DKD糖脂代谢信号通路富集分析
运用DAVID数据库,对上述黄芪和苍术活性成分对应的97个基因靶点进行分析,GO功能分析得到1 220个条目,其中1 069个具有统计学意义(P<0.05),其中生物过程(BP)条目944个,主要涉及细胞增殖的调节、凋亡、程序性细胞死亡、对内源性刺激的反应、分子功能的正向调节、对类固醇激素刺激的反应等生物学过程;分子功能(CC)条目60个,主要涉及细胞外空间、胞质、膜筏等;细胞组成(MF)65个,主要涉及蛋白质结合、蛋白质二聚化活性、类固醇激素受体活性、细胞因子活性、配体依赖性核受体活性、蛋白激酶调节活性等方面,见图4。
KEGG富集分析筛选到58条通路,其中55条具有显著意义(P<0.05),其中有关糖脂代谢通路有11条,主要涉及mTOR信号通路、胰岛素信号通路、脂肪细胞因子信号通路、Jak- STAT信号通路、糖尿病信号通路等(见图5)。
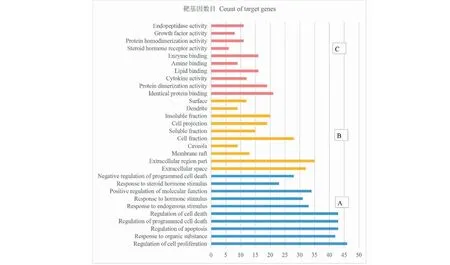
图4 黄芪- 苍术治疗DKD潜在靶点的生物学功能分析Fig.4 GO enrichment analysis of potential target of S.membranaceus and A.lancea for the treatment of diabetic kidney disease注:A:生物过程;B:细胞组分;C:分子功能。Note:A:biological process;B:cellular component;C:molecular function.
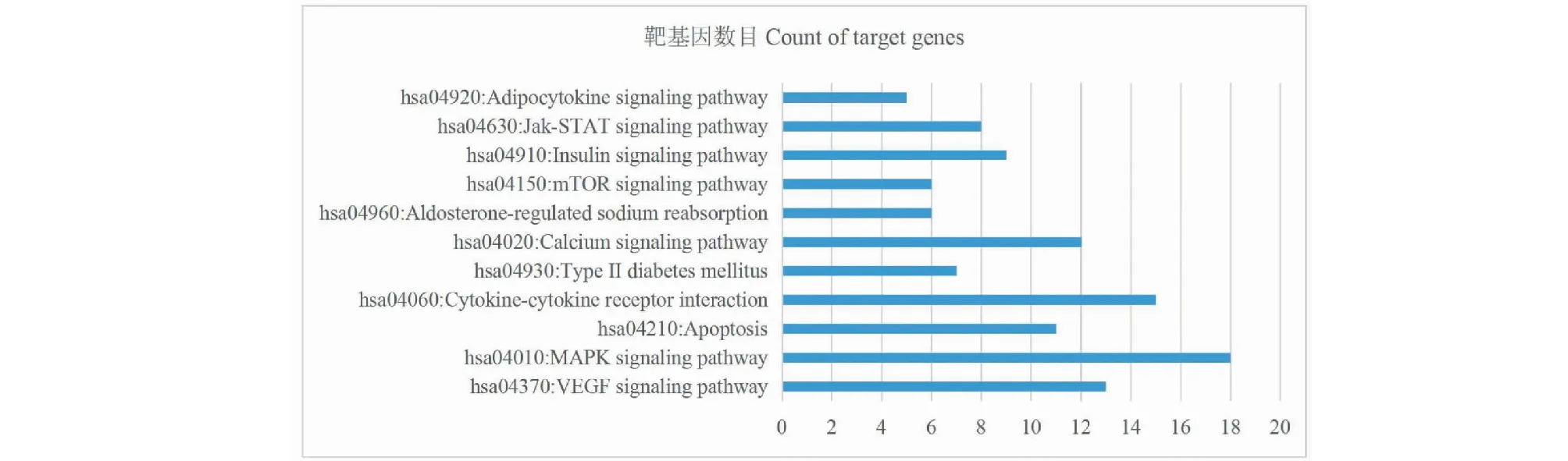
图5 黄芪- 苍术改善DKD糖脂代谢相关信号通路的KEGG分析Fig.5 KEGG analysis of potential target of S.membranaceus and A.lanceafor the treatment of glucose and lipid metabolism in diabetic kidney disease
3 讨论
本次研究的目的是,通过网络药理学方法分析黄芪- 苍术改善糖尿病肾病糖脂代谢的有效活性成分、作用靶点及相关信号通路,探讨其中可能的作用机制,结果发现黄芪- 苍术可能是通过mTOR信号通路、胰岛素信号通路、脂肪细胞因子信号通路、Jak- STAT信号通路、糖尿病信号通路等多条信号通路发挥改善DKD糖脂代谢的作用。研究结果显示,黄芪和苍术的有效活性成分为29个,预测出对应的潜在作用靶点218个。活性成分- 靶点网络分析结果显示,槲皮素和山奈酚的靶点最多,还有汉黄芩素、异鼠李素、常春藤皂甙元、芒柄花素等对应的靶点也较多,活性成分对应靶点主要有PIK3CG、AKT1、MAPK1、IGF2等。提示这几种成分很可能是黄芪- 苍术发挥作用的主要成分。以往研究表明,槲皮素和山奈酚都具有广泛的药理学作用,槲皮素有抗氧化、降血糖、降血脂、抑制肿瘤、抗炎等作用[18]。还有研究认为,槲皮素对DKD具有保护作用,可延缓糖尿病患者肾小球硬化的进程,通过降低TGFβ1/Smad表达抑制高糖引起的肾小球系膜细胞增殖[19]。山奈酚具有抗炎、抗凋亡、抗氧化等多种生物学活性[20]。一项研究显示,山奈酚通过调控p38- MAPK信号通路抑制高糖刺激下大鼠肾系膜细胞增值[21]。这充分表明药物与靶点的复杂网络关系,验证了黄芪- 苍术是以多成分、多靶点的方式发挥改善DKD的作用。
本研究GO富集分析结果显示,黄芪- 苍术中的有效活性成分广泛涉及细胞增殖的调节、凋亡、程序性细胞死亡、对内源性刺激的反应、分子功能的正向调节、对类固醇激素刺激的反应、蛋白质结合、蛋白质二聚化活性、类固醇激素受体活性、细胞因子活性、配体依赖性核受体活性、蛋白激酶调节活性等多种生物学过程。KEGG富集分析显示,黄芪- 苍术改善DKD糖脂代谢通路有11条,主要涉及mTOR信号通路、胰岛素信号通路、糖尿病信号通路、脂肪细胞因子信号通路、Jak- STAT信号通路、MAPK信号通路等。这一结果提示黄芪- 苍术具有多靶点- 多通路改善DKD糖脂代谢的重要作用。目前研究认为DKD发病机制主要涉及糖脂代谢改变、氧化应激、胰岛素抵抗、细胞凋亡、炎症等方面。研究发现,高糖环境下产生糖基化终产物激活PKC、NF- κB、MAPK、Jak- STAT等信号通路,促进细胞外基质合成及沉积[22,23]。这些证据表明mTOR信号通路、胰岛素信号通路、Jak- STAT信号通路等在DKD发生发展中发挥重要作用,与本研究的研究结果一致,同时也表明,疾病的调控机制存在复杂且相互交叉的关系。
综上所述,本研究应用网络药理学方法,从理论上初步分析了黄芪- 苍术改善DKD糖脂代谢的主要活性成分及可能机制,探讨了黄芪- 苍术对DKD相关信号通路的作用,为进一步实验及临床研究探讨黄芪- 苍术的确切机制提供线索。对黄芪- 苍术改善DKD糖脂代谢的复杂分子网络关系进行研究,体现中药多成分、多靶点、协同作用的特点,也为今后研究中药复方改善DKD的分子作用机制提供依据。
