蔗渣-纳米氧化银保鲜剂的制备
2020-01-07马瑞佳蔡晨晨雷财玉王友法陆登俊
马瑞佳,蔡晨晨,雷财玉,王友法,陆登俊*
(广莫大学轻工与食品工程学院,广莫 南宁 530004)
近年来,保鲜剂的研究已经成为热点之一。食品在生产和贮存过程中极易受到微生物的污染而发生变质现象,带来了极大的经济损失,所以延长食品的货架期显得尤为重要。蔗渣作为甘蔗制糖工业的一种副产品,仅将其用于锅炉燃料回回所产生的经济效益是极低的[1-2]。Mishra等[3]探索了各种木质纤维素原料使用不同的无机酸作为分离馏分回回最大数量的可发酵糖,提供了蔗渣利用的一条新途径。蔗渣主要成分是纤维素、半纤维素、木质素等,这些成分决定了蔗渣具有吸附功能。刘雪梅等[4]以甘蔗渣为原料,将其在真空环境下炭化制得甘蔗渣炭,研究了甘蔗渣炭对废水中Cr(VI)的吸附效果。Juchen等[5]将酿造过程的副产品麦芽甘蔗渣作为活性蓝色BF-5G染料的生物吸附剂。
纳米材料的研究在近几年来也取得了引人注目的成就,纳米材料由于其尺寸介于原子、分子和宏观体系之间[6],性能更加符合人们的要求。银基抗菌材料抗菌效果优于其他金属基材料,比如铜基、氧化锌、二氧化钛等[7]。纳米氧化银作为一种纳米材料,其性能远远优于氧化银,目前国内外对纳米氧化银的研究很多,其在数据存储和光伏电池等方面均有应用[8]。殷立峰等[9]用纳米氧化银开发了一种光电化学太阳能电池。Prasher等[10]提出随着多重耐药超级细菌的发现,纳米氧化银作为对抗致病超级细菌的新一代治疗药物,具有可调的物理化学效力。无论是单独作用还是与主流抗生素协同作用,都具有广泛的抗菌活性,使纳米氧化银作为潜在的抗菌素具有重要的研究意义。Archana等[11]利用纳米氧化银的抗菌性开发了一种新型的伤口愈合材料。金盈等[12]在改性纤维上负载纳米氧化银,从而赋予纳米复合纤维良好的抑菌性能。虽然已有不少学者对纳米氧化银进行开发应用,但是利用蔗渣负载纳米氧化银制备保鲜剂的研究鲜见报道。纳米氧化银也作为一种纳米抗菌材料被广泛应用,具有发全、高效、广谱、不易产生抗药性和耐热性等特点[13]。
蔗渣是甘蔗制糖工业的副产品,资源丰富,本研究通过蔗渣预处理,将其作为纳米氧化银的载体,有助于纳米氧化银在载体上分布均匀,大大减少了纳米氧化银团聚的现象。此新型防腐剂,为蔗渣的综合利用提供了新途径。
1 材料与方法
1.1 材料与试剂
蔗渣(100 目筛)、大肠杆菌、枯草芽孢杆菌广莫大学轻工与食品工程学院实验室提供;蔗糖酯广莫高通食品科技有限公司;NaOH、AgNO3(均为分析纯) 国药集团化学试剂有限公司;无水乙醇(分析纯) 天津市富宇精细化工有限公司。
1.2 仪器与设备
Zetasizer Nano S纳米粒度分析仪 英国马尔文公司;KQ-500DE型数控超声波清洗机 昆山市超声仪器有限公司;LG10-2.4A型离心机 磁海普力斯发防工程有限公司;UV-1100紫外-可见分光光度计 上海美谱达仪器有限公司;XW-80A旋涡混合器 上海精密科学仪器有限公司;S-3400N型扫描电镜(scanning electron microscope,SEM) 日本日立公司;4153B172型X射线衍射(X-ray diffraction,XRD)仪 日本理学公司。
1.3 方法
1.3.1 纳米氧化银的制备
用容量瓶配制NaOH和AgNO3溶液。将一定量的蔗糖酯加到配制好的NaOH溶液中搅拌均匀,将烧杯置于超声波清洗器中10 min后,在超声环境中缓慢滴加AgNO3溶液,溶液逐渐变成黑褐色。反应结束后,进行离心分离,产物用蒸馏水和无水乙醇各洗涤2 次。洗净后的产物置于60 ℃真空干燥箱中干燥1 d,得到纳米氧化银保鲜剂。通过改变NaOH、AgNO3浓度、蔗糖酯质量浓度、超声场中反应时间和功率得出纳米氧化银颗粒生成的最佳条件。
1.3.2 纳米氧化银粒径的测定
纳米氧化银的粒径用马尔文Zetasizer Nano S激光粒度仪进行测量,取一定量的纳米氧化银水悬液于烧杯中,用蒸馏水稀释至适当浓度,放入粒度仪中进行测量。
1.3.3 蔗渣-纳米氧化银的制备
在得出纳米氧化银颗粒制备的最优工艺条件后,在该最优工艺条件基础上制备蔗渣-纳米氧化银,用容量瓶配制NaOH和AgNO3溶液。方一定量蔗渣和蔗糖酯中加入AgNO3溶液,搅拌均匀。将烧杯置于超声波清洗器中10 min后,在超声环境中缓慢滴加NaOH溶液,溶液逐渐变成黑褐色。反应结束后,进行离心分离,产物用蒸馏水和无水乙醇各洗涤2 次。洗净后的产物置于60 ℃真空干燥箱中干燥1 d,得到蔗渣-纳米氧化银保鲜剂。
1.3.4 XRD分析
称取一定量的蔗渣-纳米氧化银样品,烘干研磨,将制得的蔗渣-纳米氧化银粉末铺撒于玻璃片凹槽中,使样品覆盖整个凹槽,压平样品,然后放入衍射仪中扫描,衍射角2θ扫描范围为20°~80°,扫描速度10°/min,扫描电压40 kV,扫描电流100 mA。
1.3.5 SEM分析
取少量液体导电胶滴在样品台上,用镊子取微量蔗渣-纳米氧化银粉末撒在液体导电胶中,使样品达到半浸没状态,待液体导电胶干后置于电镜载物台上,对保鲜剂样品进行形貌和显微结构的表征分析。
1.3.6 抗菌性能测定
采用最小抑菌浓度(minimal inhibit concentration,MIC)的标准方法考察蔗渣-纳米氧化银保鲜剂对大肠杆菌和枯草芽孢杆菌的抑菌性能,参考HG-T 3794—2005《无机抗菌剂——性能及评价》[14]。
1.3.6.1 培养基的配制
采用牛肉膏蛋白胨培养基:蛋白胨5 g、氯化钠2.5 g、牛肉膏2.5 g、琼脂9 g、蒸馏水500 mL。
方烧杯内加蒸馏水100 mL,加入牛肉膏2.5 g、蛋白胨5 g、氯化钠2.5 g,用电炉加热。待烧杯内各组分溶解后,加入琼脂,不断搅拌以免黏底。琼脂完全溶解后补足失水,用NaOH调整pH值到7.2~7.4,分装在锥形瓶里,用高压蒸汽灭菌:121 ℃维持20 min。
1.3.6.2 菌悬液的配制
菌悬液的配制在无菌操作台上进行,以除去杂菌影响。用接种环取出实验菌种放入无菌水中,用涡旋混合器混合20 s,将菌种均匀分散到溶液中形成菌悬液。将悬菌液用无菌水稀释成10-1、10-2、10-3、10-4梯度。
1.3.6.3 抗菌液的配制
抗菌液的配制采用二倍稀释法[15],取标记为1~4号共4 支试管排列于试管架上。称取23.173 mg蔗渣-纳米氧化银样品于烧杯中,加入20 mL无菌水,配制蔗渣-纳米氧化银抗菌液,混合均匀。1号试管中加入14.0 mL蔗渣-纳米氧化银水悬液,其余试管均加入7.0 mL无菌水。吸取1号试管中7.0 mL纳米氧化银溶液加入到2号试管中,混合均匀,再从2号试管中吸取7.0 mL加到3号试管中,以此类推,直至第4管。
1.3.6.4 MIC的测定
取56 个无菌培养皿分为14 组,7 组培养大肠杆菌,7 组培养枯草芽孢杆菌,每组4 个。其中第5组加入等量无菌水作对照,第6组加入与第1组抗菌液中所含等量的纳米氧化银作对照,第7组加入与第1组抗菌液中所含等量的蔗渣作对照。用移液枪分别吸取1~4号蔗渣-纳米氧化银抗菌液1.0 mL对应加于无菌培养皿中,即1号抗菌液加入到第1组无菌培养皿。方已加入抗菌液的培养皿中倾注约15 mL的培养基,将培养皿盖好,轻摇使培养基与抗菌液充分混匀,摇匀后平放,待琼脂凝固后备用。
培养基凝固后,用移液枪吸取菌悬液0.1 mL接种到培养皿中,用涂布棒将菌悬液均匀分布在培养皿表面。接种后水平放置20 min,倒置恒温培养24 h。
1.4 数据处理与分析
2 结果与分析
2.1 纳米氧化银粒径测定结果
2.1.1 AgNO3浓度对纳米氧化银粒径的影响
在NaOH浓度0.02 mol/L、蔗糖酯质量浓度1.0 g/L、反应温度40 ℃、反应时间30 min、超声功率350 W的条件下考察AgNO3浓度对纳米氧化银粒径的影响。由图1可知,随着AgNO3浓度增加,纳米氧化银粒径逐渐减小,当AgNO3浓度超过0.02 mol/L时,纳米氧化银粒径逐渐增加。在低浓度AgNO3范围内,增大其浓度有利于加快反应速率,生成数量多、粒径小的纳米氧化银颗粒。当AgNO3浓度过大时,纳米氧化银生成速率小于生长速率,同时生成的大量纳米氧化银粒子容易发生碰撞团聚,甚至过量的银离子会在原有晶核的基础上二次成核,故纳米氧化银粒径增大。纳米氧化银粒径越小,其比表面积越大,氧化银抗菌性越强,分散性越好,越易被蔗渣吸附。在AgNO3浓度为0.02 mol/L时,纳米氧化银粒径最小,为107.6 nm。
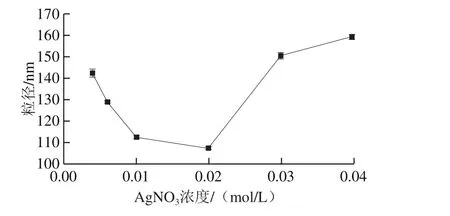
图1 AgNO3浓度对纳米氧化银粒径的影响Fig. 1 Effect of AgNO3 concentration on particle size of nano silver oxide
2.1.2 NaOH浓度对纳米氧化银粒径的影响
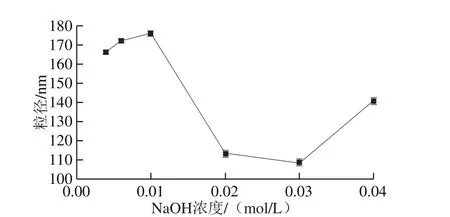
图2 NaOH浓度对纳米氧化银粒径的影响Fig. 2 Effect of NaOH concentration on particle size of nano silver oxide
NaOH浓度对纳米氧化银粒径的影响很大。在AgNO3浓度0.02 mol/L、蔗糖酯质量浓度1.0 g/L、反应温度40 ℃、反应时间30 min、超声功率350 W的条件下考察NaOH浓度对纳米氧化银粒径的影响。由图2可知,当NaOH浓度增加,纳米氧化银粒径先增加后减小再增加。当NaOH在低浓度范围内,由于NaOH不足,纳米氧化银生成速率较慢而生长速率较快,故粒径较大。当NaOH浓度超过一定值后,其反应速率增加,纳米氧化银生成速率大于生长速率,故纳米氧化银粒径逐渐较小。由于蔗糖酯在低碱度稳定,在高碱度容易发生水解使其亲水性能下降[16],降低其对纳米氧化银粒子的保护作用,故纳米氧化银粒径会增大。在NaOH浓度为0.03 mol/L时,纳米氧化银粒径最小,为108.4 nm。
2.1.3 蔗糖酯质量浓度对纳米氧化银粒径的影响
在AgNO3浓度0.02 mol/L、NaOH浓度0.03 mol/L、反应温度40 ℃、反应时间30 min、超声功率350 W的条件下考察蔗糖酯质量浓度对纳米氧化银粒径的影响。由图3可知,纳米氧化银粒子粒径随着蔗糖酯浓度先减小后增加。蔗糖酯质量浓度在0.8~1.4 g/L范围内,纳米氧化银粒径随着蔗糖酯质量浓度增加而减小,这是因为蔗糖酯在纳米氧化银生成反应中能吸附纳米氧化银粒子抑制其生长,降低纳米氧化银生长速率。但是由于蔗糖酯会增加溶液的黏度,同时过量的蔗糖酯会吸附在纳米氧化银-蔗糖酯溶胶颗粒上,降低粒子的稳定性。所以当蔗糖酯用量过多时,纳米氧化银粒径反而增加。当蔗糖酯质量浓度在1.4 g/L时,纳米氧化银粒径最小,为97.38 nm。
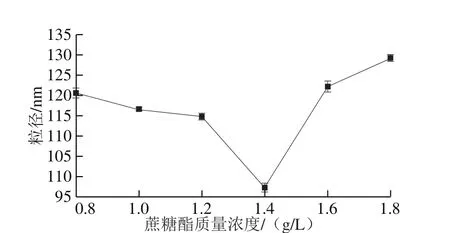
图3 蔗糖酯质量浓度对纳米氧化银粒径的影响Fig. 3 Effect of sucrose ester concentration on particle size of nano silver oxide
2.1.4 反应温度对纳米氧化银粒径的影响
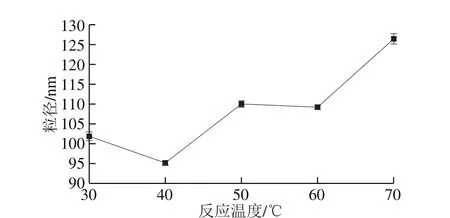
图4 反应温度对纳米氧化银粒径的影响Fig. 4 Effect of reaction temperature on particle size of nano silver oxide
在AgNO3浓度0.02 mol/L、NaOH浓度0.03 mol/L、蔗糖酯质量浓度1.4 g/L、反应时间30 min、超声功率350 W的条件下,考察反应温度对纳米氧化银粒径的影响。由图4可知,反应温度在40 ℃时纳米氧化银粒径最小,为91.22 nm。当反应温度低于40 ℃时,由于温度过低,纳米氧化银生成所需的能量不足[17],故反应速率低于生长速率,纳米氧化银粒径较大。当反应温度超过40 ℃,随着反应温度的升高,纳米氧化银粒径主要呈增加的趋势。这是由于随着反应温度升高,布朗运动增加,纳米氧化银颗粒碰撞团聚现象加剧[18],故粒径增加。此外,纳米氧化银在高温下容易分解成银单质[19],所以在反应温度为40 ℃时最佳。
2.1.5 反应时间对纳米氧化银粒径的影响
在AgNO3浓度0.02 mol/L、NaOH浓度0.03 mol/L、蔗糖酯质量浓度1.4 g/L、反应温度40 ℃、超声功率350 W的条件下考察反应时间对纳米氧化银粒径的影响。由图5可知,在上述实验条件中,反应时间对纳米氧化银粒径影响很大。纳米氧化银生成反应过程中,反应体系先生成小颗粒,然后再逐渐长大,最后形成稳定的纳米氧化银粒子。在反应时间30~110 min范围内,纳米氧化银粒径主要随着反应时间的延长而减小。这是因为生成的大量晶核可以稳定分散在溶液中,沉淀反应能够在稳定条件下反应完全,因而纳米氧化银粒径主要呈减小的趋势。但是反应完全后,随着时间的延长,纳米氧化银颗粒会发生碰撞团聚,因而粒径会有所增加。反应时间在第110分钟时,纳米氧化银粒径最小,为80.01 nm。
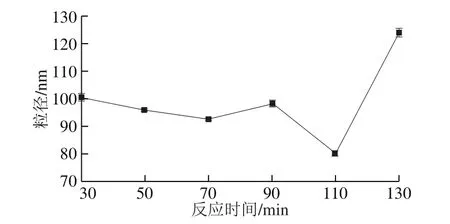
图5 反应时间对纳米氧化银粒径的影响Fig. 5 Effect of reaction time on particle size of nano silver oxide
2.1.6 超声功率对纳米氧化银粒径的影响
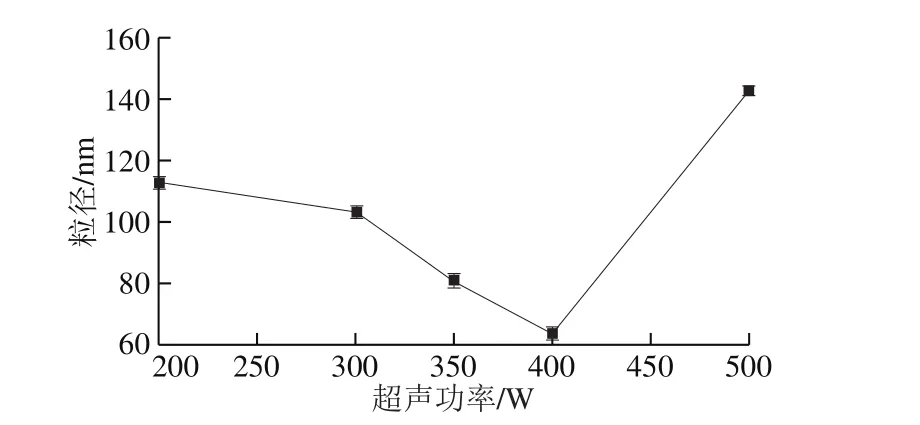
图6 超声功率对纳米氧化银粒径的影响Fig. 6 Effect of ultrasonic power on particle size of nano silver oxide
在AgNO3浓度0.02 mol/L、NaOH浓度0.03 mol/L、蔗糖酯质量浓度1.4 g/L、反应温度40 ℃、反应时间110 min的条件下考察超声功率对纳米氧化银粒径的影响。由图6可知,在上述实验条件中,纳米氧化银粒径随着超声功率的增加先减小后增加,由此可见超声功率对纳米氧化银粒径有较大影响。在溶液反应体系中,超声波所起作用与搅拌有相似之处,能加快传质速率,提高反应速率。此外,超声波空化作用所产生的微小气泡能降低氧化银晶核表面自由能[20],降低了其生长速率,故在一定超声波功率范围内,纳米氧化银粒径随着超声波功率增加而减小。但所施加的超声波功率超过一定范围后,粒径会增加,这是因为在空化作用过程中,空泡崩溃时产生的高压、高温度变化率会给反应造成一个极端的物理环境,当超声功率过大时,传质和传热过程增大,增加了颗粒相互碰撞的几率[21],剧烈的物理化学作用又会引起生成的颗粒重新团聚[22],超声空化产生的剪切力也会增加,打碎已成核的纳米颗粒,导致颗粒残缺、大小不一[23]。其次,超声波产生的空化作用能提高反应体系的温度,使其超过反应体系最佳的温度。当超声波功率为400 W时氧化银粒径最小,为63.38 nm。
2.2 蔗渣-纳米氧化银的XRD分析
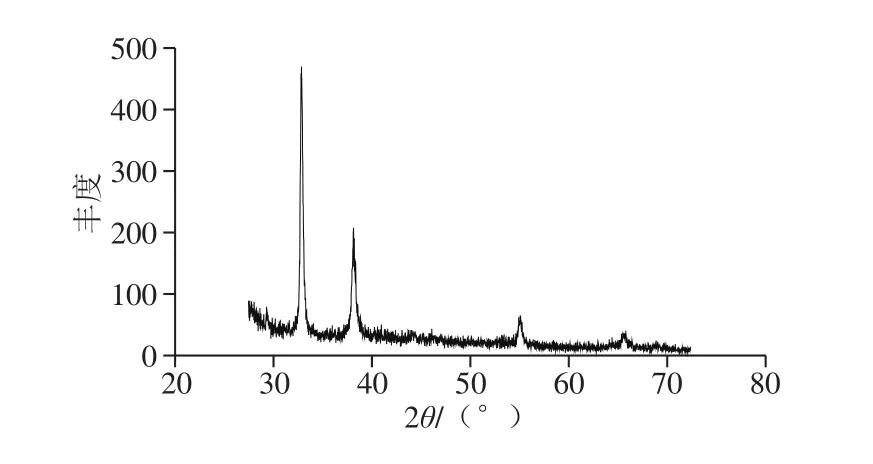
图7 蔗渣-纳米氧化银的XRD图谱Fig. 7 XRD pattern of bagasse-silver oxide particles
图7 为蔗渣-纳米氧化银XRD图谱,在2θ20°~80°有4 个特征衍射峰,与单质银标准卡(JCPDS卡编号65-2871)和氧化银标准卡(JCPDS卡编号65-6811)对比得知,产物为银和氧化银的混合物。由图7可知,纳米氧化银的强度较大,峰尖较窄且尖,说明合成的纳米氧化银结晶较好,XRD的结果表明纳米氧化银成功的吸附在蔗渣纤维上[24],单质银的产生可能是实验过程中氧化银分解所造成的。
2.3 蔗渣-纳米氧化银SEM分析

图8 蔗渣-纳米氧化银的SEM图Fig. 8 SEM photograph of bagasse-silver oxide particles
如图8所示,对蔗渣-纳米氧化银进行SEM成像,从而阐明其表面形貌和粒径的测定[25]。由电镜照片可以看出,蔗渣纤维表面呈粗糙状态,在蔗渣纤维表面分散着许多小颗粒,这些白色小颗粒亮点为纳米氧化银粒子。SEM图像清楚地显示,沉淀法[26]制备的纳米氧化银为近球状粒子,直径较小,颗粒较为分散,其吸附在蔗渣表面,团聚现象不明显,但分布无规律,只是简单分散在蔗渣表面,可能因为蔗渣纤维吸附功能较弱,可通过对蔗渣纤维进行化学改性增强其吸附功能[27]。
2.4 蔗渣-纳米氧化银抑菌性能
2.4.1 蔗渣-纳米氧化银对大肠杆菌的抗菌性能
大肠杆菌属于革兰氏阴性短杆菌,广泛分布于自然界和动物肠道中,大肠杆菌长期应对不同环境的过程中,会发生进化并增强其抗性,是一种极易造成食品污染的细菌[28]。图9为不同浓度蔗渣-纳米氧化银对不同稀释度(10-1、10-2、10-3、10-4)大肠杆菌的抗菌性能。蔗渣-纳米氧化银对稀释度为10-1的大肠杆菌的MIC为289.662 5 μg/mL,对稀释度为10-2的大肠杆菌的MIC为579.325 μg/mL,对稀释度为10-3的大肠杆菌的MIC为289.662 5 μg/mL,对稀释度为10-4的大肠杆菌的MIC为289.662 5 μg/mL。

图9 蔗渣-纳米氧化银对大肠杆菌的抗菌结果Fig. 9 Antibacterial effect of bagasse-silver oxide on E. coli

表1 蔗渣-纳米氧化银对大肠杆菌的抗菌性能Table 1 Antibacterial activity of bagasse-silver oxide on E. coli
从表1可以看出,所有蔗渣-纳米氧化银样品对大肠杆菌均有明显的抑制作用。从无菌水对照组和蔗渣对照组可知对大肠杆菌起到抑制作用的物质是纳米氧化银,蔗渣对大肠杆菌无抑制作用,蔗渣-纳米氧化银样品和纳米氧化银样品对大肠杆菌均有抑菌效果,蔗渣-纳米氧化银抑菌效果优于纳米氧化银。这是因为由于蔗渣吸附纳米氧化银颗粒,使其均匀分布于蔗渣上,使得纳米氧化银颗粒团聚现象减少,增强了其抑菌性能。对比不同蔗渣-纳米氧化银抗菌液得到其MIC为289.662 5 μg/mL。
2.4.2 蔗渣-纳米氧化银对枯草芽孢杆菌的抗菌性

图10 蔗渣-纳米氧化银对枯草芽孢杆菌的抗菌结果Fig. 10 Antibacterial effect of bagasse-silver oxide on B. subtilis
枯草芽胞杆菌是一类需氧型、内生孢子的杆状革兰氏阳性菌[29],具有较强的抗逆能力[30]。枯草芽孢杆菌具有调节肠道微生态平衡、促进畜禽对营养物质的消化吸回和增强免疫等作用,目前已在畜禽生产中广泛应用[31]。图10为不同浓度蔗渣-纳米氧化银对不同稀释度(10-1、10-2、10-3、10-4)枯草芽孢杆菌的抗菌性能。纳米氧化银对稀释度为10-1的枯草芽孢杆菌的MIC为289.662 5 μg/mL,对稀释度为10-2的枯草芽孢杆菌的MIC为289.662 5 μg/mL,对稀释度为10-3的枯草芽孢杆菌的MIC为579.325 μg/mL,对稀释度为10-4的枯草芽孢杆菌的MIC为579.325 μg/mL。
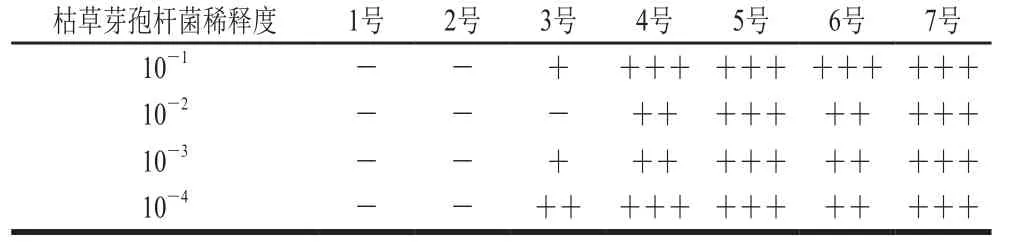
表2 蔗渣-纳米氧化银对枯草芽孢杆菌的的抗菌性能Table 2 Antimicrobial activity of bagasse-silver oxide on B. subtilis
从表2可以看出,所有蔗渣-纳米氧化银样品对枯草芽孢杆菌均有明显的抑制作用。从无菌水对照组和蔗渣对照组可知对枯草芽孢杆菌起到抑制作用的物质是纳米氧化银,蔗渣对枯草芽孢杆菌无抑制作用,蔗渣-纳米氧化银样品和纳米氧化银样品对枯草芽孢杆菌均有抑菌效果,蔗渣-纳米氧化银抑菌效果优于纳米氧化银,这是因为由于蔗渣吸附纳米氧化银颗粒,使其均匀分布于蔗渣上,使得纳米氧化银颗粒团聚现象减少,增强了其对枯草芽孢杆菌的抑菌性能。对比不同蔗渣-纳米氧化银抗菌液得到其MIC为579.325 μg/mL。
3 结 论
本实验在AgNO3浓度0.02 mol/L、NaOH浓度0.03 mol/L、蔗糖酯质量浓度1.4 g/L、反应温度40 ℃、反应时间110 min、超声功率400 W的条件下制得的纳米氧化银粒径最小,为63.38 nm。在此最优条件下制备出蔗渣-纳米氧化银保鲜剂,通过XRD和SEM得出纳米氧化银吸附在蔗渣上;对蔗渣-纳米氧化银进行抑菌性能测定,得出蔗渣-纳米氧化银抗菌液对大肠杆菌和枯草芽孢杆菌的MIC分别为289.662 5 µg/mL和579.325 µg/mL。该项研究用蔗渣作为载体,纳米氧化银作为抑菌物质制备了一种绿色、无毒的保鲜剂,为蔗渣吸附抗菌剂的研究开发提供科学依据,也为蔗渣的综合利用提供了一条新途径。
