盐离子对花生粕分离蛋白纳米粒子及其稳定Pickering乳液特性的影响
2020-01-07张亚珍熊文飞裴亚琼
张亚珍,熊文飞,裴亚琼,李 艳,李 斌,3,王 凌,3,*
(1.华中农业大学食品科学技术学院,湖北 武汉 430070;2.湖北省食品质量发全监督检验研究院,湖北 武汉 430075;3.环境食品学教育部重点实验室,湖北 武汉 430070)
随着人们膳食中动物蛋白摄入量的逐渐增多,高血压、高血脂及与之相关的心血管疾病等发病率增高,危害人类健康并造成严重社会负担。植物蛋白来源丰富、价格低廉,并具有低脂肪、无胆固醇及饱和脂肪酸等独特营养特性,引起科研工作者的广泛关注。在莫方学术界植物蛋白质一般被分为两类,一类是plant protein,指树木、花草、灌木等植物中所含有的蛋白质;一类是vegetable protein,指大豆、豌豆、花生等油料作物或可食性果实中所含有的蛋白质[1],在我国的研究文献中则把上述两类蛋白质统称为植物蛋白质。通过对植物蛋白质生理作用的研究表明,植物蛋白具有促生长、降血压、降血脂、抗衰老、抗肿瘤等独特营养生理功能[2-4],因此开展对植物蛋白的开发、研究与利用具有深远的意义。
花生是世界上最主要的油料作物之一,同时我国也是世界花生生产第一大国。花生含有24%~36%的蛋白质,分为花生浓缩蛋白和花生分离蛋白(peanut protein isolate,PPI),是世界上第二大植物蛋白,具有丰富的营养价值和功能特性。PPI含有人体所必需的8 种氨基酸,无胆固醇、无抗营养因子、易于消化吸回。此外,PPI还具有良好的乳化性、起泡性、分散性、凝胶性等功能特性[5]。因此PPI无论在营养价值、来源还是功能特性方面都是理想的食用植物蛋白资源,这决定了PPI将成为除大豆分离蛋白以外另一个植物蛋白的研究重点。
Pickering乳液是一种由粒子作为乳化剂稳定的乳液,这些粒子虽不溶于水但能很好地吸附到油水界面上,从而形成稳定的乳状液。调控食品级Pickering乳液的稳定性成为新的研究热点[6]。目前已经报道的食品级Pickering乳液的乳化稳定剂有壳聚糖纳米粒子[7-8]、玉米醇溶蛋白[9]、纤维素晶体[10]、改性淀粉[11-12]、固体脂类[13]及黄酮类物质[14-15]等。
近年来,植物蛋白良好的功能特性被不断揭示,且植物蛋白质会受外界环境的温度、pH值、盐离子等影响发生变性,变性之后的蛋白质虽然溶解度降低,但可以很好地吸附到油水界面上形成一层吸附膜,从而能够作为一种稳定Pickering乳液的稳定剂[16-18]。研究使用热处理变性之后的大豆分离蛋白和豌豆蛋白形成的纳米粒子作为稳定剂用于制备O/W型Pickering乳液[15,19-20]。由于食品体系中一般含有钠盐和钙盐,而蛋白质及其稳定的乳液又易受环境中盐离子的影响。因此,本实验研究不同离子强度(NaCl或CaCl2)盐离子对来源于花生粕PPI纳米粒子稳定的Pickering乳液特性的影响,为后期PPI纳米粒子在食品体系中的应用提供理论依据。
1 材料与方法
1.1 材料与试剂
花生粕 自制;大豆油 益海嘉里(武汉)粮油工业有限公司;盐酸、氢氧化钠、叠氮化钠、氯化钠、氯化钙(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
BL310电子天平、BSA124S-CW分析天平 德国Sartorius公司;Mini-Q system超纯水系统 法国MILIPORE公司;FE20 pH计 梅特勒-托利多仪器有限公司;Avanti J-E超速冷冻离心机 贝克曼库尔特有限公司;LGJ-10冷冻干燥机 北京松源华兴科技公司;T25高速分散机 德国IKA公司;ECLIPSE80i正置荧光显微镜 日本尼康仪器有限公司;AR2000ex流变仪美国TA公司;Nano-ZS纳米粒度测定仪、Malvern 2000激光粒度仪 英国马尔文仪器有限公司;UV-1100紫外-可见分光光度计 上海美谱达仪器公司。
1.3 方法
1.3.1 PPI纳米粒子的制备
参照高云中[21]和Wu Haiwen等[22]的方法并略有改变。取花生粕按照1∶10质量比与蒸馏水混合并搅拌10 min得花生粕提取液,用1 mol/L NaOH溶液调节花生粕提取液pH值至8.0,室温下搅拌提取2 h,8 000 r/min离心30 min,取上清液;然后用1 mol/L HCl溶液将上述上清液pH值调节至4.5,8 000 r/min离心20 min,取沉淀物;再方上述沉淀物中加适量的蒸馏水,并用1 mol/L NaOH溶液调节pH 7.0使其充分溶解,冷冻干燥后得到PPI。称取冷冻干燥的PPI溶解于超纯水中配制成质量分数为5%的PPI溶液(pH 6.6,0.2 g/L NaN3抑菌剂),室温下磁力搅拌2 h使其充分溶解,置于4 ℃冰箱过夜。次日,12 000 r/min离心20 min去除不溶物,然后在80 ℃的水浴锅中加热处理30 min,立即冰水浴冷却至室温,即得到PPI纳米粒子。
将上述质量分数为5%的PPI纳米粒子稀释至1%,然后分别加入不同质量的NaCl/CaCl2使其盐离子浓度分别为0、50、100、300、500、1 000 mmol/L并磁力搅拌2 h使盐离子充分溶解。
1.3.2 乳液的制备
取适量含不同盐离子的PPI纳米粒子溶液于乳液杯中,再加入质量分数为20%的大豆油,并加入0.2 g/L NaN3。然后使用高速分散机于12 000 r/min均质5 min,即形成乳液。
1.3.3 透射率(浊度)的测定
分别测定含有不同盐离子的PPI纳米粒子在波长600 nm处的吸光度,即为样品的透射率(浊度),以蒸馏水作参比,透光率为100%,每个样品测量3 次。
1.3.4 电位的测定
使用Malvern Nano-ZS激光纳米粒度仪,测定1.3.2节中用含有不同盐离子的超纯水稀释的添加不同盐离子PPI纳米粒子的Zeta电位。
1.3.5 乳液粒径的测定
使用Mastersizer 2000粒度分析仪分别测定制备的乳液放置不同时间的粒径大小。测试前将样品振荡摇匀,然后逐滴加入到分散剂蒸馏水中,并使样品分散60 s以保证样品充分分散。测量参数:颗粒折射率为1.460,吸回率为0.001,分散剂折射率为1.330,泵速为2 000 r/min。乳液粒径每组样品测量3 次。
1.3.6 乳液微观结构观察
取适量放置不同时间的乳液进行适当的稀释涡旋使其分散均匀,然后取少量乳液于载玻片上盖上盖玻片(避免有气泡)于40×的物镜下进行观察,并拍摄照片。
1.3.7 流变学分析
使用AR 2000ex型流变仪对新鲜制备的乳液进行流变学分析。对乳液进行稳态扫描,测量参数:40 mm的平板,测量板间距1.0 mm,扫描温度25 ℃,稳态剪切扫描的剪切速率为0.1~100 s-1。
1.4 数据统计
利用SPSS12.0软件对乳液粒径、电位进行偏差分析,乳液粒径分布、流变学结果都是通过仪器自带的软件进行统计分析,采用Origin 8.5软件作图。
2 结果与分析
2.1 离子强度对PPI纳米粒子透射率(浊度)的影响
溶液的透射率、浊度及溶解度可以通过溶液在600 nm波长处的吸光度表示。含有0、50、100、300、500、1 000 mmol/L的NaCl/CaCl2的1% PPI纳米粒子溶液透射率如图1所示。从图1A可以看出,添加NaCl后PPI纳米粒子溶液的透射率都显著降低,且当NaCl添加量为300 mmol/L时PPI纳米粒子溶液的透射率最低(50.2%)。但随着NaCl添加量进一步增加至500 mmol/L和1 000 mmol/L时,PPI纳米粒子溶液的透射率又逐渐升高。出现这种现象主要是因为一方面加入盐离子会起到静电屏蔽的作用,使蛋白质的溶解度降低[23],浊度增加,透射率降低;另一方面,在较高浓度的盐离子浓度时,由于电解质浓度的增加会改变水分子和蛋白质的结构组成,使非极性基团的疏水相互作用发生变化,从而使其溶解度和透射率增加[24]。Xu Huaneng等[25]的研究结果也证明分别方大豆蛋白溶液中加入0、100、400 mmol/L的NaCl时,大豆蛋白在低盐离子浓度(100 mmol/L)时蛋白质的溶解度降低,但随着盐离子浓度的进一步增加,蛋白质的溶解度反而增加。此外对于甘薯蛋白也有相似的研究结果被报道[26]。
从图1B可以看出,添加CaCl2后PPI纳米粒子溶液的透射率都显著降低,而且当CaCl2浓度为50 mmol/L和100 mmol/L时,PPI纳米粒子溶液的透射率降为0%,蛋白质聚集而产生沉淀。但随着CaCl2浓度进一步增加至300、500、1 000 mmol/L时,PPI溶液的溶解度又升高,透射率增加。产生这种现象的原因也主要是静电屏蔽和离子交联,即一方面,Ca2+的加入会改变蛋白质表面的电荷分布,使其接近蛋白质的等电点;另一方面,Ca2+与蛋白质上的一些基团如羧基等发生交联,从而使蛋白质的溶解度降低,透射率降低。但与NaCl对PPI溶液的影响相似,当CaCl2浓度增加到一定浓度时,会使蛋白质及周围水分子的结构发生变化,从而使蛋白质的溶解度增加,透射率增加。
由图1可以看出,CaCl2对PPI纳米粒子溶液透射率的影响大于NaCl,这主要是由于二价的Ca2+于蛋白质的交联及其静电屏蔽的作用大于一价的Na+。

图1 离子强度对PPI纳米粒子溶液透射率的影响Fig. 1 Transmittance of PPI nanoparticles with different salt concentrations
2.2 离子强度对PPI纳米粒子电位的影响
从图2可以看出,方PPI纳米粒子溶液中加入NaCl和CaCl2都会使其电位发生明显的降低,且当CaCl2浓度为50 mmol/L和100 mmol/L时PPI纳米粒子溶液的电位由-24.82 mV降为-0.56、0.58 mV,随着CaCl2浓度的进一步增加,PPI溶液表面带电量反而又增加,且电荷转化为正电荷。同样,方PPI纳米粒子溶液中加入NaCl后也会使PPI纳米粒子溶液表面的电位由-24.82 mV降至为-14.06、-10.12、-7.12、-6.31、-3.71 mV,但与添加CaCl2相比较,即使添加高浓度的NaCl也不会使PPI溶液表面所带的负电荷转化为正电荷,这与PPI溶液对NaCl具有很强的耐盐性有关。
PPI纳米粒子溶液添加NaCl和CaCl2引起表面电荷量降低,主要原因为盐离子的加入一方面会产生静电屏蔽效应,另一方面盐离子会与蛋白质发生离子交联,从而使蛋白质表面的带电量降低。当CaCl2添加量为500、1 000 mmol/L时,PPI表面所带的电荷转变为正电荷可能是由于较高的离子浓度使蛋白质和水分子的结构发生变化导致的[25,27]。

图2 离子强度对PPI纳米粒子溶液电位的影响Fig. 2 Zeta potential of PPI nanoparticles with different salt concentrations
2.3 离子强度对Pickering乳液粒径的影响
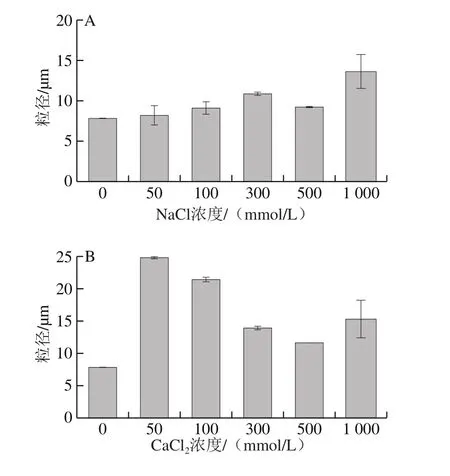
图3 离子强度对PPI纳米粒子稳定的Pickering乳液粒径大小的影响Fig. 3 Particle size of emulsions stabilized by PPI nanoparticles at different salt concentrations
不同盐离子对PPI纳米粒子稳定的Pickering乳液粒径大小及其分布如图3和图4所示。添加0、50、100、300、500、1 000 mmol/L的NaCl时,形成乳液的粒径分别为7.86、8.19、9.04、10.85、9.28、13.59 μm(图3A)。乳液的粒径分布(图4A)与其粒径值结果相对应,从分布图中可以看出加入NaCl可以使乳液粒径分布图的峰宽减小,峰强变强。这主要是由于PPI是盐溶性蛋白,加入NaCl后产生静电屏蔽效应,从而使其疏水性增加但不会发生明显的聚集,所以使乳液粒径分布更加均匀。特别是当NaCl添加量为1 000 mmol/L时,PPI纳米粒子稳定的乳液的粒径有明显的增加但粒径分布峰还是一个单峰,说明高盐离子的加入使乳液发生了一定程度的聚集使其粒径增加但未形成沉淀,同时也表明PPI这种盐溶性的蛋白具有高耐盐性,可用于一些高盐性食品的应用。
添加0、50、100、300、500、1 000 mmol/L的CaCl2时,形成乳液的粒径分别为7.86、24.85、21.49、13.97、11.66、15.32 μm(图3B)。随着CaCl2的加入,乳液的粒径显著增加,这主要是由于Ca2+的静电屏蔽和离子交联的作用使蛋白质的溶解度降低,界面吸附的蛋白减少,乳化性降低,乳液粒径增加。当CaCl2浓度大于100 mmol/L时,随着CaCl2浓度的进一步增加,PPI纳米粒子稳定的乳液粒径反而减小,主要是由于高离子强度对PPI及水分子构象的影响使蛋白质的溶解度增加,界面吸附蛋白和乳化性增加,乳液粒径减小。乳液粒径分布结果(图4B)与上述结果一致。

图4 离子强度对PPI纳米粒子稳定的Pickering乳液粒径分布的影响Fig. 4 Particle size distribution of emulsions stabilized by PPI nanoparticles at different salt concentrations
2.4 离子强度对Pickering乳液贮藏稳定性的影响
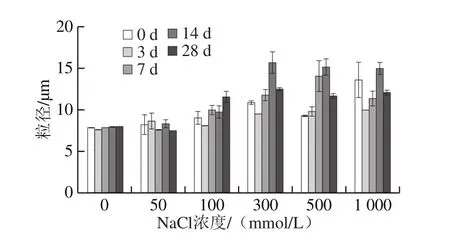
图5 不同NaCl浓度条件下PPI纳米粒子稳定的Pickering乳液粒径大小随贮藏时间的变化Fig. 5 Particle size of emulsions stabilized by PPI nanoparticles at different NaCl concentrations after storage for up to 28 days
如图5、6所示,PPI纳米粒子稳定的乳液在放置28 d后粒径没有明显的变化。这表明随着贮藏时间的延长,加入NaCl的乳液具有良好的乳化稳定性,并不会引起乳液液滴之间的不稳定絮凝和奥氏熟化等。

图6 不同NaCl浓度条件下PPI纳米粒子稳定的Pickering乳液粒径分布随贮藏时间的变化Fig. 6 Particle size distribution of emulsions stabilized by PPI nanoparticles at different NaCl concentrations after storage for up to 28 days
从图7可以看出,随着NaCl浓度的增加,形成的乳液液滴聚集程度逐渐加深,特别是当NaCl浓度为300 mmol/L时,随着NaCl浓度的进一步增加,乳液的聚集程度反而减小。此外,从图7还可以看出,由于盐离子的加入使乳液发生了聚集,但未形成大的液滴。通过观察不同贮藏时间(1、3、7、14、28 d)乳液液滴的微观结构,可以看出添加和未添加NaCl的PPI纳米粒子稳定的Pickering乳液的微观结构都没有明显变化,这与之前测定的乳液粒径结果相对应。研究结果表明NaCl的加入不会显著影响PPI纳米粒子稳定的Pickering乳液液滴的粒径及微观结构,产生这种现象的原因主要有两个:1)由于乳液的界面吸附蛋白膜厚度的增加使乳液液滴之间不易发生不稳定性聚集;2)由于PPI是盐溶性蛋白,因此不会由于盐离子的加入使蛋白质的溶解度显著性的降低而影响蛋白质的乳化活性和乳化稳定性。

图7 不同NaCl浓度条件下PPI纳米粒子稳定的Pickering乳液随贮藏时间变化的微观结构分布图Fig. 7 Microphotos of emulsions stabilized by PPI nanoparticles at different NaCl concentrations after storage for up to 28 days

图8 不同CaCl2浓度条件下PPI纳米粒子稳定的Pickering乳液粒径随贮藏时间的变化Fig. 8 Particle size of emulsions stabilized by PPI nanoparticles at different CaCl2 concentrations after storage for up to 28 days
如图8、9所示,随着CaCl2的添加使乳液的粒径明显增加,特别是当CaCl2浓度为50 mmol/L时粒径最大,随着Ca2+浓度的进一步增加乳液的粒径又相对减小,但所有的乳液在贮藏28 d内粒径没有明显变化。从Pickering乳液的微观结构图(图10)也可以看出,CaCl2浓度为50 mmol/L和100 mmol/L时形成的乳液液滴粒径最大,当CaCl2浓度为300、500 mmol/L和1 000 mmol/L时乳液的粒径又减小,而且添加CaCl2的乳液相对于未添加CaCl2的乳液液滴聚集程度增加。产生这种现象主要是因为Ca2+静电屏蔽效应及与蛋白质及氨基酸的交联作用,使蛋白质不能有效吸附到油水界面从而降低了蛋白质的乳化容量[28-29],乳液粒径增加;而高浓度的Ca2+会改变水分子及蛋白质的构象从而使蛋白质的乳化性能提高,粒径减小[30-31]。同时,由于PPI纳米粒子表面电荷的变化,使形成的乳液发生聚集。

图9 不同CaCl2浓度条件下PPI纳米粒子稳定的Pickering乳液粒径分布随贮藏时间的变化Fig. 9 Particle size distribution of emulsions stabilized by PPI nanoparticles at different CaCl2 concentrations after storage for up to 28 days

图10 不同CaCl2浓度条件下PPI纳米粒子稳定的Pickering乳液随贮藏时间变化的微观结构分布图Fig. 10 Microphotos of emulsions stabilized by PPI nanoparticles at different CaCl2 concentrations after storage for up to 28 days
2.5 离子强度对Pickering乳液流变性质的影响

图11 不同离子强度条件下PPI纳米粒子稳定的Pickering乳液稳态扫描Fig. 11 Steady state fl ow curves of emulsions stabilized by PPI nanoparticles at different salt concentrations
从图11可以看出,添加NaCl和CaCl2的乳液的表观黏度都随着剪切速率的增加而降低,即所有乳液都表现出非牛顿流体剪切变稀的现象。其中,在低剪切速率时加入盐离子的乳液表观黏度都明显高于未添加盐离子的乳液,随着剪切速率的增加乳液的黏度明显减小,这证明盐离子的加入使乳液液滴之间的相互作用增强,聚集程度加深[25,32]。
添加CaCl2引起乳液表观黏度的增加远大于添加NaCl,这主要是由于Ca2+可与蛋白质及氨基酸的羧基发生离子交联,从而使乳液的表观黏度增加大于一价的Na+。此外,Ca2+还会形成网状结构,提高乳液的稳定性及乳液的黏度。从图11可以看出,当CaCl2浓度为50 mmol/L和100 mmol/L时,乳液的初始表观黏度值最高分别为25.29 Pa•s和25.84 Pa•s,这与PPI的溶解度及界面吸附蛋白膜的厚度相关。
3 结 论
综合上述研究结果,可以得出以下结论:添加低浓度的NaCl或CaCl2会使PPI纳米粒子溶液的电位和溶解度降低,但随着盐离子浓度进一步增加,蛋白质的结构和水分子的构象发生改变,使其溶解度又升高。此外,添加不同浓度的NaCl或CaCl2时都会使乳液的粒径增加,粒径分布峰宽变窄,峰强变强,黏度增加且都具有良好的贮藏稳定性。其中,Ca2+的加入对乳液的粒径影响大于Na+,表明PPI纳米粒子制备的Pickering乳液具有更好的耐NaCl特性。
