新疆伊犁牧区传统手工奶酪中微生物多样性及其功能分析
2020-01-07王春艳李宇辉李应彪李宝坤王腾斌石秀如
王春艳,李宇辉*,李应彪,*,李宝坤,王腾斌,石秀如
(1.石河子大学食品学院,新疆 石河子 832003;2.新疆农垦科学院农产品加工研究所,新疆 石河子 832000)
新疆奶酪又称为奶疙瘩,是哈萨克族、蒙古族等少数民族喜欢食用的一种乳制品,哈萨克语称奶疙瘩为库鲁特(Kurut)[1]。Kurut的生产环境与波兰奶酪[2]非常相似,通常不使用发酵剂,仅由牛奶本身和环境中存在的微生物群通过自然发酵形成[3]。随着便携方便食品种类的日益丰富以及现代化生活方式不断方牧区渗透,使得传统奶酪的种类和加工量不断减少,其中蕴藏的微生物资源也逐渐消失。因此,对传统奶酪中微生物多样性的研究将有助于保护其中的微生物资源。
奶酪营养价值极高,但我国居民对奶酪、黄油等高附加值乳品消费极少[4],主要原因之一为奶酪的感官品质较差[5]。众多研究发现,奶酪中的微生物主要包括乳酸菌[6-8]、酵母菌[9]以及霉菌[10-11]等三大类群,其中乳酸菌对奶酪感官品质的改善发挥着重要作用。有研究表明,乳酸菌在奶酪发酵初期产生的酸性物质有利于奶酪凝固[12],并能促进干酪的成熟,提高干酪营养及强化风味物质的产生[13]。此外,乳酸菌在改善奶酪质地、拉伸性、气孔形成以及抑制病原微生物生长等方面也发挥着重要作用[14-15]。除乳酸菌之外,奶酪中含有的其他细菌微生物群如丙酸杆菌、凝固酶阴性葡萄球菌、哈夫尼菌以及某些需氧放线菌等也有助于奶酪风味和颜色的形成[16-17]。高通量测序技术作为近年来新兴的分子生物学技术,已被广泛应用于土壤、食品及动物肠道等样本微生物多样性的研究[18],它能够对样品中复杂和低丰度的微生物群落进行全面覆盖,在属甚至种水平上分析微生物群落多样性[19];而传统培养法作为微生物鉴定的经典方法,可将分离出的微生物进行后续研究及应用。
伊犁传统奶酪属于自然发酵乳制品,其中蕴含的微生物种类繁多,目前采用高通量测序技术结合传统培养的方法研究奶酪中微生物多样性的报道相对较少[20],且很少有人对伊犁牧区手工奶酪中的微生物进行研究。因此,本研究在采用Illumina MiSeq高通量测序技术对奶酪中细菌多样性进行分析的基础上,结合传统培养法对奶酪中的乳酸菌进行分离鉴定,并根据其16S rRNA基因序列对其进行功能预测分析,旨在探明伊犁地区传统奶酪中微生物种类及其基因功能信息,为挖掘和保护其中的微生物资源提供保障,同时为评估传统奶酪的发全性提供理论基础。
1 材料与方法
1.1 材料与试剂
14 种奶酪样品分别采自新疆阿勒泰、北屯及额敏地区的牧民家,样品经无菌采样袋密封好后用4 ℃便捷式冰箱立即运往实验室贮存于-20 ℃冰箱,在24 h内进行实验。阿勒泰地区的奶酪样品编号为B6、B7、T1及T2,北屯地区的奶酪样品编号为B1、B2、B3及B4,额敏地区的样品编号为E1、E2、E3、E4、E5及E6。
MRS培养基、营养明胶培养基、醋酸铅培养基、硝酸盐培养基、半固体琼脂培养基 青岛海博生物技术有限公司;细菌DNA提取试剂盒 美国Biomiga公司;2×Taq Master Mix (Dye Plus) 南京诺唯赞生物科技有限公司;琼脂糖 莫班牙Biowest公司;Magnetic Soil And Stool DNA Kit试剂盒 天根生化科技(北京)有限公司。
1.2 仪器与设备
22331型高速冷冻离心机 德国Eppendorf AG公司;HP1020凝胶成像系统、T100型聚合酶链式反应(polymerase chain reaction,PCR)仪 美国Bio-Rad公司;CX23LEDRFS1C生物显微镜 奥林巴斯(广州)工业有限公司;LDZX-30KBS立式压力蒸汽灭菌器上海申发医疗器械厂。
1.3 方法
1.3.1 细菌多样性分析
采用Magnetic Soil And Stool DNA Kit试剂盒提取样品总DNA,每个样品3 个平行,利用NanoDrop2000型微量紫外分光光度计检测DNA的浓度及纯度。PCR扩增引物为:27F(5’-AGAGTTTGATCCTGGCTCAG-3’)和533R(5’-TTACCGCGGCTGCTGGCAC-3’),PCR体系为:4 μL 5×FastPfu Buffer,2 μL 2.5 mmol/L dNTPs,0.8 μL Forward Primer(5 µmol/L),0.8 μL Reverse Primer(5 µmol/L),0.4 μL FastPfu Polymerase,0.2 μL BSA,10 ng Template DNA补dd H2O至20 μL。程序如下:95 ℃预变性3 min,95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,循环数为27,72 ℃最终延伸10 min。扩增结束后,采用2%琼脂糖凝胶电泳检测扩增产物的纯度。使用凝胶回回试剂盒切胶回回PCR产物进行文库构建后,在Illumina MiSeq PE 300平台上进行高通量测序分析。参照田建军等[21]的方法进行数据分析及绘图,并运用PICRUSt软件对样品中的微生物进行16S rRNA功能预测分析。
1.3.2 乳酸菌多样性分析
1.3.2.1 菌株的分离、纯化
将奶酪置于无菌条件下用研钵将样品充分研碎并混匀,取适量研碎的样品置于50 mL MRS液体培养基中进行扩增培养,37 ℃培养24 h。吸取1 mL扩增培养液用生理盐水进行10 倍梯度稀释,每次稀释均需用移液枪把液体充分混匀并更换无菌枪头。分别吸取10-3~10-5梯度的稀释液100 μL稀释液均匀涂布于MRS培养基中,每个梯度做4 个平行,于37 ℃恒温培养箱中培养48 h。挑取不同形态的菌落进行划线培养,重复划线多次,直至用显微镜观察至纯种,记录其菌落、细胞形态。将纯化后的乳酸菌用50%甘油-菌液(1∶1,V/V)于-80 ℃冰箱保存备用。
1.3.2.2 生理生化实验鉴定
样品中乳酸菌的生理生化鉴定实验按照文献[22-23]的方法,包括:菌落及细胞形态的观察、过氧化氢实验、革兰染色实验、明胶液化实验、硫化氢实验、硝酸盐还原实验、运动性实验、耐盐性实验、pH 4.5生长实验以及糖发酵实验。
1.3.2.3 16S rDNA测序鉴定
采用美国Biomiga公司的细菌gDNA提取试剂盒分离菌株基因组DNA,具体步骤按照说明书进行,使用微量核酸定量仪检测基因组D N A浓度以及纯度(OD260nm/OD280nm)。扩增引物为27F(5’-AGAGTTTGATMTGGCTCAG-3’),1492R(5’- TACGGYTACCTTGTTACGACTT-3’)。PCR扩增体系(50 μL)及条件:上下游引物各2.0 μL,模板2.0 μL,2×TaqMaster Mix 25 μL,Nuclease-free Water 19 μL。PCR扩增循环参数为:95 ℃预变性5 min,94 ℃变性30 s,52 ℃退火30 s,72 ℃延伸30 s,循环30 次,72 ℃最终延伸5 min,-20 ℃保存。取5 μL的PCR产物加入到1%的琼脂糖凝胶(含0.01%的goldviewII型核酸染色剂)点样孔中,在电压100 V、电流90 mA、电泳液为1×TAE缓冲液中电泳40 min。将符合测序要求的PCR产物寄往测序公司进行测序操作,所得序列在NCBI中进行BLAST比对,将测序菌株与模式菌株同源性大于99%的序列利用MEGA 7.0软件构建系统发育树,数据自展重抽样次数1 000 次。
2 结果与分析
2.1 奶酪中细菌多样性分析
2.1.1 细菌序列信息及α多样性
常用到的α多样性指数包括丰富度指数(Sobs指数、Chao1指数)、多样性指数(Simpson指数、Shannon指数)以及群落覆盖度指数Coverage等[24]。本研究中所得到的奶酪样品序列信息及α多样性指数如表1所示,14 份奶酪样品共得到的细菌原始序列为561 955 条,质控过滤后得到的有效序列为545 560 条。在物种丰度上,阿勒泰地区T2样品的Sobs和Chao1指数最大,说明其细菌数目最多,且与其他样品差异显著;阿勒泰地区B7和额敏地区E2样品的Sobs和Chao1指数较小,其细菌数目较少,B7与E2样品的Sobs指数无显著差异,但其Chao1指数存在显著差异。在物种多样性上,样品T2的Simpson指数最小,Shannon指数最大,说明其细菌多样性最高,且与其他样品有显著差异;样品B7的Simpson指数最大,Shannon指数最小,说明其细菌多样性最低。14 份样品的Coverage指数均接近于1,说明样品中的序列基本都被完全测出,测序结果能够充分反映样品中的细菌多样性,但B7样品的Coverage指数与其他样品差异显著。

表1 14 份奶酪样品的序列信息及α多样性指数Table 1 Sequence information and α diversity values of 14 traditional cheeses samples
2.1.2 细菌群落结构分析
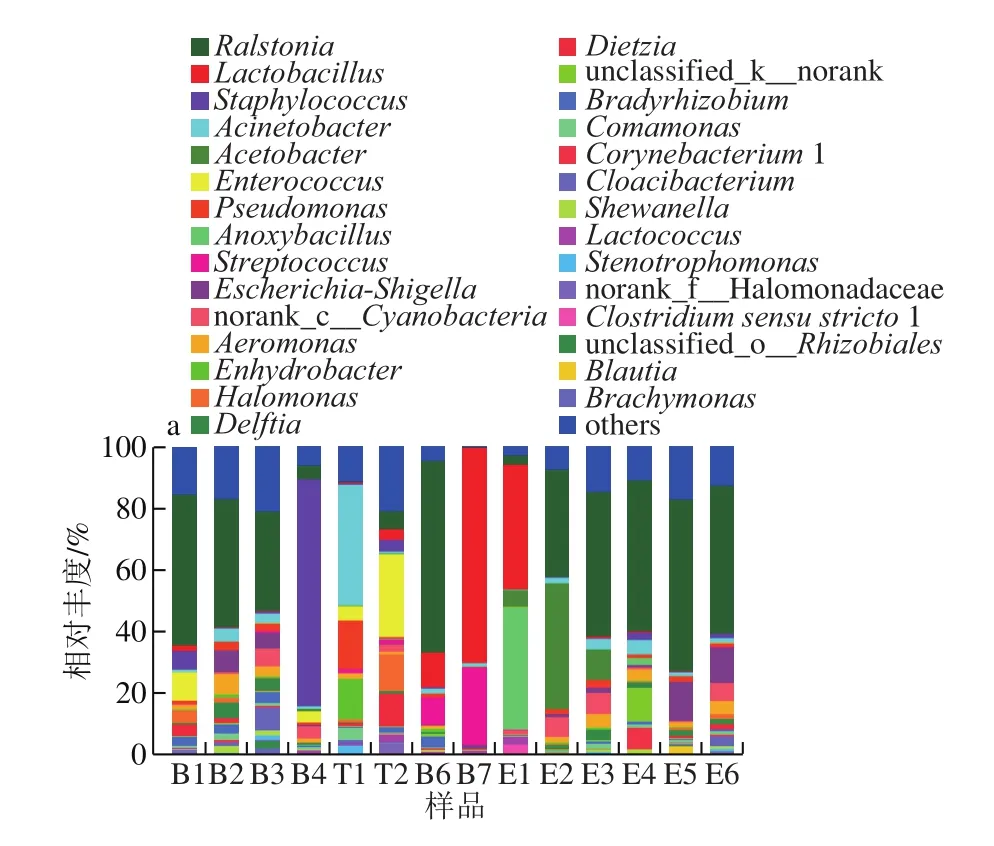

图1 属(a)和种(b)水平下的细菌群落组成Fig. 1 Relative abundance of bacteria at genus (a) and species (b) levels from all cheese samples
在细菌属水平上(图1a),14 份奶酪共测出29 种相对丰度大于2%的属,相对丰度排名前10的细菌属依次雷尔氏菌属(Ralstoniaspp. 30.41%)、乳杆菌属(Lactobacillusspp. 9.17%)、葡萄球菌属(Staphylococcusspp. 6.32%)、不动杆菌属(Acinetobacterspp.4.62%)、醋酸杆菌属(Acetobacterspp. 3.98%)、肠球菌属(Enterococcusspp. 3.15%)、厌氧芽孢杆菌属(Anoxybacillusspp. 2.96%)、志贺氏菌属(Escherichia-Shigellaspp. 2.92%)、norank_c__Cyanobacteria(2.67%)、链球菌属(Streptococcusspp.2.61%),这与Dalmasso等[25]报道的Ralstoniaspp.在奶酪中并不常见或者含量极低(0.01%~0.000 1%)的结果并不一致。目前,关于Ralstoniaspp.在食品中存在的报道并不多,Soto等[26]利用高通量测序技术研究驴奶中的细菌多样性时,发现其中的优势细菌属为Pseudomonasspp.、Ralstoniaspp.、Acinetobacterspp.,由于伊犁传统手工奶酪制作过程中没有添加外源发酵剂,因此考虑奶酪中的Ralstoniaspp.可能来源于原料乳。Selvasankar等[27]利用高通量测序技术分析了墨莫哥奶酪中的细菌群落,结果发现Streptococcusspp.、Lactococcusspp.、Lactobacillusspp.、Aerococcusspp.和Weisellaspp.是主要菌群,本研究与其相同之处在于奶酪中均存在Streptococcusspp.、Lactobacillusspp.、Weisellaspp.、Lactococcusspp.,而未发现Aerococcusspp.;这说明上述共同菌群是大部分传统手工奶酪中的常见菌种,但由于制作手法及气候条件的不同可能会导致奶酪中的微生物群落结构有所差异。
在细菌种水平上(图1b),14 份奶酪共测出39 种相对丰度大于2%的种,大部分都属于unidentified(24.38%)、unclassified(16.75%)和uncultured(10.63%),能准确鉴定到种的只有瑞士乳杆菌(L. helveticus3.06%)、苹果醋杆菌(Acetobacter malorum3.01%)、大肠埃希氏杆菌(Escherichia coli2.97%)、粪肠球菌(Enterococcus faecalis1.64%)、Halomonas desiderata(1.54%)、埃氏慢生根瘤菌(Bradyrhizobium elkanii1.38%)、皮特不动杆菌(Acinetobacter pittii1.33%)、产碱假单胞菌(Pseudomonas alcaligenes1.18%)、巴氏醋杆菌(Acetobacter pasteurianus1.01%)、琼氏不动杆菌(Acinetobacter junii0.71%)、赫曼尼肠球菌(Enterococcus hermanniensis0.4%)、Acinetobacter tandoii(0.21%)。HTS结果显示出奶酪样品中的优势乳酸菌种为L.helveticus,且大部分存在于额敏地区的E1样品中,说明不同地区或不同样品中的优势菌种存在明显差异[28]。本研究结果显示出Illumina MiSeq测序技术在种水平上的鉴定能力较差,无法将大多数微生物鉴定到种水平,这与陈泽斌等[29]的描述结果一致。
2.1.3 不同样品细菌群落组成差异
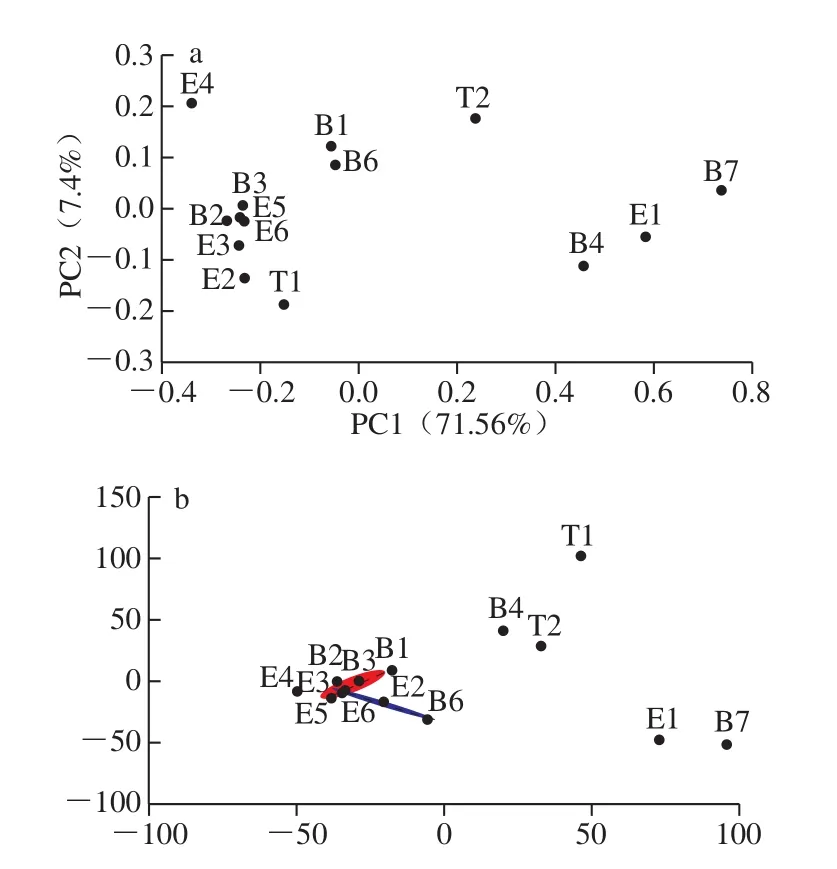
图2 基于Weighted UniFrac的不同样品PCoA图(a)及样本菌群分型分析图(b)Fig. 2 PCoA plot (a) and bacterial classification plot (b) of cheese samples at genus level based on weighted UniFrac
14 份奶酪样品尽管其原材料均为牛奶且制作过程中也均未添加任何外源发酵剂,但由于其制作工艺、生产温度及奶源本身微生物种类的差异[30]等原因,14 份奶酪的细菌群落组成也会有所差异。从PCoA图(图2a)可以看出,14 份奶酪样品的细菌群落组成大致可以分为2 个类型:其中B2、B3、E5和E6样品在图中的分布较为集中,说明这4 份样品的细菌群落结构较为相似。结合图1a可以看出,这4 个样品都含有丰度较大的Ralstonia spp.,且其菌群组成及相对丰度差异也都较小。另外10 个样品在图中的分布较为分散,说明这10 个样品的细菌群落结构差异较大。这10 个样品中虽然B1、B6、E2、E3及E4样品的优势菌群均为Ralstonia spp.,B7和E1的优势菌群为Lactobacillus spp.,但其他菌群组成及相对丰度差异较大;其余3 个样品的优势菌群不仅各有不同,而且其他菌群组成及相对丰度也都差异较大(图1a)。
从样本菌群分型分析图(图2b)可以看出,14 份奶酪样品根据其菌群组成的不同可以分为2 个大型类群和6 个小型类群。2 个大型类群中B1、B2、B3、E3、E5及E6聚成了一个类群且于E4的距离较近,E2和B6聚成了另外一个类群但与B1形成的类群具有重叠之处。结合图1可以看出,B1、B2、B3、B6、E2、E3、E4、E5及E6样品中的优势菌群均为Ralstonia,但B6和E2除含有丰富的Ralstonia,其余菌群组成和丰度都与其他样品存在差异,故E4与B1形成的类群之间的距离较近,而B6与E2单独形成了一个类群。其余5 个样品形成的5 个单独类群不仅优势菌群各不相同而且菌群组成差异较大,故在图中各自形成了单独类群且距离较远。
2.1.4 不同地区样品细菌种类差异分析
不同地区样品中的微生物组成会随着地域环境及样品制作方法的不同而有所差异[31]。本研究利用Venn图对3 个地区样品中所含有的微生物种类在属和种水平上进行比较分析,结果显示不同地区样品中存在的微生物种类差异较为明显。在细菌属水平上(图3a),额敏、阿勒泰和北屯3 个地区14 份样品中所含有的细菌总数为493 种,其中3 个地区特有的细菌种数依次为62、171、60 种,共有的细菌种数为100 种,占细菌总数的12.6%。在细菌种水平上(图3b),3 个地区所含有的细菌总数为780 种,其中额敏、阿勒泰和北屯地区特有的乳酸菌种类依次为102、320、124 种。综上可知,在属和种两个分类学水平上,阿勒泰地区奶酪中的微生物种类最为丰富,而额敏地区奶酪中的微生物种类较少。Jin Hao等[32]利用PacBio测序技术研究了来自Buryatian 7 份手工奶酪中的细菌多样性,结果显示7 份奶酪共存在82 个细菌属和145 个细菌种,优势细菌属为Lactococcus(51.46%)和Streptococcus(17.81%),这与本研究结果不同,本研究结果揭示了伊犁手工奶酪中的微生物群落组成更为复杂,其原因可能是伊犁手工奶酪生产环境中的微生物群落较为复杂[33]且这些微生物也适于在奶酪中生存。
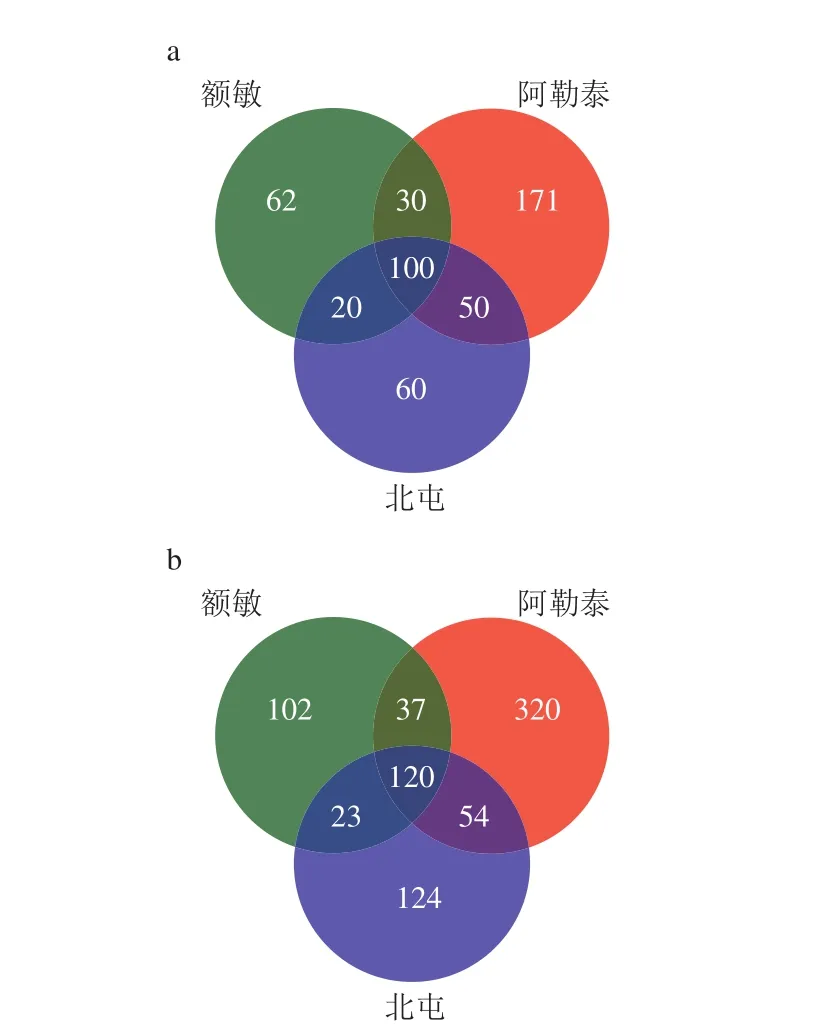
图3 不同地区样品在属(a)和种(b)水平下细菌种类Fig. 3 Bacterial species at genus (a) and species (b) levels in samples from different regions
2.2 乳酸菌多样性分析
2.2.1 乳酸菌形态学观察
从MRS培养基中分离出68 株疑似乳酸菌,其中有20 株球菌(29.4%)、48 株杆菌(70.6%)。在MRS固体培养基上为乳白色或微黄色,部分透明,边缘规则或齿状,圆形隆起或扁平且大部分表面光滑。革兰染色发现均为阳性、过氧化氢均为阴性,细胞形态为球状或杆状,呈单个、成对或链状排列(图4)。

图4 不同乳酸菌的菌落形态(a)及革兰染色后的细胞形态(b)Fig. 4 Colony morphology (a) and cell morphology (b) of different lactic acid bacterial strains
2.2.2 乳酸菌的生理生化鉴定及16S rRNA基因同源性分析
如表2所示,68 株乳酸菌均为革兰氏阳性、过氧化氢阴性菌,能在pH 4.5、0% NaCl、4.5% NaCl和6.5% NaCl的环境中生长,能发酵葡萄糖、麦芽糖;都不能液化明胶、不能还原硝酸盐、无运动性、不能在10% NaCl、无碳源的环境中生长且不能利用淀粉作为碳源。在硫化氢实验中,只有2 株融合魏斯氏菌(Weissella confusa)能够产生硫化氢,使醋酸铅培养基变成黑色。短乳杆菌(Lactobacillus brevis)和大部分融合魏斯氏菌能够发酵葡萄糖产气,其余菌株能发酵葡萄糖但不产气。在糖发酵实验中,68 株乳酸菌中有2 株瑞士乳杆菌(Lactobacillus helveticus)不能利用七叶灵、核糖,2 株短乳杆菌不能利用半乳糖、1 株融合魏斯氏菌不能利用果糖。大多数菌株都能够发酵苦杏仁苷、纤维二糖、甘露醇、乳糖、甘露糖、水杨苷、蔗糖、蕈糖、阿拉伯糖、糊精,不能发酵蜜二糖、山梨醇、松三糖、棉籽糖、木糖等。所有乳酸菌中瑞士乳杆菌能够利用的糖类最少,植物乳杆菌能够利用的糖类最多,其余菌种可利用的糖类也都有所差别。
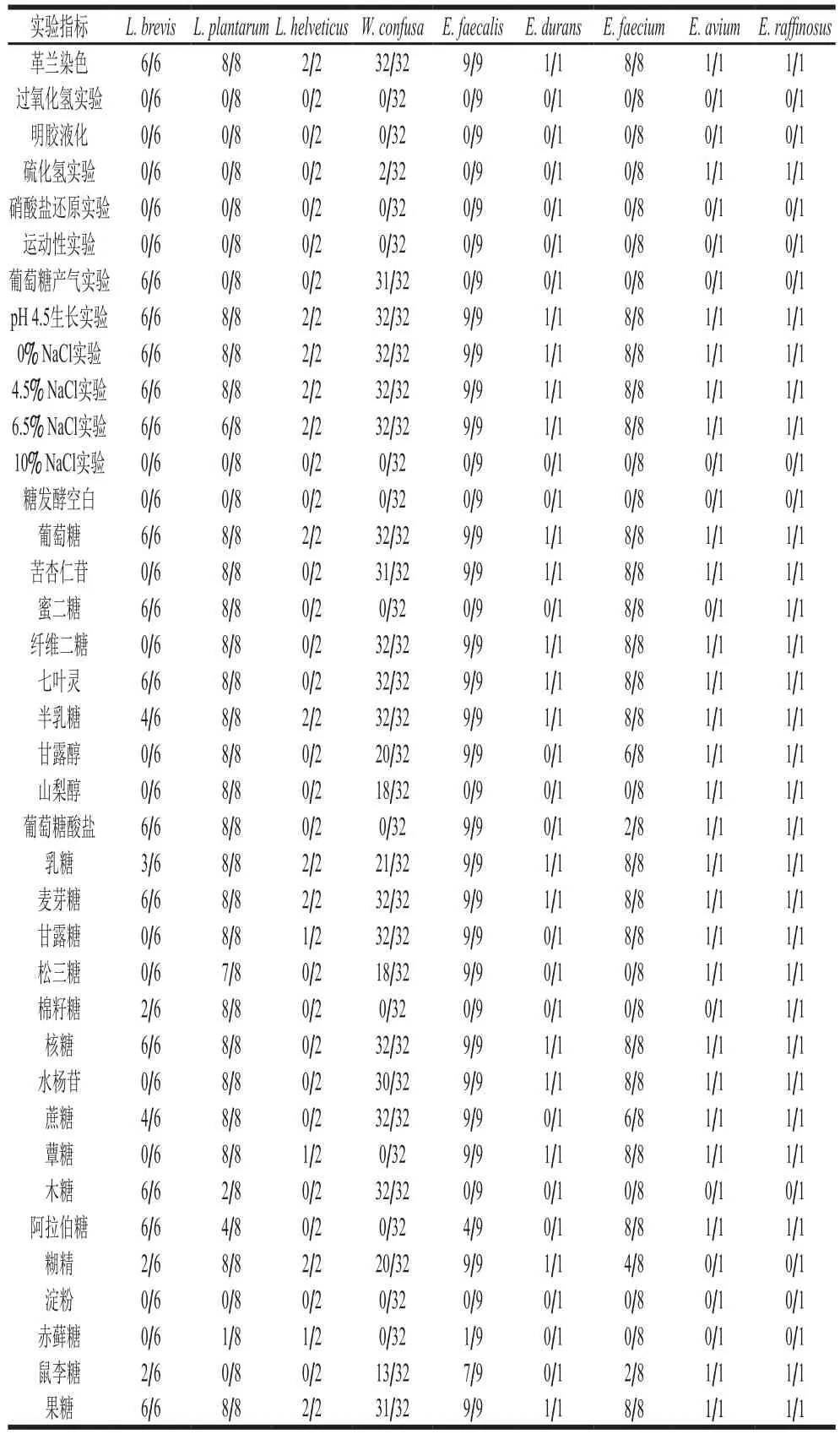
表2 68 株乳酸菌的生理生化特性Table 2 Physical and chemical properties of lactic acid bacteria isolated from cheese samples

图5 本研究分离的乳酸菌与相近类群的系统发育树Fig. 5 Phylogenetic tree of lactic acid bacteria isolated in this study and their related groups
将68 株乳酸菌的16S rRNA基因序列输入到在线的EzBioCloud数据库中进行相似性搜索,以序列相似性大于等于98.7%为同种标准归类,下载相似性最高的模式菌株序列与测序序列利用MEGA7.0软件构建系统发育树(图5)。本研究根据16S rRNA基因序列鉴定结合生理生化实验结果,将68 株乳酸菌归为3 属9 种,其中T2-2等32 株菌为融合魏斯氏菌、B4-4为耐久肠球菌(Enterococcus durans)、B4-5为鸟肠球菌(Enterococcus avium)、E1-5和E3-3为瑞士乳杆菌、B1-8等8 株菌为屎肠球菌(Enterococcus faecium)、B2-10等6 株菌为短乳杆菌、E6-2等8 株菌为植物乳杆菌(Lactobacillus plantarum)、B4-6为棉籽糖肠球菌(Enterococcus raffinosus)、B4-1等9 株菌为粪肠球菌(E. faecalis)。Domingos-Lopesa等[34]从Azores地区的12 份手工“Pico”奶酪中分离出了114 株乳酸菌,其中属于Enterococcus和Lactobacillus属的乳酸菌种类最为丰富,这与本研究的结果较为一致,其原因可能为本研究所选择的手工奶酪与“Pico”奶酪均为手工制作且没有添加任何外源发酵剂。
2.2.3 不同地区可培养乳酸菌差异分析
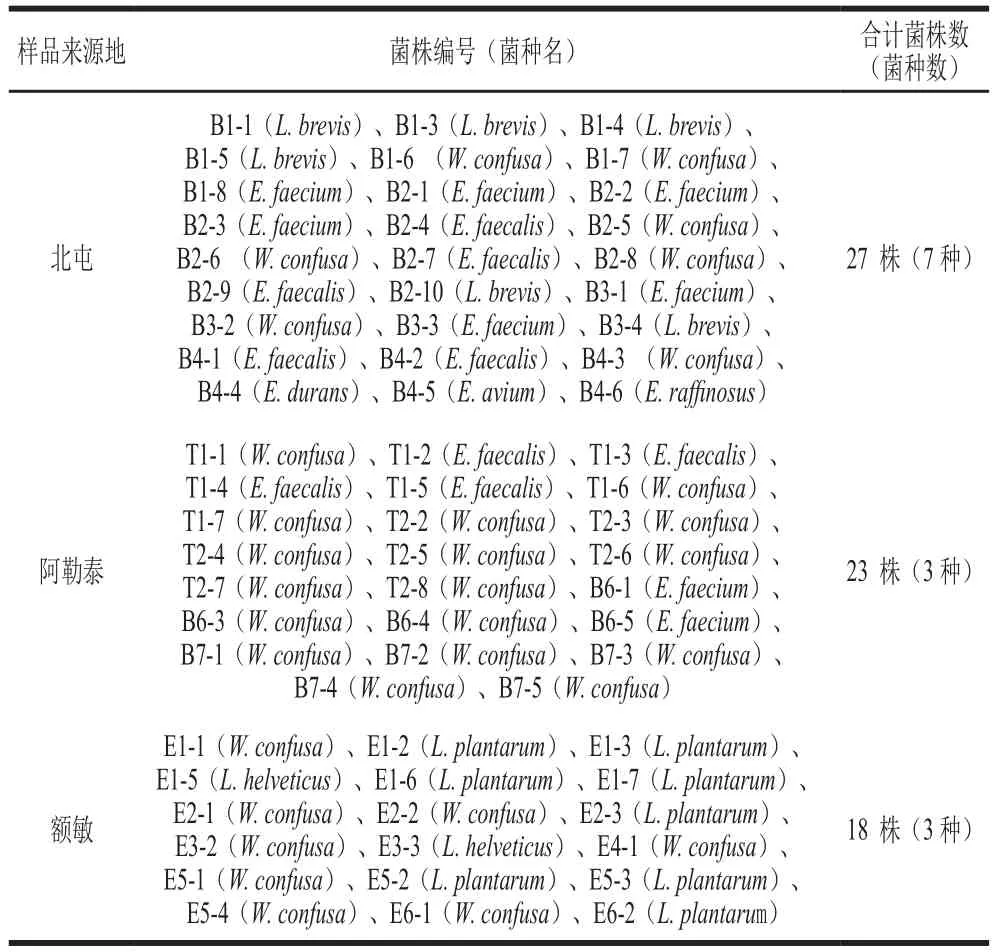
表3 不同地区分离到的乳酸菌信息统计Table 3 Statistics of lactic acid bacteria isolated from cheeses from different areas
从表3可以看出,北屯地区分离到的乳酸菌种类最为丰富,阿勒泰及额敏地区样品中所含有的乳酸菌种类较为贫乏。3 个地区所分离到的乳酸菌种类各不相同,其中北屯地区的样品中含有4 种特有乳酸菌(L. brevis、E. durans、E. avium、E. raffinosus),额敏地区的样品中含有2 种特有乳酸菌(L. plantarum、L. helveticus),而阿勒泰地区的样品中没有独特的乳酸菌种,可能是奶酪原料、成熟度、制作手法以及地理位置不同所致[28]。
2.3 不同方法在乳酸菌鉴定上的比较分析
利用Illumina MiSeq测序技术及传统培养法对14 份奶酪中鉴定出的乳酸菌进行比较分析,可以看出两种方法在乳酸菌的属种鉴定上存在明显差异(表4)。在属水平上,Illumina MiSeq测序技术鉴定出了5 类乳酸菌,传统培养法只分离出了3 类乳酸菌,但测序法未能鉴定出Weissella,传统培养法未分离出Lactococcus及Streptococcus。其原因可能为本研究的测序结果只呈现出了相对丰度大于2%(图1)的细菌属,而Weissella在奶酪中的含量可能低于2%;传统培养法由于人为去重及培养条件等原因仅能检测到易培养及优势菌的情况[35],从而未能将奶酪中的乳酸菌进行全部分离。在种水平上,传统培养法能够鉴定出更多的乳酸菌,高通量测序技术由于在种水平上的鉴定能力较弱[36],故鉴定出的乳酸菌种类较少。

表4 不同方法在属和种水平上鉴定到的乳酸菌种类Table 4 Statistics of lactic acid bacteria identified by two different methods at genus and species levels
2.4 样品微生物基因功能预测分析
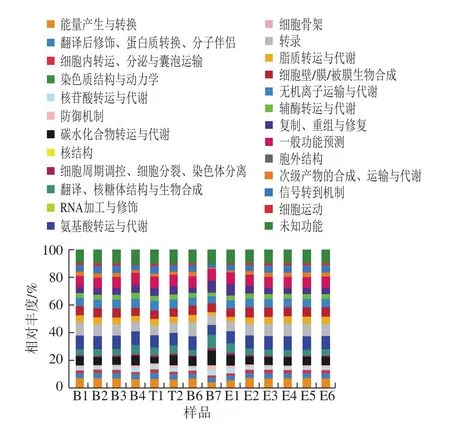
图6 COG功能预测分析图Fig. 6 COG function prediction
奶酪中的细菌类型可以调节奶酪在成熟过程中的风味产生,并且与基因组编码的代谢多样性直接相关[37]。根据COG数据库的信息,从eggNOG数据库中解析到各个COG的描述信息及其功能信息,得到的功能预测丰度如图6所示,14 份样品得到的COG功能预测信息组成基本相同,但丰度差异比较明显。奶酪中微生物一部分丰度较高的基因参与到未知功能和一般功能这两个COG分类中,其余基因大多与氨基酸(9.35%)、碳水化合物(6.49%)和脂质(4.57%)代谢、转录(8.28%)以及能量转换(6.86%)有关,这与前人的研究结果具有相似性,表明在奶酪微生物基因组中包含大量参与蛋白质与碳水化合物代谢有关的基因[38],这些化合物的代谢必然伴随着转录以及能量的产生与转换,从而图中也显示出奶酪中含有较高丰度的与转录、能量转换相关的基因。14 份样品的微生物群落组成虽存在明显差异(图1),但每个样品所具有的基因功能一致,只是丰度有所不同,其原因可能为不同菌群所具有的基因功能具有相似性[39-40]。
3 结 论
本研究采用分子生物学技术和传统培养相结合的方法研究了新疆伊犁14 份传统手工奶酪中的乳酸菌及细菌多样性。高通量测序结果揭示Lactobacillus spp.为奶酪中的优势乳酸菌属且手工奶酪中还存在着一些植物性致病菌(如Ralstonia)和动物性致病菌(如Staphylococcus);传统培养法结果表明伊犁手工奶酪中的优势乳酸菌种为W. confusa,优势乳酸菌属为Lactobacillus和Enterococcus。PICRUSt分析发现奶酪中菌群最主要的已知功能为氨基酸转运与代谢,即奶酪中大部分细菌与氨基酸转运蛋白及酶的生成有关,改变奶酪中的菌群结构可能会对这些代谢过程产生影响,从而影响奶酪的感官品质。高通量测序技术能将大多数微生物鉴定到“属”的水平,无法将大多数微生物鉴定到“种”水平;而传统培养结合生理生化及16S rRNA基因测序技术可将乳酸菌准确鉴定到种,但很难对样品中的乳酸菌进行全面分离鉴定。因此,两种方法的结合可以更全面地揭示奶酪中的微生物组成,为奶酪的工业化生产提供基础数据,同时对16S rRNA序列进行功能预测分析有利于为今后研究菌群功能奠定理论基础。
