HPLC-DAD法同时测定冠心康胶囊中4种活性成分的含量
2020-01-03黄洁文陈燕霞谭汉添
黄洁文,陈燕霞,谭汉添
0 引言
冠心康胶囊是由丹参、赤芍、降香、红花和川芎等药材组成,目前的执行标准为国家食品药品监督管理局标准YBZ06522009,具有活血化瘀,行气止痛等作用,临床主要用于血瘀气滞、心脉痹阻引起的冠心病、心绞痛等症状[1-4]。丹参中的脂溶性成分隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA具有舒张冠脉和动脉、保护心肌、抗氧化的作用[5-7],赤芍中的芍药苷也具有明显的扩张心血管、改善微循环的作用[8-10],二者的作用与其临床药效作用一致,但是现行标准仅对赤芍中的芍药苷进行含量控制,对丹参只进行薄层鉴别,没有对其含量进行质量控制。冠心康胶囊处方中,丹参用量最大,且为方中君药,在该方的活血化瘀药效中发挥重要作用。目前,对冠心康胶囊的研究主要是针对赤芍中芍药苷或者丹参中丹参酮ⅡA的单个含量测定[11-12],尚未有对其多成分含量的同时测定,因此,笔者参考中国药典和目前的文献报道[13-16],建立HPLC-DAD色谱法同时测定冠心康胶囊中芍药苷、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量的方法,来更好地全面控制冠心康胶囊的质量,为其进一步完善质量标准提供实验参考。
1 仪器与试药
LC-2030高效液相色谱仪(日本岛津仪器公司);LC labsolution 工作站;SPD-M10A检测器,Mettler AE240分析电子天平(瑞士梅特勒-托利多公司);KQ-700VDB型双频数控超声波清洗器(江苏昆山超声仪器公司);冠心康胶囊(西安大唐制药集团有限公司,规格:0.45 g/粒,批号:20170601、20170802、20180601),对照品:芍药苷(批号:110736-201136,质量分数95.7%),隐丹参酮(批号:110852-200305),丹参酮ⅡA(批号:110766-200619,质量分数98.9%);丹参酮Ⅰ(批号:110867-201607,含量为99.3%),对照品均购于中国食品药品检定研究院,乙腈为色谱纯(美国Fisher公司),水为超纯水(美国Mili-Q超纯水机);磷酸、甲醇等均为分析纯(上海国药集团化学试剂公司)。
2 方法与结果
2.1 色谱条件 Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm);流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱0~12 min(15%~20%A),12~20 min(20%~40%A),20~30 min(40%~60%A),30~50 min(60%~90%A);流速:1.0 ml/min;柱温:30 ℃;检测波长:230 nm(0~30 min)、270 nm(30~55 min),进样量:10 μl。在上述色谱条件下分别测定对照品、供试品溶液及阴性样品溶液,色谱图见图1。
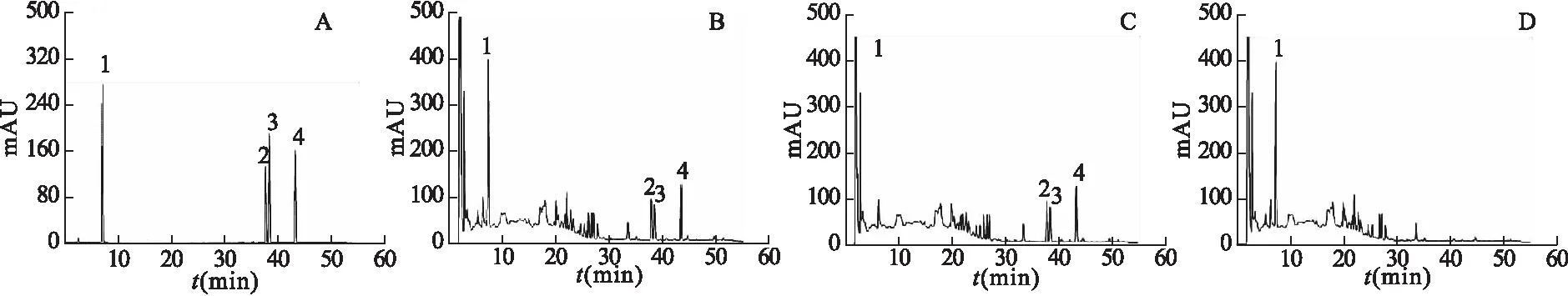
图1 混合对照品(A)、供试品溶液(B)、缺赤芍的阴性样品(C)、缺丹参药材的阴性样品(D)的HPLC色谱图
2.2 对照品溶液的制备 精密称取芍药苷对照品12.28 mg,置25 ml容量瓶中,加甲醇稀释至刻度,作为对照品储备溶液Ⅰ,精密称取丹参酮ⅡA 5.15 mg和隐丹参酮5.09 mg置同一25 ml棕色容量瓶中,加甲醇稀释至刻度,作为对照品储备溶液Ⅱ,另精密称取丹参酮Ⅰ对照品5.94 mg,置10 ml棕色容量瓶中,加二氯甲烷1 ml使溶解,然后用甲醇稀释至刻度,作为对照品储备溶液Ⅲ,分别精密吸取上述对照品储备溶液I 5 ml、储备溶液Ⅱ 2 ml、储备溶液Ⅲ 1 ml置同一10 ml棕色容量瓶中,加甲醇稀释至刻度,作为对照品溶液(每1 ml含芍药苷245.6 μg、隐丹参酮40.72 μg、丹参酮Ⅰ 59.4 μg、丹参酮ⅡA 41.2 μg)。
2.3 供试品溶液的制备 取冠心康胶囊10粒,混匀研细,精密称取粉末1.0 g置具塞锥形瓶中,精密加入甲醇25 ml,称定重量,超声处理30 min(频率:45 kHz,功率:280 W),取出,放冷,用甲醇补足减失的重量,摇匀,用0.45 μm的微孔滤膜滤过,取续滤液作为供试品溶液。
2.4 阴性样品的制备 按照冠心康胶囊处方量的1/10,分别制备缺丹参药材和赤芍药材的阴性样品,按照“2.3”项下的供试品溶液制备方法制备,按照“2.1”项的色谱条件测定,测定结果见色谱图1,结果表明,阴性样品对冠心康胶囊中4种成分的测定无干扰。
2.5 标准曲线的测定 将“2.2”项下的对照品混合溶液作为5号对照品溶液,另分别精密吸取“2.2”项下的对照品溶液各1 ml,分别置10、25、50 ml和100 ml 4个容量瓶中,加甲醇稀释至刻度,作为对照品4号、3号、2号和1号溶液,分别注入液相色谱仪,按照“2.1”项下的色谱条件进行测定,以待测成分进样量的质量(ng)为横坐标,相对应的峰面积为纵坐标进行线性回归,结果见表1。

表1 4种成分的线性方程、相关系数及线性范围
2.6 精密度 取“2.2”项下的对照品储备溶液,连续进样6次,进样量10 μl,测定各成分的峰面积,分别计算得芍药苷峰面积RSD为0.36%,隐丹参酮峰面积RSD为0.52%,丹参酮Ⅰ峰面积RSD为0.41%。丹参酮ⅡA峰面积RSD为0.66%,结果表明,该仪器的精密度良好。
2.7 稳定性和重复性试验 稳定性:取同一批供试品溶液,分别在0、1、2、4、8、12、16、24 h进行测定,进样量10 μl,连续考察24 h,记录各成分的色谱峰面积,结果显示,芍药苷、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的峰面积RSD为1.22%、1.05%、1.56%、1.37%,表明供试品溶液在24 h内稳定性良好。重复性试验:取同一批号的冠心康胶囊样品,按照“2.3”项下的方法制备6份供试品溶液,然后分别注入液相色谱仪进行测定,进样量10 μl,结果显示,芍药苷峰含量的RSD为0.40%,隐丹参酮含量的RSD为0.36%,丹参酮Ⅰ含量的RSD为1.21%。丹参酮ⅡA含量的RSD为0.31%,表明该方法的重复性良好。
2.8 加样回收率试验 精密称取已知含量的冠心康胶囊样品0.50 g,共6份,另精密称取芍药苷42.26 mg,置10 ml量瓶中,精密吸取丹参酮Ⅰ对照品储备溶液5 ml置上述同一10 ml量瓶中,加甲醇稀释至刻度,作为待加溶液1。精密称取丹参酮ⅡA 18.13 mg和隐丹参酮6.03 mg置同一25 ml量瓶中,加甲醇稀释至刻度,作为待加溶液2。分别精密吸取上述待加溶液1和待加溶液2各1 ml置上述6份供试品中,按照“2.3”项下方法制备供试品溶液,按照“2.1”项下色谱条件进行含量测定,分别计算4个成分的回收率,结果见表2。结果显示,RSD均小于3.0%,表明该方法准确度良好。

表2 4个成分的加样回收率结果(n=6)
2.9 样品的测定 取3个不同批号的冠心康胶囊样品,按照“2.3”项下供试品溶液的制备方法,每个批号分别制备3份,用“2.1”项下的色谱条件进行测定,结果求平均值,分别计算不同批次样品中4个成分的含量,测定结果见表3。

表3 4种成分含量测定结果(n=3,mg/g)
3 讨论
3.1 供试品制备的选择 本实验采用正交实验对不同的提取溶剂(甲醇、50%甲醇、70%乙醇)对供试品溶液制备方法、不同的超声时间(20、30、40 min)和不同的超声功率(120、280、320 W)进行考察,结果发现,不同溶剂对不同组分含量的影响较大,对超声功率和时间基本影响不大,故选择超声时间30 min和频率280 W。由于甲醇提取时隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的含量较大,50%甲醇提取时,丹参酮Ⅰ和丹参酮ⅡA的含量都下降50%;70%乙醇提取时,芍药苷的含量稍大,丹参酮Ⅰ含量依旧比较低。由于处方中丹参占比较大,丹参中所测成分较多,且为方中主药,综合考虑选择甲醇作为提取溶剂。
3.2 流动相和检测波长的选择 实验分别采用乙腈-水、甲醇-0.1%磷酸、乙腈-0.1%磷酸,对流动相进行了考察。结果显示,甲醇-0.1%磷酸作为流动相时,出峰时间较长,芍药苷峰形较差,乙腈-水和乙腈-0.1%磷酸作为流动相均可以洗脱分离,基线平稳。但是乙腈-水作为流动相,芍药苷峰形有拖尾现象。当采用乙腈-0.1%磷酸作为流动相时,色谱峰形良好,对称因子较高,拖尾现象明显减少,最后确定乙腈-0.1%磷酸作为本实验的流动相系统。同时,本实验采用DAD检测器对4个共有峰进行光谱扫描,结果显示,芍药苷在230 nm下具有最大吸收,隐丹参酮在265 nm、丹参酮Ⅰ在246 nm、丹参酮ⅡA在270 nm下具有最大吸收。笔者分别比较了230、250、270 nm下的结果,结果显示,在230 nm下芍药苷含量最高,270 nm下隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量之和最高,并与药典中检测波长一致,因此,本实验选择变化波长进行测定,从而保证各成分的灵敏度最高。
3.3 结果的判定 现行标准中规定,芍药苷的含量为每粒不得少于2.6 mg。本实验建立的3批样品中,芍药苷的含量折算成每粒均大于2.6 mg,均符合规定。丹参药材在处方中占35.29%,2015年版《中国药典》一部项下规定丹参药材中含丹参酮Ⅰ、隐丹参酮和丹参酮ⅡA的总量不得少于0.25%,折算后本品每粒应不得少于0.397 mg,转移率按40%计算,本品每粒含3种丹参酮类化合物的总量应不得少于0.159 mg,本实验所测3批样品含量均符合规定。
3.4 小结 本文建立了HPLC-DAD法同时测定冠心康胶囊中芍药苷、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA 4种成分含量的方法,比现行标准中仅通过芍药苷的含量进行控制更加全面,更能有效反映药品的质量,该方法经方法学验证,具有专属性强、准确度高的优点,可以用于冠心康胶囊中4种成分的含量测定。
