机械牵拉对大鼠骨骼肌卫星细胞的增殖作用及其途径的研究
2020-01-03陆耀飞
杨 璐,陆耀飞
(上海体育学院 运动科学学院, 上海200438)
骨骼肌损伤是运动中常见的运动性损伤疾病,以疼痛、局部肿胀、肌张力降低、功能障碍为主要表现。在运动引起的损伤中,骨骼肌损伤的发生率为10%~55% 不等,由于骨骼肌再生能力有限,导致自然修复效果不佳,严重影响患者的生活质量(Herridge et al.,2003)。因此,提高肌肉恢复能力和改善肌肉损伤后的治疗方法具有重要的临床价值。
骨骼肌卫星细胞作为肌源干细胞已被广泛研究。骨骼肌的损伤修复依赖于骨骼肌卫星细胞的激活、增殖、分化。有研究者发现,运动能够激活骨骼肌卫星细胞并且促进其增殖(Pallafacchina et al.,2013)。机械牵拉作为模拟运动的一种方式,近年来已被应用于骨骼肌卫星细胞的研究。有研究表明,机械牵拉能够促进骨骼肌卫星细胞的激活和增殖(Kook et al.,2008),抑制分化(史仍飞等,2012),并且与牵拉程度存在相关性。然而,机械牵拉对骨骼肌卫星细胞的调节机制尚未阐述清楚。因此,本实验通过离体培养骨骼肌卫星细胞,研究机械牵拉对骨骼肌卫星细胞增殖的作用,初步探究可能的作用途径,为骨骼肌损伤修复及细胞肥大过程提供理论依据。
1 研究对象与方法
1.1 实验动物
SPF 级雄性 SD 大鼠 2 只,2~3 周龄,体重 90 g,由上海实验动物研究中心提供,SCXK(2013-0016)。
1.2 主要实验试剂
DMEM 培养液(Gibco)、胎牛血清(Gibco)、马血清(Gibco),青霉素、链霉素(Amresco)、Ⅱ型胶原酶(Sigma)、胰酶(Gibco)、CCK-8 试剂盒(日本同仁堂)、α 横纹肌肌动蛋白(武汉博士德)、SABC 试剂盒(武汉博士德)、DAB试剂盒(武汉博士德)。
1.3 骨骼肌卫星细胞原代培养
10% 的水合氯醛以0.4 ml/100 g 的剂量腹腔注射麻醉大鼠,约5 min 后,待其疼痛反射和角膜反射均消失后,浸泡至75% 的酒精中,2 min 后,仰卧位固定大鼠。在无菌条件下分离双侧腿部比目鱼肌、腓肠肌和背部肌肉。去除筋膜、血管、脂肪等组织,充分剪碎至1 mm3。在剪碎的肌肉中加入0.1%Ⅱ型胶原酶30 ml,在37℃条件下搅拌器搅拌 1 h,1 000 转/分离心 15 min 后,弃上清。再加入 0.25%胰酶30 ml,37℃消化15 min,胎牛血清终止消化,1 000 转/分离心15 min,弃上清。加入种植培养液吹打混匀,依次通过100 目、200 目、400 目细胞筛过滤。接种于未经多聚赖氨酸包被的培养瓶中,置于37℃,5%CO2,100% 空气湿度的培养箱中培养。2 h 后将培养瓶中的细胞悬液置于未经多聚赖氨酸包被的培养瓶中。2 h 后,将第一次差速贴壁完的细胞接种于经多聚赖氨酸的包被的培养瓶中,24 h后首次换液,之后每2 天换1 次液。
1.4 骨骼肌卫星细胞传代培养
吸出培养瓶中的培养液,PBS 清洗2 次,弃去PBS。加入0.25% 胰蛋白酶2 ml,37℃消化2 min,并用巴氏吸管充分吹打瓶壁,待大部分细胞从瓶壁上脱落时,加入1 ml 胎牛血清终止消化,1 000 转/分离心10 min。弃上清,加生长培养液充分吹打制成细胞悬液后,接种到新的培养瓶中。
1.5 骨骼肌卫星细胞纯度鉴定
取第三代的细胞,将细胞密度调至3×105个/孔,接种于放有盖玻片12 孔板内,将培养板置于37℃,5%CO2,100% 空气湿度细胞培养箱中培养24 h。取出12 孔板,用PBS漂洗3次。4%多聚甲醛固定为20 min,用PBS漂洗3次,3 min/次。 以 75%、85%、95% 浓度酒精依次脱水,3 min/次,用 PBS 漂洗 3 次,3 min/次。3% H2O2灭活内源性的过氧化物酶,室温浸泡 30 min,用 PBS 漂洗 3 次,3 min/次。滴加5% BSA 封闭液,室温孵育20 min,除去多余液体。滴加一抗(1:100 稀释的横纹肌肌动蛋白抗体),4℃过夜,用PBS 漂洗3 次,3 min/次。滴加二抗(生物素化山羊抗小鼠Ig G),37℃孵育 20 min,用 PBS 漂洗 3 次,3 min/次。滴加复 合 SABC,37℃ 孵 育 20 min,PBS 洗 涤 3 次 ,5 min/次 。DAB 显色后,苏木素复染2 min。取出玻片,脱水,透明,封片。显微镜下观察,随机选取6 个视野拍照,计算细胞纯度。细胞纯度(100%)=(细胞总数-阴性细胞数)÷细胞总核×100%。
1.6 骨骼肌卫星细胞的机械牵拉
取第三代细胞,将卫星细胞的密度调制2×105个/ml后种植在牵拉板,在牵拉板上继续培养24 h 使细胞完全贴壁,然后对细胞以1 Hz 的频率进行周期性机械牵拉。将细胞分组如下:
对照组(C):不施加任何牵拉;
5% 拉伸度 4 h 组(5%S 4 h):以 5% 的机械牵拉强度牵拉4 h;
5% 拉伸度 6 h 组(5%S 6 h):以 5% 的机械牵拉强度牵拉6 h;
15% 拉伸度 4 h 组(15%S 4 h):以 15% 的机械牵拉强度牵拉4 h;
15% 拉伸度 6 h 组(15%S 6 h):以 15% 的机械牵拉强度牵拉6 h。
1.7 CCK-8检测骨骼肌卫星细胞的增殖
牵拉结束后放置培养箱中,24 h 后换液,每孔加入1 ml生长培养液和100 ulCCK8 溶液使其完全覆盖细胞,并轻轻摇晃均匀,孵育2 h 后,将待测液加入96 孔板中,以吸光度为 450 nm 测定 OD 值。
1.8 Western blotting
除去牵拉板中的生长培养液,用预冷的PBS 清洗3 次。在每孔中加入80 μl细胞裂解液,静置于冰袋上,孵育30 min,用细胞刮板刮净,收取细胞。4℃离心机上12 000转/分离心20 min。-80℃保存,待测。采用BCA 法测定细胞的总蛋白含量后蛋白变性。然后进行8% 的SDS-PAGE 电泳,将目的条带转至PVDF 膜,使用5% 脱脂牛奶封闭,然后4℃孵育一抗过夜,TBST 清洗后,室温孵育二抗2 h,ECL 超敏试剂盒显影,扫描图片,分析蛋白相对表达量。
1.9 统计学分析
采用SPSS17.0 软件,分析实验数据均以M±SD表示。针对不同牵拉强度和牵拉时间的数据,先采用双因素方差分析,确定牵拉强度、牵拉时间是否产生独立作用或交互作用,针对不同因素产生的作用,进行Post Hoc 组间两两比较,事后检验采用LSD 法。采用独立样本t检验检测不同组别与C 组的差异。P<0.05 为显著性差异,P<0.01为非常显著性差异。
2 实验结果
2.1 骨骼肌卫星细胞的形态学观察
A:骨骼肌卫星细胞贴壁1d,细胞体积小,呈圆形,折光性强(40×);
B:骨骼肌卫星细胞贴壁2d,部分细胞呈长梭形(40×);
C:骨骼肌卫星细胞贴壁4d,细胞增多,细胞体积变大,部分细胞呈梭形或多角形(40×);
D:骨骼肌卫星细胞贴壁6d,细胞明显增多,密集呈网状,相互融合(40×)。
2.2 骨骼肌卫星细胞的鉴定
本实验计数1 000 个细胞,阴性细胞数为24 个。
细胞纯度(100%)=(1 000-24)/1 000×100%=97.6%
细胞纯度≥95%,达到的纯化的要求。
2.3 不同机械牵拉强度对骨骼肌卫星细胞增殖的影响
如图2 所示,双因素方差分析显示,不同的牵拉强度对骨骼肌卫星细胞增殖作用显著(P<0.05)。15% 牵拉强度比5% 牵拉强度促增殖效果更好(P<0.01)。

图2 机械牵拉对骨骼肌卫星细胞增殖的影响Figure 2. Effects of Mechanical Stretch on the Proliferation of Skeletal Muscle Satellite Cells
与C 组相比,15%S 4 h 组和15%S 6 h 组均能促进骨骼肌卫星细胞的增殖(P<0.01),5%S 4 h 组和5%S 6 h 组的骨骼肌卫星细胞增殖没有显著性变化。
2.4 机械牵拉对骨骼肌卫星细胞增殖相关蛋白的影响
2.4.1 牵拉结束即刻Akt、P38、ERK、JNK的变化
如图 3 所示,不同牵拉强度对 Akt、P38、JNK 的磷酸化作用显著(P<0.05)。与5% 牵拉强度相比,15% 牵拉强度活化Akt、P38、JNK 效果更好(P<0.01)。不同牵拉强度和牵拉时间均对ERK 的磷酸化作用显著(P<0.01),且两者之间出现交互作用(P<0.05),ERK 的磷酸化结果显示5%S 6 hvs15%S 6 h(P<0.01)、5%S 4 hvs15%S 4 h(P<0.05)、15%S 4 hvs15%S 6 h(P<0.01)、5%S 6 hvs15%S 4 h(P<0.01)。
15%S 4 h 组和 15%S 6 h 组的 Akt、P38、ERK、JNK 的磷酸化在牵拉结束即刻显著高于C 组(P<0.01),5%S 4 h 组和 5% 6 h 组的 Akt、P38、ERK、JNK 的磷酸化水平在牵拉结束即刻与C 组相比未有显著变化。
2.4.2 牵拉结束24 h后Myf5和MyoD的蛋白表达
如图4,不同的牵拉强度和牵拉时间对Myf5 和MyoD 作用不显著,且牵拉时间与牵拉强度之间没有出现交互作用。
如图 4A,与 C 组相比,15%S 6 h 组 Myf5 蛋白表达显著增加(P<0.01),5%S 4 h 组、5%S 6 h 组、15%S 4h 组的Myf5 蛋白表达均无显著性差异。如图4B,与C 组相比,15%S 4 h 组和15%S 6 h 组的MyoD 的蛋白表达显著增加(P<0.01),5%S 4 h 组、5%S 6 h 组的 MyoD 的蛋白表达无显著变化。
2.4.3 牵拉结束24 h后Akt、P38、ERK、JNK的变化
不同牵拉强度和牵拉时间对Akt 的磷酸化没有显著影响,但牵拉强度和牵拉时间的交互作用显著(P<0.05),Akt 的磷酸化结果显示 5%S 6 hvs15%S 6 h(P<0.01)、15%S 4 hvs15%S 6 h(P<0.05)、15%S 6 hvs5%S4 h(P<0.01)、5%S 6 hvs15%S 4 h(P<0.05)。不同牵拉强度和牵拉时间对P38、ERK 和JNK 的磷酸化没有显著影响,同时牵拉时间与牵拉强度之间均没有出现交互作用。
如图 5,牵拉结束 24 h 后,15%S 4 h 组和 15%S 6 h 组的Akt、P38、ERK、JNK 的磷酸化显著高于C 组(P<0.01),5%S 4 h 组和 5%S 6 h 组的 Akt、P38、ERK 和 JNK 的磷酸化未有显著性。
3 分析讨论
骨骼肌卫星细胞是肌源性干细胞,简称卫星细胞,具有极强的增殖能力。Mauro 等(1961)首次从蛙的胫骨前肌中发现了位于肌膜与基膜之间的卫星细胞。此后,对卫星细胞进行了很多研究。在成年骨骼肌中,卫星细胞是静止的,疾病或者损伤等一些刺激,会激活静止的卫星细胞,卫星细胞通过不对称分裂方式,一部分分裂为活化的卫星细胞,来修复肌肉损伤,另一部分则补充卫星细胞池,以保持细胞池的相对稳定。
有研究表明,一次性力竭运动能够激活静息期的卫星细胞,但不足以诱导其分化(Snijders et al.,2012);短期的抗阻运动能够使卫星细胞数目的增加,以及肌纤维肥大(Kadi et al.,2004);长期的力量训练能使肌细胞核和卫星细胞的数目增加,并且使肌纤维横截面积增大(Snijders et al.,2009)。这些研究均证实,运动可以通过激活骨骼肌中的卫星细胞,进而促进肌肉的肥大。机械牵拉通过模拟运动的方式,已在多种细胞研究中被应用,例如骨髓间充质干细胞、C2C12 细胞、心肌细胞、骨细胞等。其中,骨骼肌卫星细胞对机械牵拉反应相当敏感,有学者发现,机械牵拉能够导致卫星细胞活化和增殖。许多可以调节机械转导的细胞因子也参与了卫星细胞活化(Thornell et al.,2003;Wang et al.,2006)。有关机械牵拉促进卫星细胞增殖的作用机制尚未研究透彻,现在的大多数研究使用成肌细胞系而不是原代培养的卫星细胞来探究机械牵拉在调节肌生成中的作用(Chen et al.,2007;Kumar et al.,2004)。本实验通过体外提取具有干细胞功能的骨骼肌卫星细胞,而不是使用被转化的细胞系,能更好的分析关 于机械牵拉介导的肌生成的调节机制。

图3 机械牵拉结束即刻骨骼肌卫星细胞增殖相关通路的变化Figure 3. Changes of Signaling Pathways Associated with the Proliferation of Stretch of Skeletal Muscle Satellite Cells Immediately after Mechanical Stretch

图4 机械牵拉结束24 h后骨骼肌卫星细胞增殖相关蛋白的变化Figure 4. Changes of Protein Expressions Associated with the Proliferation of Stretch of Skeletal Muscle Satellite Cells at 24 Hours after Mechanical Stretch
3.1 机械牵拉对骨骼肌卫星细胞增殖的影响
有研究显示,细胞对牵拉的反应与牵拉程度有关,如5% 强度周期性牵拉能促进角膜成纤维细胞的增殖,但是抑制迁移(Suetta et al.,2010);15% 的强度持续牵拉膀胱平滑肌细胞,细胞的收缩功能先下降后上升(Honsho et al.,2009);结缔组织细胞培养后,给予其 10% 强度、4 h 的牵拉后,可引起细胞增殖(Hatton et al.,2003)。机械刺激可以促进大鼠肌腱干细胞的分化,4%、2 Hz 牵拉24 h 促进成腱分化,8%、1 Hz 牵拉 24 h 促进成骨分化,8%、2 Hz 牵拉48 促进成脂肪分化(李跑等,2017)。
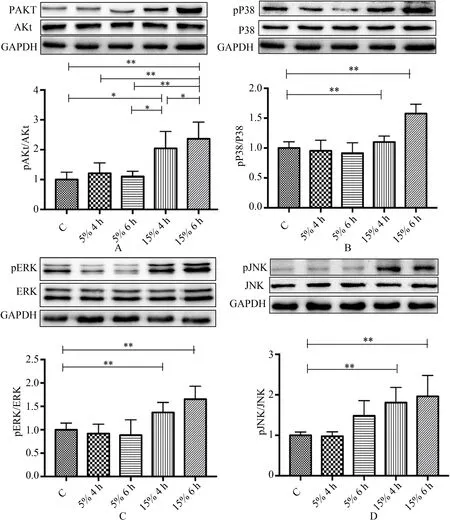
图5 机械牵拉结束24 h后骨骼肌卫星细胞增殖相关通路的变化Figure 5. Changes of Signaling Pathways Associated with the Proliferation of Stretch of Skeletal Muscle Satellite Cells at 24 Hours after Mechanical Stretch
有关机械牵拉对骨骼肌卫星细胞影响的研究发现,10% 的周期性牵拉能够促进牛肌卫星细胞的增殖并抑制其分化(Kook et al.,2008);同样,史仍飞等(2012)发现5%、15%、25% 的拉伸度,频率为1 Hz 的周期性牵拉都能促进大鼠骨骼肌卫星细胞的增殖,其中以15% 牵拉强度的增殖效果最为显著,我们所得到的结果与上述的结果相一致。我们通过对肌卫星细胞施加1 Hz、拉伸度为5%和15%、牵拉时间为4 h 和6 h 的的周期性牵拉,在牵拉结束24 h 后,采用CCK8 比色法检测增殖情况,发现不同牵拉强度对骨骼肌卫星细胞增殖作用显著,15% 牵拉强度比5% 牵拉强度促增殖效果更好,说明在同牵拉时间(4 h,6 h)和频率(1 HZ)的条件下,一定范围内增加牵拉强度,能起到促进骨骼肌卫星细胞增殖的作用。综上所述,机械牵拉对骨骼肌卫星细胞的增殖作用与牵拉强度存在相关性。15% 的牵拉度可以使肌卫星细胞的增殖能力显著提高,而5% 的拉伸度对肌卫星细胞没有促增殖作用。有其它研究发现5% 的拉伸度能够促进细胞的增殖,这与我们得出的结论不一样,推测可能是由于机械牵拉对细胞的影响会根据细胞种类、种属来源的不同而有所不同(Bullard et al.,2007;Zhao et al.,2016)。
3.2 机械牵拉可能通过调控MyoD 和Myf5 的表达来促进卫星细胞的增殖
骨骼肌的生成依赖生肌调节因子(MRFs)家族的参与。Myf5 和MyoD 是MRFs 中的成员,在肌肉早期发育、形成过程中起着重要的作用(陶志云等,2012)。实验发现,单独敲除MyoD 基因,出生的小鼠会有正常肌肉的形成,当同时去除MyoD 和Myf5 时,小鼠无肌肉形成(Rudnicki et al.,1994)。Myf5 是参与肌细胞增殖、分化、肌纤维形成过程中最早表达的因子,Myf5 一旦被激活,MRFs 家族的其他因子将相继被激活,整个肌肉发育过程才能完整而顺利的进行下去。Cooper 等(1999)通过实验证实,小鼠骨骼肌再生时,肌卫星细胞激活早期MyoD 基因,在所有增殖的肌卫星细胞中,MyoD 也都显著表达,因此在成体骨骼肌中,MyoD 被认为是卫星细胞激活的一个很好的标志。活化的骨骼肌卫星细胞中会有MyoD 和Myf5 的表达,在卫星细胞增殖的过程中,MyoD 和Myf5 的蛋白表达增加。本实验结果发现,不同的牵拉强度和牵拉时间对Myf5 和MyoD作用不显著,说明MyoD 和Myf5的蛋白表达对牵拉时间和牵拉强度的变化没有依赖性。拉伸度为15%,在牵拉4 h 和6 h后24 h 时,MyoD 蛋白表达显著增高,说明卫星细胞被大量激活,进入增殖状态,这与CCK8 测得的结果相符;Myf5 的蛋白表达在拉伸度为15%,牵拉6 h 也显著增高。而拉伸度为15%,牵拉4 h未增高,这与CCK8结果并不统一,本实验选取检测Myf5蛋白表达的时间点是牵拉结束24 h,并未检测牵拉结束24 以内以及牵拉结束24 以后Myf5 蛋白表达的变化,推测出现此种结果的原因可能是Myf5 的蛋白表达处于升高阶段,还未到达峰值,具体原因需通过进一步实验来获取。
3.3 机械牵拉可能通过调控Akt、P38、ERK、JNK 通路来调节骨骼肌卫星细胞增殖
PI3K/Akt/mTOR 通路是影响蛋白变化的关键通路,并且参与机械牵拉引起细胞增殖的过程。Akt 是PI3K 下游的关键效应分子,Akt 被激活后,磷酸化水平升高,进而激活下游的 mTOR,促进肌肉的合成(Rommel et al.,2001)。一定程度的机械牵拉能够通过活化Akt 的途径来促进心肌的肥大;有研究表明,10% 的拉伸度能显著提高血管平滑肌的Akt 活性,并且这种变化对时间有依赖性(Won et al.,2013);相同的,15% 的拉伸度牵拉主动脉平滑肌,持续6 h,能激活 PI3K/Akt 通路(Liu et al.,2015)。Akt 的活化被证实与肌肉的存活和凋亡密切相关,机械牵拉引起骨骼肌的质量改变也是通过PI3K/Akt/mTOR 这条通路介导的(Chen et al.,2014)。对C2C12细胞进行周期性牵拉仅30 min,就能引起mTOR 下游蛋白p70S6K 的磷酸化,进而促进肌肉的合成(Alexander et al.,2004)。由此可以推测,机械牵拉促进骨骼肌卫星细胞的增殖作用可能是通过PI3K/Akt/mTOR/p70S6K 这条通路介导的。
MAPK(丝裂素活化蛋白激酶)通路是参与细胞应激和损伤反应的主要信号通路,能将多种细胞外刺激产生的信号从细胞膜外传递到细胞核内,在细胞的增殖、分化和对外环境应激中起着非常重要的作用(Amiram et al.,2013)。 在哺乳动物体内主要有 ERK 通路、JNK 通路和P38 通路,这些信号的传导对细胞调节具有重要的影响。ERK 通路是MAPK 家族中研究最早的通路,许多细胞外刺激可以激活ERK 通路,以Ras/Raf/MEK/ERK 这条通路最为常见,活化后的ERK 移动到细胞核,活化众多与细胞功能相关的转录因子,进而对细胞进行调控。JNK 通路可被多种因子激活,例如,LPS、TNF-α、JNK 可从胞浆进入细胞核,与转录因子结合,调控细胞相关基因的表达(Weston et al.,2002)。P38 通路被认为是 MAPK 家族中最经典的通路,P38 一般位于静止细胞的胞质和胞核,被激活后形成pP38,进而激活多种转录因子,诱导细胞表面基因表达,加速蛋白合成和细胞骨架重构(Chen et al.,2011)。
机械牵拉能够通过激活细胞内的MAPK 通路,来促进蛋白的合成。15% 拉伸度的机械牵拉可以激活C2C12 细胞中 P38、ERK、JNK 的磷酸化(Nakai et al.,2010);人的成纤维细胞接受10% 的机械牵拉后,P38 的活化显著增高;有关大鼠平滑肌的调查发现,20% 的拉伸度牵拉5~10min就可以使 P38 和 JNK 的活性显著升高(Xu et al.,2012);对牛内皮细胞进行周期性拉伸,JNK、ERK 和P38 的磷酸化水平都显著升高(Kito et al.,2000)。 这些结果都表明,MAPK 家族在机械牵拉调控的细胞增殖中具有重要的作用。
本实验中,在牵拉结束即刻,不同牵拉强度对Akt、P38、JNK 的磷酸化作用显著。与5% 牵拉强度相比,15%牵拉强度活化Akt、P38、JNK 效果更好,说明在同牵拉时间(4 h,6 h)和频率(1 HZ)的条件下,一定范围内增加牵拉强度能使Akt、P38、JNK 活化增加;不同牵拉强度和牵拉时间均对ERK 的磷酸化作用显著,推测ERK 通路的活化对牵拉强度与牵拉时间的变化均有依赖性,在同牵拉时间(4 h,6 h)和频率(1 HZ)的条件下,一定范围内增加牵拉强度,或者同牵拉强度(5%,15%)和频率(1 HZ)的条件下,一定范围内延长牵拉时间,可能使ERK 的活化增加。5%S 4 h 组和 15%S 6 h 组的 Akt、P38、ERK、JNK 的磷酸化显著高于C 组。由此可以看出,在牵拉结束即刻这个时间点,骨骼肌卫星细胞内与增殖相关的部分蛋白磷酸化就已升高,根据牵拉结束 24 h 后,15%S 4 h 组和 15%S 6 h 组的 Akt、P38、ERK、JNK 的磷酸化依然显著高于 C 组的结果,可推测,与骨骼肌卫星细胞增殖相关的磷酸化蛋白在牵拉即刻就可开始升高,部分蛋白的磷酸化可能持续增高直到牵拉结束24 h 后。当然也有截然不同的研究结果,通过培养大鼠膀胱平滑肌细胞后进行牵拉发现,机械牵拉对与细胞生长密切相关的ERK 通路无关,而与P38 通路和 JNK 通路密切相关(Nguyen et al.,2000)。机械牵拉使牛的肌卫星细胞中ERK 的磷酸化水平显著增高,而P38的磷酸化水平呈降低的趋势。这些都有可能是由于细胞的类型或者是种属的不同,而产生不同的结果。
本实验的结果表明,15% 拉伸度牵拉4 h 和6 h,均可以骨骼肌卫星细胞的增殖,在牵拉结束即刻Akt、P38、ERK、JNK 的活性已经显著升高,并且在牵拉结束24 h 后,Akt、P38、ERK、JNK 的活性依然呈现显著升高的状态。以往的研究只是对选取某个时间点进行研究,而本研究选取了牵拉结束即刻和牵拉结束24 h 后这2 个时间点进行比较,能更好的探究与骨骼肌卫星细胞增殖相关的通路蛋白的变化,这也是本文的创新点。由于条件限制,本研究并未使用各个通路蛋白的特异性抑制剂进行研究,也没有检测各个通路下游蛋白的表达,因此只能得出初步结论。
4 结论
1)15% 的拉伸度,牵拉4 h 和6 h 可以促进体外培养的大鼠骨骼肌卫星细胞增殖。
2)机械牵拉可能是通过激活Akt、P38、ERK、JNK 这些通路来促进骨骼肌卫星细胞增殖的。
