Ag2Cu1/H-ZSM-5 合金催化剂在NH3-SCO 反应中的性能研究
2020-01-01周明东白继峰王景芸
周明东,孙 强,白继峰,王景芸
(辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺113001)
众所周知,NH3不仅对人的身体健康造成严重危害,而且还会导致严重的环境问题[1-5]。据估计,每年大约有4 000 万吨NH3排放到大气中(不包括海洋排放源)[1]。因此,NH3与NOx、SOx和NMVOC一起并称为四大大气污染物[2]。NH3选择性催化氧化成N2和H2O,无论是从经济或技术角度考虑都是氨消除的理想技术,在过去的几十年中已被广泛研究[2]。 到目前为止,银或铜基催化剂被研究的最为广泛,每种催化剂的优缺点都很明显。铜基催化剂具有较高的N2选择性,但缺点是在350 ℃以下的活性较低。与铜基催化剂相比,银基催化剂在350 ℃以下具有很高的活性,甚至优于Pt、Pd 等贵金属催化剂[1,6],但N2的低选择性(NO/N2O 形成)限制了它们的广泛应用。负载型催化剂中Ag、Cu 双组分金属元素的复合和协同作用有效地改善了这一问题,在低于320 ℃的条件下能够将NH3完全氧化,获得的N2选择性在95%以上[7]。
近期,许多努力致力于合成Ag-Cu 双金属纳米材料[8-9]。Ag-Cu 合金结构纳米材料由于其独特的催化性能而引起了人们的极大兴趣[10]。此外,Ag-Cu 合金结构可以有效地保持Ag 和Cu 的金属状态以及结构稳定性[11],这可能对NH3氧化的低温高活性、N2的高选择性以及热稳定性都是非常有利的。ZSM-5 由于其良好的择形性、优异的水热稳定性以及可调控的酸性而广泛应用于NH3-SCO 领域。鉴于此,本文合成了Cu、Ag 合金纳米颗粒,并将其负载到H-ZSM-5 上,以探求H-ZSM-5 对Cu、Ag 合金催化剂NH3-SCO 反应活性的促进作用。
1 实验部分
1.1 试剂及原料
拟薄水铝石、正硅酸四乙酯(TEOS)、无水硫酸钠、氢氧化钠(NaOH)、水合肼溶液、硝酸铵和硝酸银(AgNO3),分析纯,国药集团化学试剂有限公司;质量分数25%的四丙基氢氧化铵(TPAOH)、四水甲酸铜、二甲苯、正己胺,分析纯,阿拉丁试剂有限公司;去离子水,Milli-Q,青岛生物能源与过程研究所。
1.2 催化剂的制备
1.2.1 Ag2Cu1合金纳米颗粒的合成 分别量取2 mL 的正己胺和10 mL 的二甲苯倒入50 mL 的烧杯中混合均匀,然后称取一定量的AgNO3和四水甲酸铜,分别加入其中(AgNO3和四水甲酸铜的总量为4.5 mmol,Ag、Cu 物质的量比为2∶1),磁力搅拌至完全溶解。待完全溶解后,将混合溶液与80 g 无水硫酸钠在研钵中研磨混合,目的是使混合溶液均匀地覆盖在无水硫酸钠表面。然后将混合物置于管式加热炉中,在3 °C/min、300 ℃,高纯空气气氛下反应1 h。降至室温,得到的固体粉末溶解于0.1 mol/L 的水合肼溶液,洗涤过滤,重复3 次以上。80 ℃真空干燥12 h,得到Ag-Cu 合金纳米颗粒催化剂,记作Ag2Cu1。
1.2.2 Ag2Cu1/H-ZSM-5 催化剂的制备 称取合成的0.4 g Ag2Cu1催化剂和0.8 g H-ZSM-5 分子筛于玛瑙研钵中(称取前Ag2Cu1和H-ZSM-5 100 ℃真空干燥12 h),用研杵将二者充分研磨5 min 以上,直到观察不到细微的白色H-ZSM-5 粉末为止,200 ℃下氢气还原4 h,升温速率为2 ℃/min,制得Ag2Cu1和H-ZSM-5 整体式粉末催化剂,简写为Ag2Cu1/HZSM-5。催化剂在压片后粉碎过筛,得到20~40 目的催化剂颗粒后,用于测定催化剂的催化性能。
1.3 催化剂的表征
采用Bruker D8 ADVANCE X 射线衍射光谱仪(XRD)对所得样品的晶体结构进行表征分析。测试条件为广角粉末衍射管,Cu-Kα 靶射线,电压40 kV,波长λ= 0.154 056 nm,电流100 mA,扫描范围2θ 在5°~80°,扫描速度4(o)/min,步长0.02°。
使用美国麦克(Micromerritics)公司生产的ASAP2020 型表面分析仪在液氮温度下进行N2的吸附-脱附。测试前,在300 ℃真空状态下脱气8 h,-196 ℃下进行吸脱附过程。数据结果利用BET方法计算样品的比表面积,BJH 方法计算样品的总孔容和孔径分布情况。
利用Hitach S-4800 型冷场发射SEM 对催化剂表面微观形貌包括粒度及其分布、形态、晶体结构和厚度等进行观察,加速电压为0.5~30 kV,放大倍数为20~800 000。测试前,样品在表面进行喷金以消除催化剂表面在测试过程中的电荷累积。
采用美国FEI 公司生产的FEI TECNAI G2 F20 型TEM 对催化剂的形貌进行微观分析,最高加速电压200 kV,放大倍数(25~1 030)×103倍,点分辨率0.24 nm,线分辨率0.102 nm,信息分辨率0.14 nm。
X 射线光电子能谱(XPS)测试采用的是美国赛默飞世尔科技公司制造的Thermo ESCALAB 250XI 型多功能成像电子能谱仪,测定合成催化剂表面物种Ag、Cu 和O 的电子价态及其含量。
催化剂的NH3吸附强度和吸附量通过在AutochemⅡ2920 型化学吸附仪上对NH3程序升温脱附进行分析,并利用所配软件定量计算样品的NH3吸附量。
1.4 催化剂的活性评价
采用固定床反应器在常压下进行实验。反应温度为100~350 ℃,催化剂颗粒为20~40 目。测试前,催化剂掺入颗粒为40~60 目的石英砂。为了保证活性组分量的一致性,Ag2Cu1/H-ZSM-5 催化剂的使用质量是Ag2Cu1的3 倍。进料气组成(体积分数)为0.1% NH3,10% O2,N2为平衡气。反应气体的总流速为100 mL/min。采用NH3分析仪(JFQ-1150L,北京均方理化科技研究所)分析入口和出口气体NH3的浓度。利用NH3转化率对催化剂的NH3-SCO 催化性能进行评价。具体计算方法见式(1):
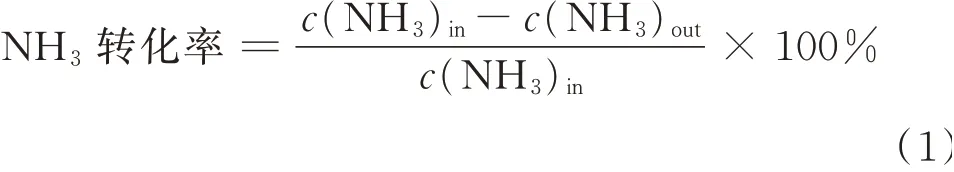
2 结果与讨论
2.1 不同催化剂的活性评价
对Ag2Cu1和Ag2Cu1/H-ZSM-5 整体式粉末催化剂在富氧条件下的NH3-SCO 反应催化性能进行考察,结果如图1 所示。
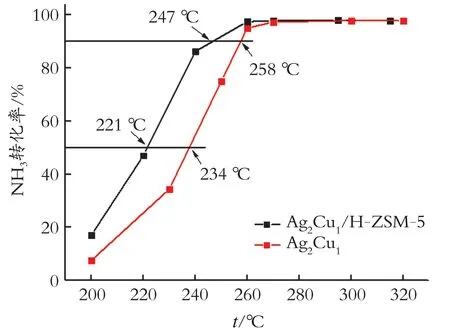
图1 不同催化剂的NH3转化率和反应速率Fig.1 Ammonia conversion and reaction rate of different catalysts in NH3⁃SCO
由图1 可见,在200~320 ℃,这两种催化剂的NH3转化率均随着温度的升高而增大,最大的NH3转化率出现在270 ℃以后。Ag2Cu1和H-ZSM-5 混合制备成Ag2Cu1/H-ZSM-5 整体式粉末催化剂后,NH3-SCO 催化活性明显得到改善。详细地说,Ag2Cu1催化剂在234 ℃(T50)获得50%NH3转化率,258 ℃(T90)获得90%的NH3转化率。掺入H-ZSM-5 分子筛之后,Ag2Cu1/H-ZSM-5 催化剂的催化活性进一步提高,反应温度向更低温度移动,T50和T90分别降至221、247 ℃。可见H-ZSM-5 分子筛可以明显改善Ag2Cu1合金纳米颗粒催化剂的低温(<300 ℃)NH3-SCO 反应催化活性。
2.2 催化剂表征结果及分析
分别采用XRD、BET、TEM 和XPS 等手段对H-ZSM-5、Ag2Cu1和Ag2Cu1/H-ZSM-5 的物理化学性质进行表征,结果见图2-7。
2.2.1 XRD 分析 图2 所示为Ag2Cu1催化剂在2θ=38.1°,44.3°,64.4° 和77.4°的位置显示出4 组特征衍射峰,分别归属于纯银面心立方结构的(111)、(200)、(220)和(311)晶 面[12]。由 此 看 出,Ag2Cu1催 化剂具有与纯Ag 相似的多晶晶体结构,证明Ag2Cu1是一种Ag-Cu 合金纳米粒子结构的催化剂[11]。在H-ZSM-5 的XRD 谱图中,2θ 为7.8°、8.8°和22°~24°的ZSM-5 特征衍射峰能够被清晰地观察到,表明其MFI 骨架结构完好[13-14]。而Ag2Cu1/H-ZSM-5 催化剂则同时显示出了ZSM-5 特征衍射峰和Ag2Cu1催化剂中纯银的4 组特征衍射峰,表明H-ZSM-5 分子筛和Ag2Cu1催化剂经机械混合后,ZSM-5 的MFI 骨架结构和Ag2Cu1的Ag-Cu 合金纳米结构均没有被破坏。此外,对比Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂的XRD 谱图可以发现,Ag2Cu1/H-ZSM-5 催化剂中 的(111)、(200)、(220)和(311)晶 面 的4 组特征衍射峰强度有所降低,这可能是由于Ag-Cu 合金纳米颗粒在H-ZSM-5 表面高度分散所导致的。相比较HZSM-5 谱图,虽然Ag2Cu1/H-ZSM-5 催化剂仍能够保持ZSM-5 晶型,但其特征峰强度下降幅度比较大,这可能由两个原因造成,一个是机械混合制备过程中部分ZSM-5 的MFI 骨架结构被破坏,另一个原因可能是部分Ag2Cu1纳米颗粒聚集覆盖在HZSM-5 表面,降低了其特征峰强度。

图2 不同催化剂的XRD 谱图Fig.2 XRD patterns of the different catalysts
2.2.2 BET 表征分析 图3 显示了H-ZSM-5 分子筛和Ag2Cu1/H-ZSM-5 催化剂的N2吸附-脱附等温曲线和孔径分布,其孔结构性质见表1。从图3 可以 看 出,H-ZSM-5 和Ag2Cu1/H-ZSM-5 催化 剂 在相对压力p/p0小于0.05 时,N2的吸附数量急剧升高,这说明H-ZSM-5 和Ag2Cu1/H-ZSM-5 都存在大量的微孔,并且由表1 可知二者拥有相近的微孔孔体积,表明H-ZSM-5 的微孔结构在制备Ag2Cu1/HZSM-5 催化剂的一系列过程中并未被破坏,保存完好。当相对压力p/p0在0.45~1.00 时,这两种催化剂的氮气吸附-脱附等温曲线上均出现了较为微弱的滞后环,说明有一定量的介孔存在,这可能是由无定型颗粒聚集产生的狭缝状孔导致的。与HZSM-5 相比,Ag2Cu1/H-ZSM-5 催化剂的孔径分布较宽,这应该是纳米载体H-ZSM-5 与Ag2Cu1催化剂相互堆积所导致的。另外H-ZSM-5 和Ag2Cu1/H-ZSM-5 催化剂的BET 比表面积分别是297.7、201.7 m2·g-1,二 者 相 差近100 m2·g-1,导致这种情况的原因应该是Ag2Cu1纳米颗粒高度分散覆盖在H-ZSM-5 的表面,堵塞孔道,降低了其表面积。

表1 H-ZSM-5、Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂的质构性质Table 1 Textural properties of H⁃ZSM⁃5,Ag2Cu1 and Ag2Cu1/H⁃ZSM⁃5
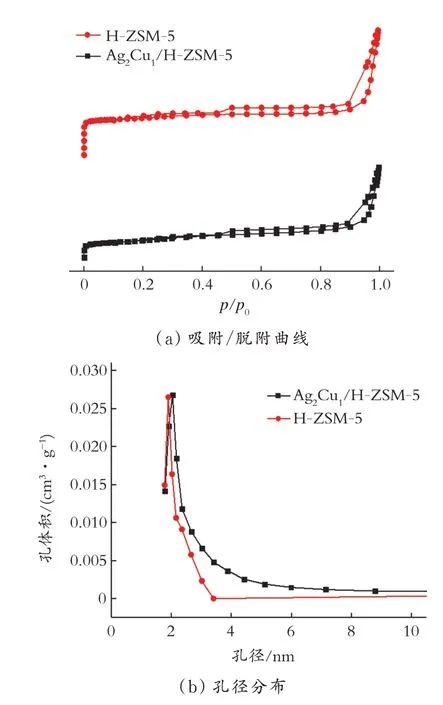
图3 H-ZSM-5 和Ag2Cu1/H-ZSM-5 催化剂的N2物理吸附/脱附曲线和孔径分布Fig.3 Nitrogen adsorption/desorption isotherms and pore size distribution of H⁃ZSM⁃5 and Ag2Cu1/H⁃ZSM⁃5 catalysts
2.2.3 SEM 表征分析 图4 为样品的SEM。由图4 可以看出,H-ZSM-5 分子筛晶粒尺寸较为均一,呈直径大小约为200 nm 的圆台状,并且表面较为光滑。Ag2Cu1催化剂(见图4(b))表现出形态大小分明的球形Ag-Cu 合金纳米粒子结构,颗粒直径大小不一,相互聚集,并且还有部分孔道结构形成。与H-ZSM-5 分子筛(见图4(a))相比,Ag2Cu1/H-ZSM-5催化剂SEM(见图4(c、d))中的H-ZSM-5 分子筛圆台状的晶粒结构没有被破坏,保持相对完整。但是,其表面变得较为粗糙,红色圆圈标注的区域可以明显地观察到Ag2Cu1催化剂的Ag-Cu 合金纳米颗粒附着在H-ZSM-5 分子筛表面,表明Ag2Cu1催化剂和H-ZSM-5 分子筛均匀地混合在一起,Ag-Cu合金纳米颗粒在H-ZSM-5 表面高度地分散,有利于更多活性组分的暴露,这或许是Ag2Cu1/H-ZSM-5催化剂表现出更加优异NH3-SCO 反应活性的一个重要原因。

图4 样品的SEMFig.4 SEM images of the samples
2.2.4 TEM 表征分析 由图5(a)可知,Ag2Cu1催化剂拥有形貌规整的细小球形纳米合金结构,颗粒尺寸3~24 nm,平均直径为11 nm(见图5(e))。H-ZSM-5 分子筛(见图5(b)是具有规则形态的晶体结构(晶体尺寸为100 nm×160 nm)。 同时,Ag2Cu1/H-ZSM-5 催化剂的TEM 图像中发现Ag2Cu1纳米颗粒和H-ZSM-5 分子筛存在两种不同结合的现象。一种如图5(c)所示,每个H-ZSM-5 分子筛单晶晶体表面覆盖着大量微小的Ag2Cu1纳米颗粒。经统计,其表面颗粒的大小在2 ~14 nm,平均直径约为6 nm,统计结果见图5(f)。另一种情况则与之相反,如图5(d)所示,较大的Ag2Cu1纳米颗粒仅仅少量负载在H-ZSM-5 分子筛上;经统计(见图5(g)),这种较大颗粒的尺寸在10~25 nm,平均直径约为17 nm。结果表明,直径越小的Ag-Cu 合金纳米颗粒与H-ZSM-5 分子筛表面的作用力越强。因而H-ZSM-5 分子筛的加入增强了Ag2Cu1催化剂中微小Ag-Cu 合金纳米颗粒的分散性,增大了反应物与活性组分的接触面积。此外,高度分散、粒径更小的金属颗粒对NH3-SCO 反应更有利[15],因而Ag2Cu1/H-ZSM-5 催化剂显示出了比Ag2Cu1催化剂更加优异的催化性能。
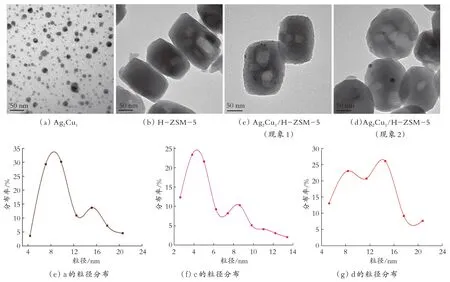
图5 样品的TEM 图像及Ag-Cu 合金纳米颗粒粒径分布Fig.5 TEM of the samples and nanoparticles size distributions of a、c and d respectively
2.2.5 XPS 表征分析 如图6(a)所示,Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂Ag 3d 的XPS 图谱都仅在368.2 eV 和374.2 eV 位置处出现两个结合能峰,分别归属于Ag 的3d3/2和3d5/2轨道[12]。两个峰之间的距离为6.0 eV,而且没有发现伴星峰和肩峰的存在,表明这两种催化剂表面Ag 物种主要以金属态的方式存在。催化剂表面Cu 物种的XPS 分析结果见图6(b),可以观察到932.5 eV(934.5 eV 是它的一个肩峰)和952.4 eV 位置各存在一个铜物种的峰。根据相关报道所述[5,16-17],金属Cu 存在两组自旋轨道峰,其中在932.9 eV 附近是Cu2p3/2主峰的位置,在934.5 eV 的位置是它的一个肩峰,而Cu2p1/2的主峰位置在952.8 eV 左右。此外,氧化铜在催化剂表面是否存在主要是以伴星峰的出现为依据,其中Cu+的特征峰在932.2~931.1 eV 的位置,图中并未观察到,而942.5eV 位置的伴星峰被归属为Cu2+的特征峰[18]。由此可以得出结论,催化剂表面存在少量的Cu0被氧化成Cu2+。另外,通过拟合分析Cu2p3/2主峰和其肩峰(934.5 eV)的积分面积得出,Cu0在Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂表面铜物种中所占的比例是相同的,均是0.82(见表2)。由此可知,Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂表面Ag 和Cu 价态的表征结果一致,说明在机械混合制备Ag2Cu1/H-ZSM-5 粉末催化剂的过程中并未对其造成影响,间接证明了Ag-Cu 合金纳米颗粒的结构稳定性。每个所测样品的O1s XPS 光谱如图6(c)所示。O1s主峰通过分峰拟合分为三个峰,在533.0 eV 附近的O1s 峰归属为表面吸附的微量水(H2O),以531.2 eV 为中心的O1s 峰(标记为Oβ)表示的是表面化学吸附的氧物种(O22-或O-),最低结合能529.8eV 的位置对应的是晶格氧O2-(标记为Oα)[19-22]。通过比较O1s 三个峰的积分面积(见表2)发现,由于Ag-Cu 合金纳米颗粒和H-ZSM-5 载体之间的强相互作用,Ag2Cu1/H-ZSM-5 催化剂表现出了更高的Oβ/(Oα+Oβ+H2O)相 对 浓 度(0.85)。 结 果 表 明,Ag2Cu1/H-ZSM-5 表面拥有更多的活性氧。在氧化反应中,化学吸附氧物种(Oβ)由于其较高的迁移率而被认为是比晶格氧(Oα)具有更高反应活性的物种[23-26]。因而Ag2Cu1/H-ZSM-5 表现出比Ag2Cu1催化剂更加优异的NH3-SCO 反应催化性能。
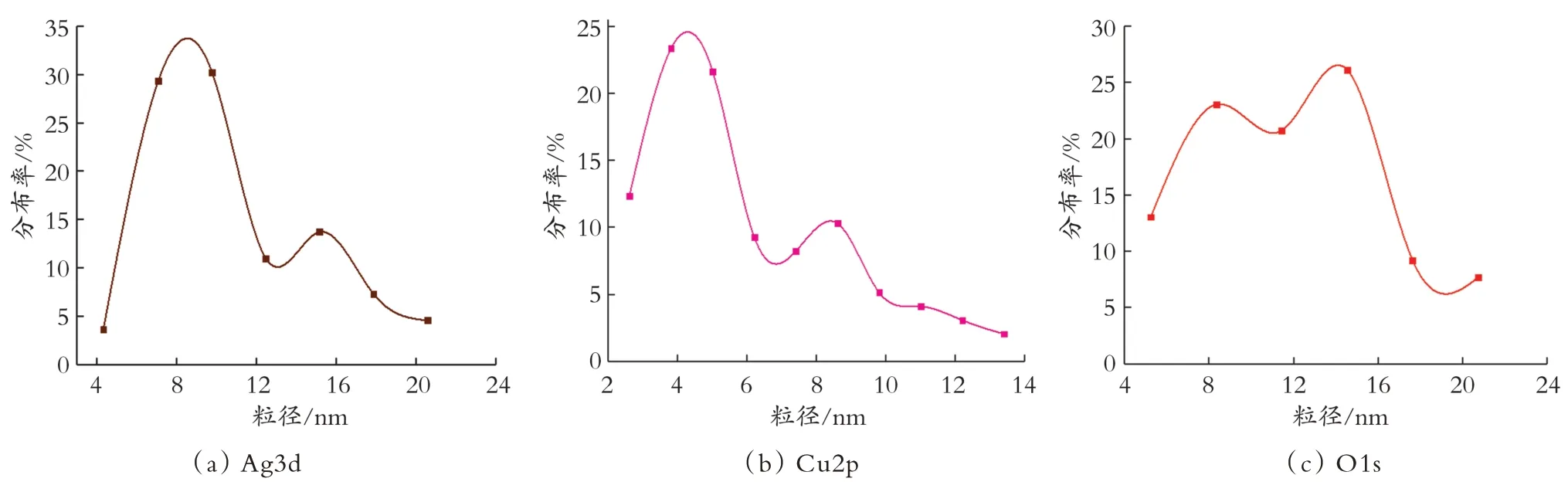
图6 催化剂的Ag3d、Cu2p 和O1s 的XPS 谱图Fig.6 XPS spectras of the Ag3d,Cu2p and O1s for the synthesized catalysts

表2 催化剂的NH3-TPD 和XPS 结果Table 2 The NH3⁃TPD and XPS results for the synthesized catalysts
2.2.6 NH3-TPD 结果分析 为了考察NH3吸附性能对Ag2Cu1和Ag2Cu1/H-ZSM-5 催化剂之间反应性能的影响,对所合成的Ag2Cu1,H-ZSM-5 和Ag2Cu1/H-ZSM-5 样品进行了NH3-TPD 测试,结果见图7。

图7 催化剂的NH3-TPD 结果Fig.7 TPD profiles of NH3 from catalysts
由图7 可知,在这3 个样品中均存在两组主要的NH3脱附峰,说明催化剂上存在两种不同强度的氨吸附中心。其中低温段(170 ℃左右)的NH3脱附峰归属于氨的弱吸附中心;而高温段(300~700 ℃)的NH3脱附峰则归属于氨的中强度吸附中心[27-29]。结合NH3-TPD 结果计算各样品不同强度下的NH3吸附量(见表2),可以发现所有样品在弱、中强度吸附中心NH3吸附量的顺序是:H -ZSM -5 <Ag2Cu1<Ag2Cu1/H-ZSM-5,并且Ag2Cu1/H-ZSM-5 表面弱吸附位的NH3吸附量是H-ZSM-5 与Ag2Cu1之和的1.7 倍之多,证明Ag-Cu 合金纳米颗粒和H-ZSM-5 之间的强相互作用极大地促进了NH3在其表面的吸附,这对氨氧化反应是非常有利的。
3 结 论
通过直接机械混合法将Ag2Cu1催化剂和HZSM-5 分子筛研磨混合制备成Ag2Cu1/H-ZSM-5 粉末催化剂,并将其应用于富氧条件下的低温NH3-SCO 反 应,以考 察H-ZSM-5 分 子筛对Ag-Cu 合金纳米颗粒催化剂活性的促进作用。通过实验得到以下结论:
(1)在所考察的Ag-Cu 合金纳米颗粒催化剂中,Ag2Cu1/H-ZSM-5 催化剂表现出最佳的低温氨氧化性能,其T50和T90分别降至221、247 ℃。
(2)通过不同的表征手段考察了催化剂的物理化学性质。结果表明,Ag2Cu1/H-ZSM-5 催化剂中的MFI 骨架结构和Ag-Cu 合金结构均没有被破坏,保持完好,Ag-Cu 合金纳米颗粒高度分散地分布在H-ZSM-5 表面,进而加强细小Ag-Cu 合金纳米颗粒(2~14 nm)与H-ZSM-5 分子筛表面的作用力。这种强相互作用促进Ag2Cu1/H-ZSM-5 表面拥有更多的活性氧和氨气的吸附,进而提高氨氧化反应的速率。
