透明质酸酶治疗透明质酸动脉栓塞兔耳皮肤缺血性病变的疗效观察
2019-12-27庄岩刘春军杨明勇
庄岩 刘春军 杨明勇
透明质酸(Hyaluronic acid,HA)是目前使用最为广泛的面部注射填充材料。常见并发症包括淤青、红肿和结节[1]。最严重的并发症莫过于血管栓塞造成的组织缺血[2-3],栓塞严重或未及时治疗,病灶缺血程度将逐渐加重,并最终出现皮肤软组织坏死、瘢痕形成、面容不同程度损毁[4-11]。除了阻塞于注射点局部的动脉,HA 栓子还能够在注射压力的作用下沿受累动脉逆行,阻塞于视网膜动脉和脑动脉[12-15]。
对于HA 引起的动脉栓塞并发症目前尚缺乏确切和统一的治疗。在条件允许的情况下,溶栓、再通血管治疗是改善急性动脉栓塞组织缺血的最佳方式。传统的溶栓药物(如尿激酶、链激酶等)只能针对性地溶解血栓栓子,尚无证据表明其对HA 栓子有效。在兔耳动脉栓塞模型上,我们尝试在血管内应用透明质酸酶(hyaluronidase,HAase)来溶解HA 栓子,以探索HAase 血管内应用的可行性及其效果。
1 实验对象与方法
1.1 实验动物
成年新西兰大白兔25 只,体质量3.4~3.6 Kg,雌雄不限。分为5 组(每组5 只):纯栓塞对照组(Control 组)、生理盐水全身静脉溶栓对照组(Intravenous thrombolysis with NaCl,IVT-NaCl 组)、HAase全身静脉溶栓治疗组(Intravenous thrombolysis with HAase,IVT-HAase 组)、生理盐水选择性动脉溶栓对照组(Intra-arterial thrombolysis with NaCl,IATNaCl 组)、HAase 选择性动脉溶栓治疗组(Intra-arterial thrombolysis with HAase,IAT-HAase 组),均行右耳手术,经左耳耳后静脉外侧支或耳前静脉注射荧光素钠进行荧光造影检查。
1.2 试剂与仪器
注射用修饰透明质酸钠凝胶(华煕福瑞达生物医药有限公司),注射用荧光素钠溶液(3 mL/0.6 g,广州白云山明兴制药有限公司),注射用HAase(1 500 U/瓶,上海第一生化药业有限公司)。
气密性Hamilton 100 μL 微量进样器(瑞士Hamilton 公司),365 nm 紫外线手电筒(安富电子有限公司),静脉留置针(24 G×19 mm/Y-G,威海洁瑞医用制品有限公司)。
1.3 实验方法
1.3.1 建立兔耳岛状皮瓣HA 动脉栓塞皮肤缺血模型
参照文献[16],注射20 μL HA 进行动脉栓塞。
1.3.2 全身静脉溶栓治疗
IVT-NaCl 组:将12 mL 生理盐水装在20 mL注射器内并安装在KL-60 注射泵上,在HA 动脉栓塞皮瓣制作完成后40~50 min 经后肢隐静脉给药,给药速度为12 mL/h,连续给药1 h。
IVT-Haase 组:按10 000 U/Kg 计算HAase 给药剂量,并将其溶于12 mL 生理盐水内,给药方式、速度和时间同IVT-NaCl 组。
1.3.3 经颈外动脉选择性溶栓治疗
HA 动脉栓塞皮瓣制作完成后,实验兔仰卧位,颈部备皮消毒,在颈部正中及右侧下颌角水平设计T 形切口;切开并寻找右侧颈总动脉,在舌骨端离断下颌舌骨肌,更好地暴露颞浅下颌干和舌面干;结扎并离断舌面干,结扎点尽量远离颞浅下颌干和舌面干分叉处。动脉夹临时夹闭颈外动脉主干近端、颞浅下颌干远端,之后经舌面干断端插入24 G 静脉留置针并用7-0 聚丙烯缝线结扎固定,静脉留置针针尖位于颈外动脉主干之内。确定无出血后打开动脉夹和输液泵开关,开始给药。可根据情况适当调节插管深度,但针尖不能超过颈内动脉发出水平。
IAT-NaCl 组:直接给以12 mL 生理盐水,给药速度12 mL/h,连续给药1 h。
IAT-HAase 组:按10 000 U/Kg 计算HAase 给药剂量,并将其溶于12 mL 生理盐水内,给药方式、速度和时间同IAT-NaCl 组给药完成后,在舌面干近端预置7-0 聚丙烯缝线,双人操作,在拔出静脉留置针的同时结扎缝线;确定无出血后缝合皮肤,切口涂红霉素药膏。
1.3.4 术后观察
1.3.4.1 大体观察
观察实验兔进食、排泄、体质量等全身状况;观察IVT-NaCl 组和IVT-HAase 组后肢隐静脉穿刺处皮肤情况,以及IAT-NaCl 组和IAT-HAase 组颈部切口情况
1.3.4.2 皮瓣观察
观察皮瓣颜色和肿胀程度,以及皮瓣下有无出血、积液、积脓、皮瓣有无坏死;术后4 h、3 d、7 d 拍照并记录,同时进行FA 检查,观察皮瓣灌注情况。麻醉后20%荧光素钠15 mg/Kg 经左侧耳后静脉外侧支或耳前静脉注射,10 min 后暗室下365 nm 紫外线手电筒照射皮瓣,观察荧光充盈范围和部位,拍照记录。
1.3.5 术中要点及术后注意事项
两种溶栓治疗过程中,均需保证麻醉状态,尤其是选择性动脉溶栓时,麻醉不足可导致插管脱出;分离和暴露颈外动脉及其分支时,可见粗大的迷走神经,不可损伤,否则会影响呼吸运动;分离颈外动脉远端分支时,有舌面干主干缺如的情况,此时可同时结扎并离断舌动脉和面动脉,以保证两种不同的解剖分支情况下,药物最终均进入颞浅下颌干中,无额外的面动脉或舌动脉分流;在掌握颈外动脉分支解剖、双人熟练手术操作的基础上,通常可在HA 动脉栓塞皮瓣制作完成后40~50 min 开始选择性动脉给药治疗。在完成颈外动脉插管后需尽早开启输液泵开关,否则静脉留置针前端可有血栓形成。
1.4 结果评价
观察各组术后4 h、3 d、7 d 皮瓣成活和灌注情况,计算并比较各组术后7 d 皮瓣灌注面积百分比的差异。
1.5 统计学分析
以SPSS16.0 进行单因素方差分析,P<0.05 表示差异具有统计学意义。
2 结果
2.1 全身状况
每次麻醉苏醒后,实验兔可逐渐恢复饮水、进食和活动,但进食量均少于术前。术后前3 天,IATHAase 组、IAT-NaCl 组进食减少相对明显,体质量下降100~300 g 不等,之后进食情况逐渐改善,术后7 d 基本接近术前水平。其余各组实验白兔全身状况无明显变化。所有实验白兔两便正常,尿液呈黄绿色,具有荧光性。
2.2 隐静脉穿刺处皮肤/颈部切口情况
IVT-NaCl 组、IVT-HAase 组后肢隐静脉穿刺处周围皮肤可见轻度水肿,未见血肿、皮肤坏死发生。IAT-NaCl 组、IAT-HAase 组所有颈部切口愈合良好,无感染和切口裂开发生。
2.3 皮瓣肉眼观察及FA 检查
各术后4 h、3 d、7 d 皮瓣肉眼观察显示:所有皮瓣水肿程度相似,各组均有不同程度的皮瓣下积液出现;术后6 d,IAT-NaCl 组有1 例皮瓣发生切口部分裂开;术后7 d,除IAT-HAase 组的1 例皮瓣完全成活外,其他皮瓣均有不同程度的坏死,坏死灶位于皮瓣的远端或者边缘。
各组术后4 h、3 d、7 d 皮瓣FA 检查结果显示:术后4 h,除IAT-HAase 组的1 例皮瓣荧光充盈均匀、边界清晰外,其他所有皮瓣的荧光均呈现花斑状,边界不清;术后3 d,所有皮瓣近心端荧光充盈均匀、边界清晰;术后7 d,所有皮瓣的灌注范围均大于各自术后3 d 时的检查结果,除IAT-HAase 组的1 例皮瓣100%荧光充盈外,其他皮瓣远端均有不同程度的无灌注区。
2.4 术后7 天各组皮瓣灌注面积百分比比较
术后7 d,Control 组、IVT-NaCl 组、IVT-HAase组、IAT-NaCl 组、IAT-HAase 组皮瓣平均灌注面积百分比分别为(76.54%±6.92%)、(74.08%±9.14%)、(76.94%±6.68%)、(76.95%±8.72%)和(95.47%±3.38%)。其中,IAT-HAase 组皮瓣灌注面积百分比显著高于其他4 组(P<0.05),其他4 组两两比较均无显著差异(P>0.05)(图1)。
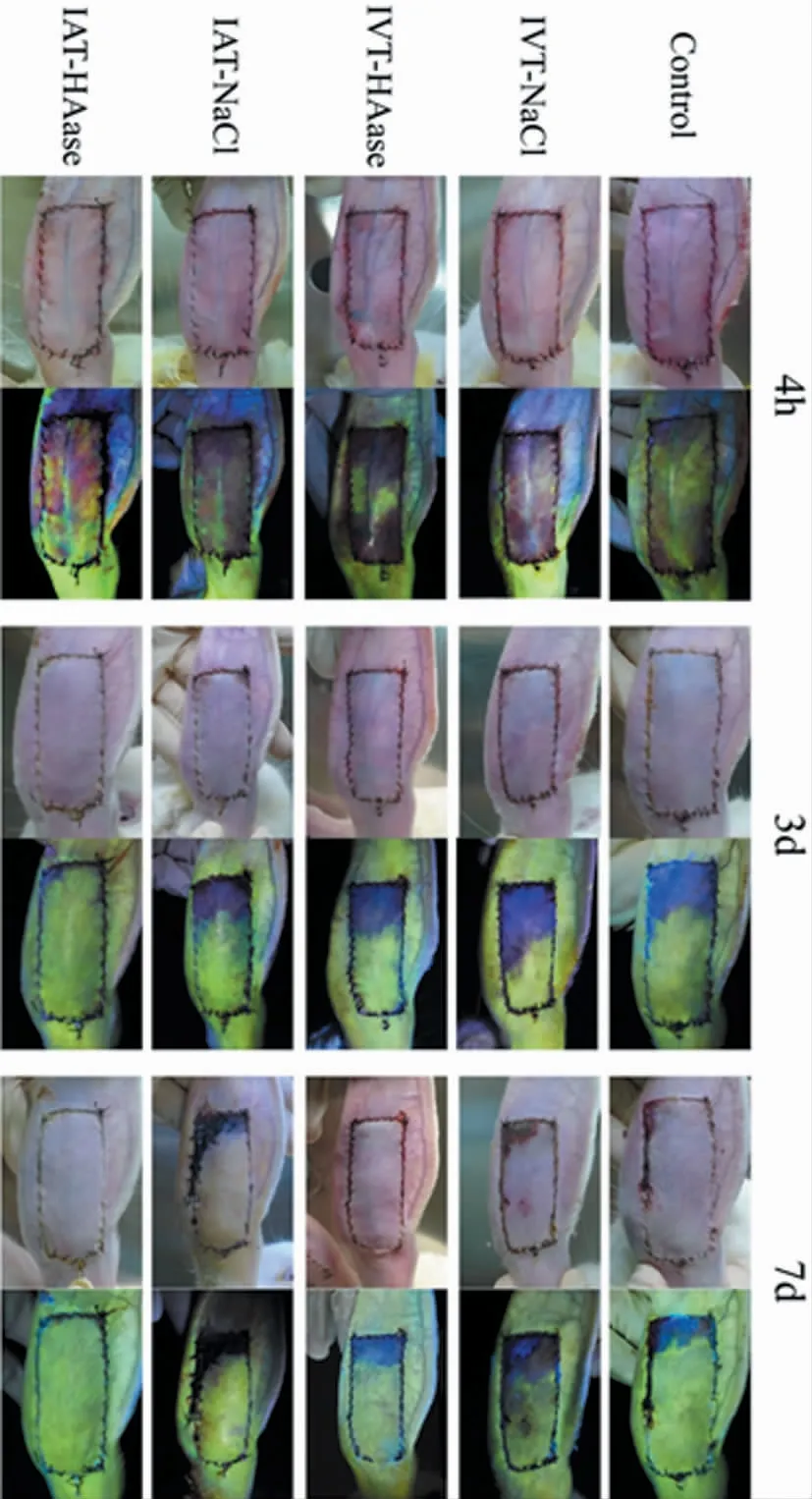
图1 各组术后各时间点皮瓣观察和FA 检查Fig.1 Flap and FA examination of each group at different time points
3 讨论
血管栓塞造成的组织缺血是HA 注射后最严重的并发症[2-3],不但会导致患者面容不同程度的损毁,还可能造成视网膜动脉甚至脑血管栓塞[4-15]。虽然,HA 动脉栓塞的发生率低,但因庞大的注射人数和不断上升的趋势,其总体发病例数不容小觑。近年来,该并发症屡见报道,其后果和代价是极为惨痛的。
HAase 亦称为玻璃酸酶,是一种能够降低HA活性、提高组织中液体渗透能力的酶。在整形外科领域,HAase 常用于矫正HA 注射后的各种并发症。HA 填充过度引起皮下肿块或硬结时,局部注射HAase 可使肿块或结节缓解吸收[17]。HA 意外注射进入动脉可引起鼻唇沟、鼻部、眉间、额部等处皮肤缺血甚至坏死[4-8,11,18]。除热敷、按摩、氧疗、扩血管、抗凝等非特异性治疗外[19],若早期行HAase 局部注射治疗,有可能阻止缺血进展而导致的组织坏死[11,20]。但不同文献对局部注射HAase 缓解皮肤缺血的应用剂量相差甚远。Vartanian 等[21]认为应从5~10 U 开始小剂量使用。Hirsch 等[18]使用的剂量为30 U。Sun 等[11]是将150 U HAase 溶于1 mL 生理盐水中进行注射治疗,严重者使用300 U HAase 溶于2 mL 生理盐水中。DeLorenzi[1]建议尽可能使用大剂量HAase,发生血管栓塞并发症时最大用量可到1 500 U。虽然部分组织缺血情况可以得到改善,但是局部注射的HAase 是跨血管直接溶解了动脉内外源性HA 栓子而改善了组织缺血,还是通过溶解组织基质中的HA 成分、易化了组织养分供给而间接发挥改善组织供血的效应尚不得知。临床上因注射层次深浅不一、血管间存在吻合、血管走行变异等因素,往往很难确定动脉栓塞的准确位置。此外,局部皮下注射HAase 并不适合治疗栓塞部位远离HA 注射点的眼部和脑部动脉栓塞这两种严重的栓塞并发症。上述因素共同限制了HAase 局部注射改善HA 动脉栓塞在组织缺血中的应用。
全身应用HAase 的研究早在上世纪70 年代就有报道,当时主要是静脉给药用于治疗急性心肌梗死[22-27]。通过阻断狗的冠状动脉建立急性心梗模型,Wolf 等[28]发现5 000 U/Kg 的HAase 单次静脉滴注能够降低心肌组织内HA 含量。Nilsson 等[22]证实了HAase 对大鼠梗死心肌的保护作用。Maroko 等[25]采用多次HAase 静脉给药的方式治疗了24 例心梗患者,单次药物剂量为500 U/Kg,证实HAase 能够减轻人心肌缺血性损伤。2000 年,Johnsson 等[29]给予同种异体心脏移植后的大鼠静脉HAase 治疗,最小剂量为5 000 U/Kg·h,单次快速静脉注射并持续静脉滴注2 h,最大使用剂量为20 000 U/Kg·h,单次快速静脉注射并持续静脉滴注4 h,结果发现心肌中HA 和心肌间质含水量明显降低,且使用剂量越大,治疗效果越明显。HAase 心肌保护作用的机制主要包括减轻心肌水肿、通过解聚黏多糖增加营养物质流入缺血区、促进有害代谢物流出、保留心肌血流、对微血管的直接保护作用[23]。
HAase 静脉使用具有良好的药物安全性[25,30]。以狗和兔子为研究对象时,快速静脉注射HAase 500 U/Kg,每日6 次,连续2 周,脑、心肌及瓣膜、肺、大动脉、肝脏、脾、性腺、眼、晶体、椎间盘,组织病理学检查均未见异常。健康人静脉注射HAase 500 U/Kg,每日5 次,连续48 h,亦未见临床并发症,生命体征、血磷酸肌酸激酶、乳酸脱氢酶、谷-草转氨酶、血电解质、胆红素、尿素氮、尿液分析、血常规、心电图和胸片检查均未见异常[25]。
Seifter 等[30]指出,静脉注射HAase 后5 min,血中HAase 水平达到峰值,30 min 时活性降低一半,60 min 后无法检测到HAase。Wolf 等[31]发现,静脉注射的HAase 在人、狗、大鼠的循环中半衰期均小于10 min。实验狗结果显示,500 U/Kg 和5 000 U/Kg组血清HAase 活性分别在给药后10 min 和45 min下降到无法检出的水平。血浆HAase 活性降低是物理性排泄清除的结果,而非酶的活性受到抑制或失活。上述两项药物代谢动力学研究结果说明,HAase在循环中将被迅速清除,重复静脉注射并不能使血浆HAase 浓度持续升高。
基于HAase 静脉使用的可行性和安全性,本研究首先进行了HAase 全身静脉给药溶栓的研究。虽然国内外尚无HAase 静脉滴注治疗外源性交联型HA 的报道,但考虑到HAase 在循环中的半衰期非常短,为了保证HAase 可以更好地发挥溶栓作用,必须保证足够的药物浓度和给药时间。因此,本研究采用连续输液1 h 的给药方式,并设定了较高的给药剂量10 000 U/Kg(1 只3.6 Kg 的实验白兔需24支HAase)。遗憾的是,Control 组、IVT-NaCl 组、IVTHAase 组术后7 d 时皮瓣灌注面积百分比并无显著性差异,也就是说在单次剂量10 000 U/Kg、连续静脉给药1 h 的情况下,HAase 并没有显示出溶栓作用。为了进一步验证HAase 的溶栓作用,在给药方式不变的情况下,需要继续提高给药剂量,但随之而来的是可能伴发的药物副作用。此外,研究进行过程中,HAase 采购形势严峻,一药难求,也限制了继续提高药物剂量进行静脉溶栓的可行性。
全身静脉溶栓时,药物首先经下腔静脉回心,再经左心进入主动脉,只有很少一部分HAase 经右侧颈外动脉最终进入到右侧耳郭后动脉,即HA 动脉栓塞的部位,因此绝大部分药物并未在HA 动脉栓塞处发挥作用。HAase 在循环中半衰期短,经过若干个体循环再次回心并进入耳郭后动脉的HAase 活性已经开始降低,溶栓作用进一步变弱。对于血栓栓塞的病例,临床研究已经证实选择性动脉溶栓的效果明显优于静脉溶栓[32-33]。因此,在HAase 半衰期短、全身静脉溶栓无效、药品数量有限的情况下,本研究变换了给药方式,从静脉溶栓转换为选择性动脉溶栓,通过提高局部药物浓度验证HAase 的溶栓作用。有关HAase 动脉应用的研究,此前尚未见相关文献报道。
制作HA 动脉栓塞皮肤缺血模型时栓塞的耳郭后动脉系颞浅动脉的主要分支,后者系颈外动脉的分支之一,故可以经颈外动脉注射HAase 进行选择性动脉溶栓效果的研究。在不具备数字减影血管造影设备和研究经费有限的情况下,本研究选择通过颈外动脉的其他分支(舌面干/舌动脉/面动脉)向颈外动脉置管给药,进行选择性动脉溶栓。
术后7 d,IAT-NaCl 组和Control 组相比,皮瓣灌注面积百分比无统计学差异,也就是说颈外动脉置管、局部给药所造成的血流动力学改变并未影响到皮瓣的灌注。而IAT-HAase 组皮瓣灌注面积百分比显著高于Control 组、IVT-NaCl 组、IVT-HAase组、IAT-NaCl 组,充分证明了HAase 选择性动脉溶栓治疗的有效性。
HAase 在循环中的半衰期非常短,从理论上讲主要在早期发挥溶解HA 栓子的效应,但术后4 h FA 检查荧光边界不清、很难计算皮瓣灌注面积。有关HAase 动脉溶栓的机制,我们推测始动环节是局部高浓度的HAase 直接溶解了部分HA,进而产生以下几方面的后续效应:①直接减少了栓子数量、缩小了缺血组织的范围;②栓子数量减少可以减轻动脉的扩张,从而减少对血管内皮造成的影响;③降低了栓塞动脉内的压力、提高了动脉灌注压,有利于组织再灌注;④栓子中非交联的HA 成分被溶解后,交联的HA 颗粒间可能会出现微小空隙,有利于HA在动脉内重新分布,并为血液和氧的弥散创造可能的空间;⑤即便不能够被充分溶解,但部分交联的HA 颗粒可能在HAase 的作用下变小,有助其通过微循环或者动静脉吻合,甚至通过静脉回流被带出缺血皮瓣。其他可能的机制还包括HAase 跨血管溶解了组织中的HA、减轻了皮瓣水肿、进而改善了循环,HAase 对微血管的直接保护作用等[23]。本研究采用岛状皮瓣验证HAase 血管内应用的溶栓效果,HAase 进入缺血皮瓣的途径仅为阻塞的单一动脉。若采用的皮瓣为非岛状皮瓣,将有更多HAase 被带入缺血区,HAase 有可能会发挥更好的溶栓效果。
本研究初步证实了HAase 选择性动脉溶栓的有效性,为医源性HA 动脉栓塞寻找了新的治疗可能,该方法不但可用于改善皮肤软组织缺血,还有望治疗眼动脉和脑动脉栓塞这两种更为严重的HA 动脉栓塞并发症。
本研究的局限性:①样本观察量小;②仅采用了单一剂量的单次治疗,并未进行不同剂量HAase 溶栓效果的比较观察;③由于HAase 对不同性状(单相或双相,交联或非交联型)、不同交联度、不同生产工艺的HA 产品分解能力不同,本研究结果并不能用于其他剂型的HA 产品。无论是静脉全身溶栓,还是选择性动脉溶栓,均属于HAase 商品标识外用药(超适应证、超用药途径),且研究中HAase 使用剂量远大于Maroko 等用来评价药物安全性的剂量[25],后续研究还需进一步评价此剂量使用的安全性,尤其需要警惕大剂量使用时过敏的风险。
