比阿培南与甲氨蝶呤、呋塞米在大鼠体内的药代动力学相互作用
2019-12-25李婷婷邱志霞李文艳
董 婧 李婷婷 邱志霞 陆 燕 李文艳
1.上海市浦东新区公利医院药剂科,上海 200135;2.中国药科大学药学院,江苏南京 210009;3.中国药科大学中药学院,江苏南京 210009
比阿培南属于碳青霉烯类抗菌药物,对革兰阳性菌、革兰阴性菌、厌氧菌及多重耐药菌均有效,主要用于中、重度下呼吸道、泌尿道和腹腔等部位感染的治疗[1]。甲氨蝶呤通过抑制二氢叶酸还原酶,阻止癌细胞分裂,用于治疗急性白血病和乳腺癌等[2]。低剂量甲氨蝶呤也用于治疗类风湿性关节炎和银屑病等自身免疫性疾病[3]。呋塞米广泛应用于治疗充血性心力衰竭和水肿[4],是住院老年患者使用频率较高的药物之一[5]。由于比阿培南和甲氨蝶呤、呋塞米在临床上存在联合用药,而目前还没有甲氨蝶呤和呋塞米对比阿培南药代动力学影响的研究报道。因此,本研究通过考察比阿培南和甲氨蝶呤、呋塞米联用后在大鼠体内的药代动力学特征,发现可能存在的药物相互作用,为临床合理用药提供依据。
1 材料
1.1 药品与试剂
比阿培南(江苏正大天晴药业股份有限公司,批号:190111125);甲氨蝶呤(江苏恒瑞医药股份有限公司,批号:16031416);呋塞米(纯度98%,国药集团化学试剂有限公司);内标对氨基苯甲酸(PABA,纯度99.5%,国药集团化学试剂有限公司);稳定剂3-(N-吗啡啉)-丙磺酸(MOPS,纯度99%,美国Sigma 公司);乙腈(色谱纯,美国Fisher 公司);其余试剂均为市售分析纯。
1.2 仪器
Waters 2695高效液相色谱仪、Waters2998二极管阵列检测器(美国Waters 公司);XW-80A 旋涡混合器(海门市其林贝尔仪器制造有限公司);Thermo ST16R 高速冷冻离心机(美国赛默飞世尔科技有限公司);XS205标准型分析天平(千分之一,瑞士Mettler Toledoo 公司)。
1.3 实验动物
健康雄性SD 大鼠15只,体重260~280 g,7~8周龄,由上海西普尔-必凯实验动物有限公司提供,许可证号:SCXK(沪)2013-0016。
2 方法与结果
2.1 色谱条件
色谱柱:SinoChrom ODS-AP(5 μm,4.6 mm×150 mm,大连依利特分析仪器有限公司);流动相:乙腈-水(3∶97,含0.1 mol/L 醋酸钠,pH 4.5),采用等度洗脱方式;流速:1 mL/min;柱温:30℃;进样量:30 μL;紫外检测波长:300 nm。
2.2 给药方案与样品采集
应用随机数字表将大鼠随机分为比阿培南单药组(A 组)、比阿培南和甲氨蝶呤联合给药组(B 组)、比阿培南和呋塞米联合给药组(C 组),每组5只。A 组尾静脉注射30 mg/kg 比阿培南,B 组尾静脉注射30 mg/kg 比阿培南和3 mg/kg 甲氨蝶呤,C 组尾静脉注射30 mg/kg 比阿培南和30 mg/kg 呋塞米。将大鼠饲养于代谢笼内,于给药前及给药后0.03、0.08、0.17、0.33、0.5、0.75、1、1.5、2、3、4、6、8 h 眼底静脉丛取血约0.2 mL 置于肝素钠抗凝的采血管中,4℃下12 000 r/min(离心半径16.1 cm)离心5 min 后取上层血浆;于给药前及给药后0.5、1、2、4、6、8、12、24 h 收集尿液,血浆和尿液加入等体积1 mol/L MOPS 稳定剂后,置-80℃冰箱冷冻保存待测。
2.3 样品处理方法
精密吸取血浆样品200 μL,加入16 μL(200 mg/L)PABA 溶液和200 μL 30%饱和硫酸铵溶液,涡旋振荡2 min,12 000 r/min 离心10 min,(离心半径16.1 cm)取上清液30 μL 进样测定。大鼠尿液样品用流动相稀释5倍后吸取200 μL,其余处理步骤同血浆样品。
2.4 方法学验证
2.4.1 专属性 比阿培南和内标PABA 在本色谱系统中的保留时间分别为3.5、6.4 min,大鼠空白血浆和尿液中的内源性物质不干扰比阿培南的测定,色谱图见图1~2。
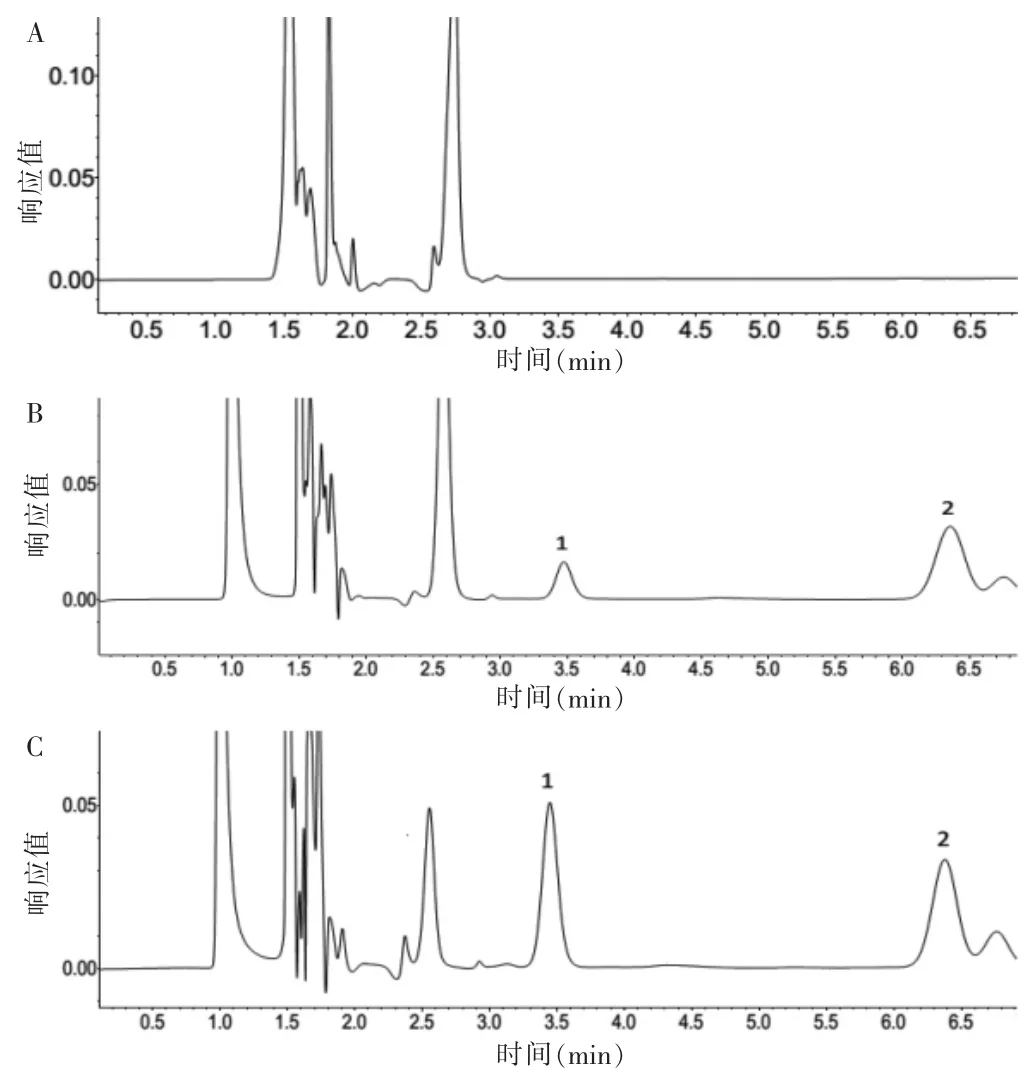
图1 血浆样品中比阿培南和内标PABA 高效液相色谱图
2.4.2 标准曲线及最低定量下限 取空白大鼠血浆或尿液90 μL,加入比阿培南工作液10 μL,使血浆中药物浓度分别为0.2、0.5、1、2、5、10、20、50、100 mg/L,使尿液中 药物浓度分别为0.5、1、2、5、10、20、50、100、200 mg/L,混匀后加入100 μL 1 mol/L MOPS 溶液,再按“2.3”项下操作。另按上述方法配制浓度为0.5、5.0、40 mg/L 的比阿培南血浆质控样品溶液和浓度为1、10、100 mg/L 的尿液质控样品溶液。以测得的比阿培南和内标峰面积比为纵坐标,比阿培南浓度为横坐标,进行权重拟合后得到血浆中比阿培南回归方程为Y=0.124X+0.009,线性范围为0.2~100 mg/L,最低定量下限0.2 mg/L;尿液中比阿培南回归方程为Y=0.0166X+0.014,线性范围为0.5~200 mg/L,最低定量下限为0.5 mg/L。

图2 尿液样品中比阿培南和内标PABA 高效液相色谱图
2.4.3 提取回收率及精密度 以质控样品中比阿培南测得的峰面积与相同浓度标准品溶液直接进样测得的峰面积之比,计算提取回收率。比阿培南提取回收率在82.2%~85.6%,日内和日间精密度均在10%以内,符合生物样品分析要求。
2.4.4 稳定性 质控样品在20℃放置4 h,在-80℃放置30 d,在-80℃放置24 h 后反复冻融处理3次,考察稳定性。结果提示,比阿培南血浆和尿液样品在各条件下均稳定。
2.5 统计学方法
比阿培南主要药代动力学参数消除半衰期(t1/2)、血药浓度-时间曲线下面积(AUC0-∞)、清除率(CL)和肾清除率(CLr)等药代动力学参数采用WinNonlin 6.3非房室模型方法计算。采用SPSS 13.0软件进行数据分析,正态分布的数据用均数±标准差()表示,非正态分布的数据用中位数(最小值,最大值)表示。对AUC0-∞(AUC 经对数转换后)进行独立样本t 检验,对MRT 和t1/2进行Wilcoxon 符号秩和检验。以P <0.05为差异有统计学意义。
2.6 大鼠体内药代动力学研究
与A 组比较,B 组AUC0-∞降低,CL、CLr增加,差异均有高度统计学意义(P <0.01);与A 组比较,C 组各药代动力学参数没有显著变化(P >0.05)。见表1。大鼠联合给予比阿培南和甲氨蝶呤、呋塞米后的AUC0-∞见图3。
表1 大鼠尾静脉注射给药后比阿培南药代动力学参数(,n=5)

表1 大鼠尾静脉注射给药后比阿培南药代动力学参数(,n=5)
注:与A 组比较,**P <0.01。t1/2:消除半衰期;MRT:平均驻留时间;AUC0-∞:血药浓度-时间曲线下面积;V:表观分布容积;CL:清除率;CLr:肾清除率

图3 大鼠尾静脉注射给予比阿培南和甲氨蝶呤、呋塞米后的比阿培南平均血药浓度-时间曲线(n=5)
3 讨论
临床上抗菌药物与其他药物的联合应用越来越普遍,联合用药会产生一定的药物相互作用,可能会导致抗菌药物治疗失败、毒副作用发生或诱导细菌耐药[6-8],药代动力学相互作用可发生在药物吸收、分布、代谢和排泄各阶段[9-11]。本研究首次考察了甲氨蝶呤和呋塞米对比阿培南在大鼠体内药代动力学过程的影响,揭示可能存在的药物相互作用。文献报道,哌拉西林/他唑巴坦[12]、羟氨苄青霉素[13]、万古霉素[14]与甲氨蝶呤联用,会使甲氨蝶呤在体内消除减慢,血药浓度增加。而头孢曲松、头孢他啶[15]、环丙沙星[16]与甲氨蝶呤不存在药代动力学相互作用,但也有研究发现环丙沙星会引起甲氨蝶呤消除减慢[17-18]。呋塞米与头孢噻啶、头孢唑啉、头孢地尔联用时,会显著减少头孢噻啶和头孢唑啉的肾清除[19],但不影响头孢地尔体内的药代动力学过程[20]。本研究发现,甲氨蝶呤使比阿培南在大鼠体内的AUC0-∞降低,CL 和CLr增加差异均有高度统计学意义(P <0.01)。呋塞米使比阿培南AUC0-∞增加,CL 和CLr减少,但差异无统计学意义(P >0.05)。提示甲氨蝶呤和比阿培南存在药代动力学的相互作用,临床上两药合用时需进行剂量调整,而呋塞米和比阿培南不存在明显的药代动力学相互作用,临床上两药合用时无需进行剂量调整。比阿培南给药后约60%以原型经肾脏排泄,甲氨蝶呤90%以原形经肾脏排泄。因此,可以推测比阿培南与甲氨蝶呤的药代动力学相互作用靶点可能是在肾脏,今后我们将进一步阐明两药相互作用的机制。
