Yb2O3/g-C3N4复合光催化剂的制备及光催化性能研究
2019-12-24王彦卫朱正如姜俊超
王彦卫 朱正如 姜俊超
(辽宁师范大学城市与环境学院,辽宁 大连 116029)
0 引 言
光催化技术是一种绿色、高效的新型污染物处理方法,常用于降解水体或空气中的重金属、染料和有机化合物质[1-2].光催化技术的关键在于光催化剂的合成和性能,常用光催化剂包括硫化物和金属氧化物等纳米材料.纳米光催化已经发展成为一门新的水处理技术,可用于污染物的吸附、检验和降解等多个方面[3].
氮化碳(g-C3N4)是一种廉价、形貌易调控的新型光催化剂,但其纯品禁带宽度大,对可见光的吸收利用效率低[4],而对g-C3N4的结构和光吸收性能的改性和优化是研究的热点.Fu等[5]设计了热氧化卷曲的g-C3N4纳米管,比普通块状g-C3N4具有更高的光催化活性;Ge等[6]将Ag掺杂进g-C3N4提高其量子效率用以光催化,Ag/g-C3N4在180 min内降解了几乎100%的甲基橙;Xiao等[7]使用石墨烯和氮化碳复合光催化剂能在180 min内降解74.02%的盐酸四环素(TTCH);Xiang 等[8]合成的石墨烯/氮化碳复合光催化剂也展示出较强的光催化制氢性能.
复合光催化剂的界面接触降低了光电子空穴对的复合重组效率,是提高光催化活性的有效方法[9-10].本课题组曾报道了一系列金属硫铟盐和氮化碳的复合光催化剂(g-C3N4/MIn2S4,M=Zn、Ni、Co),对苯酚的降解率达到72%[11].氧化镱(Yb2O3)作为一种耐热性强、稳定性好的半导体材料,被广泛应用于涂料、燃料、陶瓷、能源材料和环境催化等方面[12-14].因此,本研究以稳定性高的Yb2O3与g-C3N4为原料,利用超声混合法制备Yb2O3/g-C3N4复合材料,以构造异质结构光催化剂.
1 实验部分
1.1 实验试剂
实验所用试剂均为分析纯,包括:五水合硝酸镱(YbN3O9·5H2O)购自阿拉丁工业公司,三聚氰胺[C3N3(NH2)3]购自国药集团化学试剂有限公司,无水乙醇(C2H5OH)购自天津科密欧化学试剂有限公司.实验用水均为去离子水;所有实验均在室温下完成.
1.2 Yb2O3/g-C3N4复合光催化剂制备
纯氧化镱纳米片制备[15].称量5.00 g YbN3O9·5H2O置于带盖陶瓷坩埚中,在马弗炉中以720 ℃加热240 min,升温速率为10 ℃/min,自然冷却至室温后,研磨得到白色粉状样品.
热缩聚法制备g-C3N4[16].称量10.00 g C3N3(NH2)3置于带盖陶瓷坩埚中,在马弗炉中550 ℃焙烧240 min,升温速率为5 ℃/min,冷却至室温后,研磨得到淡黄色粉末样品.
超声混合法合成Yb2O3/g-C3N4复合光催化剂.将0.10 g的g-C3N4粉末分散在10 mL无水乙醇中,超声10 min,将0.01 g Yb2O3混合至g-C3N4悬浮液,超声分散至液体完全蒸发.将混合物置于干燥箱中180 ℃干燥24 h后转移至马弗炉中以 320 ℃煅烧90 min.得到Yb2O3/g-C3N4复合光催化剂.
1.3 Yb2O3/g-C3N4性能表征
采用日本岛津公司XRD-6000 型X射线衍射仪进行X射线衍射(XRD)测量,配备了Cu靶,扫描角度为10°~80°,扫描速度为4 °/min.采用溴化钾压片法在德国Bruker AXS公司TENSOR-27型红外光谱仪对傅里叶变换红外光谱(FTIR)进行了测量.使用日本日立公司SU8010场发射扫描显微镜(FESEM)对样品形貌进行表征,使用其配置的电镜能谱(EDS)对样品进行成分定量分析.使用美国Thermo VG公司ESCALAB250多功能表面分析系统在对X射线光电子能谱(XPS)进行了测量,使用单色化的Al Kα源,能量1 486.6 eV,束斑大小为500 μm.使用美国PerkinElmer公司紫外-可见漫反射光谱(UV-vis DRS)用Lambda 35紫外可见分光光度计测量,样品的Eg可根据αhν=(hν-Eg)1/2的相关关系进行计算[5],其中α为半导体的吸收系数、Eg是禁带宽度.光致发光光谱(PL)采用日本Shimadzu公司RF-540荧光分光光度计测量,激发波长360 nm,被测样品量约0.20 g.

图1 X射线衍射(XRD)衍射图谱(a)样品实际测量与标准谱对比;(b)3种样品的实测图谱
1.4 降解性能研究
在可见光下,以Yb2O3/g-C3N4降解苯酚和TTCH.取50 mL浓度为20 mg/L的苯酚溶液置于烧杯中,在黑暗环境中,准确称量0.01 g Yb2O3/g-C3N4样品加入苯酚溶液,搅拌形成悬浮液,达到苯酚和催化剂之间的吸附-解吸附平衡[17-18].将500 W的CEL-S500型氙灯(中教金源科技有限公司)垂直置于溶液上方30 cm处,每20 min取5 mL溶液在TG16-WS高速离心机(湖南湘仪实验室仪器开发有限公司)中以8 000转/min的速度、离心4 min,离心力约9 866×g.采用4-氨基安替比林分光光度法在溶液的最大吸收波长(λ=510 nm)处测定上清液中苯酚的浓度[19-20],在开始光照后,实验持续进行180 min;相同步骤下,在最大吸收波长为356 nm时,测量溶液中TTCH的浓度[21],在开始光照后,实验持续进行120 min.以不添加任何催化剂所进行的实验为空白实验,以Yb2O3和g-C3N4样品在相同条件下进行实验作为对照组.
1.5 稳定性研究
用Yb2O3/g-C3N4分别对苯酚和TTCH进行循环降解实验,以验证光催化剂的稳定性.离心收集使用过的光催化剂,用水和乙醇清洗,高温烘干后进行循环实验.为保证催化剂回收率,只在每次的实验结束时取5 mL溶液,以检测污染物浓度.
2 结果与讨论
2.1 XRD分析
纯g-C3N4的主峰位于27.48°(2θ),对应(002)晶面,归属于芳香烃的层间堆积[6].与文献结果一致[22],符合PDF标准卡片索引的JCPDS 87-1526.2θ在20.83°、29.62°、34.34°、36.49°、40.50°、44.20°、49.35°、54.13°、58.62°、60.07°和61.51°处的衍射峰可归于Yb2O3的衍射峰,符合PDF标准卡片索引JCPDS 87-2374的正方相Yb2O3,详细对比如图1(a)所示.在Yb2O3/g-C3N4中存在氧化镱和氮化碳的峰如图1(b),表明复合物中的确含有Yb2O3和g-C3N4.并且,Yb2O3和g-C3N4复合后,衍射峰发生偏移,证明两者并非简单的混合,而是形成了复合物质[23].XRD初步证明了Yb2O3/g-C3N4复合物的形成.除此之外,图像上并无杂峰,证明Yb2O3和g-C3N4复合并未改变g-C3N4晶体结构,并且制得的样品纯度较高.
2.2 SEM分析
将3种样品分别进行SEM表征(图2),热分解法制的Yb2O3和g-C3N4都呈纳米片状形貌,在Yb2O3/g-C3N4复合材料的图像上可以观察到Yb2O3和g-C3N4,进一步证明了此次研究成功复合了氧化镱和氮化碳,制备出Yb2O3/g-C3N4复合物样品.经过进一步的EDS分析,Yb2O3含量约为12.07%,与预期结果较一致.

图2 不同样品的扫描电子显微镜图(a)Yb2O3;(b)g-C3N4; (c)Yb2O3/g-C3N4
2.3 FTIR分析
红外光谱分析法可以研究样品微观上的表面变化,根据复合前后的红外图谱,可分析出粒子的表面性质的变化[24].样品的FTIR光谱如图3所示,Yb2O3的578 cm-1处峰与Yb—O键的振动有关[25-26].在Yb2O3/g-C3N4复合光催化剂的FTIR图中,811 cm-1处的峰归属于3-s-三嗪环;在1 240~1 650 cm-1处的特征峰可以归因于CN杂环的骨架振动[8].在3 071~3 274 cm-1处存在弱宽峰,可能属于样品表面的氨基(N—H)和羟基(O—H)官能团[27].FTIR和XRD分析结合,证明Yb2O3的掺杂并没有引起化学键断裂,改变Yb2O3和g-C3N4的结构,说明材料具有一定的稳定性.
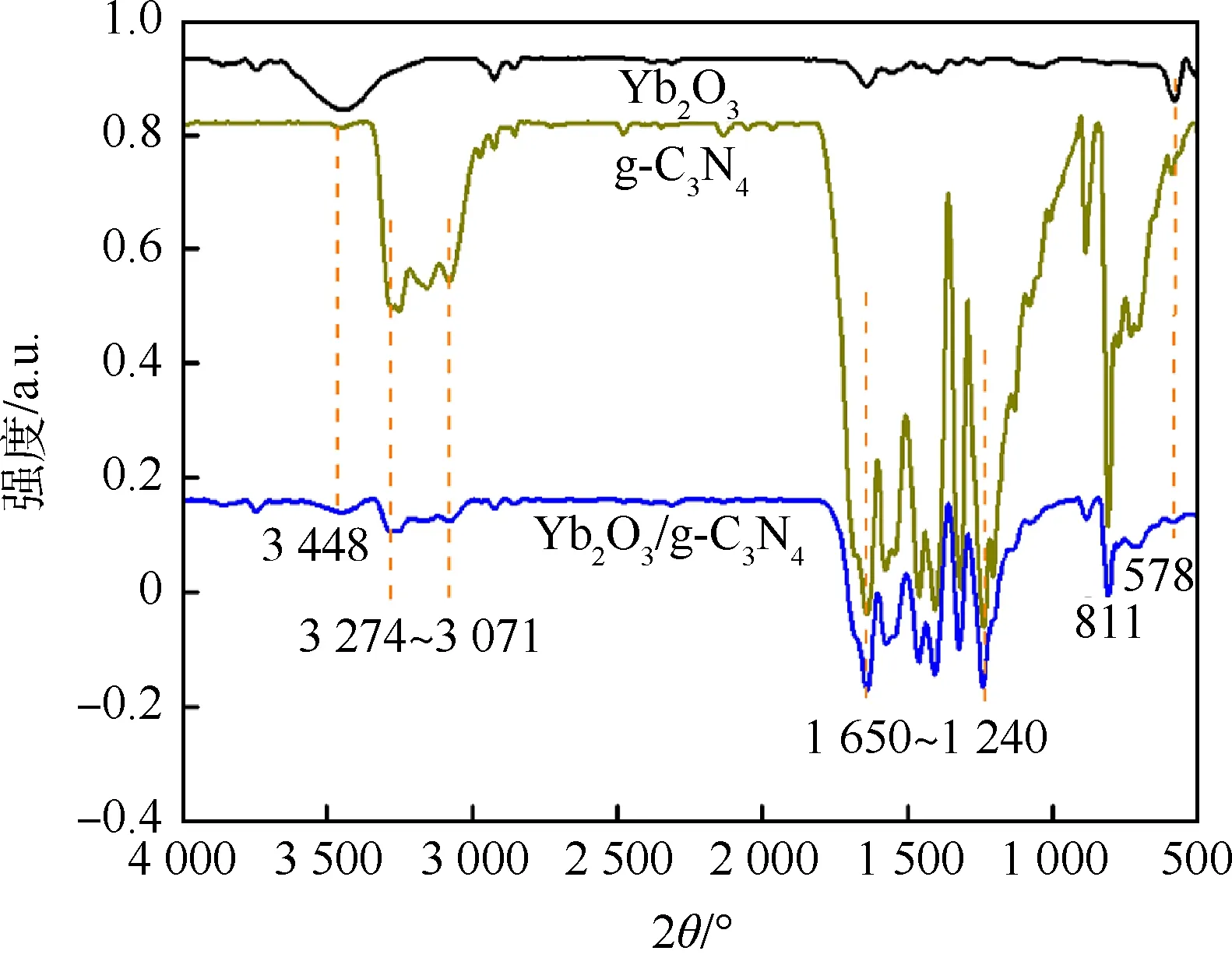
图3 Yb2O3、g-C3N4和Yb2O3/g-C3N4复合物的傅里叶变换红外光谱图
2.4 XPS分析

2.5 PL分析
光致发光被广泛应用于研究电子-空穴对复合和转移过程中.3种样品的PL谱如图5所示,复合光催化剂和g-C3N4的PL发射强度分别约为6 340和4 950 a.u.(458 nm处),Yb2O3/g-C3N4复合光催剂的PL值较小,这意味着光激电子和空穴的复合速率较低.研究表明,低的电子空穴复合率有利于光催化活性的提高[32].

图4 Yb2O3/g-C3N4的XPS谱图(a)全谱图;(b)C1s高分辨率谱图;(c)O1s高分辨率谱图;(d)N1s高分辨率谱图;(e)Yb4d高分辨率谱图
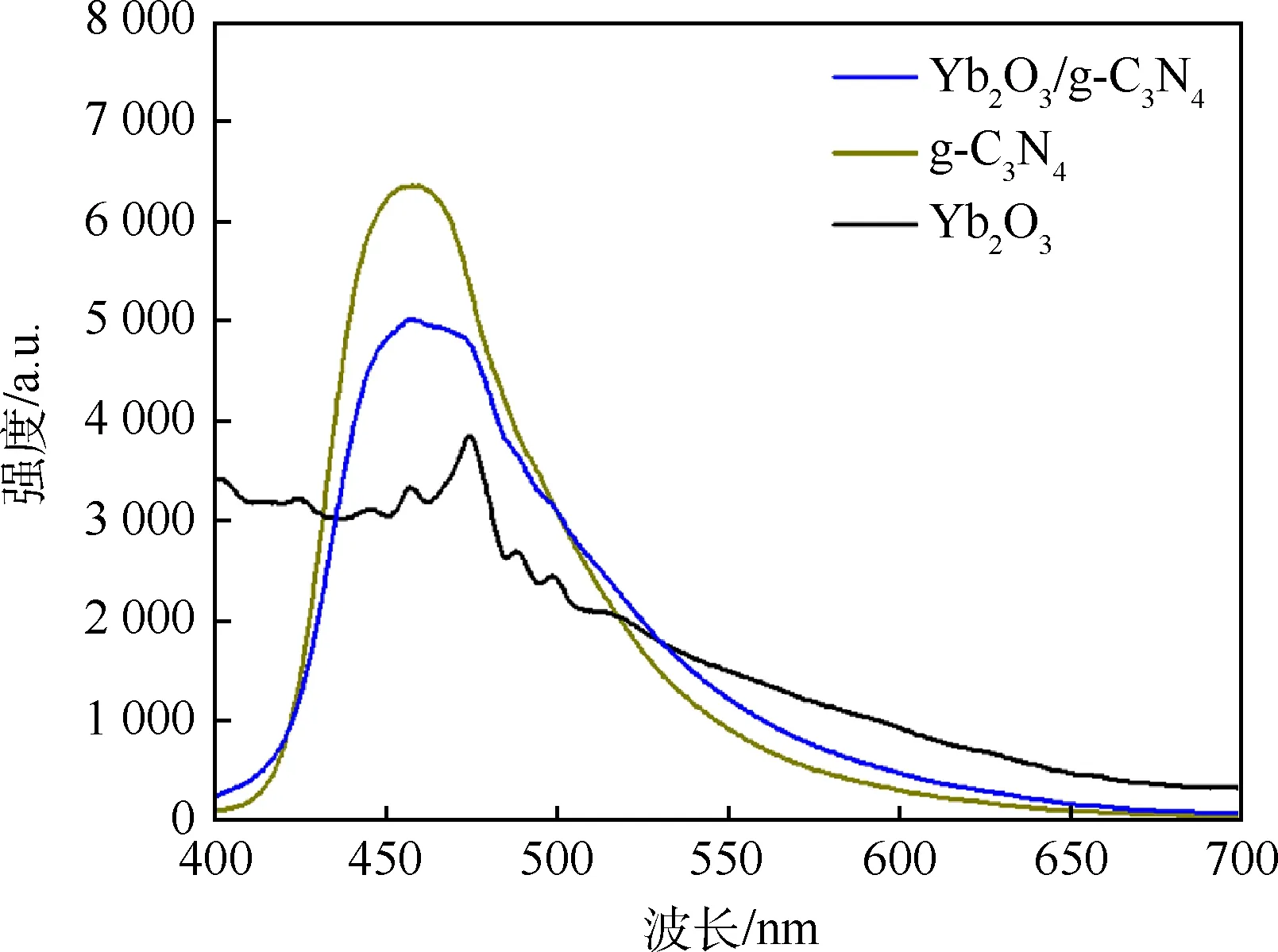
图5 Yb2O3、g-C3N4和Yb2O3/g-C3N4的光致发光图
2.6 UV-vis分析
Yb2O3、g-C3N4和Yb2O3/g-C3N4的UV-vis漫反射光谱(DRS)如图6(a),Yb2O3的主要吸收范围在紫外光区(220 nm),而Yb2O3/g-C3N4复合物的吸收范围扩大至可见光,吸收边缘在480~510 nm之间.这种现象与带隙之间活跃的能量转变有关.将(αhν)2与光能(hν)进行曲线拟合[33],如图6(b)所示.g-C3N4和Yb2O3的Eg分别约为2.90和4.98 eV.Yb2O3和g-C3N4两者复合能使样品具有更低的光谱吸收带边能量,可见光响应能力增加,这与之前的预测相吻合.
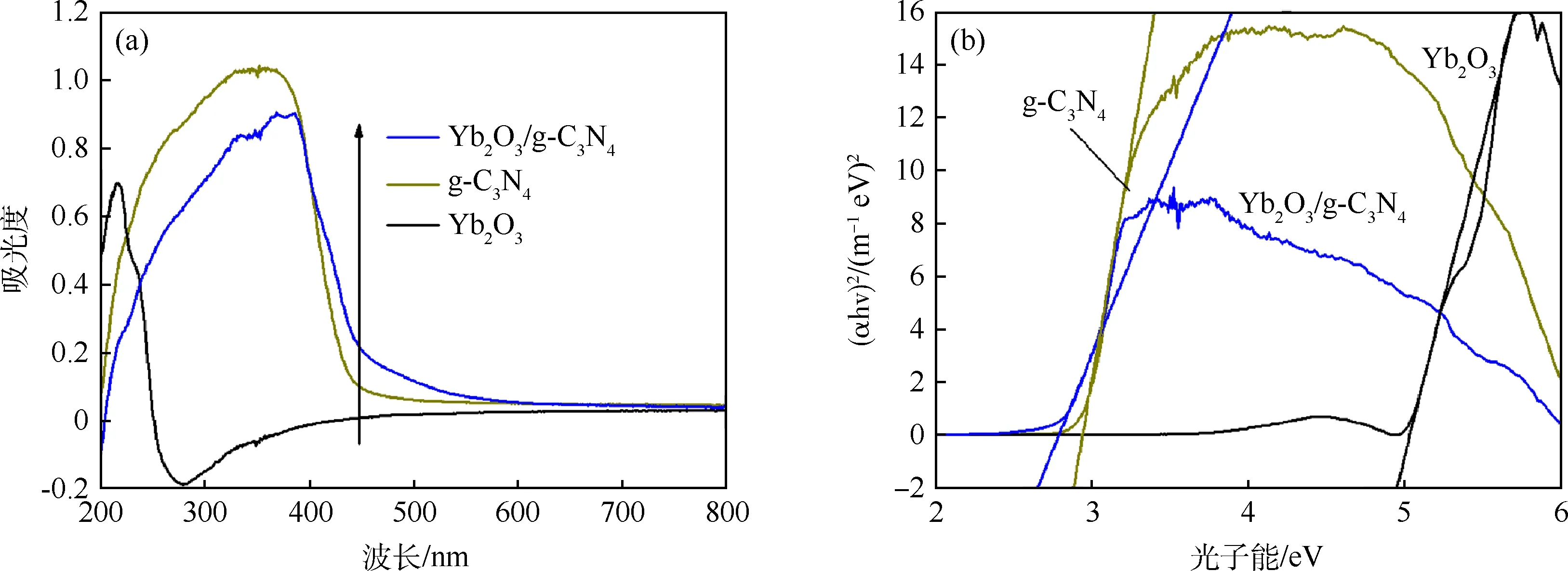
图6 Yb2O3、g-C3N4和Yb2O3/g-C3N4的(a)UV-vis漫反射光谱图和(b)禁带宽度图
2.7 降解性能分析
可见光条件下,Yb2O3、g-C3N4和Yb2O3/g-C3N4对苯酚和TTCH的降解效果如图7所示,降解率以不同时间点溶液浓度和溶液初始浓度的比(C/C0)进行计算.在不使用催化剂时,苯酚的降解率仅为9.80%.加入不同催化剂后,Yb2O3/g-C3N4催化剂的光催化性能最佳,g-C3N4的催化效果次之,而Yb2O3在可见光下对苯酚基本没有降解作用.光照3 h 后,Yb2O3/g-C3N4对苯酚的光催化降解率达到80.83%.优于以往报道g-C3N4/TiO2材料降解苯酚的效果(3 h,61%)[34].为了更直观地表达降解速率,本研究采用一阶模型拟合光催化降解数据如图7(b)所示,拟合数据显示,光催化效率与反应时间具有较好的线性关系,Yb2O3/g-C3N和g-C3N4的一级动力学反应速率常数(k)分别为0.006 45和0.001 69,拟合系数(R2)值分别为0.963 4和0.938 4.Yb2O3/g-C3N4对苯酚的降解速率是g-C3N4的3.80倍.
TTCH在自然环境中难以降解,TTCH在可见光下的自降解率仅为0.20%.加入不同催化剂后,Yb2O3/g-C3N4催化剂的光催化性能最佳,g-C3N4和Yb2O3的催化效果次之.光照3 h后,Yb2O3/g-C3N4催化剂能降解85.01%的TTCH.Yb2O3/g-C3N和g-C3N4降解TTCH的k值分别为0.015 05和0.002 29,R2值分别为0.926 6和0.987 1.Yb2O3/g-C3N4对TTCH的降解速率约为g-C3N4的6.57倍.与以往研究相比[7],Yb2O3/g-C3N4复合催化剂也展现了较为理想的光催化性能.

图7 不同催化剂在可见光下对苯酚的(a)降解效果图和(b)一阶动力学曲线图;不同催化剂在可见光下对盐酸四环素(TTCH)的(c)降解效果图和(d)一阶动力学曲线图
2.8 降解机理分析
2.9 稳定性
Yb2O3/g-C3N4光催化剂分别对苯酚和TTCH进行4次循环实验.在4次循环实验后,催化剂对TTCH的降解率分别是85.01%、82.95%、79.84%和79.59%,对苯酚的降解率分别是80.83%、80.66%、80.11%和80.32%.Yb2O3/g-C3N4降解TTCH的光催化性能逐渐下降,而降解苯酚的光催化性则较稳定.
3 结 论
本研究采用超声混合法制备Yb2O3/g-C3N4光催化剂.通过DRS和PL表征显示,新合成的光催化剂具有更加高效的可见光响应能力.Yb2O3/g-C3N4光催化剂在3 h光照下对20 mg/L苯酚的降解率为80.83%,是g-C3N4的3.80倍;在2 h光照下对20 mg/L TTCH的降解率为85.01%,降解速率约为g-C3N4的6.57倍.以往研究表明光催化技术可以将苯酚和TTCH等有机污染物分解为无害小分子物质.经验证,Yb2O3/g-C3N4复合光催化剂具有较为稳定的光催化性能.综上所述,Yb2O3/g-C3N4光催化剂是一种很有前途的光催化材料,在环境净化和可见光催化方面具有重要的应用价值.
