超声引导经皮微波消融治疗结直肠癌肝转移瘤不良事件及其影响因素
2019-12-19黄美近邓艳红黄玉笑刘广健
覃 斯,黄美近,邓艳红,陈 瑶,陈 秋,黄玉笑,刘广健*
(1.中山大学附属第六医院超声科,2.胃肠外科,3.肿瘤内科,广东 广州 510655)
热消融治疗结直肠癌肝转移瘤(colorectal liver metastases, CRLM)患者5年生存率达17%~51%,其对单发直径<3 cm的CRLM疗效与手术相当[1]。射频消融(radiofrequency ablation, RFA)和微波消融(microwave ablation, MWA)是临床应用最广泛的热消融技术。与RFA比较,MWA具有消融范围更大、消融时间更短、受“热沉效应”影响更小等优势[2],但目前针对MWA治疗CRLM不良事件(adverse event, AE)的大样本研究较少。本研究回顾性分析超声引导经皮MWA治疗CRLM的相关资料,探讨AE发生率及其影响因素。
1 资料与方法
1.1 一般资料 回顾性分析2013年6月—2018年6月于我院接受超声引导经皮MWA治疗的427例CRLM患者,男292例,女135例,年龄21~86岁,平均(56.8±11.8)岁;共消融治疗614例次、1 334个病灶,病灶直径5~67 mm、平均(15.42±7.23)mm,其中直径<30 mm者97.53%(1 301/1 334),≥30 mm者2.47%(33/1 334),36.81%(491/1 334)位于高危部位(病灶边缘距大血管、肝内胆管、胆囊、胃肠道、膈肌或肝包膜<5 mm)。
1.2 仪器与方法 采用GE Logiq E9超声仪为引导设备。所有治疗由同一位具有15年以上消融经验的主任医师操作,采用KY-2000 MWA治疗仪和KY-2450B型无菌一次性微波消融针。微波发射频率2 450 MHz,最大输出功率100 W,天线配置内部水循环降温系统。术前30 min予肌内注射杜冷丁50 mg+阿托品0.5 mg,穿刺前以2%利多卡因局部麻醉。对于靠近膈肌、胃肠道及肝包膜的病灶,消融前注射 10~30 ml生理盐水,建立水隔离带。按照消融范围完全覆盖肿瘤的原则,根据肿瘤大小和位置确定天线数目、消融功率及时间,对较大肿瘤采取多点重叠消融。
1.3 AE判定标准 AE分5级:1级,轻度AE,无需特殊治疗、有缺陷或错误但未形成事实;2级,中度AE,需行介入治疗或输血、门诊手术观察时间显著延长甚至过夜;3级,重度AE,需住院或超过原定住院时间>24 h、从普通病房转至ICU、需复杂介入治疗;4级,威胁生命或致残;5级,死亡,发生于消融后30天内[3]。按AE发生时间分3类:即时AE,消融后6~24 h内;围治疗期AE,消融后1~30天;后期AE,消融后30天后[4]。
1.4 统计学分析 采用SPSS 22.0统计分析软件。连续变量符合正态分布者以±s表示,采用t检验进行比较;分类变量比较采用四格表χ2检验;多因素分析采用Logistic回归模型,并计算优势比(odds ratio,OR)。P<0.05为差异有统计学意义。
2 结果
427例CRLM、消融614例次中,AE总发生率为4.89%(30/614),无消融相关死亡(表1)。AE中胆汁瘤最常见(图1),发生率为1.30%(8/614),无需治疗,其中 6个病灶随访3~62个月后消失,2个病灶随访 1~4个月后发生局部肿瘤进展,行手术切除。消化道穿孔发生率0.65%(4/614),消融前患者均有胃肠道手术史,且病灶靠近胃肠道,包括2例结肠穿孔(右半结肠手术史,病灶位于S6)、1例胃穿孔(胃穿孔修补术史,病灶位于S3)、1例吻合口近端小肠穿孔(右半结肠手术史,病灶位于S5);前3例消化道穿孔较小,与肝消融灶粘连并形成肝脓肿,予以超声引导腹腔及肝脓肿置管,充分冲洗并引流后好转(图2),1例吻合口近端小肠穿孔合并膈肌缺损,因病情危重行急诊手术。

表1 结直肠癌肝转移瘤微波消融后AE
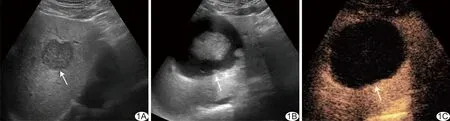
图1 患者男,46岁,乙状结肠癌肝转移 A.超声声像图示肝S4转移瘤(箭),约44 mm×37 mm; B、C.消融2个月后复查超声,消融灶呈混合回声(箭),约91 mm×78 mm(B),超声造影示病灶持续无增强,提示局部胆汁瘤形成(C,箭示病灶)
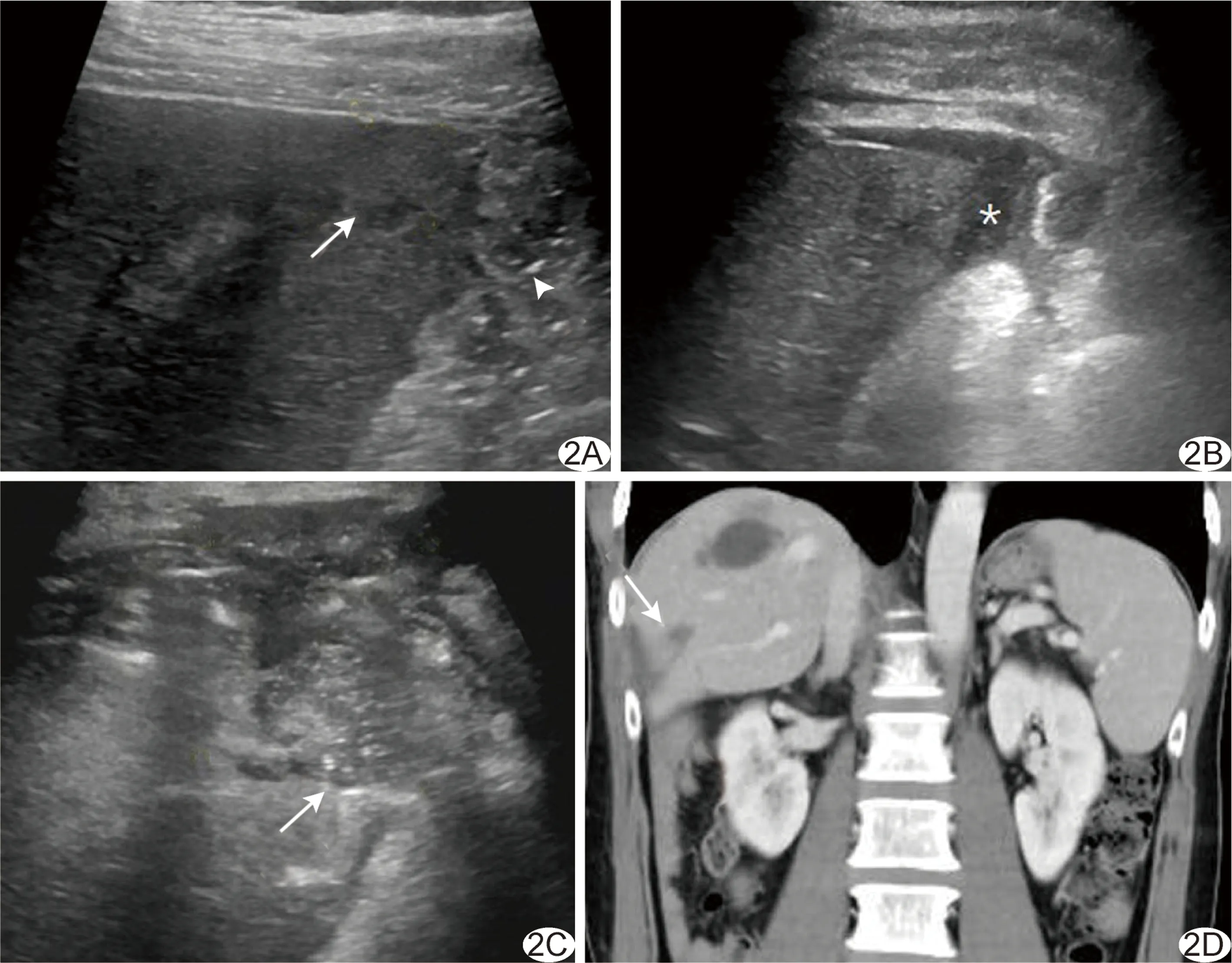
图2 患者男,47岁,右半结肠癌术后2年 A.超声声像图示肝S6转移瘤(箭),靠近结肠肝曲(箭头); B.消融后2周肝周积液(*),予超声引导穿刺置管引流; C.引流2周后复查,肝消融灶脓肿(箭)形成(予超声引导穿刺置管,持续引流冲洗1个月后拔管); D.消融后4个月复查CT,消融灶内(箭)及肝周积气、积液消失
影响AE的危险因素包括穿刺针数(OR=1.301,P=0.005)、高危部位病灶(OR=2.829,P=0.025)、病灶数>5 (OR=4.655,P=0.010)、有腹腔手术史(OR=7.716,P=0.047)及肝吸虫病(OR=17.683,P=0.005),见表2、3。
3 讨论
文献[5]报道MWA治疗CRLM后AE发生率为6.6%~29.0%,常见严重AE有肝脓肿、胆道损伤、消化道穿孔、胸膈并发症及出血等[6]。本组MWA治疗CRLM后AE发生率为4.89%,3~4级AE发生率为0.65%,需处理的AE(2~4级)发生率为2.28%(14/614),均处于较低水平,且无消融相关死亡发生,可能与以下方面有关:①MWA仪器无皮肤电极,内部水循环冷却天线能减少皮肤烫伤的发生;②同一位具有15年以上消融经验的医师实施消融,在一定程度上降低了并发症发生风险;③与肝癌患者相比,CRLM患者常无肝硬化背景,肝功能和凝血功能较好,降低了因肝功能不全而发生消融后出血、肝衰竭及死亡的风险[7]。
本研究结果显示,每例次穿刺针数及病灶数目是AE的影响因素。消融被推荐用于病灶不超过5个的CRLM患者[8]。病灶数目越多,相应穿刺针数越多,病灶数>5时AE发生率明显增高。穿刺针数亦与病灶大小及部位有关,完善的消融计划与精准的穿刺路径有利于减少穿刺针数。
消融后肝脓肿与高龄、糖尿病史、胆管吻合术史、肿瘤大小及部位等相关[9]。本组单纯性肝脓肿3例,其发生与上述因素无明显相关,但患者均于消融前2周内接受原发灶切除术,考虑肠道细菌沿胆道侵袭消融灶引起脓肿,均予置管引流处理,取得了较好疗效[9]。对消融前2周内有腹腔手术史者,围手术期内应给予积极抗感染处理。此外,腹腔手术史是AE的影响因素,术后腹腔存在不同程度粘连,消融后易发生消化道穿孔[6]。尤其对于有右半结肠手术史者,病灶接近肠道时,建议消融前进行充分胃肠道准备,建立人工腹腔积液,将病灶与胃肠道隔离,小功率消融,消融后禁食24 h,密切监测生命体征,以便早期发现穿孔[10]。
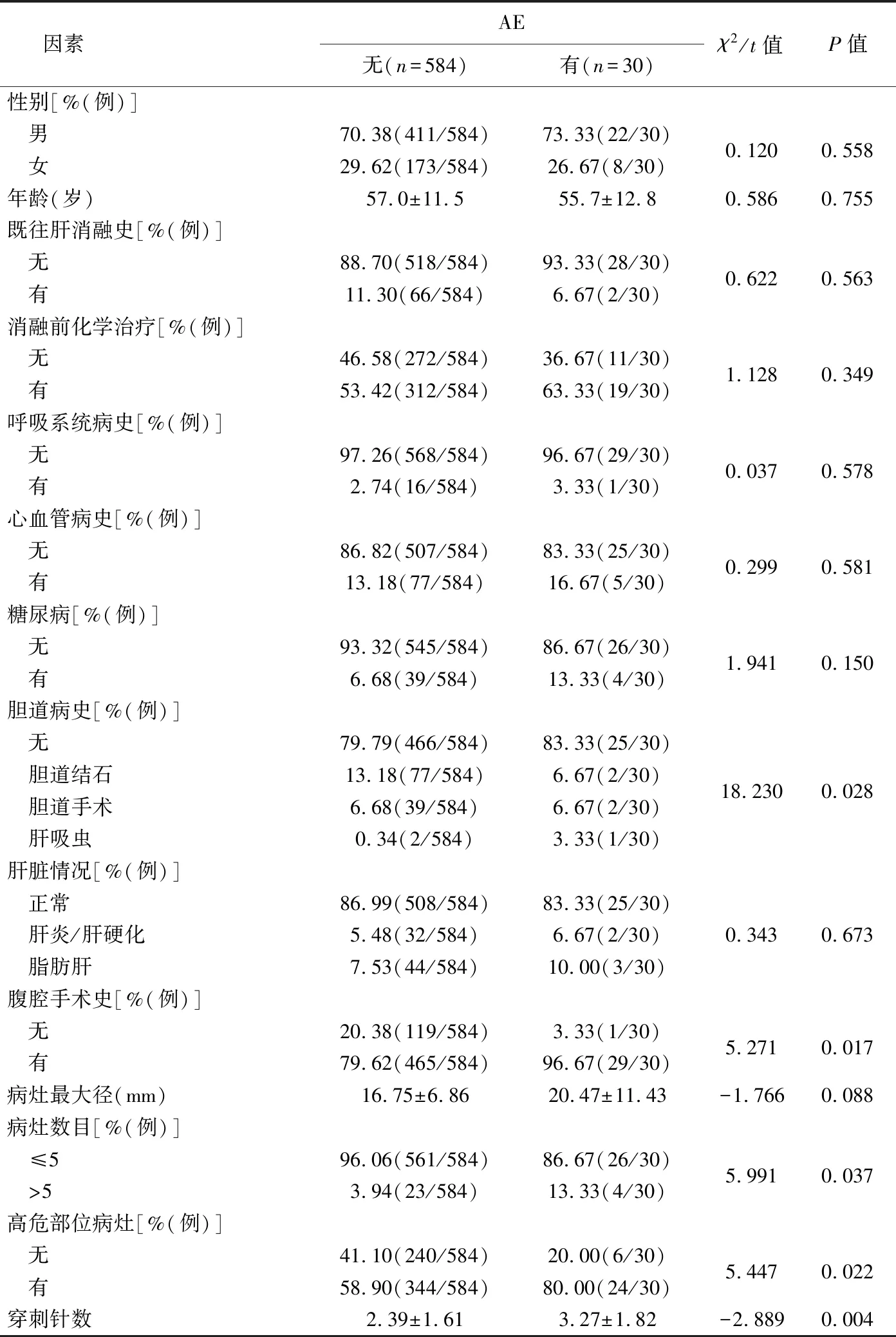
表2 结直肠癌肝转移瘤微波消融后出现AE的单因素分析
注:肝吸虫寄生于肝内胆管故归为胆道病史
肝吸虫病是AE的影响因素,本组50%肝吸虫病患者消融后出现胆汁瘤。肝吸虫寄生于肝内胆管,机械性损伤、分泌物和代谢物所引起的炎症反应可刺激胆管上皮细胞增生及进行性纤维化,引起胆管炎、胆道梗阻[11],胆管内胆汁流速远低于血液,热沉效应小,热凝作用易损伤胆管及其周围毛细血管丛,导致肝内胆管坏死,继而胆管狭窄、上游胆管扩张或破裂,胆汁于肝内局部积聚形成胆汁瘤。热消融引起胆汁瘤的发生率为0.2%~8%[12],大部分胆汁瘤无需治疗,长期保持稳定或自发消退,少量发生局部肿瘤进展,需行手术切除。
高危部位病灶治疗难度大,AE发生率高。本组胸腔积液、膈肌和邻近肺组织热灼伤、膈肌缺损见于近膈肌病灶,由膈肌热损伤引起,其中膈肌和邻近肺组织热灼伤患者消融前有慢性阻塞性肺疾病急性发作病史,予胸腔穿刺引流、抗感染对症治疗后好转。1例膈肌缺损并血气胸患者需急诊手术。对靠近膈肌的病灶,建立人工胸腔积液/膈下积液可帮助清晰显示病灶并有效保护膈肌[13]。肝周及腹腔积液见于近肝包膜病灶,积液量一般较少,予穿刺抽液或引流后好转。本组1例腹腔大量积液见于直径67 mm病灶,消融后白蛋白明显降低,考虑低蛋白血症引起腹腔积液,予补充白蛋白、腹腔穿刺引流后好转。对近肝包膜病灶,建议充分浸润麻醉肝包膜,避免直接穿刺肿瘤;消融后及时复查肝周及腹腔情况,症状明显或积液量大时予抽液或引流。消融近肝内胆管病灶易损伤肝内胆管,受损胆管上游胆管扩张和胆汁瘤是主要表现形式[14]。本组发生消融灶旁肝内胆管轻度扩张及胆汁瘤者均无症状,且血清胆红素正常,无需治疗,仅定期随访。
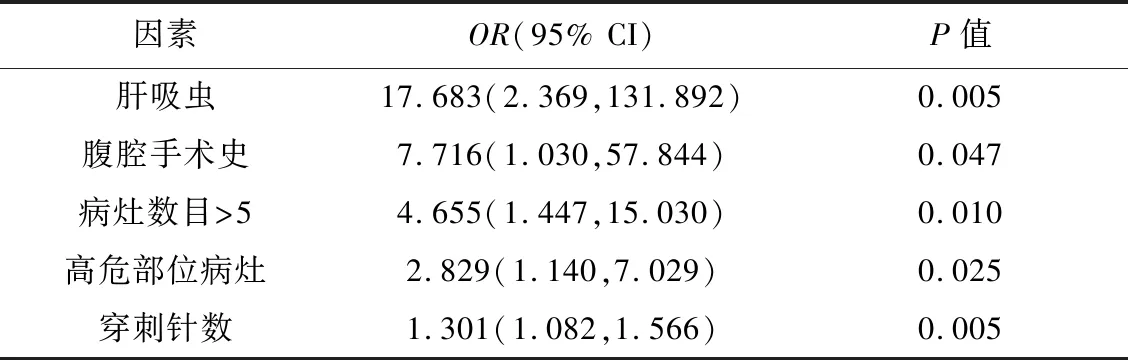
表3 结直肠癌肝转移瘤微波消融后出现AE的Logistic回归分析
综上所述,超声引导经皮MWA治疗CRLM的AE发生率不高,是安全的局部治疗方法。AE发生与病灶数目、高危部位、穿刺针数、腹腔手术史及肝吸虫病有关。对CRLM患者行MWA治疗前,需综合考虑其腹腔手术史及肝吸虫病史,综合评估病灶数目及部位,选择适当消融方案;术后密切监测患者病情变化,及时发现AE并采取有效治疗手段,以减少AE的发生及危害。