不同部位起源的室性心律失常三维心腔内超声的标测与消融
2019-12-17李康丁燕生周菁
李康 丁燕生 周菁
近年来关于右室流出道肺动脉窦室性早搏(简称室早)/室性心动过速(简称室速)瓣上消融的研究较为引起关注[1-2],消融导管头端和杆身在肺动脉内做倒“U”塑形,消融的靶点位置究竟是不是在瓣上以及是否会损伤肺动脉瓣并不容易确定[3]。左室流出道尤其是左室顶部(Summit区)结构复杂,有部分学者认为此部位及邻近区域的室早有时需要做“解剖消融”,成功靶点可能并非最早激动起源[4]。左右室的乳头肌因为结构复杂、位置多变,以往很难消融成功且复发率较高[5-6]。而His束旁室早,易发生传导束损伤,消融风险高。三维心腔内超声有助于解剖关系的判断和导管贴靠的定位,笔者探讨使用Soundstar三维心腔内超声导管(简称Soundstar导管,Johnson,美国),在Carto3三维系统中(Johnson,美国)行左右室及邻近结构的解剖重建,结合室早/室速激动标测进行精准消融的方法。
1 资料与方法
1.1研究对象 自2016年4月至2019年7月,本中心使用Soundstar三维心腔内超声导管进行特发性室早/室速标测消融17例患者,年龄[49.53±12.79(28~74)]岁,男女比例10∶7。术前常规行24 h动态心电图、经胸超声心动检查,部分患者术前接受了心脏增强核磁扫描,以除外明显结构性心脏病。
1.2标测与消融 术中常规穿刺双侧股静脉,置入6 F和8 F静脉鞘管,部分患者使用Swartz长鞘,术前根据心电图判断室早/室速为左室起源的病例则穿刺股动脉和/或采取穿刺房间隔入路,每例患者术中均置入十极可调弯冠状窦电极。标测与消融具体流程如下:
(1)经左侧股静脉置入12 F静脉鞘。
(2)经左侧12 F股静脉鞘送入10 F Soundstar导管。
(3)将Soundstar导管送至右房内打P弯贴靠右房后壁进行呼吸门控。
(4)在右房中部平卵圆窝水平的基本位(homeview)切面,可见主动脉长轴、主动脉窦无冠窦和右冠窦、右房、三尖瓣、右室。在主动脉窦无冠窦(NCC)与三尖瓣环之间标记His束心房侧所在位置,同时进行主动脉长轴建模。顺钟向旋转Soundstar导管即可完成右室长轴建模,在逐个超声扇面上标记三尖瓣瓣环附着点。
(5)Soundstar导管在右房内,右前斜位体位,平His束水平,参照上一步骤标记的三尖瓣环,打A弯前送跨越三尖瓣环进入右室内,此时松开A弯顺钟向旋转180度可进行主动脉根部(主动脉窦)短轴建模。此时Soundstar导管位于右室流出道下方,恰好邻近于右室流出道、主动脉窦的左冠窦和右冠窦。
(6)Soundstar在右室流出道下方,超声扇面打向“俯视位”可直视采集到右室乳头肌和调节束图像。逆钟向旋转Soundstar导管即可见到右室调节束插入游离壁处。
(7)Soundstar导管顺钟向旋转即贴向室间隔,调整超声扇面角度沿室间隔打L弯,将导管头端自上而下压低,即可进行左室长轴及左室乳头肌建模。
(8)完成左室长轴建模之后,松L弯,贴在右室室上嵴,逐渐旋转Soundstar导管使得超声扇面由心底部逐渐移动至心尖部,进行左室和右室短轴建模。
(9)根据体表心电图室早/室速形态,判断大致起源。对于以下情况:
①对于需要鉴别右室流出道肺动脉窦瓣上与瓣下的病例,将Soundstar导管在右房内打A弯跨三尖瓣环后松开A弯送至右室室上嵴,之后打P弯扇面指向流出道同时顺钟向转向室间隔,即可清晰展示主动脉窦短轴与肺动脉窦长轴,辨认肺动脉窦瓣上与瓣下。
②对于需要鉴别主动脉窦瓣上、瓣下和主动脉瓣-二尖瓣连接部(AMC)的病例,主动脉窦的三个窦、二尖瓣环需要在窦性心律下按照长轴+短轴交叉的原则分别精细建模。消融时Soundstar导管回到homeview切面稍打P弯超声扇面指向左上方即可展示主动脉窦长轴来判断瓣上或瓣下。
③对于需要鉴别左室乳头肌和左前/后分支起源的病例,在窦性心律下使用Soundstar导管进行左室乳头肌长轴建模,室早/室速激动标测和消融时Soundstar导管的超声扇面仍保持左室乳头肌长轴切面,以确定消融导管头端的位置和贴靠。
④对于疑似His束旁或邻近部位室早的病例,需要使用消融导管在左、右室间隔侧与主动脉窦无冠窦和右冠窦进行精细标测。Soundstar导管跨三尖瓣环后送至右室室上嵴,打L弯超声扇面向下同时显示左右室长轴和室间隔,或在右房侧接近homeview角度展示三尖瓣环,即可直视消融导管头端与三尖瓣环间隔部的贴靠。
(10)三维解剖建模完成之后,使用Tc或ST冷盐水灌注消融导管(Johnson & Johnson,美国)进行点对点逐点室早/室速激动标测,此时Soundstar导管随消融导管的移动平行打超声扇面,在实时心腔内超声直视下判断消融靶点的心室壁与毗邻解剖结构关系,如瓣环、肌小梁,以及消融导管头端的贴靠。
(11)右室流出道起源的室早/室速病例分别在肺动脉窦的瓣下和瓣上进行激动标测,主动脉窦及邻近起源的病例分别在主动脉窦的瓣上和瓣下进行标测。消融靶点室早较体表提前20 ms以上,部分患者局部有碎裂多波折电位。设置射频仪为冷盐水灌注功率模式,功率30~35 W,冷盐水灌注17 ml/h,放电30 s之内室早消失为有效消融靶点。
(12)消融后观察至少15 min,并静脉输注异丙基肾上腺素至心率上升至120次/分,再观察至心率下降到给药前水平后15 min,室早消失,室速患者重复心室刺激不能再诱发心动过速,为即刻消融成功。
(13)消融术后随访3个月以上,分别于术后1个月和3个月复查24 h动态心电图,室早负荷较术前减少≥70%或消失为有效。
2 结果
17例病例(15例室早、2例室速),消融靶点分别位于:2例主动脉窦、1例主动脉瓣-二尖瓣连接部(AMC)、4例左室乳头肌、2例左前分支、1例左后分支、3例右室流出道肺动脉窦瓣上、1例右室流出道前下、2例右室乳头肌、1例His束旁(三尖瓣环间隔部)。上述部分病例的体表心电图、X线靶点图、Soundstar心腔内超声三维重建模型、及心腔内超声图分别见图1~6。
17例患者消融术中室早/室速均消失,100%消融即刻成功。消融术后随访3个月以上(3~28个月),其中1例(5.88%)患者(起源于右室流出道肺动脉右窦)室早有复发。另外1例(5.88%)患者(起源于三尖瓣环间隔部His束旁室早)消融术后出现腹股沟血肿,后逐渐吸收,无其他不良并发症。
3 讨论
Soundstar三维心腔内超声使得室性心律失常的标测与消融可视化,对于二维透视和三维标测上“不可见”的结构可以清晰直视,并实时显示导管与特定解剖结构之间的关系,和连续观察导管头端与组织的接触与贴靠[7]。既能够提供准确的解剖定位信息,又能够提高消融有效性,还能够直视消融过程中心肌组织回声的变化,避免过度损伤。对于器质性心脏病室速还可辨认致心律失常心肌瘢痕。本组室性心律失常消融病例中,有1例为肥厚型心肌病, Soundstar直视下可见左室乳头肌异常粗大,室早起源于左后乳头肌,成功消融术后随访18个月室早未复发(见图1)。

心腔内超声可见消融导管头端贴靠在左后乳头肌的两侧进行消融。ABL:消融导管;CS:冠状静脉窦电极;Soundstar:心腔内超声导管;ICE:心腔内超声;LV:左室;APM:前乳头肌;PPM:后乳头肌;IVS:室间隔图1 合并肥厚型心肌病的左后乳头肌室早消融
以往认为临床最常见的特发性室性心律失常多数起源于右室流出道,近年来消融导管在肺动脉瓣上倒U构型消融被广泛关注和推广,导管头端贴靠是否倒U构型就在肺动脉瓣上?解剖位置仅凭借造影还不能确定,而心腔内超声则可以清晰显示(见图2)。在心腔内超声直视下的操作安全性倍增。
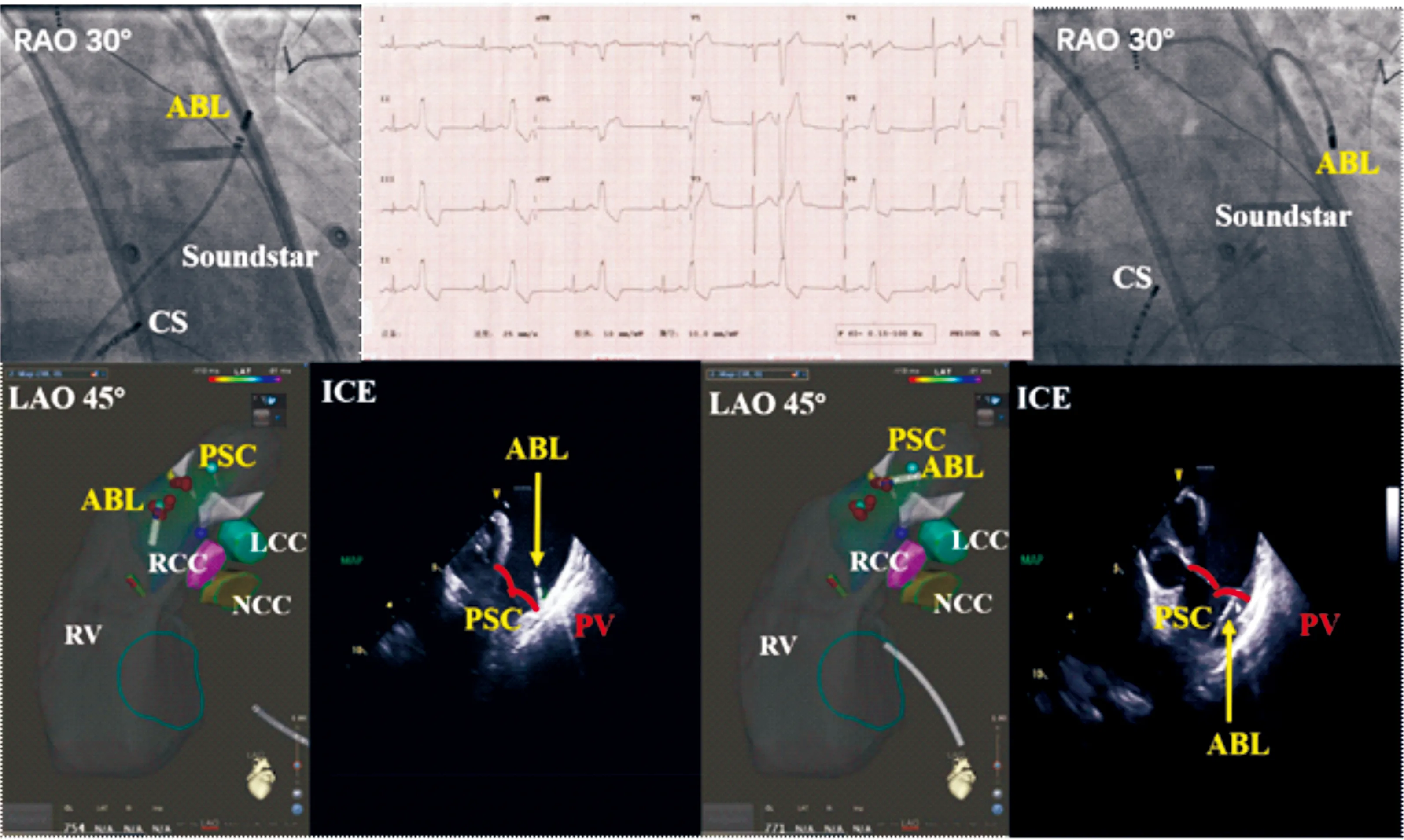
心腔内超声可显示导管头端位于瓣下和瓣上,该病例在瓣上消融成功。ABL:消融导管;CS:冠状静脉窦电极;Soundstar:心腔内超声导管;ICE:心腔内超声;LCC:左冠窦;RCC:右冠窦;NCC:无冠窦;RV:右室;PSC:肺动脉窦;PV:肺动脉瓣图2 右室流出道室早分别在肺动脉右窦的瓣下和瓣上进行消融
对于主动脉窦及邻近解剖位置起源的室早,通常称为Summit室早,此区域消融困难往往在于解剖屏障造成导管不能到达或不能贴靠,Soundstar心腔内超声可以精准重建解剖结构,并实时显示导管位置和邻近解剖关系(见图3、4)。需要注意的是靶点与冠状动脉开口的距离,如果导管头端心腔内超声确定在主动脉窦的窦底或两个窦交界处,通常距离冠状动脉开口在1cm以上,较为安全,可以无需造影。左主干冠状动脉的开口可以在主动脉窦短轴切面清晰显示,而右冠状动脉则可将Soundstar导管送至右室流出道打P弯超声扇面向上显示升主动脉长轴再顺钟向旋转至右冠窦上方,即可见右冠状动脉开口[7-8]。

心腔内超声可见消融导管头端位于右冠窦的窦底,靶点起始电位碎裂。ABL:消融导管;CS:冠状静脉窦电极;Soundstar:心腔内超声导管;ICE:心腔内超声;LCC:左冠窦;RCC:右冠窦;NCC:无冠窦;LV:左室;RV:右室图3 Summit室早在主动脉窦右冠窦内消融

消融靶点位于主动脉窦左冠窦与二尖瓣环之间,消融导管打弯跨过主动脉瓣反勾在AMC区域。ABL:消融导管;CS:冠状静脉窦电极;Soundstar:心腔内超声导管;ICE:心腔内超声;LCC:左冠窦;RCC:右冠窦;NCC:无冠窦;AMC:主动脉瓣-二尖瓣连接部;MA:二尖瓣环图4 Summit室早在主动脉瓣-二尖瓣连接部(AMC)消融
以往的经验告诉我们:乳头肌起源多数为室早,分支起源多数为室速。近年来认为束支和浦肯野氏纤维可以进入乳头肌[5]。因此通过心电图室早或室速的QRS波形态并不能肯定预判起源于乳头肌还是左前/后分支,心腔内电图中消融导管头端记录到浦肯野电位也不能完全鉴别。借助Carto三维标测系统,Soundstar心腔内超声可以展示解剖关系、导管位置、头端贴靠,提供更多信息(见图5)。可以在心腔内超声直视下沿乳头肌基底部至与腱索连接部进行连续的激动标测,分辨同组乳头肌的不同肉柱,和与心室壁的关系[6]。

心腔内超声可见消融导管贴靠在左室间隔部,而非乳头肌。ABL:消融导管;CS:冠状静脉窦电极;Soundstar:心腔内超声导管;RV:右室;ICE:心腔内超声;LCC:左冠窦;RCC:右冠窦;NCC:无冠窦;LM:冠状动脉左主干;APM:前乳头肌;PPM:后乳头肌;LAF:左前分支;LPF:左后分支图5 左后分支室速消融
His束旁室早,Soundstar导管解剖建模时需要标记His束和三尖瓣环(三尖瓣膜与瓣环附着点),点对点激动标测时精细标测三尖瓣环间隔部和左右室间隔部,出于安全性考虑,消融推荐在可调弯长鞘支撑下消融导管打“C”形弯反勾在三尖瓣隔瓣下方[9]。心腔内超声可以直视导管稳定性和与His束的空间距离(见图6)。
综上所述,对于不同部位室性心律失常,使用Soundstar心腔内超声导管和Carto三维标测系统,可直视导管位置与贴靠,有助于提高消融成功率和安全性,期待更多经验积累。
