卵母细胞的脱颗粒时间对胚胎质量和ICSI妊娠结局的影响
2019-12-13王雪肖亚玲孙正怡甄璟然郁琦邓成艳周远征王含必
王雪,肖亚玲,孙正怡,甄璟然,郁琦,邓成艳,周远征,王含必
(中国医学科学院 北京协和医学院 北京协和医院妇科内分泌与生殖中心,北京 100730)
1992年,Palermo等[1]首次将卵胞浆内单精子注射(intracytoplasmic sperm injection,ICSI)技术应用到辅助生殖技术(ART)领域,ICSI已经成为治疗男性因素不育的有效措施。在ICSI操作前,需要剥除卵母细胞周围的颗粒细胞,一方面颗粒细胞会阻碍注射针,干扰卵母细胞注射,另一方面去除颗粒细胞后可以清楚地评估卵母细胞的减数分裂状态。在胚胎学实验室,胚胎学家习惯性在获卵和卵母细胞脱颗粒以及卵母细胞脱颗粒和ICSI之间等待一定的时间,原因是卵母细胞在获卵后可能需要一定的时间来恢复。然而,对于所有操作的精确时间尚无定论。有研究认为卵母细胞脱颗粒时间和ICSI时间对成熟卵率无影响,但是对受精率有显著影响,认为脱颗粒前的孵育时间越久受精率越高,但要控制在3 h内,而脱颗粒后立即行ICSI能够达到最优受精率[2-3]。还有研究发现延迟脱颗粒可以显著提高优质囊胚形成率[4]。而有一些研究则发现卵母细胞脱颗粒时间对ICSI结局无影响,认为脱颗粒时间和ICSI时间对受精率和临床结局的影响不大[5-6]。考虑到这些结论的不一致性,本研究的目的是对获卵-脱颗粒和脱颗粒-ICSI之间的时间对ICSI结局的影响进行分析,为确定操作的最佳时间提供依据,从而进一步改善ICSI结局。
资料与方法
一、研究对象
回顾性分析2017年3月至2018年1月在本院辅助生殖中心进行ICSI治疗的380例患者(408个周期)的临床资料。患者纳入标准:(1)男方因素不育;(2)前次IVF治疗失败史;(3)年龄<42岁。排除标准:(1)合并存在内科疾病的患者,如高血压、糖尿病、肝脏疾病、甲状腺功能异常等;(2)存在肿瘤病史的患者;(3)存在夫妻双方染色体异常者;(4)卵巢储备功能下降(获卵数<5个)者;(5)行胚胎植入前遗传学筛选的患者;(6)行附睾穿刺取精患者。
二、研究方法
1. 促排卵及取卵:选择本中心常规的促排卵方案,包括激动剂长方案和拮抗剂方案,使用卵泡刺激素(FSH,果纳芬,默克雪兰诺,瑞士)进行卵巢刺激。当有3个卵泡直径达到18~20 mm时注射HCG(艾泽,250 μg/支,Serono,瑞士)250 μg,此后38 h经阴道超声引导下取卵。
2. 脱颗粒细胞及ICSI操作:按照本实验室的工作常规,将获得的卵母细胞放入受精液(G-IVF Plus,Vitrolife,瑞典)中培养一段时间,再将其放入透明质酸酶(hyaluronidase,80 U/ml,Vitrolife,瑞典)中消化片刻,时间控制在30 s内,然后将其吸出放入受精液中,用不同孔径的毛细管不断吹打,直至完全去除颗粒细胞。将拆除颗粒细胞的卵母细胞放入CO2培养箱内继续培养一段时间,准备进行ICSI。每次操作前记录时间。进行ICSI操作前,在7%的聚乙烯吡咯烷酮(PVP,Vitrolife,瑞典)液滴中选择形态正常、活动力好的精子进行制动,然后将卵母细胞放置培养液(G-MOPS Plus,Vitrolife,瑞典)中,进行ICSI操作。单精子注射时,用固定针将卵母细胞固定,并将极体放置12点位置,注射针从3点位置进入,回吸,确认卵母细胞膜破裂后将精子注入卵母细胞胞浆内,缓慢退出注射针。将注射完的卵母细胞用卵裂期培养液(G1,Vitrolife,瑞典)充分冲洗,并放置提前配置好的G1培养液中,放入37℃、6%CO2、5%O2的三气培养箱内培养。
3. 胚胎的观察和评估:ICSI后的16~18 h(受精后第1天)观察卵母细胞的受精情况,并换液,继续用卵裂期培养基培养,第3天观察卵裂球的分裂情况,根据胚胎卵裂球数目、细胞质均一性、碎片多少等进行胚胎评分,我们将卵裂球数目为6或8,评级为Ⅰ或Ⅱ的胚胎定义为优质胚胎。在移植日挑选质量最好的2枚胚胎进行移植,其他胚胎转移至囊胚培养液(G2,Vitrolife,瑞典)中继续培养。如果移植当日因特殊情况不能移植者,将此两枚胚胎冷冻保存或继续培养。在受精后第5日或第6日观察囊胚形成情况,并根据Gardner评分法[7]进行评分,挑选内细胞团质量达到A或B级的囊胚进行冷冻,C级的囊胚放弃,滋养细胞层的质量不限。具体的冷冻操作方法按照本中心常规进行。
4. 妊娠结局的判断及观察指标:移植后第7日检测血清HCG水平,HCG>5 U/L判断为生化妊娠;移植后4周行超声检查,超声下可见胎心及胎囊者判断为临床妊娠。受精率=正常受精数/MⅡ卵母细胞数×100%;优质胚胎率=优质胚胎数/卵裂数×100%;囊胚形成率=囊胚数/(卵裂数-移植数-卵裂期冷冻数)×100%;种植率=着床胚胎数/移植胚胎数×100%;临床妊娠率=临床妊娠例数/移植周期数×100%;活产率=随访获得活产的总例数/移植周期数×100%。
5. 分组标准:取卵至脱颗粒的时间定义为T1,脱颗粒至ICSI的时间定义为T2,取卵至ICSI的时间定义为T3(具体示意见图1)。本研究中T1平均值为(0.56±0.30)h(0.08~1.92 h),因此将患者分为3组,分别为A1组≤0.5 h,B1组0.5~1.0 h,C1组≥1 h。T2的平均值为(2.13±0.87)h(0.33~6.05 h),据此将患者分为3组:A2组≤2 h,B2组2~3 h,C2组>3 h。T3的均值为(2.69±0.87)h(0.67~6.77 h),亦将患者分为3组:A3组≤2.5 h,B3组2.5~3.5 h,C3组>3.5 h。
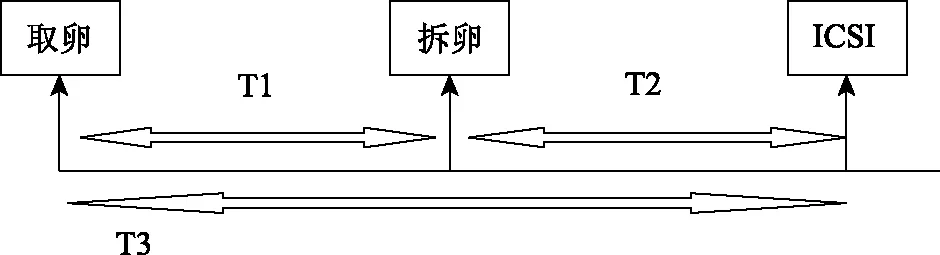
图1 T1和T2的定义示意图
三、统计学分析
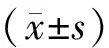
结 果
一、一般情况
本研究共纳入380例患者(408个ICSI周期)的资料,平均年龄(34.7±4.1)岁。共移植350个周期,超声下见到妊娠囊182个,种植率为25.4%(182/717),145例患者获得临床妊娠,临床妊娠率为41.4%(145/350),妊娠后流产30例,流产率为20.7%(30/145),宫外孕发生率为0.29%(1/350),活产率为32.0%(112/350)。
二、不同组别间胚胎发育情况及妊娠结局比较
1.取卵-脱颗粒时间对胚胎发育及妊娠结局的影响:不同T1时间的3组中的年龄、不育年限、FSH应用总剂量及拮抗剂方案比例比较均无显著性差异(P>0.05)(表1);3组间的受精率、优胚率、囊胚形成率、种植率、临床妊娠率、流产率和活产率比较均无统计学差异(P均>0.05)(表2)。
2.脱颗粒-ICSI时间对胚胎及妊娠结局的影响:不同T2时间的3组间年龄、不育年限及FSH应用总剂量比较均无显著性差异(P>0.05),3组间的拮抗剂方案比例比较亦无显著性差异(P>0.05)(表3)。3组间的受精率比较有显著性差异,C2组显著高于A2组和B2组(P<0.05);囊胚形成率3组间比较亦有显著性差异,C2组显著高于A2组(P<0.05);3组间的优胚率、种植率、临床妊娠率、流产率及活产率比较均无显著性差异(P均>0.05),但B2组的种植率、临床妊娠率和活产率有略高于其他两组的趋势(表4)。
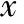
表1 不同T1三组间一般情况的比较[(-±s),%]
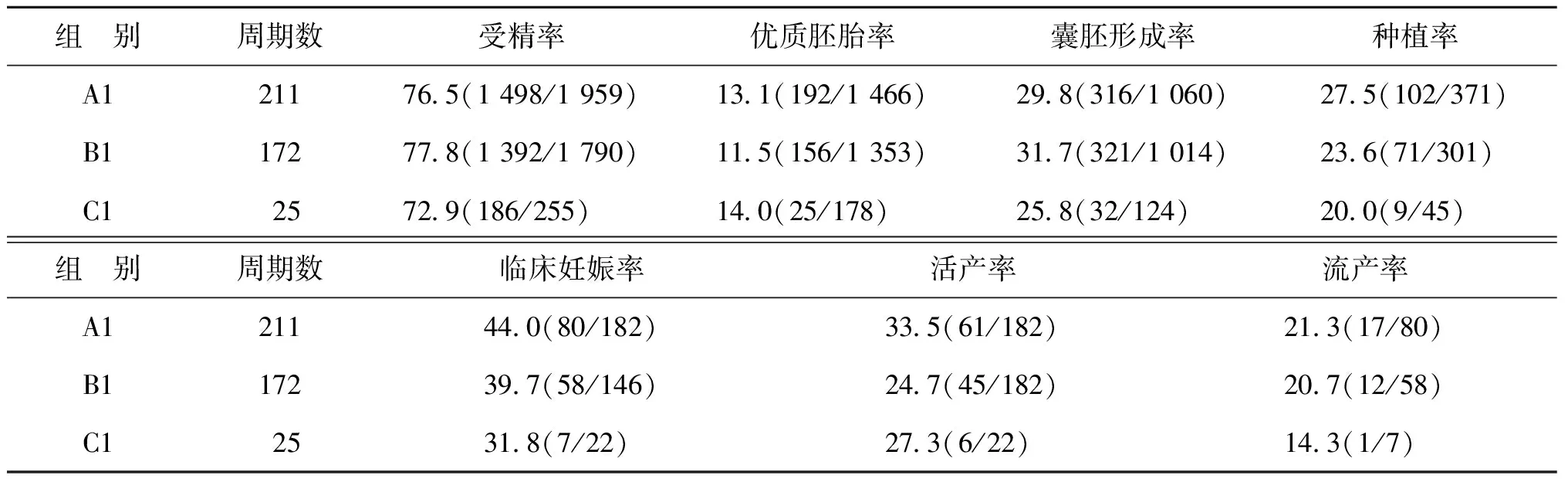
表2 不同T1三组间胚胎发育及妊娠结局比较(%)
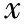
表3 不同T2三组间一般情况的比较[(-±s),%]
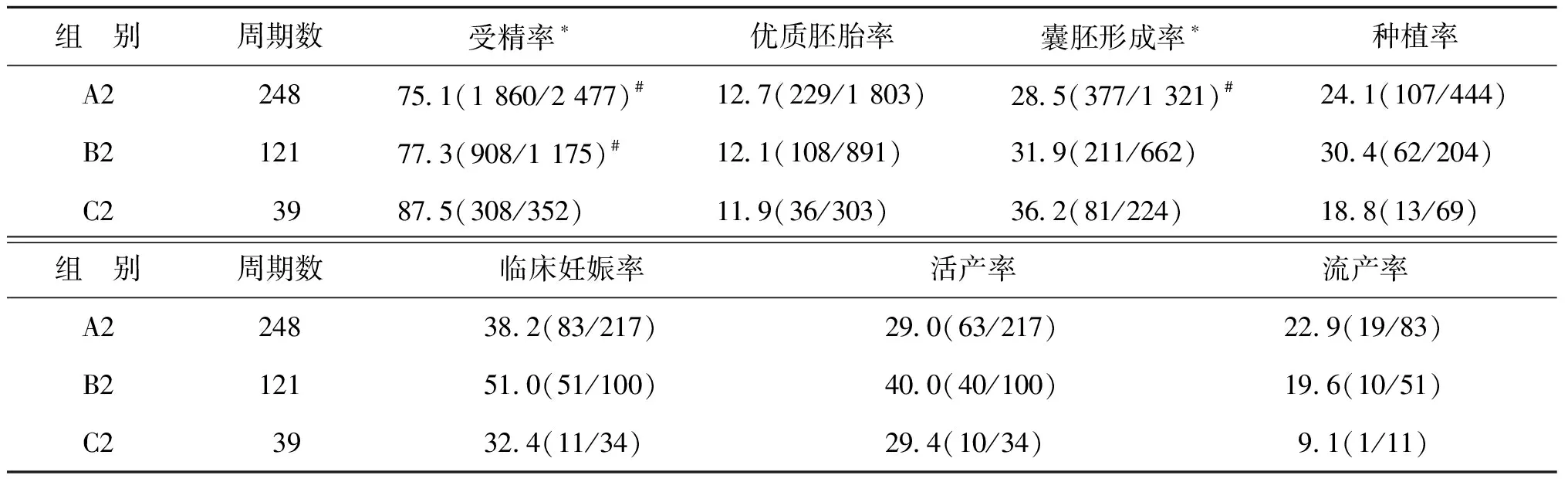
表4 不同T2三组间胚胎发育及妊娠结局比较(%)
3.取卵-ICSI时间对胚胎及妊娠结局的影响:3组间的年龄、不育年限及FSH应用总剂量比较均无显著性差异(P>0.05),3组间的拮抗剂方案比例比较亦无显著性差异(P>0.05)(表5)。3组间的受精率比较有显著性差异,C3组显著高于A3组和B3组(P<0.05);3组间的囊胚形成率比较无显著性差异,C3组有略高于A3和B3组的趋势(P>0.05);3组间的优胚率、种植率、临床妊娠率、流产率及活产率比较均无显著性差异(P均>0.05),但B3组的种植率、临床妊娠率和活产率有略高于其他两组的趋势(表6)。
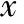
表5 不同T3三组间一般情况的比较[(-±s),%]
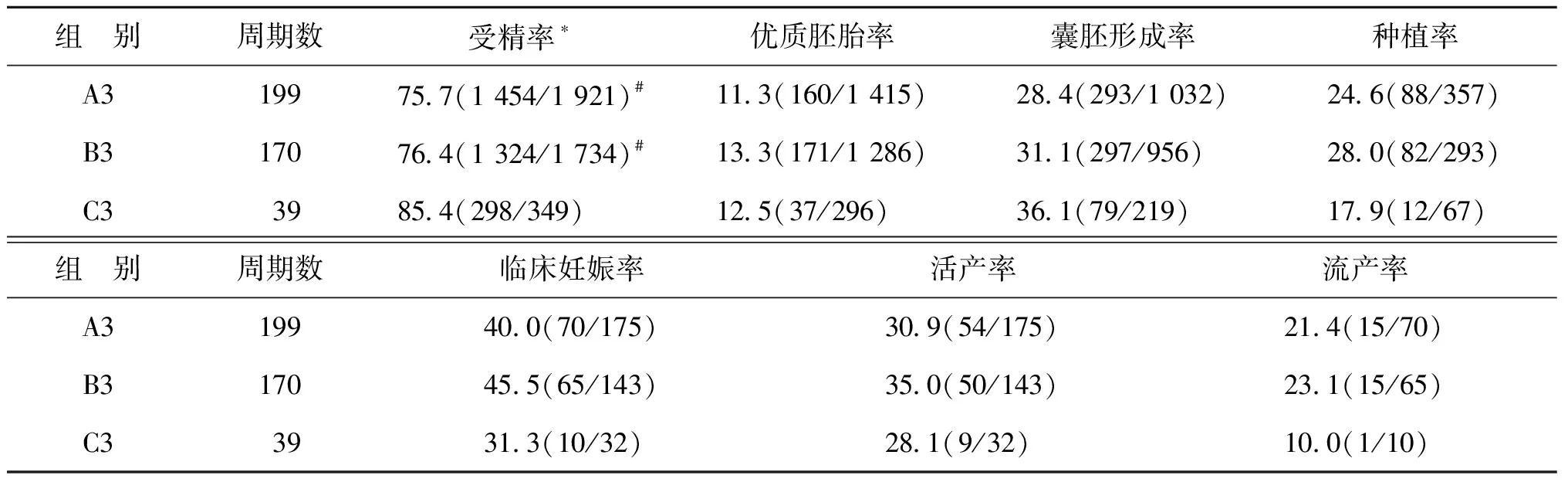
表6 不同T3三组间胚胎发育及妊娠结局比较(%)
讨 论
目前ICSI操作技术已经日趋成熟,但是脱颗粒时间和显微注射时间对ICSI结局的影响一直存在争议。早期的研究发现适当延长取卵后脱颗粒前的时间有利于卵母细胞胞浆和胞核的成熟,推荐获卵后2 h后再进行脱颗粒,从而使ICSI结局最优[2,3,8]。但也有一些研究认为脱颗粒时间对ICSI结局无影响[5-6]。目前,对于所有操作的精确时间尚无确切定论。本研究的目的是分析脱颗粒细胞时间(T1)和ICSI时间(T2)对胚胎发育和妊娠结局的影响。
在本研究中,我们发现在获卵后0.08~1.92 h内进行脱颗粒不会影响ICSI的结局。过早的拆卵(≤0.5 h)和延迟拆卵(≥1 h)对胚胎的发育潜能没有明显影响,3组的优胚率、囊胚形成率和种植率相似;对临床结局也没有明显影响,3组的临床妊娠率和活产率相似。这与之前的一些研究结论是相似的,认为在ICSI前延迟脱颗粒细胞不会提高ICSI结局[6,9]。在2016年Bárcena等[6]的研究中纳入近4 000个ICSI周期,他们发现获卵与脱颗粒之间的时间与ICSI结局无显著关系,他们认为高质量的卵母细胞体外承受能力更强,更耐受体外的各种操作,而不影响临床结局。最近Naji等[9]进行了一项研究,纳入2 051个非供卵的ICSI周期,根据取卵至脱颗粒的时间分为两组,发现脱颗粒时间在2 h以内或以上的两组的受精率、种植率、临床妊娠率和活产率比较无显著性差异;在第一组中他们又进一步分为脱颗粒时间在30 min以内和30~119 min的两组,同样发现两亚组的数据也无显著性差异。然而我们的研究结论也与之前的一些研究相反,即他们认为在脱颗粒之前,将卵母细胞培养2 h以上可以提高受精率和胚胎质量,改善妊娠结局[2]。Mizuno等[4]发现,取卵后立即脱颗粒细胞组与2 h脱颗粒细胞组的受精率、囊胚形成率、妊娠率及活产率比较无显著性差异,但是2 h脱颗粒细胞组的优质囊胚率显著高于立即脱颗粒细胞组(P<0.05),认为在ICSI之前保持完整的颗粒细胞有利于卵母细胞的成熟和后续胚胎发育。分析本研究与其他研究的差异,可能存在以下几点原因:首先,由于本实验室的工作安排,我们的脱颗粒时间为0.08~1.92 h,最高不超过2 h,因此未能评估脱颗粒时间超过2 h的情况;对于0.08~1.92 h内脱颗粒者,本研究提示取卵-脱颗粒时间短者的种植率、临床妊娠率和活产率略高于脱颗粒时间久者,尽管3组间比较无显著性差异(P>0.05)。最近关于鼠类的研究提示,有完整颗粒细胞的卵母细胞延长培养后会诱导卵母细胞出现凋亡改变,促进卵母细胞老化,从而影响胚胎质量和临床结局,建议在取卵后立即进行脱颗粒[10-11]。其次,很多研究是在HCG后(36.5±0.5)h进行取卵[2,6,12],而本研究是在HCG后38 h取卵,相当于上述研究的卵母细胞取出后在体外培养2 h后,似乎我们的取卵-脱颗粒时间较短,实际上距离HCG的时间并不短,卵母细胞的成熟度相对较好。因此,本研究认为取卵至脱颗粒的时间对胚胎发育和妊娠结局的影响并不显著。
脱颗粒后应该立即进行ICSI操作还是应该放置一段时间一直存在争议。有研究认为脱颗粒时间至ICSI时间的长短与ICSI结局无关[13]。Garor等[5]在脱颗粒后5 min~5.2 h进行ICSI操作,以≤1 h和>1 h分为两组,发现两组的受精率和妊娠率相似。认为ICSI之前延长卵母细胞的孵育时间并不能提高卵母细胞的发育程度,也不能改善妊娠结局。但也有研究发现脱颗粒后立即行ICSI能够获得较好的结局。Patrat等[2]研究发现脱颗粒至ICSI注射时间与受精率成负相关,随着脱颗粒至ICSI注射时间的延长,受精率逐渐下降,因此建议在脱颗粒后立即进行精子注射。最近Pujol等[12]进行了一项多因素的分析发现脱颗粒时间(0.5~2 h)对妊娠结局无影响,但是脱颗粒-ICSI时间每增加1 h,生化妊娠率和临床妊娠率分别降低7.5%和7.9%,而对继续妊娠率和活产率没有影响,也建议在脱颗粒后立即行ICSI操作。在本研究中,根据本实验室的工作安排,我们的T2时间为0.33~6.05 h,其中脱颗粒后短时间内(<1 h)行ICSI的仅10例,所以我们按照T2的平均时间(2 h)进行分组,我们发现C2组(>3 h)的受精率显著高于A2和B2组,C2组的囊胚形成率显著高于A2组(P<0.05);而B2组的种植率、妊娠率及活产率略高于其他两组,但3组间比较无显著性差异(P>0.05)。另外本研究还对取卵和ICSI之间的时间进行了分析,发现当T3超过3.5 h时(C3组)的受精率最好;尽管3组间尚无显著性差异(P>0.05),但B3组的妊娠率及活产率有略高于其他两组的趋势。这与上述以脱颗粒为节点进行的研究结论相一致,与Bárcena等[6]的研究结论也相似,他们认为不管是新鲜周期还是复苏卵母细胞周期,取卵至ICSI的时间对妊娠率和活产率均无显著影响。这可能是因为在脱颗粒操作中,由于透明质酸酶的化学损伤和吸管吹吸的机械损伤,导致卵母细胞膜受损或卵母细胞内部细胞器受到挤压,因此,脱颗粒后给予卵母细胞一段恢复时间后再进行ICSI比较合理。且ICSI前对卵母细胞进行适度时间的孵化可能促进细胞质的成熟,更有利于卵母细胞的全面激活和后续正常发育,可能增加受精率。然而脱颗粒后的孵化时间不宜过久,否则会造成卵母细胞老化,卵母细胞内的超微结构发生改变,基因表达改变,纺锤体异常的发生率增加[14-16],从而影响后续胚胎发育。本研究中>3 h的患者例数相对较少,可能会存在一定偏倚。
本研究对临床和实验室工作具有较重要的意义。对于极度繁忙的IVF中心,尤其是需要下午取卵的中心,如果能够缩短取卵至ICSI之间的时间而又不影响ICSI结局,可以避免实验室从业人员工作时间的显著延长,提高实验室工作效率,从而降低ICSI周期的总体成本[17]。本研究认为获卵后脱颗粒时间对ICSI结局的影响并不显著,脱颗粒后孵育2~3 h再进行ICSI的效果可能更好,但尚未表现出显著性差异,因此具体操作时间还有待于进一步研究。当然,本研究的样本量有限,后续还需要进行前瞻性的随机对照研究来进一步证实。
