Terlipressin促进肝癌合并肝硬化半肝切除术后肝再生的前瞻性非随机研究
2019-12-11许庆祎王垒张冰梁东曾永毅刘景丰
许庆祎,王垒,张冰,梁东,曾永毅,刘景丰
(福建医科大学孟超肝胆医院 肝胆外科,福建 福州 350025)
原发性肝癌为我国常见的恶性肿瘤,手术切除仍然是目前首选的治疗手段[1]。在我国80.12%的肝癌合并肝硬化[1],肝硬化是肝癌发生发展的重要环节,也是影响肝癌预后的重要因素[2-4]。肝硬化患者肝功能储备往往不足,术后肝肾功能不全、肝肾综合征、小肝综合征发生率很高[3,5]。另外,肝硬化也是影响肝切除术后肝再生的危险因素[6]。
Terlipressin(特利加压素)可选择性收缩内脏毛细血管,改善重要脏器灌注。系统综述和Meta分析证实Terlipressin可以改善肝切除术后肝肾功能的恢复,减少肝肾综合征的发生[7-9]。动物研究发现Terlipressin能有效缓解门静脉高灌注状态,降低门静脉压力,提高肝大部切除术后小体积肝存活率[10-11]。然而,Terlipressin能否改善半肝切除术后患者的肝肾功能、是否可预防肝肾综合征、能否促进肝再生,尚未见文献报道。因此,我们设计一项前瞻性非随机对照实验,观察半肝切除术后预防性使用Terlipressin的疗效。
1 资料和方法
1.1 一般资料
前瞻性分析福建医科大学孟超肝胆医院自2017年10月至2018年8月期间肝癌合并肝硬化并行半肝切除术的患者,收集患者的性别、年龄、肝肾功能以及术中情况等基线指标。研究方案经本院伦理委员会批准,并与患者家属签署知情同意书。
1.2 纳入和排除标准
患者入选标准:(1)合并乙肝肝硬化,巴塞罗那分期为A、B、C期;(2)肝功能为Clid-PughA级,或B级经术前治疗改善至A级;(3)术前临床诊断为原发性肝癌,术后病理证实为肝细胞肝癌、胆管细胞癌或混合性细胞癌;(4)半肝切除(残肝体积>40%);(5)术前吲哚菁绿滞留试验ICGR 15<15%;(6)乙肝病史;(7)术前肾功能正常。
排除标准:(1)有活动性肝炎表现;(2)肝癌合并大血管侵犯;(3)肝癌复发再次手术治疗者;(4)已知对Terlipressin过敏者;(5)活动性消化道出血、肝功能障碍、凝血功能严重减退并且无法纠正,或其他Terlipressin禁忌证者;(6)有肾脏基础疾病;(7)围手术期使用过肾脏、肝脏毒性药物。
1.3 分组和治疗方法
所有患者术前均行ICG试验评价肝储备功能,并行腹腔镜下或开腹左/右半肝切除术。试验组:对一般情况较差、肿瘤体积较大、肝储备功能不足的患者采用Terlipressin(德国辉凌制药有限公司产品),即术后第1天开始使用Terlipressin,2 mg/d,24 h持续泵入,术后连续使用5 d。对照组:不使用Terlipressin。两组患者术后均常规保肝及营养支持治疗。出现下列情况,研究将中止:剂量调整后仍出现不能耐受的不良反应,患者需要接受研究方案以外的降压素,或者患者主动要求退出研究。不能耐受的不良反应定义如下:≥3级的非血液毒性;中性粒细胞减少或发热4级;血小板减少4级;血小板减少3级合并出血;≥3级的心脏毒性;≥3级的肝脏和肾脏毒性。包含但不仅限于以上患者出现不良反应,且可能危机患者生命及诊疗过程之情形;以上所有不良反应的级别将参照NCI-CTCAE(V4.0.3)。
1.4 指标评估
1.4.1 主要结局指标:采用IQQA-Liver系统对所有患者术前、术后5 d及术后2个月的CT图像进行三维可视化重建,计算术后5 d肝再生率(liver regeneration rate,LRR5d)、术后2个月后LRR(LRR2mon)、肝继续再生率(ΔLLR=LRR2mon-LLR5d)。
肝脏三维重建:Dicom格式256层螺旋CT(荷兰飞利浦公司产品),层厚2 mm,包括平扫期,动脉期、门脉期、静脉期及延时期的影像资料,检查断层图像数据导入IQQA-Liver系统(美国EDDA公司产品)进行肝脏、肝脏脉管系统、肿瘤的三维重建。应用交互式虚拟切除技术,划定预切除肝脏脉管、肝组织范围,所有病例均模拟解剖性肝切除(均为半肝切除),计算肿瘤体积、全肝体积,剩余肝体积(remanent liver volume,RLV)。全程由1名副主任医师以上肝胆外科以实际影像医师指导完成[12]。
肝再生率:以术前全肝体积(TLV)-术中预切除肝脏体积(V)作为术后初始肝体积(initial liver volume,ILV),通过下述公式计算得出术后早期的LRR:LRR(%)=(RLV-ILV)/ILV×100。
1.4.2 次要结局指标:两组患者的腹腔日腹腔积液引流量、日平均尿量,术后肝肾功能、尿量变化,监测有无心血管意外、电解质紊乱事件发生率,记录各种术后并发症发生率。心血管事件包括术后新近出现的严重血压、心电图异常。术后并发症依据Clavien Grade分级法进行分级。
1.5 随访
采用门诊、电话及邮件方式随访,随访内容为检查患者肝肾功能、凝血功能、肿瘤指标(AFP);B超及CT检查患者肝脏再生情况。
1.6 统计学分析
采用SPSS 22.0统计软件进行分析,计数资料采用χ2检验或Fisher确切概率法,计量资料采用(±s)表示,组间比较采用两样本t检验。P<0.05为差异有统计学意义。
2 结果
2.1 入组流程及基线特征
根据入排标准,共有68例患者进入统计学分析,其中试验组37例,对照组31例(详见图1)。两组之间基线特征基本一致(详见表1)。
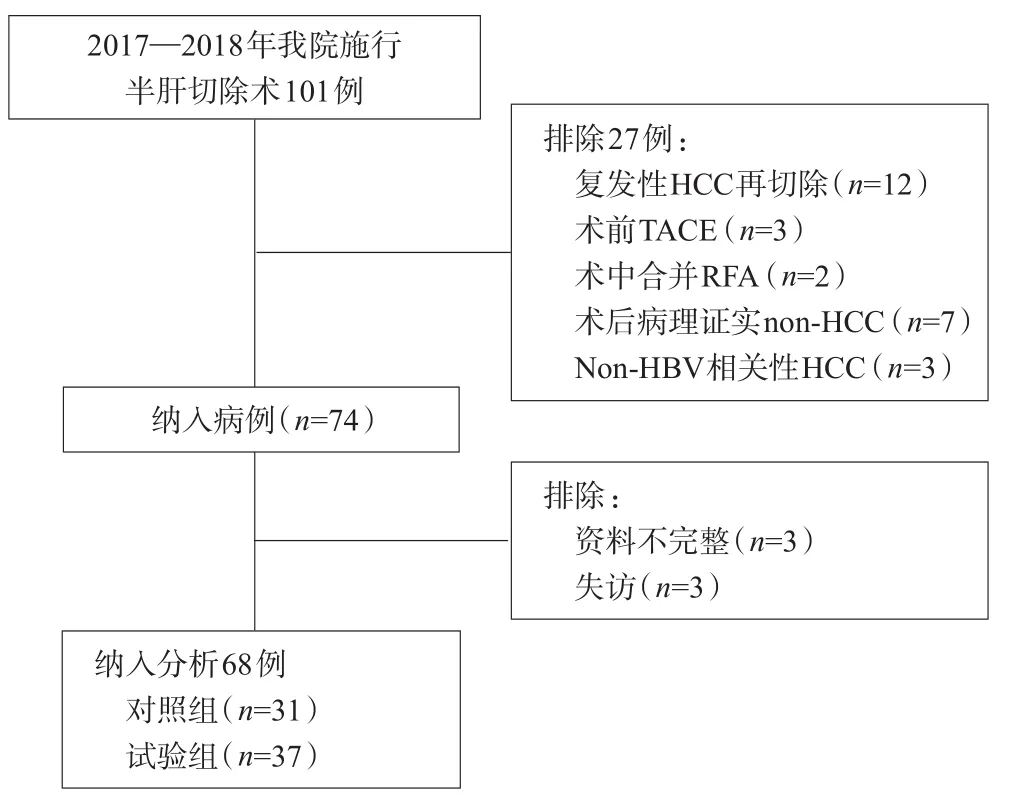
图1 患者入组流程图
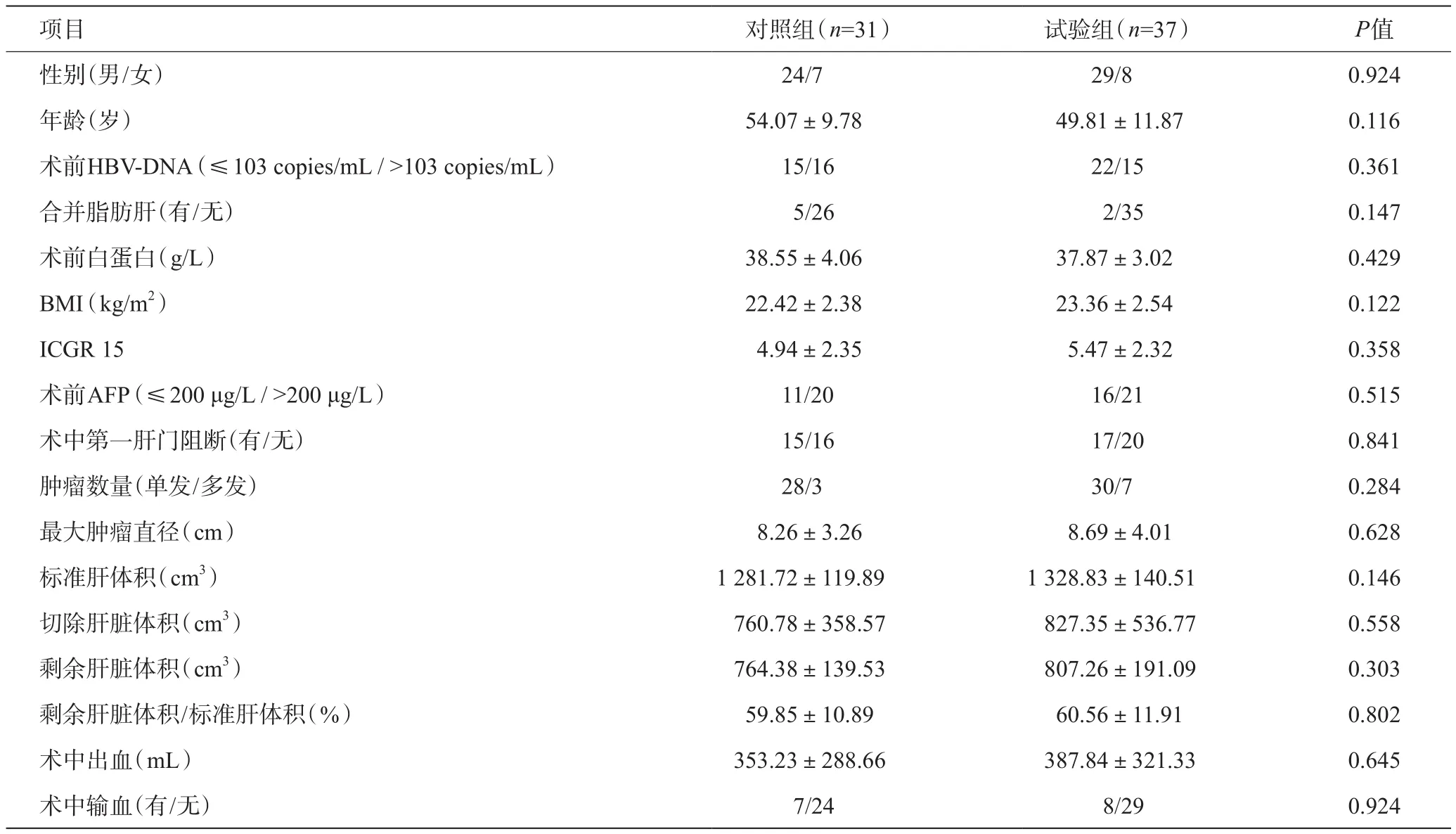
表1 两组基线特征对比
2.2 肝脏三维重建
68例患者均行术前、术后第5天、术后2个月肝脏CT扫描,并进行肝脏三维重建。三维重建结果可清楚显示肿瘤大小、全肝大小,并能精确计算肿瘤体积、全肝体积,剩余肝体积(见图2)。

图2 肝脏三维重建
2.3 肝再生率
两组术后LRR5d差异没有统计学意义(P>0.05)。两组术后LRR2mon差异有统计学意义(P=0.023)。两组术后ΔLLR差异有统计学意义(P=0.002),详见表2。
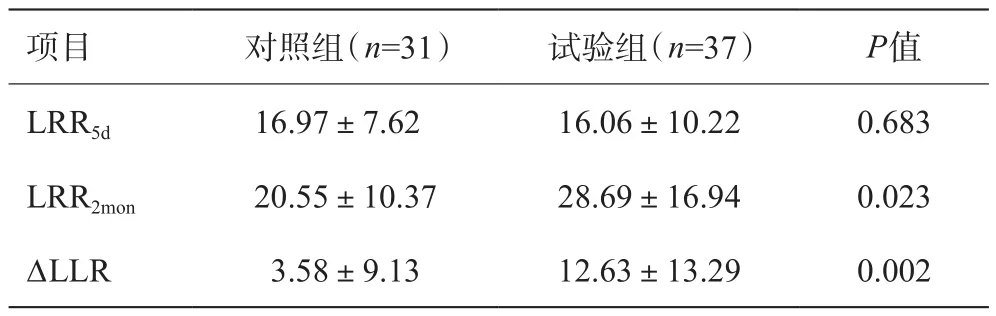
表2 两组术后肝再生率的比较(%)
2.4 肝肾功能恢复情况
两组术后第1、3、5天ALT、AST、BUN详见表3。

表3 两组术后肝肾功能比较
2.5 术后并发症
试验组术后腹腔感染率高于对照组(P=0.038),但是两组之间其他并发症发生率无统计学差异(P>0.05),详见表4。
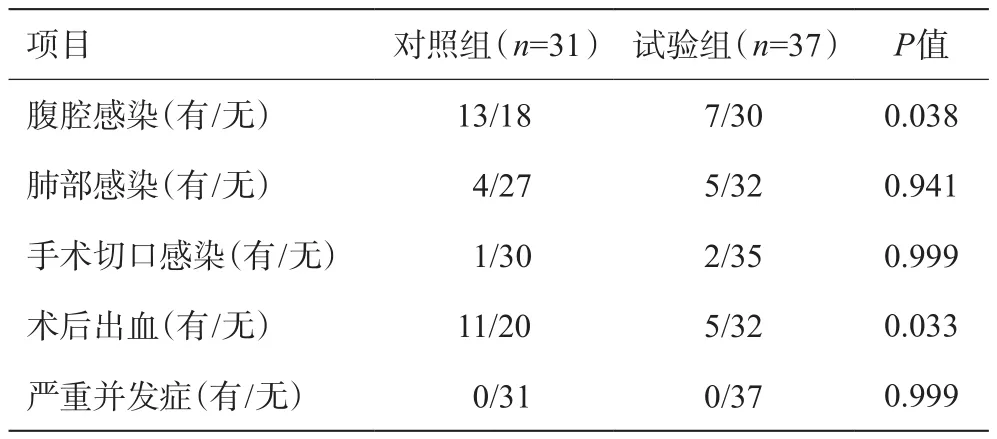
表4 两组术后并发症对比(例)
2.6 术后恢复情况
试验组术后恢复明显快于对照组(P<0.05),详见表5。
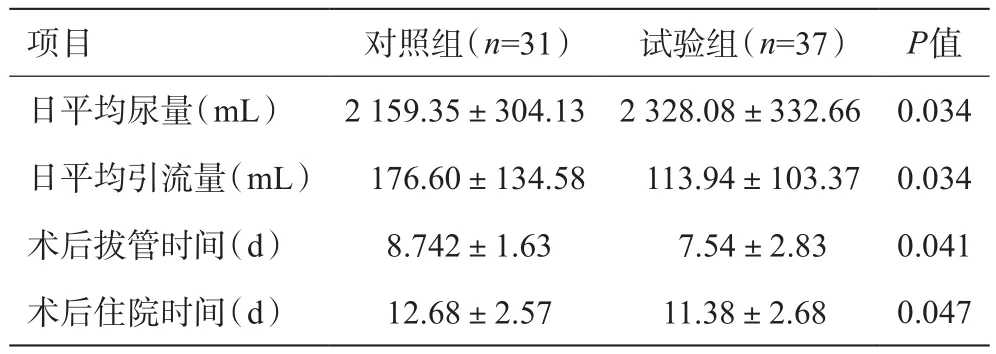
表5 两组术后恢复情况对比
2.7 术后电解质紊乱、心血管事件
两组之间术后电解质紊乱、心血管事件发生率无统计学差异(P>0.05),详见表6。

表6 两组术后电解质紊乱、心血管事件对比(例)
3 讨论
肝硬化是肝癌肝切除术后并发症的危险因素[3],也是影响肝再生的重要因素[6]。本研究前瞻性地将Terlipressin运用于肝癌合并肝硬化的半肝切除患者,结果发现Terlipressin能促进半肝切除术后残余肝的再生。
肝硬化是肝癌患者围手术期出现肝肾功能不全、肝肾综合征、小肝综合征甚至死亡的独立危险因素[3],原因可能是:(1)肝癌合并肝硬化肝功能储备不足,肝脏的合成、分泌及排泄功能减退;(2)肝癌合并肝硬化肝组织坏死范围大,肝切除范围增大,手术创伤增大,从而增加了术后肝衰竭的风险。肝大部分切除术包括半肝切除术,也会增加术后肝功能不全甚至肝衰竭的风险,原因可能是肝大部切除术后门静脉高压引起肝脏微循环紊乱、组织缺氧、肝细胞空泡样变性[13]。孙平等[14]研究发现对于肝储备功能差或肝切除范围大的肝癌患者,预防性应用Terlipressin能有效促进患者术后肝肾功能的恢复,减少肝肾综合征的发生。李民等[15]研究发现Terlipressin能减少肝癌合并肝硬化患者肝切除术后腹水的形成,缩短患者的引流管拔管时间与住院时间,促进患者的术后康复。对于肝癌合并肝硬化的半肝切除患者,本研究发现Terlipressin不仅能减少术后腹水的生成、腹腔感染的发生,还能促进患者术后肝功能的恢复、减少肝肾综合征的发生、缩短患者的引流管拔管时间与住院时间。
肝再生是肝大部切除术的基础[16],但是肝癌合并肝硬化肝再生能力大大受损。吴心强等[6]认为肝硬化肝再生过程缓慢,所需时间更长,并且再生肝细胞多不能发育成熟,再生肝脏仍为硬化肝脏。但是,研究发现部分肝切除可以促进肝癌合并肝硬化的肝再生,并且能减少残余肝的纤维化增生、改善再生肝的纤维化结构[17-18]。门静脉为肝切除术后肝再生提供必要的营养支持,但是大部肝切除或半肝切除术后门静脉高压并不利于残余肝的再生。Terlipressin具有调节门静脉压力的作用,研究发现Terlipressin可有效降低小鼠肝大部分切除术后门静脉高灌注、促进肝细胞再生[10-11,19],其机制可能与多种细胞因子、生长因子、炎症因子等相互作用有关。本研究发现,肝癌合并肝硬化的半肝切除患者术后应用Terlipressin可以提高术后2个月的肝再生率及肝持续再生率。因此,我们认为Terlipressin能维持肝癌合并肝硬化半肝切除术后残余肝的持续增长,机制可能与肝功能的改善、门静脉压的调节有关。
然而,本研究仍存在许多不足之处:(1)本研究作为一项前瞻性的探索性试验,病例数较少可能会削弱结论的可信度;(2)本研究作为一项探索性试验,未能实现随机和盲法,并且试验组多为肝功能较差的患者,具有明显的选择偏倚;(3)目前肝再生缺乏相应的“金标准”,本研究只对再生肝的“量”进行评价,而对再生肝的“质”缺少评判;(4)影响肝再生的因素除了肝硬化还包括年龄[20]、肥胖[21]、脂肪肝[22]、残余肝体积及左右半肝等,本研究对这些因素未进行严格控制;(5)本研究对肝再生的机制缺乏深入的研究,如细胞因子TNF-α、IL6等的监测[23]。
