颅内静脉窦狭窄患者眼部表现及支架术后眼底改变的相关研究
2019-12-10王淑然瞿远珍杨柳方民佟旭王素洁莫大鹏
王淑然,瞿远珍,杨柳,方民,佟旭,王素洁,莫大鹏
颅内静脉窦狭窄(cerebral venous sinus stenosis,CVSS)是脑静脉窦部分或完全狭窄,以青壮年多见,患者脑静脉系统出现血流动力学改变,若发生于优势侧静脉窦,可出现短暂性头痛,严重时可导致进行性颅内压升高,表现为头痛、视盘水肿、视物模糊及搏动性耳鸣等[1]。视盘水肿严重者可继发视神经萎缩,从而导致不可逆性视力下降,甚至失明。CVSS发病率较低,在临床中常因医师经验欠缺而被忽视,延误诊治。本文对CVSS患者的眼部表现进行回顾性总结,并分析经静脉窦支架置入术治疗后患者眼底改变情况,以期加深神经内科医师和眼科医师对CVSS患者眼部临床特征的认识,有助于该疾病的诊断,减少误诊和漏诊,并了解眼部检查在CVSS诊断和治疗随访评估中的重要意义。
1 研究对象与方法
1.1 研究对象 回顾性分析2014年1月-2018年8月在首都医科大学附属北京天坛医院神经介入中心诊治的CVSS患者资料。纳入标准:①行全脑DSA检查,证实存在静脉窦狭窄;②不存在高度近视或高度远视;③不合并其他原因引起的视神经病变或视网膜病变;④临床资料完整。排除心肝肾功能严重不全及颅内其他病变患者。
1.2 影像学检查和静脉窦压测定 患者入院后均行动脉造影、静脉造影及静脉窦内测压:经股动脉穿刺置入动脉鞘后行DSA检查,观察皮质静脉形态和引流,静脉窦狭窄程度、充盈情况;同期行股静脉穿刺,置入血管鞘后经上腔静脉进入颈内静脉行静脉窦内逆行造影,明确静脉窦形态;随后置入微导管,连接测压装置,并分别在静脉窦狭窄段远端及近端行窦内测压,计算跨狭窄压力差。
1.3 颅内压测量和眼部检查 患者入院后均行腰椎穿刺,测量颅内压。患者于治疗前1周内及随访时分别行视力及眼底检查,部分患者行动态视野检查和光学相干断层成像(optical coherence tomography,OCT)检查。采用Frisén分级体系(0~5级),根据视神经轴突肿胀和混浊程度对视盘水肿进行分级:①0级即正常视盘:无水肿;②1级即微小水肿:视盘周围可见细微浅灰色“C”形影,遮挡其下视网膜组织,颞侧边界正常;③2级即轻度水肿:视盘周围可见透明度降低的环形影,鼻侧边界隆起,视盘上方走行的视网膜血管均清晰可辨;④3级即中度水肿:视盘边缘全部隆起,边缘至少一段主要血管走行模糊不连续;⑤4级即显著水肿:视盘包括视杯全部隆起,视盘表面主要血管至少一条但非全部走行不连续;⑥5级即重度水肿:视盘表面血管全部走行不连续,至少一条血管完全模糊不可见[2]。
1.4 治疗及随访 所有患者给予降颅压、抗凝、溶栓等内科治疗,部分经内科治疗效果不佳的患者为防止病情进一步恶化行静脉窦支架置入术治疗。静脉窦内压力≥8 mm Hg作为支架置入术的指征,选择静脉窦引流优势侧置入支架。行支架置入术的患者在术后1、3和6个月通过门诊复诊进行视力和眼底检查。
1.5 统计学方法 应用SPSS 20.0软件进行分析,计量资料符合正态分布的用表示,不符合正态分布的用中位数(四分位数间距)表示;计数资料用率表示。采用Kendall’s tau-b相关分析患者的视盘水肿等级与病程、颅内压、静脉窦狭窄部位及分布、狭窄率、跨狭窄压力差的相关性,P<0.05为结果具有统计学意义。
2 结果
2.1 一般资料 共纳入125例患者,250只眼,男性29例,女性96例。平均年龄36.3±10.0岁。病程中位时间4.0(0.2~96.0)个月。其中79例患者经内科治疗效果不佳进行了静脉窦支架置入术。
2.2 治疗前眼部表现 125例CVSS患者中临床症状存在视功能损害者101例(80.8%),包括持续或间断性视物模糊或视力下降、视物变形、复视、阵发性黑蒙、视野缺损等,其中65例(52.0%)眼部症状为首发症状,35例(28.0%)仅表现出眼部症状,神经系统症状缺如。眼底检查无视盘水肿者10例(8.0%),单眼视盘水肿7例(5.6%),余108例(86.4%)均表现为双眼视盘水肿。
视盘水肿分级为3(2~4)级,右眼与左眼视盘水肿程度无统计学差异。视盘周围放射状线状或片状出血37只眼(14.8%),渗出、棉绒斑24只眼(9.6%);视网膜皱褶24只眼(9.6%),视盘水肿≥3级者可见不同程度视网膜静脉迂曲扩张;黄斑区渗出、水肿3只眼(1.2%);存在视盘色淡或苍白21只眼(8.4%)(图1)。OCT检查发现视盘水肿严重者可出现视盘周围及黄斑区视网膜神经上皮下积液。视野缺损类型变异较大,主要包括生理盲点扩大、上方或下方部分视野缺损,向心性视野缩小等。
2.3 治疗前颅内压及静脉窦狭窄情况 颅内压>330 mm H2O者55例(44.0%),余70例(56.0%)颅内压为210~330 mm H2O,平均285.8±34.5 mm H2O。
静脉窦狭窄情况:累及横窦44例(35.2%),乙状窦2例(1.6%),横窦-乙状窦交汇处79例(63.2%);单侧静脉窦狭窄,对侧正常67例(53.6%),双侧静脉窦狭窄32例(25.6%),单侧静脉窦狭窄,对侧闭塞或发育不良26例(20.8%);狭窄程度中位值为80%(70%~85%);跨狭窄压力差中位值13.5(10.0~19.5)mm Hg。
2.4 治疗前视盘水肿等级相关性分析结果 治疗前视盘水肿等级与颅内压正相关,Kendall’s tau-b相关系数为0.271,P=0.029;视盘水肿等级与病程负相关,Kendall’s tau-b相关系数为-0.261,P=0.002;视盘水肿等级与静脉窦狭窄部位及分布、狭窄率、跨狭窄压力差无相关性。
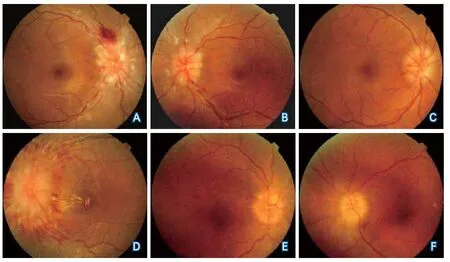
图1 治疗前静脉窦狭窄患者眼底表现
2.5 静脉窦支架置入术后视盘水肿变化情况共79例患者接受了静脉窦支架置入术,术前存在视盘水肿143只眼(90.5%),视盘水肿分级中位值3(2~4)级。治疗后1个月、3个月、6个月视盘水肿分级较支架置入前减轻程度详见表1。术后6个月复查时仅8只眼(5.1%)仍存在视盘水肿,18只眼(11.4%)表现为视神经萎缩(图2)。
3 讨论
CVSS可由先天性静脉窦发育异常、局部压迫(颅内肿物等)、腔内阻塞(大蛛网膜颗粒、静脉窦血栓纤维化等)、外伤等导致,但多数患者静脉窦狭窄病因不明,狭窄部位通常位于横窦和乙状窦结合处,其次为横窦[1,3-4]。常规MRI不能满足CVSS的诊断,很多CVSS在MRI上没有表现,因此当怀疑该病时应行MRV显示颅内静脉形态,也可以通过DSA检查明确诊断[1]。目前越来越多研究显示,CVSS与特发性颅内高压(idiopathic intracranial hypertension,IIH)有关,30%~90%的IIH患者存在不同程度的静脉窦狭窄[5-8]。
本研究显示CVSS患者视功能损害的眼部特征,包括持续或间断性视物模糊或视力下降、阵发性黑蒙、视物变形、复视、视野缺损等,眼底检查可见视盘水肿,视盘周围出血、渗出、棉绒斑,视盘周围同心圆样视网膜皱褶、视网膜静脉迂曲扩张,黄斑区渗出、水肿,视盘色淡或苍白等。视物模糊、视物变形、复视可继发于视盘水肿导致的患者屈光状态改变或黄斑区水肿、积液等病变;阵发性视物模糊或黑蒙可能是由于颅内压短时间内显著升高、视神经供血不足导致;持续性视力下降和视野缺损多由于视神经凋亡萎缩导致。视野缺损类型多样,主要包括生理盲点扩大、旁中心暗点、上方或下方弓形视野缺损、向心性视野缩小、残留鼻侧视岛等。视网膜静脉迂曲扩张见于中重度视盘水肿患者(≥3级),轻度视盘水肿患者未见,提示静脉迂曲可能继发于视盘水肿,视盘水肿至一定程度才能挤压视网膜中央静脉,引起视网膜静脉迂曲扩张;另外视网膜静脉血液通过眼上静脉进入颅内海绵窦,当颅内压及静脉窦内压力增高时可能影响视网膜静脉血液回流[9]。
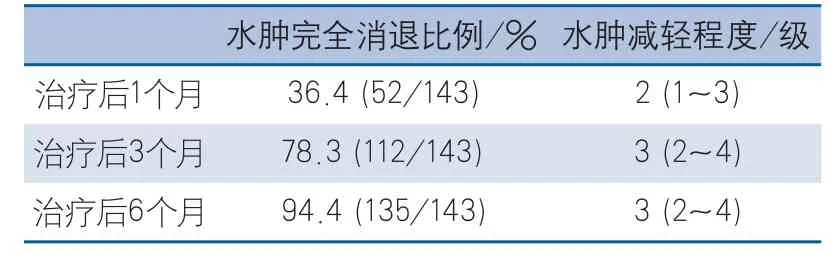
表1 静脉窦支架置入术后随访视盘水肿完全消退比例及视盘水肿减轻程度
视盘水肿是CVSS患者最常见的临床表现,高于神经系统症状发生率[4]。视盘水肿的发生与增高的颅内压相关。在视盘筛板两侧,眼内压和视神经鞘内脑脊液压力形成压力梯度,正常的压力梯度是视神经纤维轴浆流动的前提,当视神经鞘内脑脊液压力异常增高时,视网膜表层神经纤维层和视盘筛板前区域的神经纤维轴浆流动停滞,导致神经纤维肿胀,继而出现视盘水肿[10]。神经纤维和视盘肿胀进一步压迫该区域走行的小静脉,导致小静脉扩张和血管内液体渗漏至周围组织,甚至小血管破裂[10],表现为视盘周围视网膜组织水肿、皱褶,视网膜出血、渗出,视网膜下积液等。
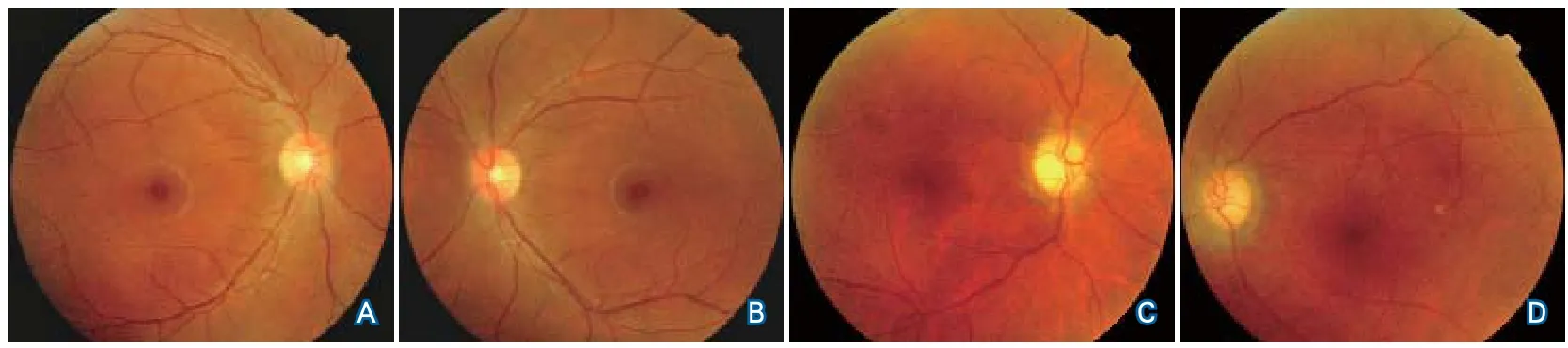
图2 静脉窦狭窄患者支架置入术后眼底改变
CVSS可以导致慢性颅内压升高,引起双眼进行性视盘水肿和视功能损害。本研究显示患者视盘水肿程度与颅内压呈正相关。急性颅内压升高可表现出显著的神经系统症状,如头痛、恶心呕吐等,这些患者多就诊于神经科,而慢性颅内压升高患者在表现出神经系统症状之前可仅存在眼部症状和体征[4]。如本研究中,65例(52%)患者眼部症状为首发症状,35例(28%)患者仅表现出眼部症状,神经系统症状缺如。当患者首诊于眼科时,医师可根据其眼部特征性表现,有针对性进行CVSS相关神经系统检查(颅内压测定、MRV、DSA等),从而及时正确诊疗。与视神经炎、缺血性视神经病变等病变不同,CVSS患者的视盘水肿通常累及双眼,发展为视神经萎缩之前,视觉诱发电位检查多正常或轻微异常,激素治疗无效。这类患者的视野缺损多表现为生理盲点扩大和下方弓形视野缺损,严重视神经损害者可表现为视野缩窄。CVSS导致的双眼视盘水肿还应与静脉窦血栓和颅内占位性病变进行鉴别[11]。
迄今多数CVSS患者静脉窦狭窄原因不明,近年来一些回顾性研究显示静脉窦支架置入术可有效减轻CVSS的颅内压增高症状和视盘水肿,且安全性较高[7-9,12-13]。静脉窦是颅内血液、脑脊液主要的引流途径,研究报道当狭窄两端压力差超过8~10 mm Hg时,可造成血流动力学明显变化,狭窄两端压力差较大提示颅内代偿引流尚未建立,行静脉窦支架置入术后,可明显改善脑静脉血及脑脊液回流,有效缓解高颅压症状[12,14]。但既往研究关于视盘水肿程度的分级不够细致,术后随诊时间较短。本研究显示,传统治疗效果不佳的患者经静脉窦支架置入术后,所有患者视盘水肿均明显缓解,且多数患者在术后1个月之内视盘水肿即有明显消退,视功能症状明显改善,术后3个月时大部分患者视盘水肿恢复正常,术后6个月时视盘水肿基本完全消退。提示对于CVSS合并视盘水肿经内科治疗无效的患者,静脉窦支架置入术是有效的,可促进视盘水肿的消退,在视神经萎缩出现之前进行手术可以防止视盘长期水肿而导致的不可逆性视神经损伤和视功能损害。
本研究中部分CVSS患者支架术后视盘水肿消退后出现视盘色淡、苍白,视功能也较差,这些向视神经萎缩方向发展的患者,多数病程较长,术前已存在视盘色淡,但由于病例数较少,无法进行统计学分析。视神经萎缩是由于神经纤维肿胀凋亡及肿胀的视盘压迫血管,导致视盘供血不足,与视盘水肿程度及水肿持续时间有关,一般情况下较轻的视盘水肿不会合并视神经萎缩[10]。还有些患者视盘水肿消退后周围出现环形视网膜脉络膜萎缩,可能由于视盘水肿较重时,盘周视网膜脉络膜组织小血管闭塞缺血,继而出现组织萎缩。本研究发现患者治疗前视盘水肿等级与病程长短呈负相关,提示随病程延长,视盘水肿可出现自行消退趋势。分析可能由于视盘持续水肿过程中,逐渐出现视神经纤维凋亡,由于视盘水肿取决于神经纤维的肿胀,一旦神经纤维数量减少,视盘水肿自然减轻,提示当视盘水肿自行缓解时视神经凋亡已开始出现,也说明病程越长,视神经损伤越重,视功能恢复的可能性越小,因为视神经凋亡是不可逆性损伤。因此在明确诊断之后,如果患者存在视盘水肿,应积极治疗,降低颅内压,内科治疗无效者需考虑尽早行静脉窦支架置入术治疗。
眼底检查是一种无创、快捷、经济的检查手段,在CVSS疾病的诊断、治疗及随访评估中都具有重要的价值。在诊断过程中,可用于评估患者颅内压情况及颅内代偿引流系统是否建立,以及治疗后评估患者静脉窦狭窄及颅内压改善情况。另外眼底检查也是评估手术必要性的一项重要观察项目,视盘水肿可作为随访静脉窦支架术后CVSS有无复发的一项重要指标。
本研究存在一些局限性,首先,这是一项单中心回顾性分析;其次,仅部分患者进行了视野和OCT检查,不能够全面反映疾病的诊疗评估及预后评价。眼科OCT检查中的盘周神经纤维层厚度检查可以客观定量检测视盘水肿程度,黄斑区节细胞复合体厚度检查可以定量检测神经节细胞的凋亡程度[15-16]。今后的研究可以常规引入OCT检查来评估患者治疗前视盘水肿程度、早期发现有无神经节细胞凋亡,预测治疗后患者视功能恢复情况及视神经萎缩的可能性。另外,可以将普通眼底照相改为立体眼底照相,以保证视盘水肿分级更加精确。这些检查项目的完善有利于对病变程度进行更加准确地判断和评估,相信在未来的研究中会收获更精准的结果和更多启示。
【点睛】脑静脉窦狭窄患者视盘水肿程度和颅内压正相关,与病程负相关。合并视盘水肿经内科治疗无效患者可考虑行静脉窦支架置入术,促进视盘水肿消退,减少视神经不可逆损害。
