超高效液相色谱法比较鲜川芎和川芎药材中6种成分含量
2019-12-05尹丹丹王运来尹登科
陈 冉,尹丹丹,杨 沫,王运来,尹登科,许 钒
(1.安徽中医药大学药学院,安徽 合肥 230012;2.中药复方安徽省重点实验室,安徽 合肥 230012)
川芎为伞形科植物川芎LigusticumchuanxiongHort.的干燥根状茎,挥发油类是构成川芎气味雄烈的主要物质。药理研究表明,川芎的药效物质基础为内酯类成分如藁本内酯、洋川芎内酯H、洋川芎内酯I、洋川芎内酯A[1-3],芳香酸类如阿魏酸[4-5]及生物碱如川芎嗪[6-7]。川芎嗪、阿魏酸及洋川芎内酯类化合物在抗氧化损伤、抗炎镇痛、抗凝及抗血小板聚集、神经保护等方面具有显著作用[8-12]。
川芎所含成分不稳定,易受到温度及光照影响发生成分损失;室温贮藏及自然光照条件下即可发生多种途径的降解行为[13-16]。因此,不同的温度及光照条件直接影响川芎中各成分的转化及含量。
鲜川芎在产地经火炕烘干后撞去泥沙和须根即为川芎药材,烘干温度小于70 ℃。笔者推测,受烘干过程中温度的影响,川芎药材与鲜川芎的化学成分间存在差异。但目前较多的研究关注川芎药材贮藏期间的成分变化,本课题旨在对鲜川芎与川芎药材中的6种活性成分(川芎嗪、阿魏酸、洋川芎内酯I、洋川芎内酯H、洋川芎内酯A)进行测定,初步比较二者化学成分差异,为川芎的产地加工提供实验依据。
1 仪器与材料
1.1 仪器 Waters Acquity UPLC-PAD色谱系统(包括二元泵、自动进样器、柱温箱、PAD检测器、Empower 2工作站):美国Agilent公司;ML303E千分之一电子天平:梅特勒-托利多上海有限公司;KQ-600DB型数控超声波清洗器:昆山市超声仪器有限公司;DFY-300多功能高速中药粉碎机:温州鼎历医疗器械有限公司。
1.2 试剂 乙腈(色谱纯)、甲醇(色谱纯):美国Fisher公司;0.22 μm有机相针式滤器:江苏津腾公司;超纯水:自制;盐酸川芎嗪(批号110817-201608,纯度≥98%)、阿魏酸(批号110773-201614,纯度≥98%)、藁本内酯(批号111737-201608,纯度≥98%):均购买于中国食品药品检定研究院;洋川芎内酯H(批号 P12J8F39794,纯度≥98%)、洋川芎内酯I(批号 P12J8F39795,纯度≥98%)、洋川芎内酯A(批号 P12J8F39796,纯度≥98%):购于上海源叶生物科技有限公司。
1.3 药材 新鲜的川芎根状茎于2017年5月收获期采集自四川彭州市敖平镇凤鹤村,川芎药材(批号:161219,产地四川)购买自安徽普仁中药饮片有限公司,经安徽中医药大学金传山教授鉴定为伞形科川芎LigusticumchuanxiongHort.的新鲜及干燥根状茎,见图1。
图1鲜川芎与川芎药材切片(A.鲜川芎;B.川芎药材)
2 方法
2.1 样品制备
2.1.1 供试品溶液制备 川芎自产地采收后,洗净泥沙,晾干水分后,作为鲜川芎。将同一批次鲜川芎于60 ℃烘箱中烘烤6 h作为川芎药材。新鲜川芎含水量较高,为降低水分对成分测定的影响,在采用超高效液相串联光电二极管阵列检测器进行含量测定前,根据2015年版《中华人民共和国药典》一部规定[17],采用甲苯法测定鲜川芎及川芎药材含水量分别为62.73%、8.73%,鲜川芎与川芎药材的质量比为7.18。将一定质量的鲜川芎和川芎药材粉碎至过三号筛,分别取5 g,采用50 mL的75%甲醇以超声功率80 W超声提取(室温25 ℃)30 min,室温放置6 h后分别取上清,过0.22 μm有机滤膜,得滤液备用。
2.1.2 对照品溶液制备 取各标准品一定量,配制盐酸川芎嗪、阿魏酸、洋川芎内酯I、洋川芎内酯H、洋川芎内酯A、藁本内酯浓度分别为65、50、30、12、400、682 μg/mL的混合标准溶液母液。
2.2 色谱条件 色谱柱为Waters Acquity UPLC BEH C18色谱柱(2.1 mm×100 mm, 1.7 μm),配备有Acquity UPLC柱在线过滤系统。采用梯度洗脱,流动相为乙腈(A)-0.1%甲酸水溶液(B)。梯度洗脱过程:0~0.5 min,5% A;0.5~8 min,5%~45% A;8~10 min,45% A;10~11 min,45%~48% A;11~16 min,48%~50% A;16~18.5 min,50%~60% A;18.5~20 min,60%~75% A;20~22 min,75%~90% A;22~23 min,90%~5% A;23~25 min,5% A。检测波长295 nm,流速0.2 mL/min,进样体积2 μL。
2.3 专属性考察 取标准品溶液、川芎药材及鲜川芎样品溶液,进样容积2 μL,按照“2.2”项下色谱条件进样分析,所得色谱图见图2、图3。
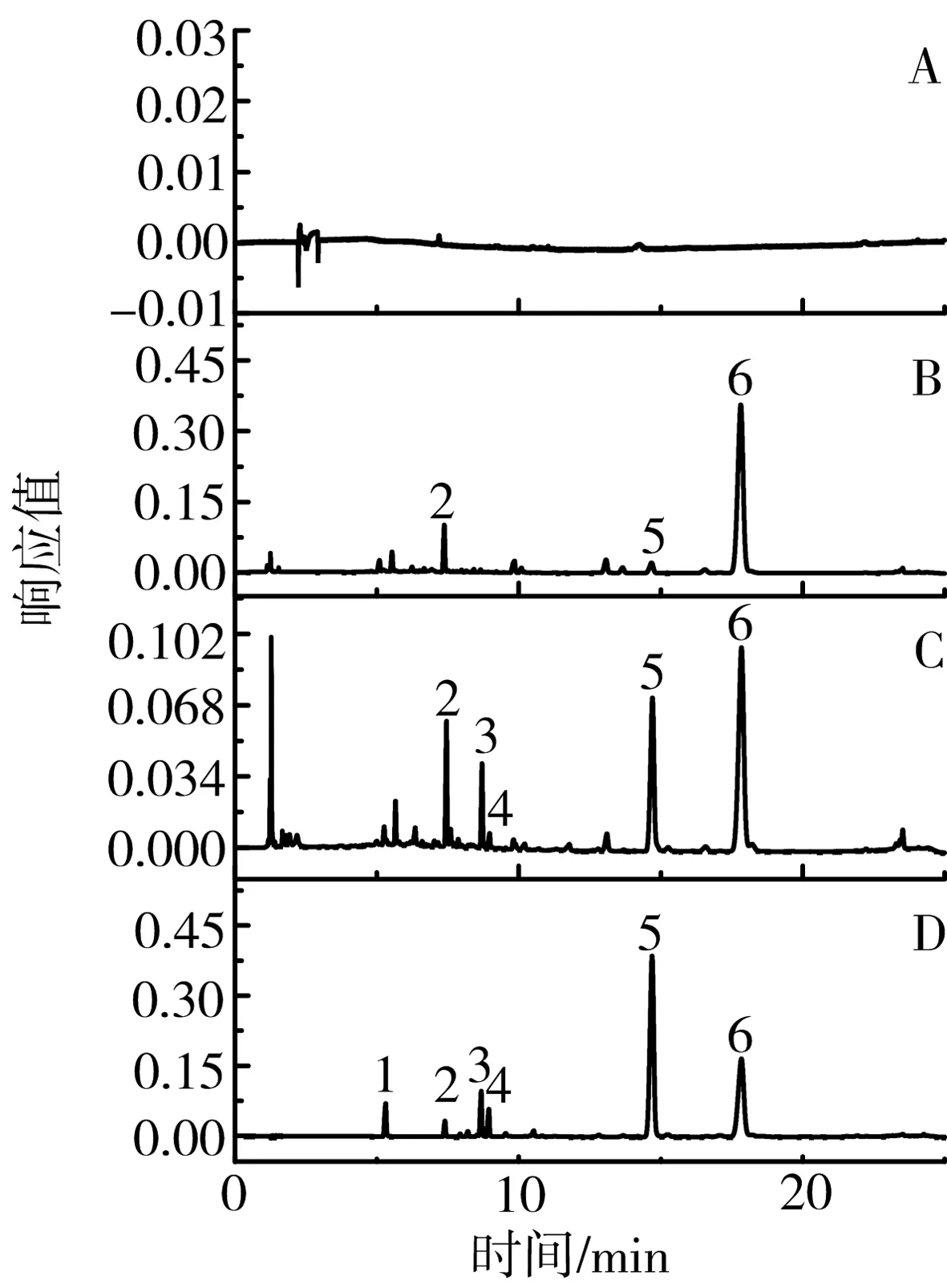
注:A.空白对照品;B.鲜川芎;C.川芎药材;D.混合标准品;1.盐酸川芎嗪;2.阿魏酸;3.洋川芎内酯I;4.洋川芎内酯H;5.洋川芎内酯A;6.藁本内酯
图2鲜川芎与川芎药材的UPLC图
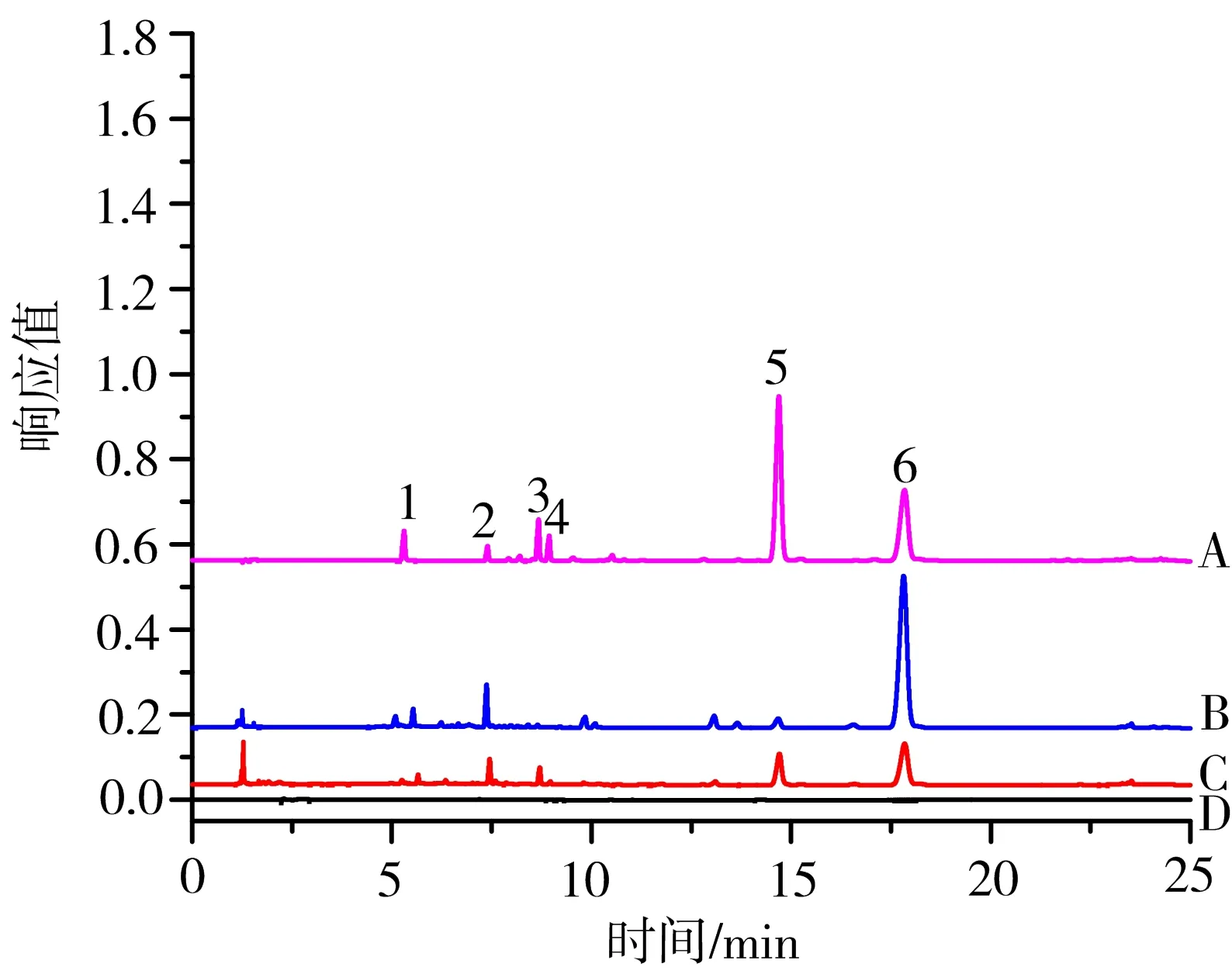
注:A.混合标准品;B鲜川芎;C.川芎药材;D.空白对照品;1.盐酸川芎嗪;2.阿魏酸;3.洋川芎内酯I;4.洋川芎内酯H;5.洋川芎内酯A;6.藁本内酯
图3鲜川芎与川芎药材的UPLC色谱图
2.4 线性范围考察 精密移取混合标准溶液母液0.125、0.25、0.50、1.00、2.50、5.00 mL,置10 mL量瓶中,加甲醇稀释,定容至刻度,摇匀,配成混合对照品溶液。按“2.2”项下色谱条件进样分析,以质量浓度(ρ)为横坐标、峰面积(A)为纵坐标,绘制标准曲线。见表1。

表1 6种成分的回归方程及线性范围
2.5 精密度试验 按照“2.2”项下色谱条件,将同一混合标准品溶液重复进样6次,记录色谱图,计算得到川芎嗪、阿魏酸、洋川芎内酯H、洋川芎内酯I、洋川芎内酯A、藁本内酯的峰面积的RSD分别为0.13%、0.89%、1.52%、1.68%、0.89%、0.94%,表明仪器精密度良好。
2.6 稳定性试验 将同一批次的供试品溶液室温下放置0、2、4、8、12、16、24 h后分别进样分析,计算得到各成分峰面积的RSD,分别为阿魏酸0.19%、洋川芎内酯H 0.92%、洋川芎内酯I 0.14%、洋川芎内酯A 0.14%、藁本内酯0.16%,表明供试品溶液在24 h内稳定性良好。
2.7 重复性试验 取同批川芎药材6份进样,按照供试品溶液制备方法制备后进样分析,对重复性试验进行考察,分别计算得到各成分峰面积的RSD,分别为阿魏酸0.34%、洋川芎内酯I 0.67%、洋川芎内酯H 1.32%、洋川芎内酯A 0.46%、藁本内酯0.27%,表明方法重复性较好。
2.8 加样回收率试验 精密称定0.25 g鲜川芎及川芎药材6份,加入各对照品溶液,按照“2.1”项下样品制备方法制备供试品溶液,按照“2.2”项下色谱条件,进样分析,计算6种成分的回收率和RSD,结果见表2。

表2 加样回收率试验结果
注:空白单元格表示该项下没有检测到相应化合物
2.9 含量测定 按“2.1”项下条件制备样品溶液,按“2.2”项下条件测定。根据川芎药材与鲜川芎质量比折算,川芎药材与鲜川芎中6种成分质量分数见表3。通过与6种物质的标准品对比,鲜川芎中检测出3种成分别是阿魏酸、藁本内酯、洋川芎内酯A;川芎药材中,除川芎嗪外,其余5种成分均被检测出。本研究未在川芎药材及鲜川芎检测到川芎嗪,川芎中川芎嗪含量较低。鲜川芎中未检测到洋川芎内酯H、洋川芎内酯I。

表3 鲜川芎及川芎药材含量测定结果
注:空白单元格表示该项下没有检测到相应化合物;w(川芎药材)=(m/M)×100%,式中m代表川芎药材中检测出该化合物的质量,M代表川芎药材的质量;w(鲜川芎)=(m/7.18M)×100%,式中m代表鲜川芎中检测出该化合物的质量,M代表鲜川芎的质量;平均质量分数分别为鲜川芎、川芎药材6个批次的平均值
3 讨论
3.1 提取方式及时间考察 川芎药材及鲜川芎中富含挥发性成分,因此在提取时选取了超声提取。本研究中使用的鲜川芎未经加工处理,含水量较大,考虑到含水量对提取率的影响,对提取时间进行了考察,分为超声提取30 min、超声提取30 min后室温放置2 h、超声提取30 min后室温放置6 h、超声提取30 min后室温放置12 h,结果表明超声提取30 min后室温放置6 h为最佳提取方式。
3.2 检测波长的选择 结合川芎嗪、阿魏酸、洋川芎内酯I、洋川芎内酯H、洋川芎内酯A、藁本内酯的光谱性质,选择了254、270、280、295、320 nm作为考察检测波长,实验结果表明,295 nm下6种活性成分响应效果较佳,因此选择295 nm作为最佳检测波长。
3.3 鲜川芎与川芎药材的成分转化 本实验将同一批鲜川芎、川芎药材纳入研究,UPLC检测结果发现鲜川芎与川芎药材间成分存在较大的差异。据报道,藁本内酯及洋川芎内酯A是川芎药材中含量较高的两种活性成分[19]。内酯类成分易发生结构改变和转化,在产地加工及储藏过程中的加热、暴晒等程序会增加川芎的成分转化。藁本内酯在自然光照下可降解为洋川芎内酯H和洋川芎内酯I[13];洋川芎内酯I在阳光照射下可形成二聚体[14]。在川芎药材的提取或贮藏过程中,阿魏酸松柏酯易水解为阿魏酸,增加川芎中游离阿魏酸的含量[15]。贮藏两年的川芎药材,阿魏酸、洋川芎内酯I、洋川芎内酯H的含量平均增加46.9%,阿魏酸松柏酯、洋川芎内酯A、藁本内酯的含量平均减少48.3%[16]。鲜川芎的产地加工有两种方式,一为阳光露晒,一为炕床烘干。受加工过程中的光照、温度影响,鲜川芎中的成分发生转化,藁本内酯、洋川芎内酯A含量降低,洋川芎内酯I和洋川芎内酯H含量增加。实验结果表明,鲜川芎与川芎药材成分存在差异。
洋川芎内酯类化合物是川芎的主要活性成分及代谢成分。藁本内酯在大鼠体内的降解产物为洋川芎内酯H和洋川芎内酯I[20],但人体内的主要代谢产物为洋川芎内酯I[21]。研究表明,洋川芎内酯I可快速入血入脑[22],这为川芎的临床治疗疾病提供了直接的物质基础。
本研究通过UPLC测定鲜川芎和川芎药材中6种活性成分的含量,发现鲜川芎、川芎药材中存在成分差异。鲜川芎及川芎药材中均未检测到川芎嗪;鲜川芎中内酯类化合物在产地加工中发生转化,藁本内酯含量降低,洋川芎内酯I、洋川芎内酯H含量增加。
