玉米HD-Zip转录因子基因ZmHOX32的克隆及功能探究
2019-11-21曹丽茹魏良明张前进王振华鲁晓民
张 新,曹丽茹,张 军,魏良明,张前进,魏 昕,王振华,鲁晓民
(1.河南省农业科学院 粮食作物研究所,河南 郑州 450002; 2.河南省蚕业科学研究院,河南 南阳 473000)
转录因子是一类可与下游靶基因DNA片段特异性结合,进而抑制或者激活目标基因表达,调节植物逆境胁迫应答和生长发育的蛋白质。同源异型域-亮氨酸拉链蛋白(HD-Zip)是高等植物特有的一类转录因子,包含高度保守的同源异型域(HD),HD羧基末端与亮氨酸拉链域(LZ)紧密相连[1-2]。其中,由60或61个氨基酸组成的HD区域折叠成由3个α螺旋组成的三维空间结构,可专一性识别目标基因5′上游区的顺式作用元件;LZ区一般由5~6个亮氨酸(Leu)残基组成[3]。另外,有研究表明,HD-Zip只对高等植物特有的发育进程具有至关重要的作用[4]。
研究发现,HD-Zip转录因子虽然序列相似,但所发挥的功能多种多样,如调控植物叶的发育、根毛的形成和避阴反应等[3]。拟南芥HD-Zip转录因子基因中的ATHB-1、ATHB-3、ATHB-13、ATHB-20和ATHB-23与子叶和叶的发育有关[5]。其中,ATHB-2基因的表达受远红外光的调控,通过响应3种不同的光敏色素,控制下胚轴的发育[6]。研究表明,ATHB12基因通过降低GA20氧化酶Ⅰ的表达量调控花序柄的生长,且正向调节叶片发育过程中的细胞生长[7]。在拟南芥中过量表达向日葵HaHB-4基因,拟南芥的茎和节间距离变短,花絮更密,有利于植株对干旱的适应[8]。也有报道,拟南芥中ATHB-5、ATHB-6、ATHB-7、ATHB-12基因均受干旱和外源脱落酸(ABA)诱导,说明它们在失水条件下可能起重要作用[9]。HD-Zip转录因子与植物激素也存在一定的关系,水稻HD-Zip转录因子基因Oshox4过量表达导致半矮型表型,添加外源GA3亦不能复原[10];HD-Zip家族成员Homeobox-leucinezipperproteinHOX22影响ABA的生物合成,通过介导ABA的信号传导途径参与调控干旱和盐胁迫的响应[11]。
HD-Zip蛋白是参与非生物胁迫响应的重要转录因子之一,但关于HD-Zip的研究主要集中在拟南芥、水稻、向日葵等植物上[12],而关于玉米HD-Zip转录因子基因对非生物胁迫和外源激素的应答模式以及特异结合目标靶基因的DNA片段等的研究鲜见报道。鉴于此,对玉米HD-Zip转录因子基因家族中的GRMZM2G178102(ZmHOX32)基因进行克隆,利用生物信息技术分析ZmHOX32基因序列的基因结构、进化特征、启动子顺式作用元件,并利用荧光定量技术分析干旱和外源ABA诱导下ZmHOX32基因的表达模式,为解析HD-Zip转录因子在玉米逆境胁迫和信号传导中的作用奠定基础,并为筛选抗逆性强的玉米种质资源提供依据。
1 材料和方法
1.1 供试材料
试验材料为河南省农业科学院粮食作物研究所提供的玉米自选系郑D58M。取大田生长的郑D58M植株并分为根、茎、芽、叶、雄穗、雌穗、花粉、胚、胚乳和营养分生组织,作为测定ZmHOX32基因时空表达的样品。挑选饱满、大小均匀的郑D58M籽粒播种到营养土中,待玉米生长至一叶一心时,将幼苗从营养土中连根部轻轻拔起,清洗掉泥土后转移至含有Hoagland营养液(pH值5.8)的盒子中,置于温室(30 ℃光照培养16 h、26 ℃暗培养8 h,相对湿度为35%~55%)进行水培。当郑D58M长至三叶一心时,选取长势一致的玉米苗进行以下3个处理:Hoagland营养液(CK)、Hoagland营养液+20% PEG、Hoagland营养液+100 mol/L ABA,处理6、12 h时分别取幼苗相同部位的叶片,然后将3个处理的幼苗均置于新鲜的Hoagland营养液中,36 h后再次取3个处理幼苗相同部位的叶片。以上所有大田和室内样品5株相同部位混匀作为1个样品,每个部位共取3个样品,之后将样品迅速放入液氮,保存于-80 ℃超低温冰箱备用。
1.2 玉米总RNA提取及cDNA的合成
采用RNeasy Plant Mini Kit(QIAGEN,USA)提取玉米RNA,反转录试剂盒PrimeScriptTM1st Strand cDNA Synthesis Kit(TaKaRa大连)反转录合成cDNA。
1.3 ZmHOX32基因的克隆
设计玉米HD-Zip基因家族中GRMZM2G178102(ZmHOX32)基因的特异扩增引物(ZmHOX32-F:ATGGCGTCGGGCGGCT和ZmHOX32-R:TCACACGAAGGACCAGTTG),利用扩增引物进行RT-PCR,RT-PCR 扩增结束后,1%琼脂糖凝胶电泳检测PCR产物,经回收纯化,连接至pMD18-T并转化大肠杆菌DH5α感受态细胞,挑选阳性单克隆送深圳华大基因股份有限公司进行测序,并利用NCBI数据库比对测序结果。
1.4 ZmHXO32转录因子的生物信息学分析
使用在线EXPASY中的Protparam对ZmHXO32转录因子的等电点(pI)、分子质量(MW)、疏水性、稳定性等属性进行计算;分别利用TMHMM Server、SOPMA和Softberry对ZmHXO32的蛋白质跨膜结构、二级结构和亚细胞定位进行分析,使用ExPASy网站的NetPhoS预测ZmHXO32的磷酸化位点;利用Plantcare预测ZmHOX32基因启动子的顺式作用元件;利用MEGA软件中的NJ法构建ZmHXO32与其他物种同源蛋白质的系统发育树;使用MEME在线分析工具对ZmHXO32的保守基序(motif)进行分析,基序的最大数目设置为12。
1.5 ZmHOX3基因的表达分析
采用qRT-PCR定量分析ZmHOX3基因的表达情况。根据ZmHOX3基因序列设计特异荧光PCR引物ZmHOX32-QF:AGCTAGCTAGATGGCGTC和ZmHOX32-QR:ACCCGCTCGAGCGCCTCGA。以玉米18 S rRNA为内参基因,设计引物18S1:5′-CCTGCGGCTTAATTGACTC-3′;18S2:5′-GTTAGCAGGCTGAGGTCTGG-3′。利用CFX96实时荧光定量PCR仪(Bio-Rad,USA),参考SYBR Premix Ex TaqTM(TaKaRa,Japan)试剂盒程序,采用两步法以不同部位和不同处理样品的cDNA为模板进行实时荧光定量PCR。根据2-△△Ct法(△Ct=Ct目标基因-Ct内参基因,△△Ct=△Ct处理后-△Ct对照)进行数据处理。
2 结果与分析
2.1 ZmHOX32基因的克隆及其编码蛋白质的结构分析
利用RT-PCR扩增ZmHOX32基因,得到大小约为3 000 bp的特异条带(图1A),测序结果显示,该基因序列包含1个完整的2 571 bp开放阅读框,编码856个氨基酸,与全基因组序列已经公布的玉米自交系B73的序列一致。序列分析显示,ZmHXO32蛋白含有Homeobox、bZIP、START_ArGLABRA2_like和MEKHLA共 4个功能域(图1B),属于典型的HD-Zip家族。
利用Protparam在线软件分析ZmHXO32蛋白的结构发现,ZmHXO32蛋白的分子质量为93.17 ku,理论等电点为6.59,分子式为C4 084H6 482N1 164-O1 245S42;不稳定指数为47.24,属于不稳定蛋白质;GRAVY值为-0.187,属于亲水性蛋白质;TMHMM Server跨膜螺旋区预测结果显示,ZmHXO32蛋白无跨膜结构域;SOPMA预测结果显示,ZmHXO32蛋白的无规则卷曲占39.95%,β折叠占4.79%,α螺旋占40.89%,该蛋白质主要以α螺旋和无规则卷曲结构为主,亚细胞定位于细胞核。NetPhoS分析显示,ZmHXO32蛋白分别含有49个丝氨酸磷酸化位点、27个苏氨酸磷酸化位点和10个酪氨酸磷酸化位点,说明ZmHXO32蛋白可能被丝氨酸、苏氨酸和酪氨酸蛋白激酶激活,从而调控下游响应基因的表达,参与植物的生长发育、信号传导等过程。
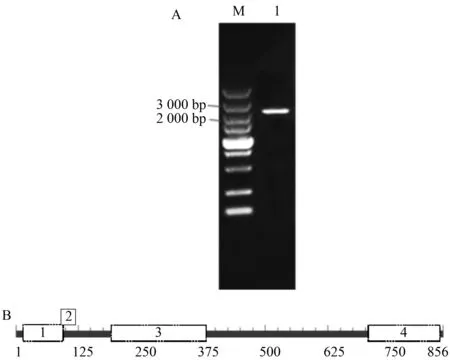
A.ZmHOX32 PCR扩增电泳结果,M.Trans2K DNA Marker,泳道1代表ZmHOX32基因的扩增片段;B.ZmHXO32蛋白结构域,1.Homeobox,2.bZIP,3.START_ArGLABRA2_like,4.MEKHLA
2.2 ZmHXO32的系统进化及保守基序分析
利用NJ法构建玉米ZmHXO32蛋白与其他单子叶和双子叶植物同源蛋白质的进化树(图2)。由图2可见,玉米ZmHXO32蛋白与谷子(Setariaitalica)、胡桃木(Panicumhallii)同源蛋白质的进化关系最为紧密。为了进一步分析ZmHXO32蛋白及其他物种同源蛋白质的保守性,利用MEME软件鉴定了12个保守基序。由图2可知,玉米ZmHXO32蛋白与谷子、胡桃木同源蛋白质不仅同源性较高,保守基序数目及位置也一致,说明不同物种间进化树遗传距离越近,其基序相似度越高,亲缘关系越近。另外,这些物种均含有这12种保守基序,说明ZmHXO32蛋白在进化中功能结构域极为保守。
2.3 ZmHOX32基因启动子顺式元件分析
为了进一步解析ZmHOX32基因的功能,利用Plantcare预测ZmHOX32基因ATG上游2 000 bp的顺式结合元件,结果见表1。由表1可见,ZmHOX32基因含有多种功能性响应元件,除了启动子本身最基本的核心元件TATA-box、CAAT-box等外,还包含如ABRE、AuxRR-core、CAT-box、CCAAT-box、DRE、GC-motif、LTR、TC-rich repeats、TCA-element等结合位点。其中,ABRE参与ABA信号传导途径,响应干旱应答;AuxRR-core是生长素响应因子,在子叶、胚乳和侧根发育中起重要作用;CAT-box调控植物的分生组织表达;CCAAT-box作为MYB转录因子结合位点,或通过受MYB转录因子的调控参与植物的逆境胁迫;DRE响应干旱和盐胁迫;GC-motif 在抗氧化反应中起重要作用;LTR响应低温胁迫,启动低温相关基因的表达;TC-rich repeats参与抵御植物的外界胁迫;TCA-element 参与水杨酸的信号传导途径。另外,还发现大量光刺激应答元件(TCCC-motif、G-box、GT1-motif和AE-box),推测ZmHOX32基因可能还参与植物光合作用和调控植物开花等光反应。

带数字的方框代表不同的基序
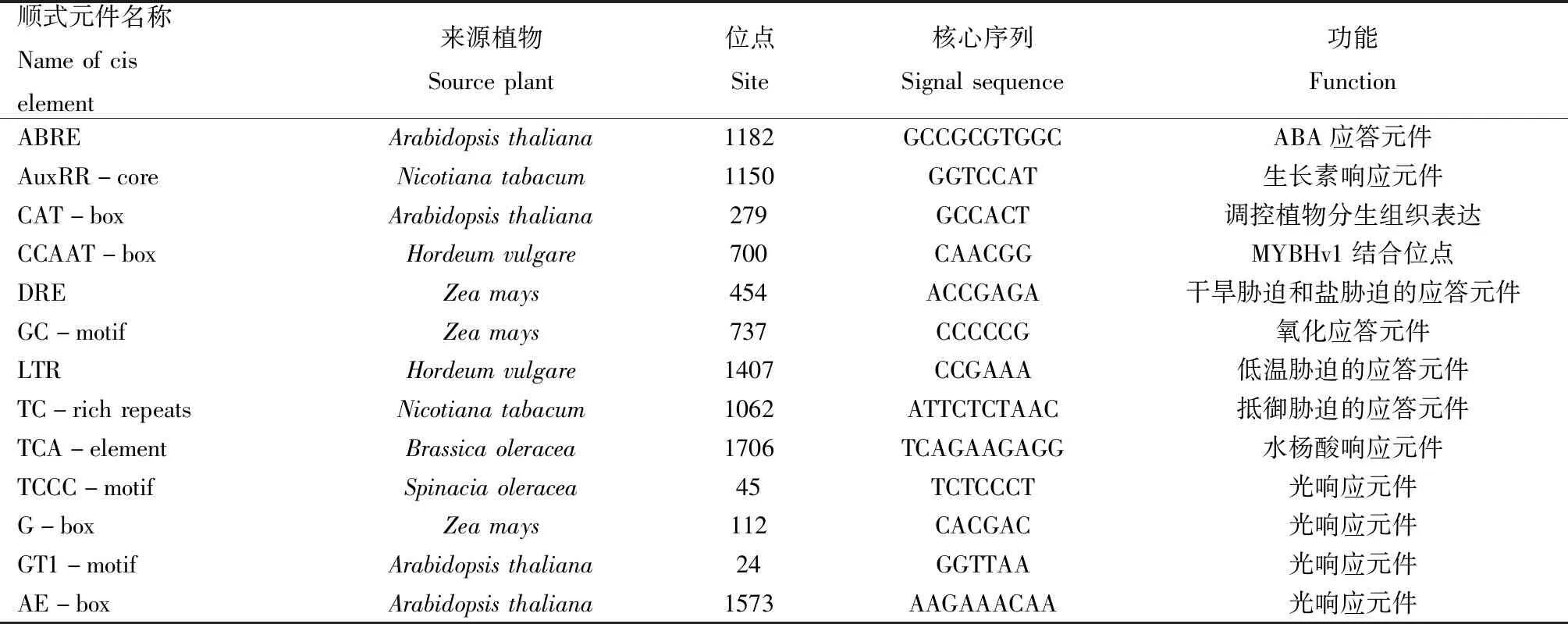
表1 ZmHOX32基因启动子顺式元件分析
2.4 ZmHOX32基因的组织表达模式分析
为了解ZmHOX32基因的组织表达模式,利用qRT-PCR分析该基因在玉米生长不同时期及不同组织的表达情况,结果如图3所示。由图3可见,ZmHOX32基因在根、茎、芽、叶、雄穗、雌穗、花粉、胚、胚乳和营养分生组织中均有表达,且在营养分生组织中表达量最高;ZmHOX32基因在胚中的表达量较在胚乳中表达量高。可见,ZmHOX32属于组成型表达基因,但不同部位的表达量存在不同程度的差异,说明ZmHOX32基因在植物整个生长发育过程中均发挥着重要作用。
2.5 ZmHOX32基因对干旱胁迫和ABA诱导的响应模式分析
由图4可见,与CK相比,PEG和ABA胁迫6、12 h时,ZmHOX32基因相对表达量均上升,且ABA胁迫下的表达量高于PEG胁迫;进一步分析恢复正常营养液培养后36 h的表达情况发现,PEG和ABA胁迫处理下ZmHOX32基因的表达量均较之前下降,与CK接近但均未达到正常水平。说明ZmHOX32基因响应干旱胁迫和ABA诱导,且受二者的正向诱导,即ZmHOX32基因可能在玉米响应干旱胁迫过程中具有重要作用。
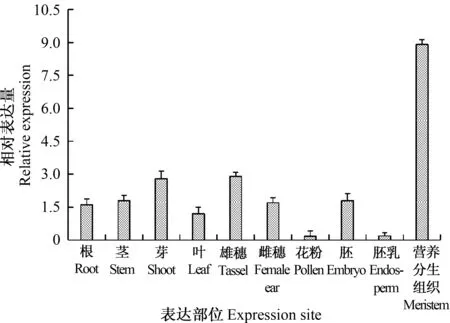
图3 ZmHOX32基因在玉米不同组织中的表达模式
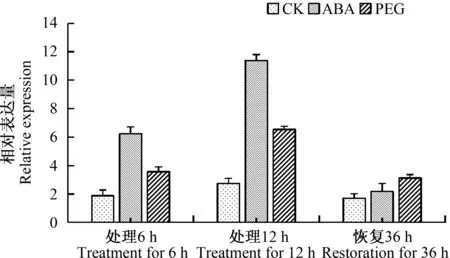
图4 ZmHOX32基因响应干旱和ABA胁迫诱导的表达模式
3 结论与讨论
HD-Zip结构域在所有真核生物中存在高度保守的DNA序列基序[13]。由3个α螺旋折叠成的HD区域可专一性地识别目标基因启动子上游区的顺式DNA序列;亮氨酸拉链是蛋白质中常见的三维结构基序,其蛋白质含有ABA反应元件,在种子和营养组织中作为ABA信号传导的重要参与者,是非生物胁迫(干旱、盐、冷)响应的关键区域[14]。本研究发现,ZmHXO32蛋白序列主要以α螺旋方式存在,ZmHOX32基因启动子区域含有ABA和水杨酸信号传导的结合位点(ABRE和TCA-element),也含有DRE、GC-motif、LTR、TC-rich repeats等抵御外界刺激和非生物胁迫的顺式结合位点。说明ZmHOX32基因在逆境胁迫和信号传导途径中起重要作用。
本研究中,ZmHOX32基因属于组成型表达基因,在根、茎、芽、叶、雄穗、雌穗、花粉、胚、胚乳和营养分生组织中均有表达,但ZmHOX32基因在营养分生组织中表达量最高;在胚和胚乳中均有表达,但在胚中表达量较高,ZmHOX32基因在植物整个生长发育过程中均发挥着重要作用。前人研究结果表明,HD-Zip转录因子基因家族的组织表达模式不尽相同,如拟南芥中的HD-Zip类转录因子基因大多数在表皮组织中特异表达,其中GL2/ATHB-10和PDF2调控细胞表皮特定基因的表达[15];Zmhdz10基因也属于组成型表达基因,但在叶片中表达水平最高[16];水稻Oxshox1属于组成型表达基因,在幼芽和成熟的叶片中呈现高表达[17]。可见,同一家族的基因在植物生长发育和逆境胁迫过程中的作用机制不同。
水稻Oshox4基因已被证实可提高水稻的抗旱性[10]。拟南芥Athb7基因受植物激素ABA调控,干旱胁迫下该基因上调表达[18]。采用ABA或者氯化钠处理植物幼苗,发现ATHB-7、ATHB-12、ATHB-6和ATHB-40的表达量上调,而ATHB-3、ATHB-23、ATHB-5和ATHB-52的表达量降低1/2[15];盐处理使ATHB-1和ATHB-16表达量减少,但ABA对其表达量无影响[19]。本研究中,玉米ZmHOX32基因在PEG和ABA胁迫以及恢复正常时均受PEG和ABA的正向诱导,但ABA诱导下基因的表达量高于PEG模拟的干旱胁迫;进一步分析恢复正常营养液后36 h的玉米植株发现,ZmHOX32基因的表达量较PEG胁迫和ABA诱导6、12 h时的表达量均有所下降,但仍未达到正常水平,说明植株受胁迫后,遭受一定程度的破坏,恢复正常生长条件后虽有一定的补偿作用,但补偿效应低于胁迫带来的损伤。以上结果为研究ZmHOX32基因在逆境胁迫和激素传导中的作用机制奠定了基础。
本研究克隆了玉米HD-Zip转录因子家族的ZmHOX32基因,ZmHXO32蛋白属于亲水性蛋白质,定位于细胞核内;进化树和保守基序分析发现,ZmHXO32蛋白与谷子(Setariaitalica)、胡桃木(Panicumhallii)同源蛋白质的保守功能域完全一致,三者序列高度同源;ZmHOX32基因的启动子序列含有响应激素(脱落酸和水杨酸)和非生物胁迫(干旱、盐、冷)及光刺激的结合元件;qRT-PCR结果显示,ZmHOX32基因属于组成型表达基因,在营养分生组织中高表达,且正向响应干旱胁迫和ABA诱导,在干旱胁迫和ABA信号传导路径中起重要作用。
