电子守恒法在配平复杂有机化学反应方程式中的应用
2019-11-19崔文辉贾如琰聂龙英
崔文辉,贾如琰,聂龙英
(陇南师范高等专科学校农林技术学院,甘肃 成县 742500)
在任何一个氧化还原反应中,氧化剂得到的电子均来自还原剂所失去的电子,且得失数目必然相等,这就是电子守恒定律。在配平时,通过分析元素化合价的变化很容易确定还原剂和氧化剂及其电子得失的数目,当使得氧化剂和还原剂电子得失数目相等时,其相应的化学式前面的计量系数已经确定。其余分子式前面的计量系数再通过相关元素原子的数目守恒原理,经过简单计算而确定。
在基础有机化学的教学内容中,与无机化学相比,需要严格配平的化学反应方程式数量相对非常少,"配平问题"通常也不是教学的重点。但是,也有个别几个有机化学反应方程式[1],仅用观察法不容易尝试出正确的结果,配平后分子式前化学计量系数并不简单,这些数字非常直观的折射出配平问题的复杂性。如图1所示乙烯使酸性高锰酸钾溶液褪色的反应[1],以及实验室用金属锡加盐酸还原硝基苯制取少量苯胺的反应等[2]。应用电子守恒法配平氧化还原化学反应方程式时,首先要分析元素化合价变化,在有机化学反应中,其中最为常见的是对C、N两种元素的化合价的确定问题,由于这两种元素在不同的有机化合物中化合价是不同的,需要对相关有机化合物分子结构信息进行分析。对于有机化合物分子结构而言,初学者因刚接触这方面的知识,经验不足而普遍感到困难,客观上需要在课堂上给予分析讲解。本文利用氧化还原反应中电子守恒原理,专门对2个有机化学反应方程式进行配平,从而进一步揭示和呈现电子守恒法在配平有机氧化还原反应方程式中独特的优势。
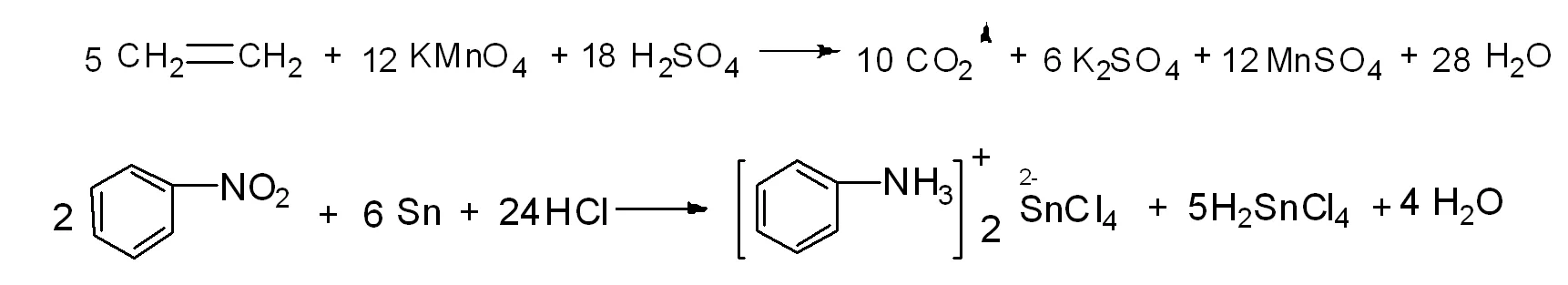
图1 化学计量系数比较大的有机化学反应方程式
1 分析反应式中各元素化合价,找出还原剂和氧化剂
也许是由于乙烯与酸性高锰酸钾反应方程式的产物的复杂性和配平的难度,在许多的大学有机化学教材中都没有给出乙烯与酸性高锰酸钾的反应方程式。学生只有通过查找资料才能写出相关反应方程式。
示例1:对于乙烯与酸性高锰酸钾反应方程式而言,通过分析反应式中各元素化合价,很容易发现C和Mn两种元素反应前后有变化,分别是还原剂和氧化剂。如图2中(1)~(3)式所示。
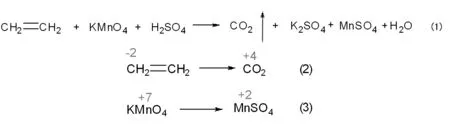
图2 元素化合价变化关系
乙烯分子中碳元素化合价分析:
在乙烯分子中每个C原子结合2个H原子,由于C元素电负性比H元素的大,C、H原子间共用电子对偏向于C原子,故认为H元素显正价,C元素显负价。此外,乙烯分子中2个C原子以双键相互键合,由于是同种元素之间成键,可认为相当于单质,化合价当作零对待。这样计算C元素化合价的代数和得出其在乙烯分子中的表观化合价为-2价,如图3中的(4)~(5)式所示。
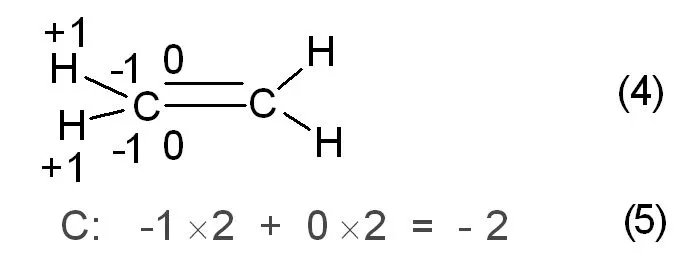
图3 乙烯分子中碳元素化合价分析
2 分析反应中单个原子反应前后电子得失数目
接下来分析C,Mn两种元素单个原子反应前后电子得失数目,如图4中的(6)、(7)式所示:
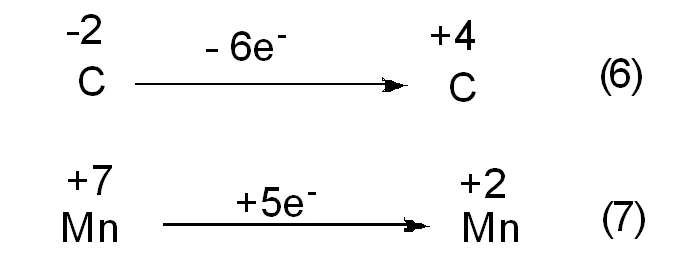
图4 反应中相关原子电子得失数目
3 根据一个分子组成中实际所含相关元素原子的数目,分别计算出反应中得与失电子的总数 ,在使电子得失数目相等时确定了氧化剂和还原剂分子式前系数
在考虑到一个分子组成中实际所含相关元素(C,Mn)原子的数目的前提下,分别计算出得与失电子的总数,并根据电子守恒原理,通过最小公倍数的方法求得还原剂和氧化剂所需各自的原子的个数,进而得到相应分子式前系数。如图5中的(8)式所示,在反应中电子转移总数为60的前提下,需要5个乙烯分子和12个高锰酸钾分子参与反应。
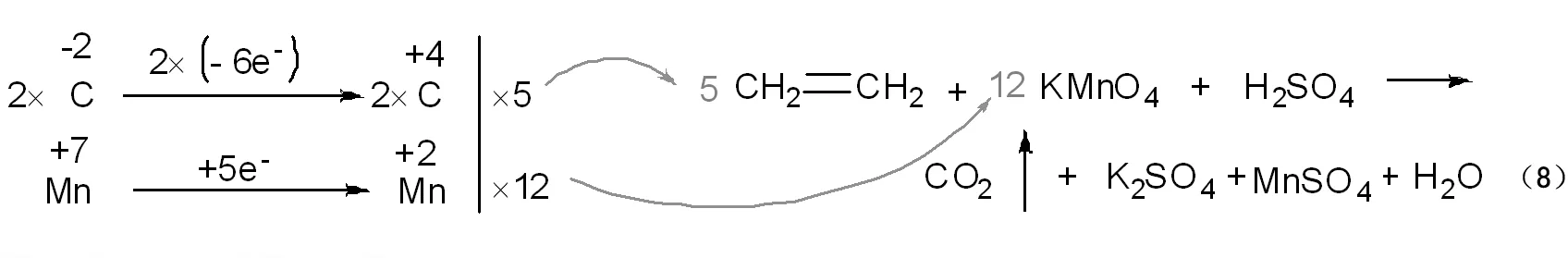
图5 氧化剂和还原剂分子式前计量系数的确定
4 用观察法配平其它元素原子个数
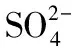
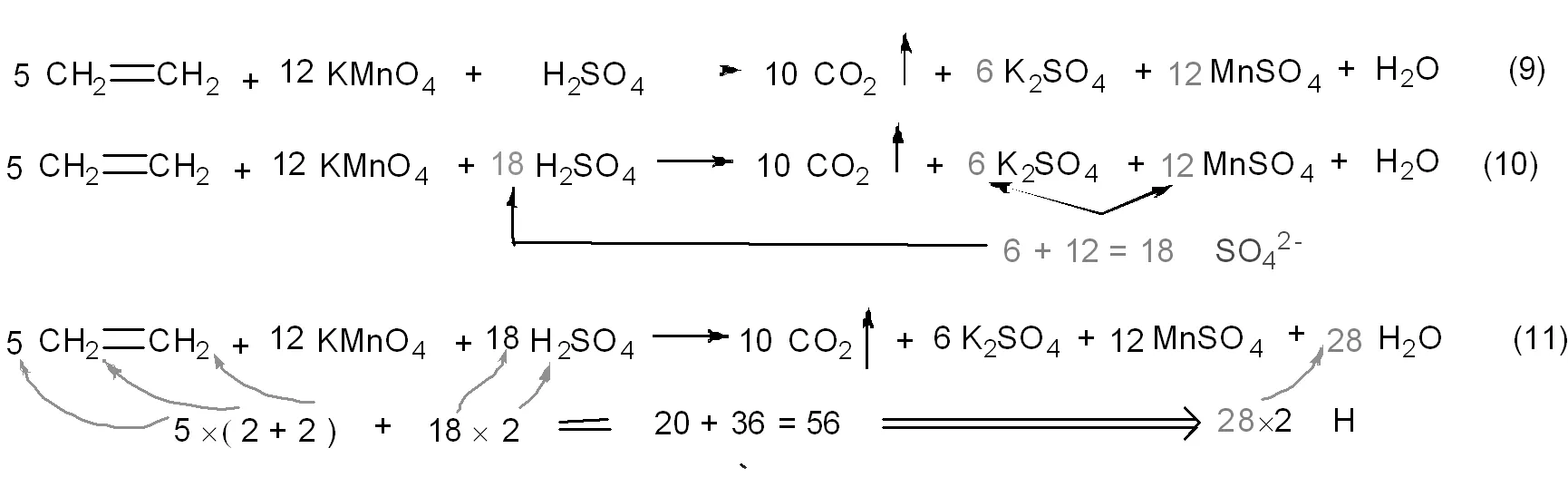
图6 观察法配平其他元素(Mn、K、S、H)原子个数
示例2:实验室制取少量苯胺常用锡加盐酸还原硝基苯的反应。
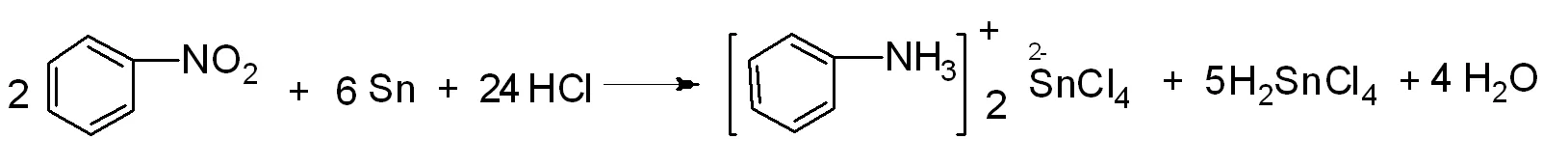
要理解该方程式的配平,首先需了解硝基的结构及其中氮元素的化合价,硝基化合物结构式如图7所示。
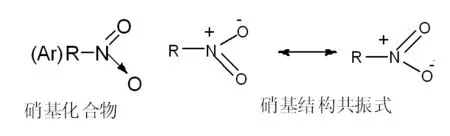
图7 硝基化合物分子结构式的常见两种写法
硝基化合物和苯胺分子中N元素化合价如图8所示,虽然N原子与2个O原子之间以一个双键和1个单键结合,但由于N-O单键是以N原子一方单独提供2个电子与氧原子空轨道配位而成的,故,共有4个电子偏离N原子而呈现+4价。同时,N原子与C原子结合的单键之中,电子对是偏向N原子的,而呈现-1价,综合考虑后计算N元素化合价的代数和是+3价。
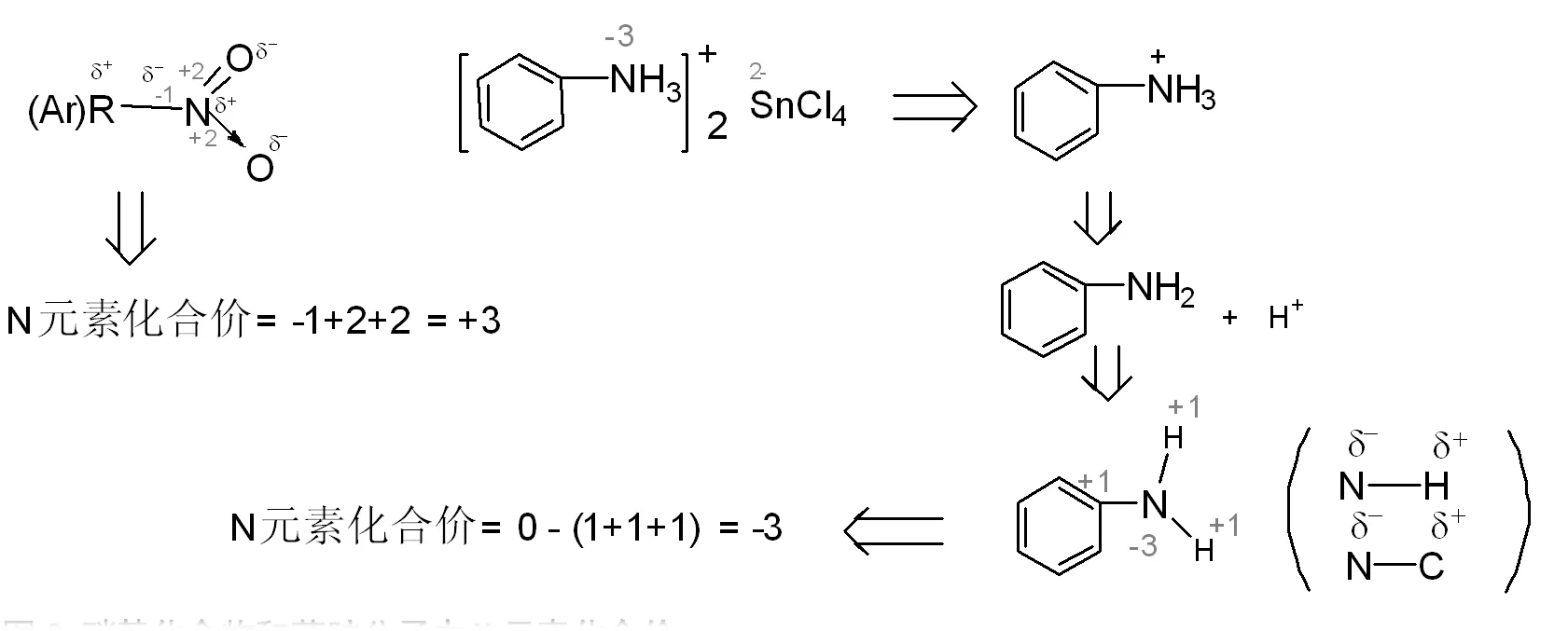
图8 硝基化合物和苯胺分子中N元素化合价分析
接下来,标出发生氧化还原反应的相关元素的化合价。
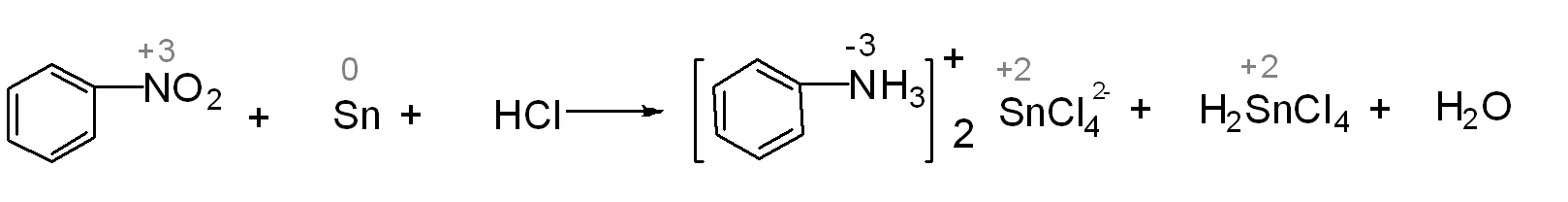
由生成物四氯络锡酸苯胺盐1个分子中有2个氮原子反推出至少需要2个硝基苯分子参与反应,所以参与得电子的N原子数至少要按2个计算。根据电子守恒原理,可首先确定与N,Sn元素原子相关的硝基苯分子和锡原子的系数,如图9所示。
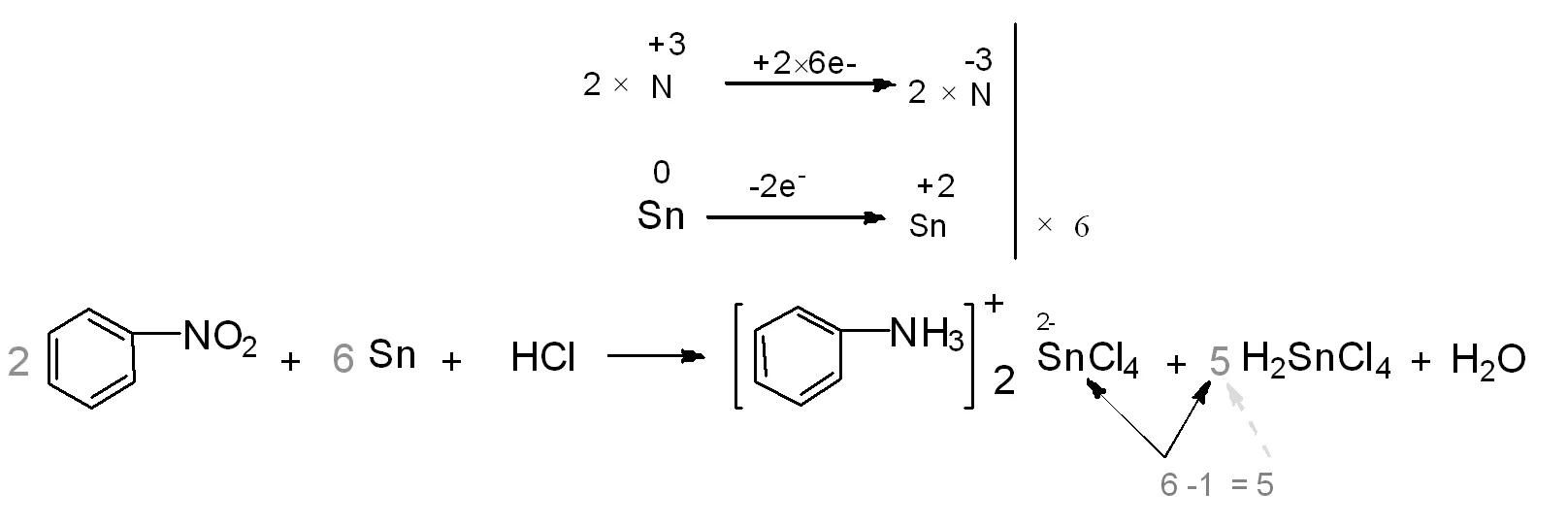
图9 硝基苯和金属锡分子式前计量系数的确定
用观察法通过计算Cl、H原子的个数确定HCl分子式前的系数,如图10所示。
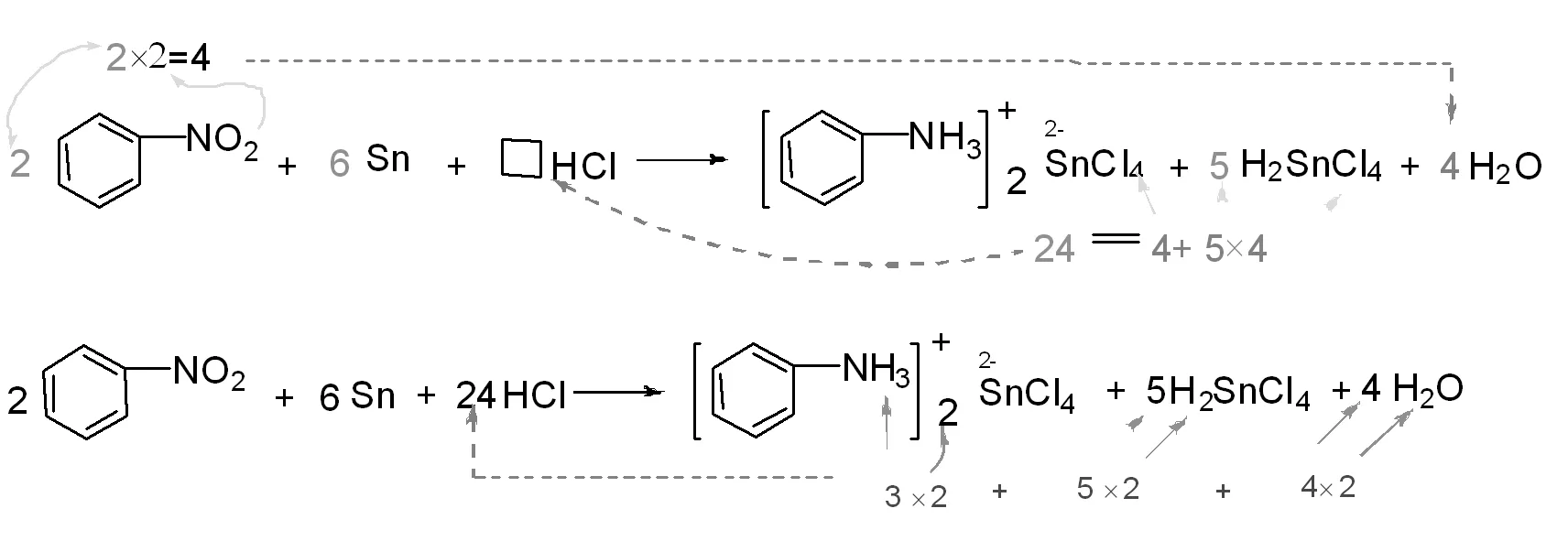
图10 HCl分子式前计量系数的确定
综上所述,电子守恒法用于配平有机氧化还原反应方程式,关键是正确分析相关有机化合物的分子结构,得出发生电子得失或偏移的元素的化合价,配平方程式时先使反应中得失电子数目相等,就是找准了问题的关键,具有准确、高效、简便等优点。
