特立氟胺治疗多发性硬化的有效性及安全性的Meta分析
2019-11-09刘洋,付锦
刘 洋,付 锦
多发性硬化是一种累及脑和脊髓的慢性炎症性自身免疫性疾病,具体表现为脱髓鞘、局灶性炎性浸润、轴突损伤等。其中CD4+和CD8+T淋巴细胞、B淋巴细胞、抗体、巨噬细胞和细胞因子在髓鞘攻击和轴突损伤中起协同作用。复发是多发性硬化的典型临床特征之一,多发性硬化的症状对患者的心理和情绪状态以及生活质量有很大的影响。随着多发性硬化的出现,给患者、家庭和社会造成了重大的经济负担。目前可供选择的复发型多发性硬化(RMS)的一线治疗药物主要有:干扰素β、醋酸格拉替雷、特立氟胺、富马酸二甲酯[1]。而在中国,仅有干扰素β、特立氟胺和芬戈莫德被食品药品监督管理局批准上市。特立氟胺(Teriflunomide)是一种口服的嘧啶合成酶抑制剂和免疫调节剂,是抗风湿药来氟米特的主要活性代谢产物。该药物抑制了参与嘧啶从头合成途径中的关键线粒体酶,二氢乳清酸脱氢酶(DHODH),阻止新生嘧啶的合成,导致DNA合成障碍,从而抑制活化的T细胞和B细胞的增值[2]。以往有研究讨论特立氟胺在RMS治疗中的有效性和安全性。然而,这些研究的样本量很小。因此,我们进行Meta分析,包括目前的随机对照试验(RCTs),进一步评估特立氟胺治疗RMS的有效性和安全性。
1 资料与方法
1.1 检索策略 检索Pubmed、Embase、Medline、Web of Science、Cochrane图书馆、万方、中国知网等电子数据库获取文献,检索时间为2019年7月截止,起始年限不限。使用检索关键词“多发性硬化”、“特立氟胺”、“multiple sclerosis”、“MS”“Teriflunomide”进行检索。将纳入的文献再通过手工的方式筛查其参考文献,以确保纳入文献的系统性和全面性。
1.2 纳入与排除标准
1.2.1 纳入标准 (1)研究对象为确诊为复发型MS患者或临床孤立综合征(CIS),MS采用McDonald等标准作为诊断标准;(2)研究方法为前瞻性的随机对照研究;(3)对照组采用安慰剂对照;(4)原始文献需提供的数据至少具有以下主要结果之一,具体包括年复发率、残疾进展、任何不良事件和严重不良事件并明确报道了疗效的评判标准,且提供各治疗组人数;(5)特立氟胺的剂量应为7 mg或14 mg;(6)原始资料为已公开发表的文献。
1.2.2 排除标准 (1)动物实验;(2)研究对象是非RMS 患者;(3)患者为儿童;(4)个案报道或综述;(5)研究对象的数量<10人或无法得知样本数量;(6)数据不完整;(7)重复发表的文献。
1.3 文献筛选 由两位研究者分别独立的对文献检索结果进行筛选,意见不一致时经讨论决定。排除重复的文献,再根据纳入标准和排除标准进行复筛,然后阅读文章题目和摘要,删除不相关文献,留取可能纳入的文献并阅读全文,最终确定纳入的文献。
1.4 数据提取及质量评价 从最终纳入的研究中首先进行一般数据的提取,提取的信息如下:第一作者姓名、出版年限、文章类型、患者类型、患者数量、干预措施、平均年龄、性别、EDSS评分等。Cochane系统评价手册5.1版RCT质量评价标准用于评估纳入研究的质量,其中评价标准包括随机序列生成、分配隐藏、盲法、结果数据是否完整、选择性报告结果、其他偏倚。对纳入的文献进一步进行效应量的提取,提取信息包括:复发率、任何不良反应、严重不良反应、导致试验中止的不良反应等。
1.5 统计学分析 对提取的效应量通过Cochane图书馆官网提供的Revman 5.3软件统计分析。二分类效应量合并采用风险比(RR)及95%可信区间(confidence interval,CI)表示。连续型变量效应量的合并采用标准化均数差(SMD)及95%CI表示,当P<0.05为有统计学意义。利用I2值作为异质性检验(test for heterogeneity)的检验标准。当I2>50%,即为存在显著异质性,采用随机效应模型(random effect model);当I2≤50%,即各研究结果间异质性较小,采用固定效应模型(fixed effect model)。对存在显著异质性的效应量,采用敏感性分析的方法来判断异质性的来源。
2 结 果
2.1 文献检索结果及质量评价 通过检索数据库获得257篇文献,经过筛选后,最终纳入8篇文献[3~10],其中7篇文献[3~6,8~10]报道了两种剂量,按14项试验处理。因此,最终纳入了8篇文献,15项试验,共有2875例患者。纳入文献的一般特征(见表1)。
2.2 特立氟胺治疗复发型MS的有效性分析
2.2.1 复发率 (1)特立氟胺7 mg组:3篇文献[4,5,7]均有复发率的统计结果,对比其复发率,异质性检验结果较高(I2=90%),以去除单项研究法在去除Paul等人[4]的研究后消除了异质性(I2=0)。剩余2篇文献[5,7](特立氟胺7 mg组610名患者,安慰剂组585名患者)效应量合并结果显示两组之间有统计学差异(RR=0.69,95%CI0.56~0.85,P=0.0007),表明与安慰剂相比,特立氟胺7 mg可降低复发型多发性硬化患者的复发率(见图1)。(2)特立氟胺14 mg组:3篇文献[4,5,7]均有复发率的统计结果,对比其复发率,异质性较高(I2=93%),以去除单项研究法在去除Paul等人[4]的研究后消除了异质性(I2=0)。剩余2篇文献[5,7](特立氟胺14 mg组584名患者,安慰剂组585名患者)效应量合并结果显示两组之间有统计学差异(RR=0.67,95%CI0.54~0.84,P=0.0004),表明与安慰剂相比,特立氟胺14 mg可降低复发型多发性硬化患者的复发率(见图2)。
2.3 特立氟胺治疗复发型MS的安全性分析
2.3.1 任何不良反应的发生率 (1)特立氟胺7 mg组:5篇文献[3,6~8,10]均有任何不良反应的统计结果,对比其不良反应,异质性检验结果为I2=0%,采用固定效应模型。5篇文献(特立氟胺7 mg组1289名患者,安慰剂组1120名患者)合并效应量结果显示两组不良反应之间无明显统计学差异(RR=1.00,95%CI0.97~1.03,P=0.94)。表明特立氟胺7 mg或安慰剂治疗在任何不良事件的发生率上无显著统计学差异(见图3)。(2)特立氟胺14 mg组:6篇文献[3,6~10]均有任何不良反应的统计结果,对比其不良反应,无异质性(I2=0%),采用固定效应模型。6篇文献(特立氟胺14 mg组1286名患者,安慰剂组1156名患者)合并效应量结果显示两组不良反应之间无明显统计学差异(RR=1.03,95%CI0.99~1.06,P=0.12)。表明特立氟胺14 mg或安慰剂治疗在任何不良事件的发生率上无显著统计学差异(见图4)。
2.3.2 严重不良反应的发生率 (1)特立氟胺7 mg组:5篇文献[3,6~8,10]均有严重不良反应发生率的统计结果,对比严重不良反应,其异质性检验结果为I2=0%,采用固定效应模型。5篇文献(特立氟胺7 mg组1289名患者,安慰剂组1120名患者)合并效应量结果显示两组严重不良反应之间无显著统计学差异(RR=1.03,95%CI0.84~1.25,P=0.81)。表明特立氟胺7 mg或安慰剂治疗在严重不良事件的发生率上无明显统计学差异(见图5)。(2)特立氟胺14 mg组:6篇文献[3,6~10]均有严重不良反应的统计结果,对比其严重不良反应,无异质性(I2=0%),采用固定效应模型。6篇文献(特立氟胺14 mg组1286名患者,安慰剂组1156名患者)合并效应量结果显示两组严重不良反应之间无明显统计学差异(RR=1.13,95%CI0.92~1.38,P=0.24)。表明特立氟胺14 mg或安慰剂治疗在严重不良事件的发生率上无显著统计学差异(见图6)。
2.3.3 导致试验中止的不良反应发生率 (1)特立氟胺7 mg组:5篇文献[3,6~8,10]均有导致试验中止的不良反应发生率的统计结果,对比导致试验中止的不良反应,其异质性检验结果为I2=41%,采用固定效应模型。5篇文献(特立氟胺7 mg组1289名患者,安慰剂组1120名患者)合并效应量结果显示两组导致试验中止的不良反应之间存在统计学差异(RR=1.35,95%CI1.06~1.71,P=0.02)。表明特立氟胺7 mg相比安慰剂在治疗上可能会因为其某种不良反应导致药物研究试验中止(见图7)。(2)特立氟胺14 mg组:6篇文献[3,6~10]均有导致试验中止的不良反应发生率的统计结果,对比其导致试验中止的不良反应,异质性检验结果为I2=59%,大于50%,采用随机效应模型。6篇文献(特立氟胺14 mg组1286名患者,安慰剂组1156名患者)合并效应量结果显示两组导致试验中止的不良反应之间有统计学差异(RR=1.51,95%CI1.01~2.26,P=0.04)。表明特立氟胺14 mg相比于安慰剂在治疗方面可能会因为其某种不良反应导致药物研究试验中止(见图8)。
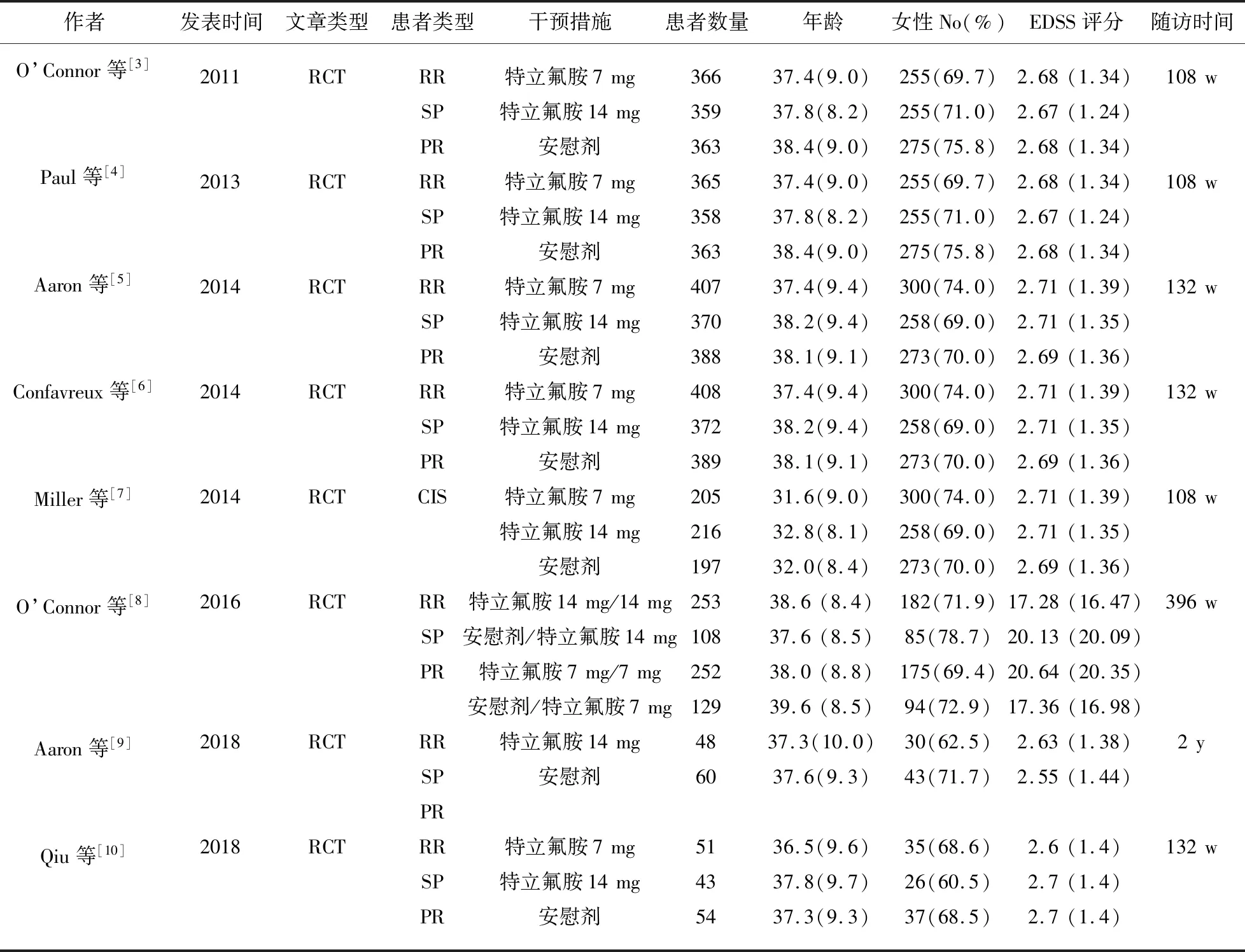
表1 纳入文献的一般特征

图1 复发率森林图(特立氟胺7 mg)
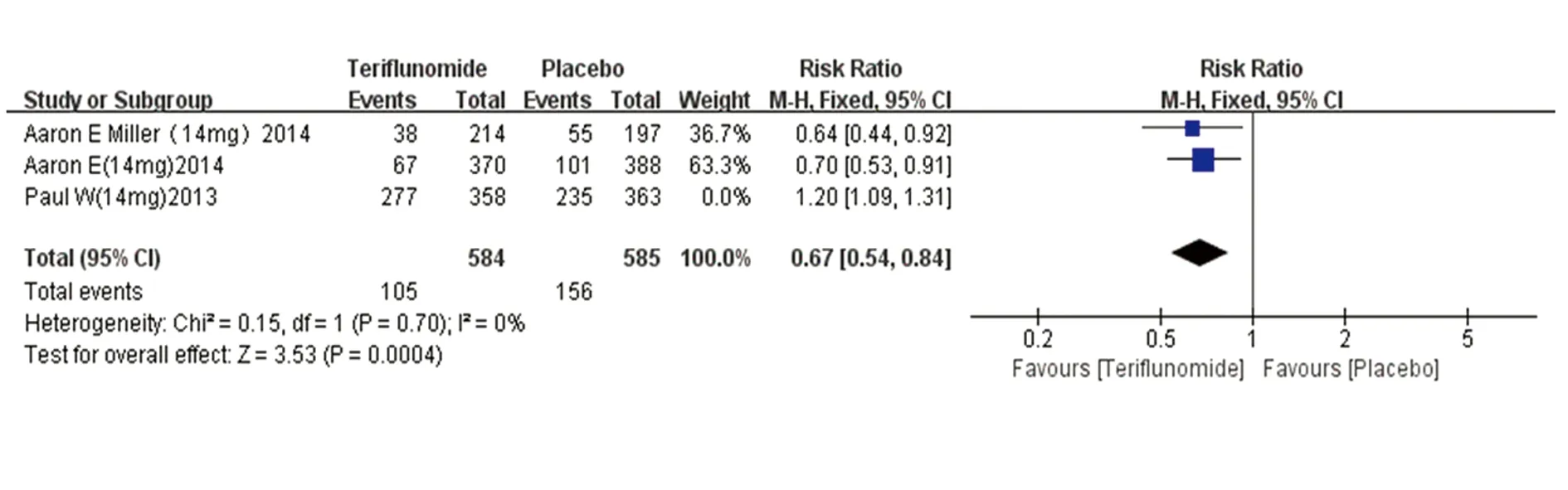
图2 复发率森林图(特立氟胺14 mg)
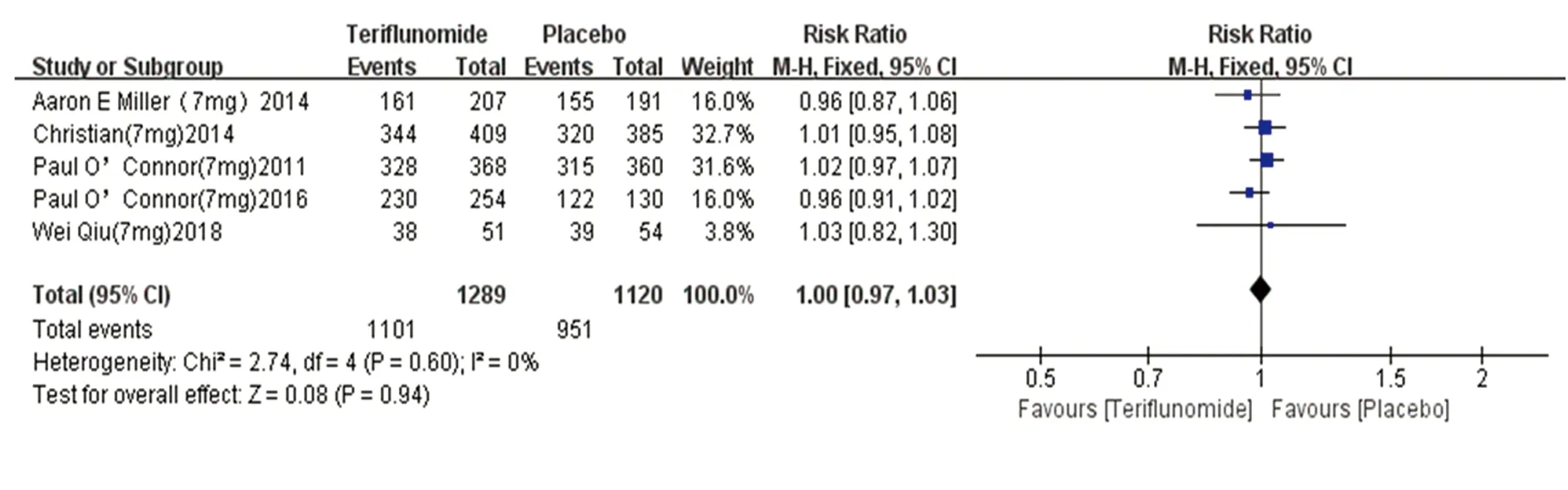
图3 任何不良反应的发生率森林图(特立氟胺7 mg)

图4 任何不良反应的发生率森林图(特立氟胺14 mg)
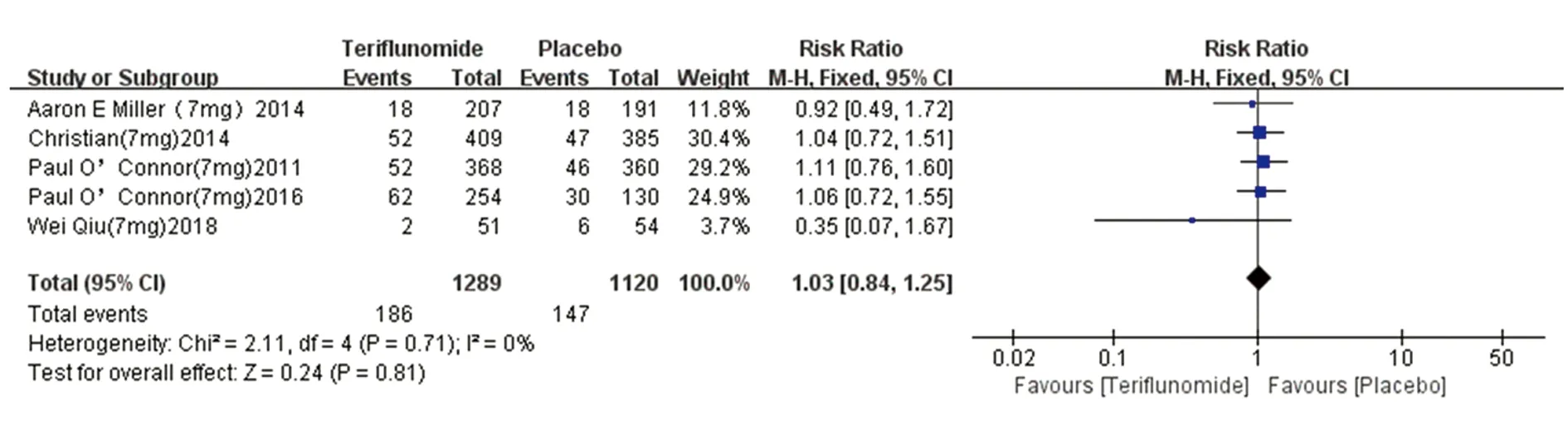
图5 严重不良反应的发生率森林图(特立氟胺7 mg)

图6 严重不良反应的发生率森林图(特立氟胺14mg)
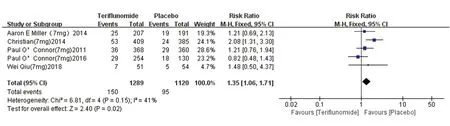
图7 导致试验中止的不良反应发生率森林图(特立氟胺7 mg)

图8 导致试验中止的不良反应发生率森林图(特立氟胺14 mg)
3 讨 论
多发性硬化是一种免疫介导的中枢神经系统脱髓鞘疾病,它是一种受遗传和环境因素影响的疾病,作为免疫反应的触发剂和激活剂,促进中枢神经系统的炎症和退行性病变。MS主要影响年轻妇女,是造成年轻人残疾的最常见原因之一。60多年来,MS的治疗一直是其研究的热点。目前,在临床上常用的治疗药物主要包括:急性期采用糖皮质激素,当无效或无法耐受时采用血浆置换或注射免疫球蛋白;缓解期治疗则以控制疾病进展为主要目标,应用疾病修饰药物(disease-modifying drugs,DMDs)进行长期的治疗。目前在国际上常用的一线治疗药物有干扰素β、醋酸格拉替雷、特立氟胺、富马酸二甲酯;二线药物有芬戈莫德、奥克雷珠单抗、阿仑单抗、那他珠单抗;三线药物有米托蒽醌(Mitoxantrone)、克拉屈滨(Cladribine)等以及一些尚处于试验阶段的单克隆抗体,如利妥昔单抗、奥法木单抗等等。特立氟胺作为我国首个用于治疗多发性硬化的口服新药,很大程度上减少了注射类DMDs给多发性硬化患者带来的不便,大大的提高了患者的依从性和满意度,但是其疗效以及安全性还需进一步的临床评价。因此,我们进行了Meta分析,以期进一步评估特立氟胺治疗RMS的有效性和安全性。
我们的Meta分析为特立氟胺治疗RMS的有效性和安全性提供了一个精确的评估,我们的研究结果表明:(1)在有效性方面,特立氟胺与安慰剂相比,每日口服特立氟胺可显著降低年复发率;(2)在安全性方面,接受特立氟胺的受试者在随访中发生任何不良反应和严重不良反应的风险与接受安慰剂的受试者相似。然而,两种剂量的特立氟胺均增加了因不良反应导致的研究药物停用的风险。与特立氟胺有关的最常见的不良反应包括腹泻、恶心、头发稀疏、ALT升高、中性粒细胞减少等。这些不良发应很少导致研究药物的中断,但确实受特立氟胺剂量的影响。本Meta分析通过采用随机效应模型替代固定效应模型的方式来进行敏感性分析,其结果并没有本质性的改变,说明本篇Meta分析可靠性较好,其结果对临床一线治疗具有一定的参考作用。
由于本研究为二次研究,其质量主要依赖于原始研究的质量,故可能存在一定的局限性:(1)纳入研究的基本特征略有不同;(2)本研究仅检索了部分数据库,对尚未发表的文献暂无收集,且检索语种仅为中文和英文,所以可能存在数据库偏倚、语种偏倚;(3)目前特立氟胺在临床仍然处于使用过程中,所以在使用过程中出现的新问题和新发现还需要持续追踪,以期更加完善;(4)所纳入的文献中部分效应数据不具有统一性,有些效应数据不足以进行合并,遂未对其进行合并;(5)本研究主要基于RCT试验,没有纳入用药过程中出现的罕见不良事件的病例报道,因此还需补充相关个案报道以供完善。
综上所述,通过本Meta分析可以得出特立氟胺显著降低了年复发率,与安慰剂相比在有效性方面更占有优势,且其安全性和耐受性与安慰剂相似。特立氟胺能够减少严重复发的事实进一步支持了它在RMS患者中的应用。然而,由于我们的研究样本有限,还需要大的多中心RCT来证实我们的发现。
