黄连、肉桂配伍与二甲双胍干预奥氮平引起体重增加的药效比较
2019-11-08
江西省九江市第五人民医院精神科,江西 九江 332000
奥氮平治疗精神分裂症疗效佳,耐受性显著优于第一代抗精神病药,已成为抗精神病药首选药物[1],但其长期作用易引起体重增加等代谢障碍,进而增加心脑血管并发症和早逝的风险[2]。针对奥氮平引起体重增加的日常生活方式干预、行为治疗等非药物方式干预远远不够,目前主要药物干预手段是二甲双胍,疗效并不理想,不良反应报道不详细[3]。前期研究发现黄连与肉桂配伍改善奥氮平致糖脂代谢紊乱的效果显著优于二甲双胍,肉桂可提高黄连的药效[4]。黄连的主要有效成分黄连素干预奥氮平引起体重增加的外周组织信号通路的研究较多[5-6],干预奥氮平引起体重增加的中枢5羟色胺(5-hydroxytryptamine,5-HT)信号通路的研究尚未见报道。本研究旨在通过二甲双胍、黄连与肉桂配伍干预奥氮平引起体重增加的药效比较,为探寻奥氮平等第二代抗精神病药引起体重增加的中枢5-HT信号通路的干预机制提供依据。
1 资料与方法
1.1 一般资料 选取2018年1月至2018年7月住院单一口服奥氮平15mg/d治疗后引起体重增加大于10%的精神分裂症患者60例,按门诊号顺序随机分配到黄连与肉桂颗粒配伍+模拟盐酸二甲双胍缓释片组(A组,30例) 、盐酸二甲双胍缓释片+模拟黄连与肉桂颗粒配伍(B组,30例) 组。A组患者因病情好转出院失访3例,27例患者中男19例、女8例,年龄(26.15±7.07)岁,精神分裂症病程(6.89±2.42)个月;B组患者因病情好转出院失访2例,28例患者中男20例、女8例,年龄(25.57±6.05)岁,精神分裂症病程(7.25±1.90)个月。两组性别、年龄、病程差异均无统计学意义(P>0.05),具有可比性。本研究经九江市第五人民医院医学伦理委员会审查批准(九五医伦字[2017]6号)。
1.2 纳入标准 精神分裂症诊断采用《国际疾病分类(第10版)》标准;年龄在18~45周岁,未服过抗精神病药、病程未超过1年;所有受试者对本研究方案内容知情并签署同意书。
1.3 排除标准 严重自伤自杀、伤人毁物行为等难以管理者;伴有高血压、心脏病、糖尿病等内分泌疾病以及肝肾功能异常等重大躯体疾病者;妊辰或哺乳期妇女;结核病、艾滋病等慢性感染者;药物依赖者。
1.4 干预方法 奥氮平(批号:171007,江苏豪森药业集团有限公司)从5 g/d开始,10d内加到15 g/d,入组患者研究期间均维持奥氮平15 g/d剂量不变。A组给予黄连与肉桂颗粒(1∶0.5)(每0.5 g黄连颗粒相当于黄连生药3 g,批号:1710001W;每1g肉桂颗粒相当于肉桂生药3 g,批号:1711001W,华润三九医药有限公司提供)配伍治疗。每次黄连6 g与肉桂3 g,早、晚饭后各冲服1次;模拟盐酸二甲双胍缓释片,用法:每次500 g,每日口服2次。B组给予盐酸二甲双胍缓释片(批号:C012017316,北京中惠药业有限公司)治疗,每次500 g,每日口服2次;模拟黄连与肉桂颗粒配伍,用法:模拟黄连颗粒6 g与模拟肉桂颗粒3 g,早、晚饭后各冲服1次。两组疗程均为12周。
1.5 评定指标 计算BMI;阳性和阴性症状量表:包括阳性症状分量表7个症状条目、阴性症状分量表7个症状条目、一般精神病理症状分量表16个症状条目,共30项内容。严重度评分标准:采用1~7分的7级评分法;不良反应量表(treatment emergent symptoms scale,TESS):采用0~4分的5级评分法评定。
1.6 评定方法 1名专职护士统一负责治疗基线和治疗第4、8、12周末测量患者的身高、体重、腰围;治疗基线和治疗第12周末评定PANSS、TESS,对评定者实施随机方案隐藏,由4名不参加本课题研究的精神科主治医师评估,对评定PANSS、TESS者进行一致性培训,严格按照统一的指导语进行,并于培训结束后对评定者进行笔试和专家面试考核,考核合格的评定者对患者进行问卷调查,组内相关系数(ICC)≥0.96。
1.7 血样采集及检测 禁食12 h,清晨7时空腹抽取肘静脉血2 mL用于检测血清TG、TC、HDL-C、LDL-C水平。
1.8 安全性评定 治疗基点、第12周末分别对两组患者进行生命体征观察,包括体温、心率、血压、呼吸,治疗基线和治疗第12周末进行心电图、血常规和全套血生化检查,评定TESS。

2 结果
2.1 体重、腰围、BMI水平比较 治疗基点两组体重、腰围和BMI水平差异无统计学意义(F=0.312~0.011,P=0.579~0.916);治疗第12周末,两组体重、腰围和BMI水平较治疗基点显著降低(t=41.213~3.217,P=0.000~0.003),且A组体重、腰围和BMI水平均显著低于B组(F=9.314~4.995,P=0.003~0.026)。见表1。

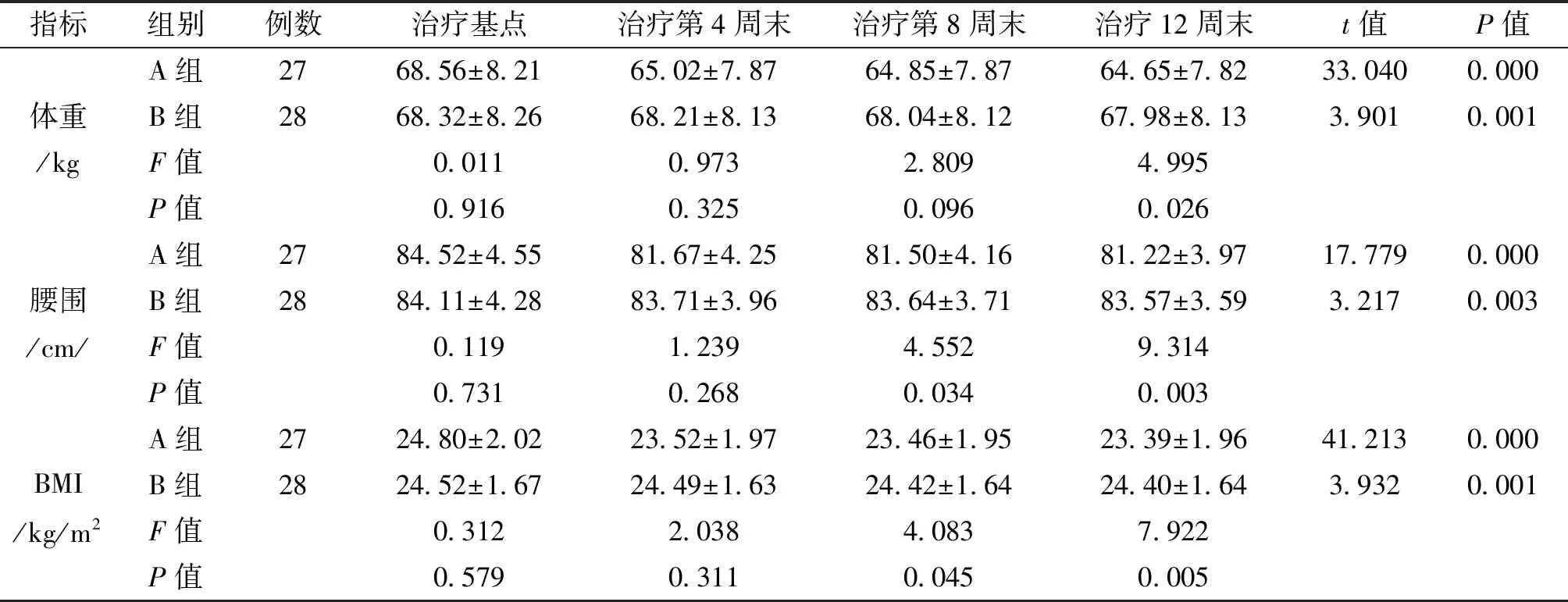
指标组别例数治疗基点治疗第4周末治疗第8周末治疗12周末t值P值体重/kgA组2768.56±8.2165.02±7.8764.85±7.8764.65±7.8233.0400.000B组2868.32±8.2668.21±8.1368.04±8.1267.98±8.133.9010.001F值0.0110.9732.8094.995P值0.9160.3250.0960.026腰围/cm/A组2784.52±4.5581.67±4.2581.50±4.1681.22±3.9717.7790.000B组2884.11±4.2883.71±3.9683.64±3.7183.57±3.593.2170.003F值 0.1191.239 4.5529.314P值 0.7310.268 0.0340.003BMI/kg/m2A组2724.80±2.0223.52±1.9723.46±1.9523.39±1.9641.2130.000B组2824.52±1.6724.49±1.6324.42±1.6424.40±1.643.9320.001F值 0.3122.0384.0837.922P值 0.5790.311 0.0450.005
注:t值为同一组治疗基点与治疗12周末比较的t检验值。
2.2 血清TG、TC、HDL-C、LDL-C水平比较 治疗基点两组TG、TC、HDL-C、LDL-C水平差异无统计学意义(F=0.354~0.005,P=0.554~0.947);治疗第12周末,两组TG、TC、LDL-C水平较治疗基点显著降低(t=6.555~3.698,P=0.000~0.001),且A组TG水平显著低于B组(F=11.280,P=0.001)。见表2。


指标组别例数 治疗基点 治疗第4周末 治疗第8周末 治疗12周末t值P值TGA组27 3.37±1.013.00±0.712.44±0.402.28±0.35 6.279 0.000B组28 3.29±1.063.17±0.972.75±0.622.51±0.30 4.935 0.000F值0.0800.148 3.98511.280P值0.7780.701 0.0480.001TCA组27 5.78±0.755.76±0.735.54±0.445.39±0.33 3.698 0.001B组28 5.67±0.645.66±0.645.54±0.545.49±0.50 4.570 0.000F值0.3540.678 0.3290.006P值0.5540.412 0.5670.937HDL-CA组27 1.24±0.231.25±0.201.26±0.141.28±0.13 -1.499 0.146B组28 1.25±0.371.25±0.321.25±0.281.27±0.24 -0.897 0.377F值0.0050.0030.0090.035P值0.9470.9590.9250.852LDL-CA组27 3.45±0.613.23±0.633.22±0.612.92±0.53 5.732 0.000B组28 3.41±0.633.36±0.593.24±0.563.01±0.54 6.555 0.000F值0.0410.1650.156 0.452P值0.8400.6850.694 0.502
注:t值为同一组治疗基点与治疗12周末比较的t检验值。
2.3 PANNS总评分比较 治疗基点两组阳性症状、阴性症状和PANNS总评分差异无统计学意义(F=0.023~0.000,P= 0.879~0.982);治疗第12周末,两组阳性症状、阴性症状和PANNS总评分差异均无统计学意义(F=0.127~0.006,P=0.723~0.938)。见表3。
2.4 药物不良反应比较 A组在研究期间出现恶心、便秘、椎体外系反应共6例,B组出现恶心、便秘、腹泻、椎体外系反应共7例,两组患者不良反应发生率分别为22.22%(6/27)、25.00%(7/28),差异比较无统计学意义(F=0.150,P=0.928);出现不良反应的两组患者TESS评分分别为(2.43±0.53)、(2.50±0.55)分,差异比较无统计学意义(F=0.148,P=0.864)。治疗12周末两组患者肝肾功能、血常规、心电图检查均正常。

表3 治疗基点、治疗第12周末两组PANNS总评分比较 (分,
注:t值为同一组治疗基点与治疗12周末比较的t检验值。
3 讨论
3.1 黄连与肉桂配伍激活中枢5-HT信号通路 奥氮平抑制糖转运蛋白活性可能是体重增加的原因之一,而奥氮平引起体重增加的主要原因可能是拮抗中枢5-HT2A/2C等神经递质受体的作用结果[7],引起食欲增强,机体能量的摄入超过消耗,多余的能量以脂肪形式贮存,引起体重增加。二甲双胍可增加机体能量消耗[8]、减少白色脂肪组织积累[9]、降低患者的食欲以及抑制肠道葡萄糖的吸收[10]。黄连的主要有效成分黄连素能上调解偶联蛋白2而促进能量消耗,也能抑制小肠上皮细胞上二糖酶(主要是蔗糖酶、麦芽糖酶)活力而减少肠道吸收葡萄糖[11]。本研究结果表明,二甲双胍、黄连与肉桂配伍均能显著降低奥氮平引起的体重增加,但黄连与肉桂配伍降低体重增加的效果显著优于二甲双胍。奥氮平等第二代抗精神病药拮抗5-HT2A/2C受体,引起5-HT对中枢系统的厌食欲作用减弱[12],导致食欲增强、体重增加。近来有研究发现,交泰丸(黄连与肉桂配伍)可显著提升大脑中缝核、海马5-HT水平[13],激活5-HT1A受体(2~3周后突触前5-HTlA受体激活的敏感性降低, 突触后5-HT1A受体的敏感性不受影响),直接抑制食欲肽能神经元活动[14],下调Orexin表达,抑制食欲。说明黄连与肉桂配伍可通过激活中枢5-HT信号通路干预奥氮平引起体重增加。
3.2 黄连与肉桂配伍多路径调控脂代谢 Oh等[15]研究发现,奥氮平等第二代抗精神病药可抑制单磷酸腺苷酸活化蛋白激酶通路而促使脂肪合成增加、脂肪酸的氧化过程减弱,从而导致血脂异常。二甲双胍、黄连主要有效成分黄连素可显著增加AMPK磷酸化水平[16-17],抑制固醇调节元件结合蛋白mRNA的表达,减少脂质合成[15]。本研究结果与上述文献报道相近,二甲双胍、黄连与肉桂配伍均可显著降低TG、TC、LDL-C水平,但黄连与肉桂配伍降低TG水平存在明显优势。可能原因有:黄连素能明显增强肝脏超氧化物歧化酶的活性,阻止类脂质的吸收及游离脂肪酸通过黏膜上皮细胞的再脂化作用[18];黄连素可增强脂蛋白脂肪酶活性,有利于催化乳糜微粒和极低密度脂蛋白中TG的分解,同时黄连素具有降低血清游离脂肪酸的作用[19]。表明黄连与肉桂配伍较二甲双胍有更多路径调控脂代谢紊乱。
3.3 黄连与肉桂配伍多靶点作用中枢系统 黄连与肉桂配伍可增加中枢突触间隙5-HT水平,加强对中枢多巴胺(DA)功能的抑制,改善精神分裂症阳性症状[20]。本研究结果显示,两组治疗后阳性症状、阴性症状和PANNS总评分较治疗基点显著降低,但两组间差异没有统计学意义,与上述报道结果不一致。正常精神活动状态是中枢各种功能系统相互作用所形成的动态平衡(内稳态)状态,精神病症状是中枢机能动态平衡失调的表现。由此推测黄连与肉桂配伍不仅上调中枢突触间隙5-HT水平,还可能多靶点作用于中枢系统,且相互作用不影响中枢机能动态平衡。本研究中患者出现的不良反应很少、很轻微,没有被试者因不良反应而退出。
综上,黄连与肉桂配伍干预奥氮平引起体重增加的效果显著优于二甲双胍。但观察疗程较短,二甲双胍、黄连与肉桂配伍对奥氮平引起体重增加和脂代谢异常的远期效果有待进一步观察;黄连与肉桂配伍干预奥氮平阻滞中枢5-HT信号通路的作用机制有待进一步深入研究。
