(3,5-二甲基苯基氨基甲酸酯)衍生的纤维素手性固定相
2019-11-07谌学先何义娟袁黎明
谌学先, 张 鹏, 何义娟, 徐 文, 袁黎明
(云南师范大学, 能源与环境科学学院, 化学化工学院, 昆明 650500)
手性是自然界的基本属性之一,与生命也有着密切的关系。研究手性识别的最主要原动力来自于手性药物,除此之外其与化学、化工、环境、农药、食品、香料、材料等领域也有非常广阔的联系。早在1992年,美国食品药品管理局(FDA)就要求,新研制的具有手性的药物必须提供单个对映体的药理学和药物代谢动力学实验数据,因为对映体之间常常具有不同的药效。
色谱分析法由于其非常优秀的分辨能力,是目前应用最广的手性拆分方法[1-4],其中高效液相色谱又是色谱分析法中应用最为普遍的[5,6]。1973年,Hesse G和Hagel R[7]首先制备出了具有实用价值的多糖衍生物——微晶三醋酸纤维素,随后以Okamoto Y为代表的研究者进行了大量的研究[8],先后合成了数百个多糖类的衍生物[5,6],成功开发了基于纤维素和直链淀粉的商品化手性分离材料。在HPLC以及制备液相色谱手性分离柱中,多糖类无疑是目前使用最为广泛的,有90%左右的手性样品可以在该类分离柱中识别。而在这些商品柱中,纤维素三(3,5-二甲基苯基氨基甲酸酯)(CTDMPC)又是最杰出的代表。
1986年第一次报道了CTDMPC固定相[9],随后大量的作者都参考该文将多糖涂渍在氨丙基化的硅胶表面,制备涂渍型的多糖手性柱,且所用硅胶种类多样[10-15]。但到目前为止,尚未见不同程度衍生的纤维素(3,5-二甲基苯基氨基甲酸酯)以及不同硅胶包括粗制硅胶、氨丙基粗制硅胶、精制硅胶、氨丙基精制硅胶、大孔硅胶、氨丙基大孔硅胶作为支撑体对该手性固定相分离能力的影响的系统研究。本研究有助于人们更深刻地理解和更好地设计高效液相色谱手性柱的制备方法。
1 实验部分
1.1 试剂与仪器
粗制硅胶(YQG80球形硅胶,粒径5 μm,孔径10 nm,青岛美高化工有限公司;因该硅胶价格相对较低,在文中简称粗制硅胶);精制硅胶(粒径5 μm,孔径10 nm,苏州纳微科技股份有限公司;因该硅胶价格相对较高,在文中简称精制硅胶);大孔硅胶(粒径7 μm,孔径100 nm,日本Daisogel公司);微晶纤维素、3-氨丙基三乙氧基硅烷、盐酸、吡啶、甲苯、丙酮、正己烷、异丙醇、甲醇(天津市风船化学试剂科技有限公司); 3,5-二甲基苯基氨基异氰酸酯(Adamas-Beta试剂有限公司);手性化合物(Sigma-Aldrich和Adamas-Beta试剂有限公司)。
高效液相色谱仪(配有Elite P 1201高压恒流泵、Elite UV 1201紫外检测器、EC 2006型色谱工作站,大连依利特分析仪器有限公司);不锈钢色谱柱(250 mm×2.0 mm)和液相色谱装柱机(美国Alltech公司); S-3000N扫描电子显微镜(SEM,日本Hitachi Science Systems公司); Bruker Avance Ⅲ 500MHz核磁共振仪(德国Bruker公司);全自动比表面及孔径分析仪(日本BELSORP-max Ⅱ公司)。
1.2 手性固定相的合成
CTDMPC的合成[8,9]: 150 mL的圆底烧瓶中加入2 g微晶纤维素,在100 ℃下真空干燥5 h,冷却至室温。在N2保护下,依次加入80 mL无水吡啶和7.8 mL 3,5-二甲基苯基氨基异氰酸酯,于90 ℃下回流24 h,得到透明溶液,冷却后转移到800 mL甲醇中,有白色沉淀析出,减压抽滤,用大量甲醇洗涤至无吡啶味,60 ℃下真空干燥5 h,得到白色固体。
纤维素-2,3-二(3,5-二甲基苯基氨基甲酸酯)(CDDMPC)的合成[10-12]: (1)纤维素6-位伯羟基保护:150 mL的圆底烧瓶中加入2 g微晶纤维素,在100 ℃下真空干燥5 h,冷却至室温。在N2保护下,加入30 mL无水N,N-二甲基乙酰胺,于100 ℃下回流24 h,然后再加入3.0 g氯化锂、120 mL无水吡啶,在100 ℃下回流12 h,最后加入7.6 g三苯基氯甲烷,于100 ℃下反应50 h,冷却后转移到800 mL甲醇中沉淀、过滤,用甲醇洗涤至无吡啶味,于60 ℃下真空干燥5 h,得到黑色固体3.4 g。(2)纤维素2-,3-位仲羟基异氰酸酯化:150 mL的圆底烧瓶中加入1.5 g的上一步所得产物,在100 ℃下真空干燥5 h后,依次加入60 mL无水吡啶、4.5 mL 3,5-二甲基苯基氨基异氰酸酯,于90 ℃下反应24 h,冷却后转移到1 000 mL甲醇中沉淀、过滤,用甲醇洗涤至无吡啶味,于60 ℃下真空干燥5 h,得到灰色固体3.3 g。(3)纤维素6-位伯羟基去保护:取上一步反应所得产物3.3 g,加入到500 mL的圆底烧瓶中,然后依次加入250 mL甲醇和7.5 mL浓盐酸,室温下搅拌24 h,过滤、用甲醇洗涤,于60 ℃下真空干燥5 h,得到浅灰色固体2.7 g,即为目标产物。
氨丙基硅胶(APS-硅胶)的制备:在N2气保护下,在150 mL圆底烧瓶中分别加入10 g粗制硅胶、100 mL含量为10%的盐酸,在100 ℃条件下回流12 h,冷却至室温,用蒸馏水洗涤至中性,真空干燥6 h。将该活化的硅胶加入到150 mL圆底烧瓶中,在N2保护下依次加入1.2 mL无水吡啶、100 mL无水甲苯、1.6 mL 3-氨丙基三乙氧基硅烷,在90 ℃的条件下回流24 h,冷却至室温,用G4型砂芯漏斗减压抽滤,之后依次用正己烷、甲醇、丙酮洗涤至无吡啶味,最后真空干燥6 h得到白色固体,即为氨丙基硅胶。
1.3 (3,5-二甲基苯基氨基甲酸酯)衍生的纤维素手性固定相的制备
在6个50 mL的烧瓶中分别加入0.4 g CTDMPC和8 mL四氢呋喃,将其溶解,分别涂覆于1.6 g的下述6种硅胶表面,即得到相应的固定相:CTDMPC-粗制硅胶(CSP-1)、CTDMPC-APS-粗制硅胶(CSP-2)、CTDMPC-精制硅胶(CSP-3)、CTDMPC-APS-精制硅胶(CSP-4)、CTDMPC-大孔硅胶(CSP-5)、CTDMPC-APS-大孔硅胶(CSP-6)。按照同样的方法制得:CDDMPC-粗制硅胶(CSP-7)、CDDMPC-APS-粗制硅胶(CSP-8)、CDDMPC-精制硅胶(CSP-9)、CDDMPC-APS-精制硅胶(CSP-10)、CDDMPC-大孔硅胶(CSP-11)、CDDMPC-APS-大孔硅胶(CSP-12),这些固定相中纤维素衍生物的涂渍重量为20%。另外,在50 mL的烧瓶中,取1.2节的微晶纤维素-DMAc-LiCl溶液1.5 mL,均匀地涂覆于1.6 g大孔氨丙基硅胶表面,得到纤维素-APS-大孔硅胶(CSP-13)手性固定相,该固定相中纤维素的涂渍重量为5.6%,这主要是因为该纤维素溶液的黏度太大而难于涂渍,降低了该纤维素的涂渍重量。

图1 3种硅胶的孔径分布图
1.4 色谱柱的制备
在装柱前,先将上述制备的13种手性固定相过250目筛,然后分别将1.5 g固定相加入20 mL正己烷/异丙醇(9∶1, v/v)中形成悬浮液,倒入匀浆罐,在40~50 MPa压力下,用正己烷/异丙醇(9∶1, v/v)作为顶替液装柱。在进行实验之前,需用正己烷/异丙醇作为流动相,以0.1 mL/min的流速冲洗色谱柱至基线平稳。
1.5 色谱分离条件
流动相:正己烷/异丙醇(9∶1, v/v);流速:0.1 mL/min;色谱柱柱温:25 ℃;进样量:5 μL;紫外检测波长:254 nm或230 nm。正己烷和异丙醇使用前需用0.45 μm滤膜过滤,并超声脱气处理。用流动相分别将各种外消旋体样品配制成1 g/L的溶液。
2 结果与讨论
2.1 3种硅胶的元素分析
商品化的色谱硅胶,其制备方法是厂家不公开的技术。为了能更好地了解硅胶对固定相手性分离的影响,3种硅胶分别进行元素分析(见表1)。出乎作者意料的是,三者C、H、N的含量相差甚远。因此可以看出,粗制硅胶与另外两种硅胶在制备方法上应该是不同的,而精制硅胶与大孔硅胶之间至少在制备工艺上存在着明显的差异。
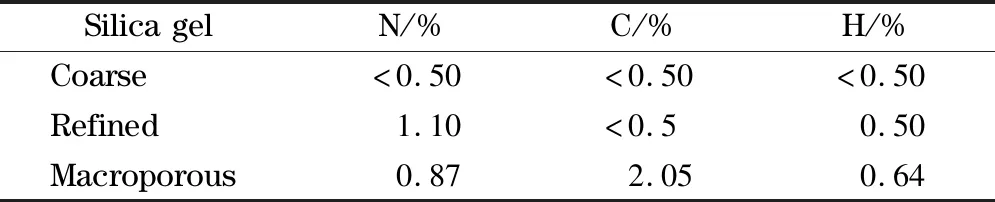
表1 3种硅胶的元素分析数据
2.2 3种硅胶的比表面积及孔径分析
分析了3种商品硅胶的比表面积及孔径。分别测得粗制硅胶、精制硅胶、大孔硅胶的比表面积为189.46、389.20、21.96 m2/g,孔径分别为6.75、6.75、58.08 nm。3种硅胶的孔径分布如图1所示。
2.3 3种硅胶的扫描电镜分析
图2是3种硅胶的扫描电镜图。可以看出,3种硅胶的粒径大小有差异,尤其是粒径分布有较大的不同。粗制硅胶的尺寸在2.0~3.9 nm范围,精制硅胶的尺寸在6.6~10.6 nm范围,大孔硅胶的尺寸在6.2~10.9 nm范围。尤其是粗制硅胶的颗粒不但偏小一些,一些硅胶的球形还不完整,其中夹杂着一些小块,而且表面更加粗糙。另外大孔硅胶的孔径也开始可见。

图2 3种硅胶的扫描电镜图
2.4 表面涂渍CTDMPC的3种硅胶的扫描电镜分析
高分子溶液就像胶水。将高分子溶液涂渍到硅胶表面后尽量让硅胶颗粒不粘连在一起,而保证固定相颗粒的高度分散性,这是商品化的多糖手性柱厂家不公开的技术。图3是表面涂渍CTDMPC的3种硅胶的扫描电镜图。可以看出,由于粗制硅胶的颗粒偏小、硅胶球形常不完整以及表面更粗糙,涂渍CTDMPC时很容易将硅胶颗粒团聚在一起。大孔硅胶由于孔大的原因,可以使很大一部分涂渍溶液进入到大孔的内部,有效地减少了硅胶之间的黏结。对于精制硅胶,其涂渍效果则介于粗制硅胶和大孔硅胶之间。

图3 表面涂渍CTDMPC的3种硅胶的扫描电镜图

图4 3,5-二甲基苯基氨基甲酸酯衍生的纤维素的核磁氢谱
2.5 3,5-二甲基苯基氨基甲酸酯衍生的纤维素的核磁氢谱分析
纤维素与3,5-二甲基苯基异氰酸酯反应后,在核磁氢谱上最明显的变化就是在化学位移为1.5~2.5之间出现甲基氢信号。比较图4 a和b,化学位移为2.3处,图4b中的峰降到很低,表明该纤维素衍生物的6位上基本没有3,5-二甲基苯基氨基甲酸酯中的甲基氢。这表明该实验成功地合成了纤维素三(3,5-二甲基苯基氨基甲酸酯)与纤维素-2,3-二(3,5-二甲基苯基氨基甲酸酯)。
2.6 自制的13根纤维素手性柱分别拆分16对外消旋体
为了评价不同程度衍生的(3,5-二甲基苯基氨基甲酸酯)纤维素,以及不同硅胶(粗制硅胶、氨丙基粗制硅胶、精制硅胶、氨丙基精制硅胶、大孔硅胶、氨丙基大孔硅胶)作为支撑体对该柱手性分离能力的影响,将1.3节中的固定相填充到色谱空柱中,自制了13根手性色谱柱。
按照1.5节中的色谱分离条件,分别考察了其对16种外消旋体的拆分能力。外消旋体及编号分别为:(1)2,2,2-三氟-1-(9-蒽基)乙醇、(2)1-(1萘基)-乙醇、(3)1,1′-联-2-萘酚、(4)联糠醛、(5)1,2-二苯乙醇酮、(6)二氢黄酮、(7)反-1,2-二苯基环氧乙烷、(8)特罗格尓碱、(9)3,5-二硝基-N-(1-苯乙基)苯甲酰、(10)华法林、(11)马来酸氯苯那敏、(12)盐酸普萘洛尔、(13)美托洛尔、(14)扁桃酸、(15) DNB-亮氨酸、(16)吡喹酮。CSP-1~CSP-13典型的色谱图见图5。

图5 13种手性柱拆分外消旋体的色谱图

表2 外消旋化合物在6种色谱柱CSP-1~CSP-6上的拆分数据

表3 外消旋化合物在6种色谱柱CSP-7~CSP-12上的拆分数据
2.6.1纤维素三(3,5-二甲基苯基氨基甲酸酯)涂覆的6种硅胶柱
将纤维素三(3,5-二甲基苯基氨基甲酸酯)涂覆于6种不同的硅胶上,制备的手性柱分别为1.3节的CSP-1、CSP-2、CSP-3、CSP-4、CSP-5、CSP-6。流动相为正己烷/异丙醇(9∶1, v/v)。考察这6种色谱柱对16种外消旋体的拆分性能(见表2)。实验结果表明,这6种色谱柱对手性化合物表现出较好的拆分性能,共有13种外消旋体得到拆分,其中有7种能在全部6种色谱柱上得到不同程度的拆分。同时,实验结果也表明,同种硅胶的氨丙基化与否对外消旋体的拆分有影响。通常认为,氨丙基硅烷化处理硅胶的目的是通过氢键作用,让纤维素衍生物能够固定得更牢固,另外由于硅胶表面性质的改变,也会一定程度地影响纤维素衍生物高分子在硅胶表面的聚集与组装状态,从而影响固定相的手性识别特性。因此,对某些样品而言,氨丙基化的硅胶可能具有较好的拆分效果,而对于另外一些样品,非氨丙基化的硅胶拆分效果似乎会更好一些。不同硅胶作为色谱基质材料时,精制硅胶和大孔硅胶的分离效果优于粗硅胶;但大孔硅胶由于孔更大,硅胶间黏结度低一些,所以柱压更低。将纤维素三(3,5-二甲基苯基氨基甲酸酯)涂覆于不同色谱基质材料表面,对手性样品的拆分还具有一定的互补作用。
2.6.2纤维素-2,3-二(3,5-二甲基苯基氨基甲酸酯)涂覆的6种硅胶柱
将纤维素-2,3-二(3,5-二甲基苯基氨基甲酸酯)涂覆于6种硅胶上制备的手性柱,分别为1.3节中的CSP-7、CSP-8、CSP-9、CSP-10、CSP-11、CSP-12。流动相同样为正己烷/异丙醇(9∶1, v/v)。考察了这6种色谱柱对16种外消旋体的拆分性能,它们也都表现出了一定的拆分性能(见表3)。共有8种外消旋体得到拆分,其中有3种手性样品能在全部6种色谱柱上得到不同程度的拆分。与纤维素三(3,5-二甲基苯基氨基甲酸酯)涂覆的硅胶柱相比,少拆分开了5个外消旋体,但在纤维素三(3,5-二甲基苯基氨基甲酸酯)涂覆的硅胶柱上不能拆分的3号和10号,却在纤维素-2,3-二(3,5-二甲基苯基氨基甲酸酯)柱上得到了拆分。另外,实验结果同样也表明,同种硅胶的氨丙基化与否对外消旋体的拆分有影响,不同硅胶作为色谱基质材料时,精制硅胶和大孔硅胶的分离效果优于粗制硅胶。我们的实验也表明,大孔硅胶的柱压低于精制硅胶。该类手性柱之间也有互补性。
2.6.3纤维素溶液涂覆的氨丙基大孔硅胶柱
由于环糊精也由多个单糖构成,非衍生化的环糊精也有一定的手性识别能力,而文献中多将多糖衍生物涂渍在氨丙基硅胶的表面[5,6],因此,我们将N,N-二甲基乙酰胺和氯化锂溶解的纤维素溶液也直接涂敷于氨丙基大孔硅胶表面,得到CSP-13固定相而制成手性柱(CSP-13)。流动相为正己烷/异丙醇(9∶1, v/v)。考察了其对16种外消旋体的拆分性能,结果只能拆分开4个外消旋体样品(见表4)。与同种支撑体的CSP-6、CSP-12色谱柱相比,CSP-13拆分开的4种中,有3种是CSP-6和CSP-12未能拆开的,因此3种柱间的互补性较强。

表4 不同程度衍生的(3,5-二甲基苯基氨基甲酸酯)纤维素色谱柱手性拆分结果的比较
因为非衍生化的环糊精手性柱常在正相、极性有机相、反相3种模式中使用,因此我们用CSP-13,在以甲醇为流动相的模式下拆分了外消旋体1、3、4号,Rs分别为2.58、2.66、3.62;在乙腈/水(1∶1, v/v)为流动相的反相模式下拆分了外消旋体1、4、6、7、8、16号,Rs分别为0.31、0.50、0.49、0.55、0.59、1.13。因此在16种外消旋体中,CSP-13能识别的手性化合物也达到了50%。
3 结论
该文详细地研究了不同程度衍生的纤维素(3,5-二甲基苯基氨基甲酸酯)以及不同硅胶作为支撑体对该柱手性分离能力的影响。研究结果显示,纤维素的取代度和不同的硅胶支撑体皆对手性柱的选择性产生不同程度的影响,这些不同的手性柱之间可产生一定的互补性。该研究结果有助于更好地制备高效液相色谱手性柱。