纳武单抗对晚期非小细胞肺癌的疗效和安全性的单中心分析
2019-11-05李静文曹淑慧
李静文,周 严,曹淑慧,王 悦,钟 华
上海交通大学附属胸科医院呼吸内科,上海 200030
肺癌是世界上最常见的恶性肿瘤,也是癌症相关死亡最常见的原因[1]。肺癌分为小细胞肺癌和非小细胞肺癌(non-small cell lung cancer,NSCLC),其中NSCLC约占85%,传统上分为3种类型,即腺癌、鳞癌以及大细胞癌[2]。手术切除是目前唯一可能使肺癌患者获得治愈的治疗手段,但很多患者确诊肺癌时已是晚期(Ⅲ或Ⅳ期),失去了手术治疗的机会,因此,含铂双药联合化疗仍然是晚期非小细胞肺癌的主要治疗手段,但其效果也较局限[3]。如今肺癌免疫治疗的研究为NSCLC的治疗开辟了一条新的道路,免疫检查点抑制剂抑制程序性死亡[蛋白]-1(programmed death-1,PD-1)/程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)生物学轴成为晚期NSCLC二线治疗的一种有效手段。纳武单抗(nivolumab)于2018年6月获得国家药品监督管理局(Natinal Medical Products Administration,NMPA)正式批准,是国内第一个上市的用于肺恶性肿瘤的针对PD-1的免疫治疗药物,用于治疗既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性NSCLC成人患者。本文收集了上海市胸科医院2016年1月—2019年4月期间接受纳武单抗治疗的晚期NSCLC患者30例,进行疗效和安全性的临床研究。
1 资料和方法
1.1 一般资料
研究对象:此临床试验选取来自上海市胸科医院接受纳武单抗治疗的30例NSCLC患者(表1)。该研究已获上海市胸科医院伦理委员会批准,所有患者签署知情同意书并遵从研究方案。
入选条件:①组织学或细胞学明确诊断为NSCLC、ⅢB期/Ⅳ期、多模式治疗(放疗、手术切除或根治性放化疗)后复发或疾病进展的受试者;②受试者既往接受过一种含铂剂二联化疗(卡铂或顺铂)方案治疗且发生疾病进展;③≥18岁的男性和女性;④美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力状况评分≤1。
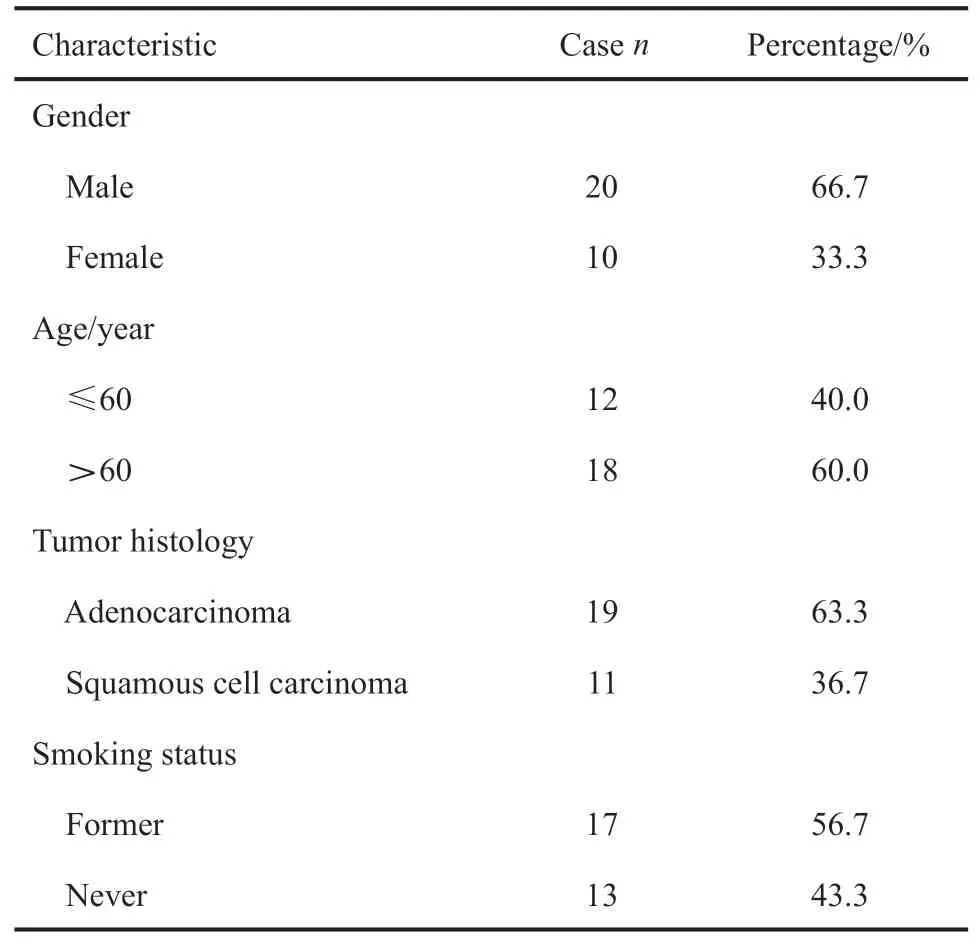
表1 患者的基本情况Tab.1 Basic characteristics of patients
排除标准:①有癌性脑膜炎;②有活动性中枢神经系统转移;③任何自身免疫性疾病的患者;④以前接受过抗肿瘤疫苗(如DC疫苗)或其他具有免疫刺激作用的抗肿瘤药治疗;⑤以前用过抗PD-1抗体(如Keytruda)、抗PD-L1抗体(如atezolizumab)、抗CTLA-4抗体(如ipilimumab)治疗;⑥乙型肝炎病毒表面抗原(hepatitis B virus surface antigen,HBsAg)或丙型肝炎病毒抗体(hepatitis C virus antibody,HCV Ab)阳性;有活动性肺结核感染;⑧有表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变和间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)基因易位的受试者。
1.2 治疗方法
按3 mg/kg的剂量静脉输注纳武单抗,每次输注60 min,每2周1次,直到出现疾病进展或不能接受的毒性。
1.3 评价指标
1.3.1 疗效评估
按照实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors,RECIST)1.1标准评价入选患者的疗效。患者将在第6周(±7 d)进行治疗期的首次影像学评价,后续每隔6周进行一次影像学评价,直到疾病进展、失访或死亡。患者停用研究药物后,将继续对患者的药物相关毒性进行随访,直到这些毒性消退、恢复到基线级别或视为不可逆为止。
按照RECISIT 1.1标准评价目标病灶:完全缓解(complete response,CR)、部分缓解(partial release,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。无进展生存期(progression-free survival,PFS)为从入组之日开始,到第一次记录肿瘤进展或最后一次随访日期或因任何原因死亡的日期之间这段时间。
1.3.2 不良事件
治疗期间药物不良反应采用常见不良事件评价标准(Common Terminology Criteria for Adverse Events,CTCAE)4.0版,将其分为1~5级。
1.4 统计学处理
采用SPSS 22.0统计软件进行处理。P<0.05为差异有统计学意义。
2 结果
2.1 疗效评估
至随访截止,30例患者的PFS曲线见图2。患者的中位PSF为2.27个月(95% CI:1.25~3.28个月)。

图1 男性腺癌患者CT诊断图Fig.1 CT scan of a male patient with advanced-stage adenocarcinoma

图2 患者PFS曲线图Fig.2 The PFS curve of patients
2.2 不良事件
本研究30例患者中有25例至少报告了1个不良事件,有21例患者报告了药物相关不良事件。药物相关不良事件有疲劳、咳嗽、气喘、腹泻、红疹、发热、纳差、贫血、胃胀、眼睛充血等,其中以疲劳(50%)最常见。有3例患者出现3级药物相关不良事件:疲劳、贫血和总胆红素升高,没有出现4~5级不良事件。其中有患者出现治疗相关性免疫介导不良事件,主要表现为甲状腺功能紊乱、口腔干燥综合征和间质性肺炎。其中1例患者T4和FT4升高、促甲状腺激素(thyroid-stimulating hormone,TSH)下降,为2级甲亢,经治疗后出现甲减,现予甲状腺素口服维持治疗,有2例为免疫相关性间质性肺炎,予肾上腺皮质激素处理后好转。不良事件级别大多数较低,无需特殊处理,其中1例患者右眼充血,为2级不良事件,予玻璃酸钠滴眼液处理后好转,另一例患者出现2级肝功能损伤,予对症治疗后好转。至随访结束,无患者因不良事件而停药或死亡(表2)。

表2 患者接受纳武单抗治疗的相关不良事件基本情况Tab.2 Treatment-related adverse events reported in patients treated with nivolumab
3 讨 论
PD-1是T细胞协同刺激受体CD28家族的成员之一,主要表达在活化的T细胞、B细胞以及髓样细胞表面[4]。PD-1的配体有2个,即PD-L1和PD-L2,其中PD-L1表达在各种类型的细胞表面,包括血管内皮细胞、胰岛细胞、上皮细胞、间充质干细胞以及B细胞、T细胞、巨噬细胞、树突状细胞和肿瘤细胞等[5-6]。PD-1主要通过与其配体PD-L1/PD-L2结合来调节T细胞的活性,抗原提呈细胞(antigen presenting cell,APC)吞噬肿瘤抗原后加工提呈给T细胞,T细胞被激活不断扩增、分泌大量炎性因子并抑制细胞凋亡,T细胞产生的IFN-γ可以上调肿瘤细胞以及APC表面PD-L1的表达,过度表达的PD-L1与PD-1结合后抑制了T细胞的扩增分泌以及存活,从而抑制了T细胞的抗肿瘤活性,使得肿瘤细胞得以逃脱[7-8]。纳武单抗是一种全人源化的IgG4同型单克隆抗体,对PD-1具有高度特异性和亲和力,通过与T细胞表面的PD-1结合来阻断肿瘤细胞对T细胞的抑制,从而恢复T细胞的抗肿瘤免疫反应[8]。
纳武单抗最初因在黑色素瘤的治疗上显示出较大的生存获益而引起了人们的关注,于是研究者们猜想纳武单抗对于NSCLC以及其他肿瘤患者是否也可以提高生存率[9]。003试验是一项在晚期实体瘤患者中进行的Ⅰ期临床研究,主要研究免疫检查点抑制剂在晚期实体肿瘤患者中的安全性和抗肿瘤活性,其中包括NSCLC[10]。后续Checkmate063、Checkmate017和Checkmate057研究表明,纳武单抗在中位生存期、1年总生存率以及客观反应率上均显著优于多西他赛,Ⅰ、Ⅱ及Ⅲ期研究中显示的疗效改善支持其用于晚期或转移性NSCLC患者的二线治疗[11-13]。
本研究所选取的30例晚期NSCLC患者在使用纳武单抗后,中位PFS为2.27个月(95% CI:1.25~3.28个月),因样本量较小只有30例,中位PFS未显示出明显的生存优势,差异无统计学意义。30例患者中,有5例患者PFS较长,可达13~14个月,有1例患者肿瘤缩小较为明显(图1),而在疗效不明显的患者中,PFS只有1~2个月,提示纳武单抗在敏感人群中持续有效的时间较长,患者可以有较长的生存获益,这也表明了寻找潜在的获益人群和有效的生物标志物至关重要。在安全性方面,在的CheckMate017和O57临床试验中,纳武单抗最常见的治疗相关性不良事件有疲劳、食欲减退、虚弱、恶心等[11-13]。本次临床研究结果与既往相似(表2)[14],最常见的治疗相关性不良事件为疲劳,其中1例出现了3级疲劳不良反应,这在Ⅱ期研究Checkmate063中已经报道过此3级不良事件[11]。还有一些其他常见的不良事件如咳嗽、气喘、红疹、关节痛等均在Ⅱ期和Ⅲ期研究中出现过,多数为1~2级,患者大多可以耐受,无需特殊处理。纳武单抗是一种靶向免疫细胞表面PD-1的单克隆抗体,在增强抗肿瘤免疫反应的同时也会引起一些免疫相关的不良事件,常见的有肺炎、皮疹以及内分泌系统紊乱和消化系统疾病,除了肺炎外,大多数免疫相关性不良事件症状较轻(1~2级)[15]。在内分泌系统紊乱中,甲状腺疾病(如甲状腺功能亢进或减退,甲状腺炎症等)较下垂体炎、肾上腺功能不全等更为常见[16]。曾在国外的一项Ⅰ期临床试验中显示,纳武单抗以3 mg/kg静脉注射的亚组中出现过甲亢和甲减各一例[10]。本次研究中有6例患者出现治疗相关性内分泌系统紊乱:3例TSH异常以及游离三碘甲状腺素(free triiodothyron,FT3)升高,检查甲状腺功能无异常,2例甲状腺功能降低,均未做特殊处理;还有1例患者为2级甲状腺功能亢进,对症治疗后好转,与前期研究结果相符。
在本次临床研究观察的30例患者中,没有出现4~5级不良事件,也没有患者因药物相关不良事件而停药或死亡。而在前期研究中,曾出现患者因免疫治疗相关性肺炎而停止用药。CA209-003临床试验显示有3例(1%)患者死于药物治疗相关性肺炎(2例NSCLC患者),另9例(3%)出现药物相关性肺炎的患者,其中3~4级肺炎有3例(1%),早期发现的低级别肺炎患者在停药后病情可以逆转[10]。日本的一项纳武单抗Ⅱ期临床研究出现了8例(7.2%)间质性肺炎,其中7例患者在使用激素治疗后症状缓解,还有1例因症状不能缓解而死于呼吸衰竭[17]。本研究中出现2例间质性肺炎,有1例为2级不良事件,及时停药后予激素处理,症状好转。纳武单抗作为中国首个上市的针对肺恶性肿瘤的PD-1抑制剂,将在临床上逐渐展开应用,尽管国外已经做了大量的前期临床研究,但在国内经验尚且不足,在治疗过程中我们需要密切关注患者是否出现较为严重的不良事件,尤其在出现间质性肺炎后,应立即停止使用纳武单抗。
总的来说,免疫检查点抑制剂纳武单抗在NSCLC二线治疗的应用疗效较好,常见的药物相关不良事件级别较低,患者耐受性较好,具有较好的安全性。
