儿童医院94例新生儿药品不良反应分析
2019-11-02王晓燕
王晓燕
(山东大学齐鲁儿童医院,山东 济南 250022)
药品不良反应(adverse drug reaction,ADR)是指合格的药品在正常用法用量下出现的与用药目的无关的有害反应。新生儿是指从出生至生后28 d的婴儿,这个时期各器官生长发育变化快,各项生理生化机能不成熟,药物代谢酶分泌不足或缺少,机体防御功能差,容易受环境因素的影响,从而导致药物在体内敏感。
早在1962年,Shirkey就提出了儿科人群是“治疗孤儿”的概念[1]。由于儿童药物研发长期受到忽视和限制,儿童专用药品及用药信息缺乏,加之儿童生理状态和疾病状态更加复杂。因而比成年人更易发生ADR。据报道,儿童ADR发生率是成人的2倍,新生儿作为儿科治疗中的特殊群体,考虑疾病治疗的同时还须考虑其生理状态的迅速变化,故不良反应发生比例更高[2]。
目前关于儿童药品不良反应分析的报道比较常见,而新生儿药品不良反应相关文章鲜见报道。本文通过对我院2012~2018年上报国家药品不良反应中心的ADR新生儿病例进行回顾性统计、分析,了解新生儿药品不良反应发生的特点及规律,以期促进新生儿合理用药,为其安全用药提供依据。
1 资料与方法
1.1 资料来源 我院2012年1月1日~2018年12月31日收集并上报国家药品不良反应监测中心的儿童药品不良反应病例共2 035例,性别:男性1 295例,女性740例;年龄:为1 d~14岁,具体性别、年龄情况详见表1。其中,上报新生儿ADR病例共94例。

表1 发生ADR患儿的年龄分布
1.2 统计方法 对2012~2018年94例新生儿ADR病例进行信息提取,从患儿体重、性别、日龄、相关药物、给药途径、用药原因、ADR临床表现、ADR结果、对原患疾病的影响、报告人职业等情况分别进行统计。
2 结果
2.1 ADR患儿体重、性别、年龄等基本情况 94例新生儿药品不良反应病例中,患儿的体重范围在1.86~5.3 kg之间,年龄在1~28 d不等;男孩55例(55.51%),女孩39例(41.49%),男女比例为1.41∶1;严重的ADR病例54例,一般ADR病例40例;新的药品不良反应共6例,其中2例为新的严重的,4例为新的一般的ADR。
2.2 ADR涉及的药物种类 94例ADR病例共涉及9类药物,38个品种,具体ADR分布情况,详见表2。导致新生儿ADR前10位的药品品种中,抗菌药物占9种,其中,β-内酰胺类6种、碳青霉烯类1种、糖肽类1种。具体用药品种前10位见表3。
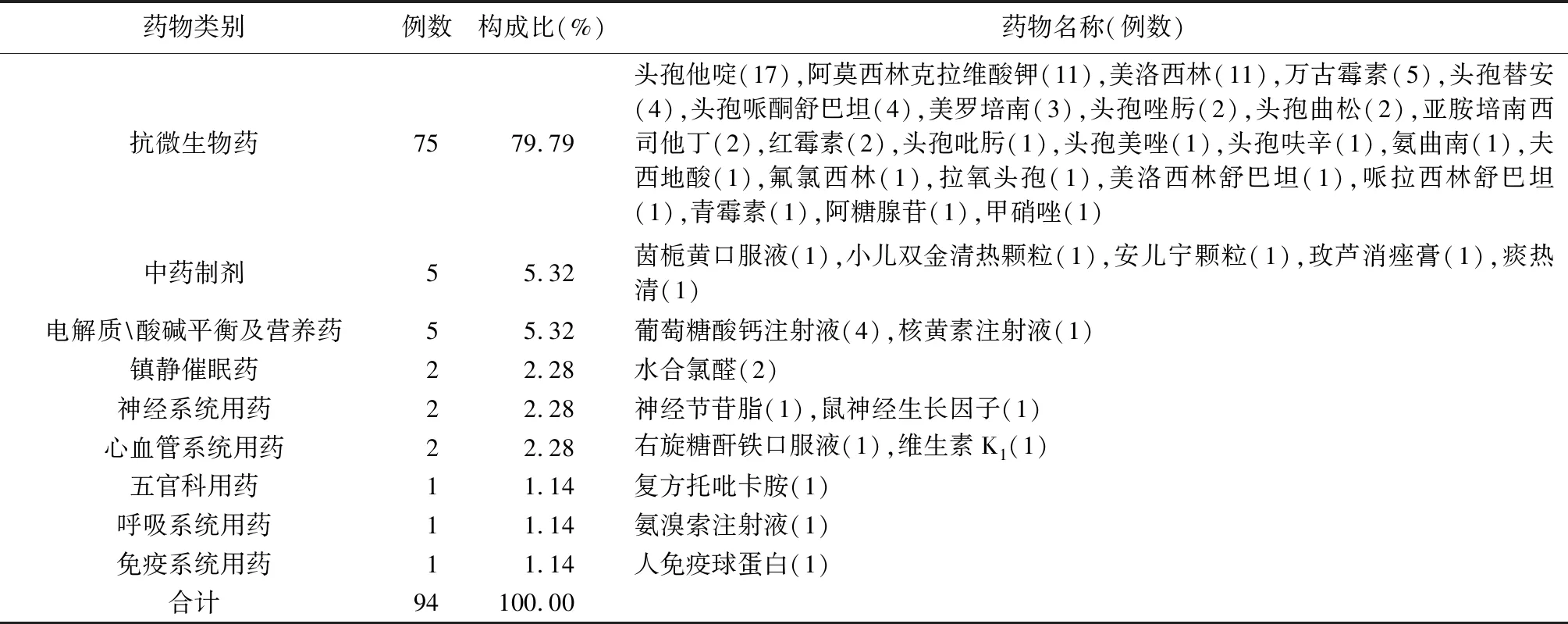
表2 ADR涉及的药物品种、例数及构成比
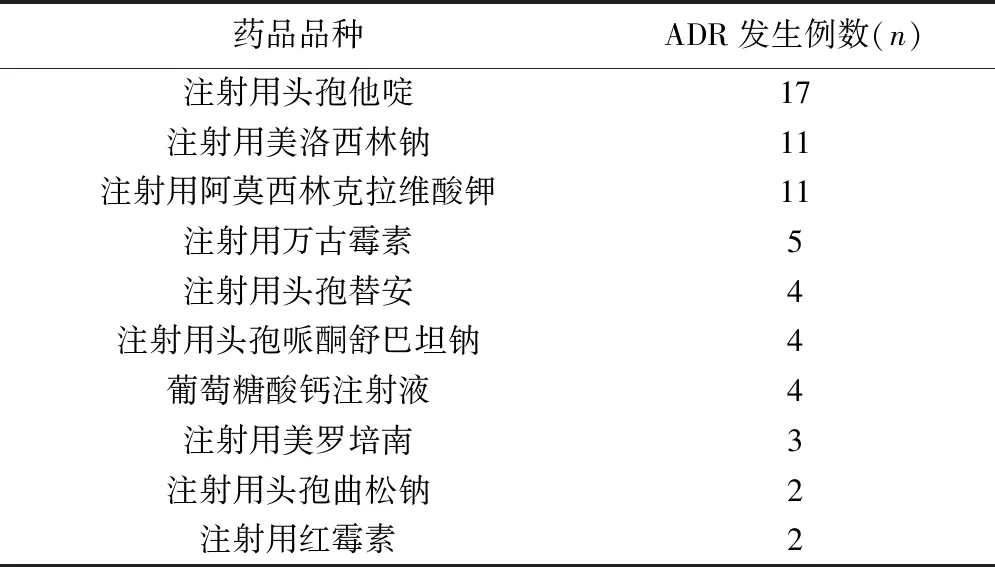
表3 导致新生儿发生ADR的药品品种前10位统计表
2.3 用药原因与ADR的关系 发生药品不良反应的新生儿病例的用药原因统计结果是主要为感染性疾病:包括新生儿肺炎、败血症、支气管炎、感染等共76例(76/94,80.85%),其次为低血钙症共4例(4/94,4.23%)。具体用药原因前10位详见表4。
2.4 给药途径与ADR的关系 94例ADR患儿给药途径统计:静脉滴注给药79例,泵内注射给药6例,口服给药5例,经眼给药、局部给药、直肠给药、吸入给药各1例。详见表5。
2.5 ADR发生时间分布 对94例新生儿病例发生ADR时间进行统计,其中发生ADR在0~≤1天共32例(34.04%),≥1~3 d共28例(29.78%),≥3~5 d共15例(15.96%),≥5~9 d共15例(15.96%),≥9~15 d共4例(4.26%)。
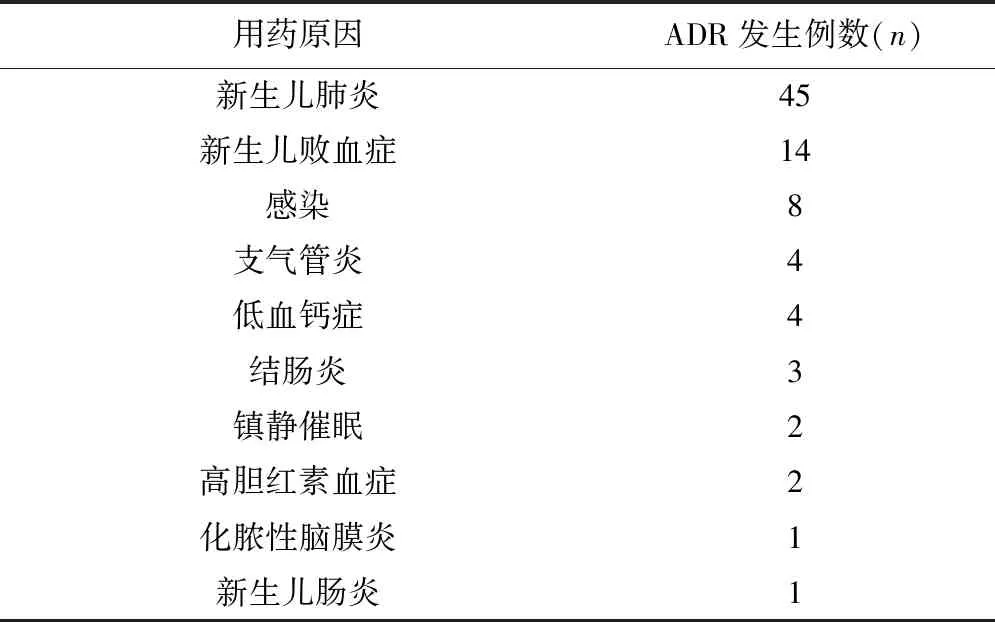
表4 发生新生儿ADR的用药原因前10位统计表
2.6 ADR累及的系统/器官及主要临床表现 根据《WHO药品不良反应术语集》对94例新生儿ADR病例累及的系统/器官进行统计,详细结果见表6。
2.7 超说明书用药情况统计
2.7.1 导致新生儿ADR的38个药品,说明书有新生儿用法用量的仅8个品种、有婴儿用法用量7个、有儿童用法用量的13个、无儿童用用法用量的有10个,具体情况详见表7。

表5 发生ADR的新生儿给药途径统计表
2.7.2 葡萄糖酸钙注射液致新生儿ADR用法用量及不良反应表现情况统计 葡萄糖酸钙注射液用法用量项下示:小儿用于低钙血症,按体重25 mg·kg-1缓慢静注,但因刺激性较大,一般不用于小儿。我院4例葡萄糖酸钙注射液导致的新生儿ADR用法用量情况统计见表8。
2.8 ADR对原患疾病的影响及归转情况 94例新生儿药品不良反应报告中,ADR的发生对原患疾病病程影响不明显的共73例(73/94,77.66%),导致患儿病程延长的19例(19/94,20.21%),致使患儿病情加重2例(2/94,2.13%)。经过停药、治疗后,患儿ADR临床表现痊愈的77例,好转的17例,无一例死亡。

表6 ADR累及的系统/器官及主要临床表现

表7 药品说明书中儿童用药用法用量情况统计表

表8 葡萄糖酸钙注射液用药剂量情况及不良反应表现统计表
2.9 ADR对原患疾病的影响 94例ADR对新生儿原患疾病的影响结果显示:病情加重2例,病程延长19例,不明显73例。
2.10 ADR报告人职业 新生儿发生药品不良反应报告人的职业为:医生93人,药师1人。
3 讨论
新生儿作为一特殊的群体,由于其药动学、药效学与儿童及成人相比具有明显的差异性,目前对于新生儿ADR的研究,明显少于大龄儿童及成人,故应引起高度重视。
3.1 新生儿性别与药品不良反应的关系 我院94例新生儿ADR病例性别比例为1.41∶1,发生不良反应的新生儿男性明显多于女性,第六次人口普查资料显示:我国0岁儿童男女比例为1.14∶1,可能和我国新生儿男性多有一定关系;由表6可见:新生儿ADR临床表现主要为皮肤及附件的不良反应,占总数的70.16%,皮肤及附件损害引起的皮疹,位于体表,往往伴有瘙痒,易于观察,且容易辨别;其他器官系统损害较为隐匿,不易判断;另外抗菌药物抗原性较强,常引起皮肤变态反应,故ADR以皮肤及附件损害最为多见。据Tran等[3]报道ADR皮肤反应发病率,男性为56.9%,女性43.1%;王士凡等主编的《药物不良反应》示:在药物性皮炎中,男性发生率高于女性,比率约为3∶2[4],进一步说明新生儿药品不良反应跟性别有一定的关系,男孩多于女孩。
3.2 新生儿生理特点对ADR的影响 新生儿期是婴儿最脆弱的时期。新生儿较高的发病率和死亡率证实这一时期生命的脆弱。在此阶段,新生儿需要完成宫外生存所需的多种生理性调整[5],如出生后1~2周开放的卵圆孔关闭,动脉血流通过的方向发生改变,直至导管最后关闭。如果是早产儿,患透明膜或感染性疾病的新生儿,这种过渡的循环可能持续到出生许多周以后,这将使药物的代谢方式发生改变。
3.2.1 新生儿生理特点对药物吸收、分布、代谢、清除的影响 新生儿出生时胃液pH为6~8,但出生24~48 h内下降为2~3[6],影响药物电离、消化道内稳定性和吸收;新生儿出生时肠道通透性高,7 d内逐渐降低[7],胃排空、肠转运时间、肠道代谢酶水平、内脏血流量及肠道菌群水平等明显差异影响了新生儿的药物吸收。
新生儿出生时细胞內液占体重33%,至4月龄时则升至37%,药物分布可使血药浓度降低,与体液的浓度与细胞内、外液分布比例密切相关,由于新生儿血脑屏障尚未发育完全,中枢神经系统易受某些药物的影响。
药物代谢主要通过肝脏代谢,新生儿肝脏占总体质量比例较大,肝血流量比大童及成人都高,故新生儿药物清除率可能较高。据报道[8]新生儿肝内代谢酶与成人也有明显的差异,如:成人中常见的亚型CYP3A4 mRNA,新生儿检测不到,成人中检测不到的CYP3A7在新生儿出生第1周迅速下降,CYP3A4表达水平逐渐增加,由于出生后酶始动的速度不同,新生儿药代动力学个体差异很大,肝中代谢药酶的变化,可能导致药物途径改变,影响肝脏对药物的代谢。
肾的药物排泄主要通过肾小球滤过、肾小管分泌和重吸收,这些过程受到新生儿肾发育的影响,其中,肾小球滤过率影响最大。通常胎儿的肾单位数量在妊娠36周达成人水平,但其滤过率远低于成人,新生儿出生时肾小球滤过率为10~15 mL·(min·m2)-1生后2~3周可升至20~30 mL·(min·m2)-1[9],需要6个月左右肾小球和肾小管分泌达到全功能,其肾小球滤过率(GFR)约为13~100 mL·(min·1.73 m2)-1[8],比如万古霉素PK研究显示,总清除率新生儿(<1个月)为1.14 mL·(min·kg)-1,婴儿(1-12个月)1.91 mL·(min·kg)-1,儿童(>1岁,平均5.8岁)3.17 mL·(min·kg)-1,成人0.92 mL·(min·kg)-1[10-11],故药物清除率不同的年龄段,具有各自不同的特点。另外肾小管转运体的发育变化、尿液的pH均影响药物的重吸收。
发育变化是新生儿药代动力学重大影响因素,药物的分布、代谢及排泄与大龄儿童及成人的存在较大的差异,影响新生儿体内的血药浓度,从而介导不良反应的发生。
3.2.2 新生儿生理特点对药效学的影响 新生儿成长过程中细胞外的水分明显减少,亲水性药物表现出更大的VD和较低的血药浓度;但新生儿又含有较高的体脂含量,可引起高脂溶性药表观分布容积的增加;新生儿血脑屏障发育未全,中枢神经系统易受某些药物的影响。药物与血浆蛋白的结合取决于所结合的蛋白的浓度、药物与蛋白结合的亲和力、结合部位的数目、有关病理生理情况或可以改变药物与蛋白质相互作用的物质(外源性或内源性的)[12]。新生儿血浆蛋白总量低;未酯化的脂肪酸较高,它可与白蛋白产生可逆性结合;新生儿胆红素与白蛋白呈非共价键性,易于可逆的结合,其新生儿期胆红素是变化的过程,新生儿与成人的血浆蛋白结合特性有所不同,因而游离药物浓度与新生儿的生理状态密切相关,可影响药物治疗的疗效和安全。
3.2.3 疾病对药物处置的影响 新生儿的疾病起源于宫内、产时或产后即时,可由基因突变、染色体畸变、获得性疾患和损伤造成的,先天畸形是死产和新生儿死亡的主要原因,它可引起急性疾病,包括代谢性疾病和长期患病。窒息、透明膜性疾病、坏死性结肠炎、败血症和出血可能严重损伤肾灌注[13]。疾病状态对药物的处置影响很大,这些影响可来自机体的理化状态和特殊器官功能的改变。对新生儿患者的药物治疗,既要关注日龄对器官发育成熟的影响,还需要关注患儿疾病生理、病理的相互作用。
3.3 临床用药对新生儿产生不良反应的影响
3.3.1 用药原因对ADR的影响 据估计2017年有630万名15岁以下儿童死亡,其中250万名儿童在出生后第一个月内死亡,虽然营养因素对5岁以下儿童死亡的贡献率达到约45%,但新生儿死亡的主要原因仍然是肺炎、腹泻及疟疾等感染性疾病[14]。由表3可以看出,我院新生儿用药原因主要为感染性疾病,如新生儿肺炎、新生儿败血症,支气管炎、新生儿肠炎等感染性疾病与世界卫生组织统计结果相一致。当机体处于感染状态下,患儿体内各种炎症因子如IL-2、IL-6等明显增高,炎性因子的增高是造成ADR发生的重要因素[15]。
3.3.2 用药品种对ADR的影响 抗菌药物的影响:94例新生儿用药品种前十位中,其中9个品种为抗菌药物,仅1个属电解质、酸碱平衡及营养类药物。表3可以看出,新生儿用药原因主要为感染类疾病,尽管因为母体IGE可通过胎盘,使新生儿具有一定的被动免疫,新生儿仍然是各种感染的易感人群,故抗菌药物的使用频率明显高于其他类药物。新生儿抗菌药物使用范围窄,如氯霉素可引起新生儿灰婴综合征,禁止使用;氨基糖苷类抗菌药物具有耳肾毒性;喹诺酮类对软骨有损害;四环素类药物可引起牙齿、骨骼发育不良,牙齿黄染;磺胺类及呋喃类抗菌药物,新生儿红细胞缺乏葡萄糖-6-磷酸脱氢酶而引起溶血性贫血,所以多种抗菌药物受限,应权衡利弊选择使用。β-内酰胺类抗菌药物,安全有效,毒副作用小,成为新生儿感染性疾病首选抗菌药物,也是β-内酰胺类抗菌药物导致不良反应较多的原因之一。抗菌药物的治疗剂量通常是由高峰血药浓度所确定,许多因素可以影响血浓度的达峰时间,包括抗菌药物种类、剂型、给药途径、注射速度及所用输液泵的类型等。新生儿相同日龄的患儿体重差别较大,不同的日龄患儿生理状态个体各有不同,新生儿个体之间和同一个体对抗菌药物的治疗反应也存在差异,再加上临床用药资料有限,对体内血药浓度影响因素较多,不易掌控,极易导致不良反应的发生,据报道儿童药品不良反应发生率平均达到12.9%,新生儿高达24.4%,为成人的2倍和4倍[16]。在临床应用中,不同个体应用固定给药方案往往会产生疗效差异及不良反应,尤其是新生儿人群中,加大剂量常导致不良反应,而剂量不足又会导致耐药乃至治疗失败,加强抗菌药物血药浓度监测及制定最佳给药方案,可提高临床治疗效果并减少耐药菌的出现[17]。合理应用抗菌药物是提高疗效,降低药品不良反应发生率及减少或延缓细菌耐药发生的关键。
电解质药物影响:新生儿具有独特的生理特点,身体的各个器官都尚未发育完善,且发生着巨大的变化,代谢功能也不健全,故对影响水盐代谢酸碱平衡的药物非常敏感,应严格控制补液量与静脉滴注的速度。
3.3.3 用药途径对ADR的影响 新生儿吞咽功能较儿童及成人差,胃酸分泌很少,胃排空时间长,肠蠕动不规则,影响药物的吸收,故口服给药尽管简便,对新生儿不太适宜;新生儿肌肉组织和皮下脂肪少,局部血流灌注不足,肌内纤维软弱,血流变化大,易在局部产生蓄积,导致药物释放缓慢,故肌内或皮下给药很难准确计算吸收量,不推荐肌肉注射或皮下给药;直肠给药方便、安全、吸收快、起效快,尽管推荐使用,但由于品种受限,未得到广泛使用;静脉给药可将药物直接进入血液,不经肝脏首过效应,血药浓度较高,最大程度地发挥治疗作用,故是新生儿最常选择的用药途径,我院94例新生儿不良反应病例中,静脉给药途径占90.42%。与新生儿静脉用药为主的治疗方式密切相关。由于静脉给药作用直接而强烈,受静脉注射液的稳定性、pH值、渗透压、残存微粒、内毒素等及输液器材质量、输液速度、输液环境等诸多因素的影响,故易发生药品不良反应。
3.3.4 超说明书用药对ADR的影响 对38种发生新生儿不良反应的药品品种进行统计分析可知:使用药物中仅8种药物说明书明确具有新生儿用药的用法用量,其余30种中7个有婴儿的用法用量,13个有儿童用药的用法用量,10个品种完全没有儿童用法用量,均可判定为超人群超说明书用药。儿科治疗尤其是新生儿治疗经常出现超说明书使用药物增加了治疗无效或发生不良反应的风险,合理的儿童用药特别是在新生儿到幼儿期间,达到安全和有效的暴露,需要对影响药物的药代动力学(PK)发育过程中的生理变化有一个全面的认知,但儿童(尤其是婴幼儿)药代动力学信息严重匮乏,导致儿童用药存在巨大的潜在风险[18]。寇晨等[17]研究表明:新生儿个体差异较大,不同胎龄、不同体重的新生儿拉氧头孢药代动力学过程不尽相同,但拉氧头孢的清除率主要影响因素是当日体重与校正胎龄,同时还是影响该药分布容积主要影响因素。新生儿用药数据缺乏,尤其是新生儿药代动力学数据的缺乏是目前新生儿治疗缺乏科学性的根本原因。
10%葡萄糖酸钙注射液是纠正新生儿低钙血症最常用的方法。本次统计我院葡萄糖酸钙注射液引起新生儿ADR共4例,均用于低钙血症,符合说明书的适应证用药。钙可以维持神经肌肉正常兴奋,促进神经末梢分泌乙酰胆碱,血钙降低时可出现神经肌肉兴奋性升高,发生抽搐,血钙过高,则兴奋性降低,出现软弱无力等。葡萄糖酸钙说明书不良反应项下示:注射过快,可产生心律失常,甚至心跳停止、恶心、呕吐等。血钙过高可致皮肤毛细血管扩张,血流量增加,全身发热出现发绀;可兴奋心肌,产生心律失常,引起血压下降、呼吸减慢,甚至出现心跳呼吸停止;钙剂渗入皮下组织间隙后产生很强的刺激,出现注射部位皮肤发红、皮疹和疼痛,甚至脱皮和组织坏死[19]。10%葡萄糖酸钙注射液说明书用法用量项下示:小儿用于低钙血症,按体重25 mg·kg-1缓慢注射。由于葡萄糖酸钙注射液说明书无明确新生儿剂量,只能按小儿剂量给药,据表6可以看出:4例ADR葡萄糖酸钙使用剂量均明显偏大,是说明书用法用量的6~8倍,属于超大剂量超说明书用药,大剂量葡萄糖酸钙注射液迅速进入血管,引起严重的不良反应。
4 减少新生儿药品不良反应的对策
4.1 药物在新生儿中的代谢不同于儿童及成人,早产儿、和足月儿也有较大的区别,安全有效用药的基础,来自于药物的药代动力学数据。相对于成人可招募药代动力学志愿者,由于新生儿血容量低,常限制采血量以减少PK研究的风险。新生儿药代动力学研究面临巨大的挑战,管理部门可通过鼓励群体PK建模、干斑采样、机会性采样和非血源基质策略,促进新生儿药代动力学研究,补充完善药品说明书相关信息,为新生儿安全用药提供依据。
4.2 医生开具处方以国家处方集为依据。《英国国家处方集(儿童卷)》有电子版和纸质版,电子版每月更新,纸质版每年更新一次。儿童处方集包含针对所有年龄段的儿童处方,从新生儿到青少年不仅提供常规处方,也提供超说明书用药处方,且表明那些适应证已获得政府许可[20],建议我们国家对处方集尤其是儿童卷定期进行更新修订,使临床可及时获得新的儿童(尤其是新生儿)用药信息,以达到安全、合理用药的目的。
4.3 合理用药是减少药品不良反应的有效措施,规范制定包括给药途径、给药剂量、给药时间和疗程长短等用药方案,尽量严格按药品说明书规范用药,新生儿个体差异大,临床医师应根据患儿日龄、体重等因素,综合考虑其生理、病理因素静脉给药时应严格计算新生儿输液液体量,做到个体化给药。超说明书用药存在较大的潜在用药风险,正确的适应证给药,正确的给药剂量,条件允许的情况下进行血药浓度监测,可有效减少ADR的发生风险。
4.4 医疗机构应加强用药安全培训,将相关安全用药信息及时传递给临床医师、药师,医护人员与药师,各科室联合报道潜在、新的ADR,加强对新生儿药品不良反应监测,积累临床用药经验,降低新生儿ADR的发生率。
4.5 目前我国儿童用药严重匮乏,据肖瑛等[22]报道:1 132份样品说明书,儿童专用药品仅有35种(占3.09%),新生儿专用药品少之又少。儿童使用成人药物存在安全隐患,鉴于我们现有儿童药品情况,国家出台了一系列政策,鼓励儿童(包括新生儿)用药产品的研发生产,从源头上降低儿童(尤其是新生儿)药品不良反应的发生率。
4.6 加强上市后评价与监测,健全儿童药物不良反应监测。建议国家药品不良反应监测中心及时、不定期发布《药品不良反应信息通报》,反馈某些药品可能对儿童存在的安全隐患信息,对儿童(包括新生儿)的用药安全,具有重要意义。
